文档内容
专题突破卷 04 非金属及其化合物
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.化学与生产:生活及环境密切相关。下列说法正确的是
A.太阳能电池的主要材料是 B.新冠疫苗应冷藏存放,以避免活性降低
C.84消毒液可与洁厕灵(盐酸)混合使用 D. 具有强氧化性,可用于漂白纸浆
2.下列物质能使品红溶液褪色,且褪色原理基本相同的是:①活性炭②新制氯水③二氧化硫④臭氧⑤过
氧化钠⑥过氧化氢溶液
A.①②④ B.②③⑤ C.②④⑤⑥ D.③④⑥
3.有些科学家提出硅是“21世纪的能源”,下列说法正确的是
A.晶体硅具有半导体性质,可用于生产光导纤维
B.玻璃中含有的SiO 可与NaOH溶液反应,故常用NaOH溶液雕刻玻璃纹饰
2
C.碳化硅(SiC)俗称金刚砂,类似金刚石结构,是一种耐高温的半导体材料
D.陶瓷、水泥、石英玻璃都属于硅酸盐材料
4.用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)
A B C D
双氧
X 中试剂 浓盐酸 浓硫酸 浓氨水
水
Y 中试剂 MnO C HOH MnO NaOH
2 2 5 2
气体 Cl C H O NH
2 2 4 2 3
A.A B.B C.C D.D
5.如图所示,在A处通入未经干燥的氯气。当关闭B处的弹簧夹时,C处的红布条看不到明显的现象;当打开B处的弹簧夹后,C处的红布条逐渐褪色,则D瓶中盛放的溶液可能是
①饱和NaCl溶液 ②NaOH溶液 ③HO ④浓硫酸
2
A.①② B.①③ C.②④ D.③④
6.下列材料的特性及用途的说法中不正确的是
A.光导纤维传导光的能力很强,是非常好的通讯材料
B.氧化铝陶瓷具有两性,不可以用于制耐高温设备
C.氮化硅陶瓷耐高温且不易传热,可用来制造轴承
D.人造刚玉硬度高,可用来制造刚玉球磨机
7.下列实验说明浓硫酸有强腐蚀性的是
A.浓硫酸慢慢地注入水中产生大量的热
B.含有水蒸气的氧气通过浓硫酸得到干燥的氧气
C.浓硫酸久置在空气中质量增加
D.用小木棍蘸少量浓硫酸,小木棍变黑
8.探究铜和浓硫酸的反应,下列装置或操作错误的是
A.上下移动装置甲中的铜丝体现绿色化学的思想
B.装置乙可用于收集 气体C.将试管中的液体倒入装置丙中稀释,观察颜色可确定 的生成
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出
9.以下关于铜跟浓、稀HNO 反应的说法中错误的是
3
A.1mol浓HNO 被还原转移2mol电子
3
B.Cu与浓HNO 反应剧烈,故氧化性浓HNO 强于稀HNO
3 3 3
C.Cu与浓、稀HNO 反应都不需加热
3
D.生成等量的Cu(NO ),消耗浓HNO 的量多
3 2 3
10.已知某物质X能发生如下转化:
下列有关上述转化关系中物质及其反应的叙述正确的是
A.若X为C,则Y可以和氢氧化钠反应生成盐和水
B.若X为S,则A为硫酸
C.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
D.X一定是非金属单质或非金属氢化物
11.只用一种试剂,将NH Cl、(NH )SO 、NaSO 、NaCl 4种物质的溶液区分开,这种试剂是
4 4 2 4 2 4
A.AgNO 溶液 B.Ba(OH) 溶液 C.NaOH溶液 D.BaCl 溶液
3 2 2
12.在新制氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一
致且正确的是
A.新制氯水呈浅黄绿色,且有刺激性气味,说明溶液中有 分子存在
B.用强光照射新制氯水一段时间后,溶液 增大,说明溶液中有 存在
C.将 加入新制氯水中,有无色气泡产生,说明溶液中有 存在
D. 溶液中滴加新制氯水,溶液变成棕黄色,说明新制氯水中有 存在
13.下列颜色变化与氧化还原反应无关的是
A.将SO 通入滴有酚酞的NaOH溶液中,溶液红色褪去
2
B.将新制氯水滴入紫色石蕊溶液中,溶液先变红后褪色
C.久置的氯水,颜色逐渐变浅D.久置的浓硝酸显黄色,通入空气后颜色变浅
14.实验室进行性质探究实验,将 通入 溶液至饱和的过程中,始终未观察到溶液中出现浑浊,
若再通入另一种气体 ,则产生白色沉淀。制备气体 的试剂不能是
A.大理石和稀盐酸 B. 和
C. 和浓硝酸 D. 和浓盐酸
15.溴、碘均为卤族元素,下列关于溴、碘说法错误的是。
A.将 分别通入NaBr溶液和NaI溶液中,可以得到溴单质和碘单质
B.溴单质和碘单质在四氯化碳中的溶解度均大于它们在水中的溶解度
C.碘酒可以使淀粉碘化钾试纸变蓝
D.通常将 固体添加到食盐中来制作碘盐
二、填空题(本题包括4小题,共55分)
16.(12分)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路
线,其中一种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为 ;当有1 mol C参
与反应时,该反应转移的电子数是 。
(2)还原炉中发生的化学反应方程式为: 。(3)上述工艺生产中循环使用的物质除 外,还有 。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为 。
(5)关于硅及其相关化合物的叙述正确的是 。
A.自然界中存在天然游离的硅单质
B.玻璃、水泥、陶瓷都是传统的硅酸盐产品
C. 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
E.已知C与Si的最高正价都是正四价,由于 ,用类比法得知,
17.(14分)A是由四种短周期常见元素组成的正盐,D是红棕色气体、G能使品红溶液褪色;A与其他
物质在一定条件下存在如下转化关系(部分产物略去):
试回答下列问题:
(1) A、E的化学式依次为 、 。
(2)写出下列反应的化学方程式:
①C→D: 。
②F→G: 。
(3)检验A溶液中阳离子的方法是 ;若B→C的反应中转移2.5mol电子,则生成的C
在标准状况下的体积为 。
(4)将D和G同时通入水中,生成C和一种强酸,则反应的离子方程式为 。
18.(14分) 作为一种广谱型的消毒剂,将逐渐用来取代 ,成为自来水的消毒剂。已知 是一
种易溶于水的气体,实验室制备 的原理是用亚氯酸钠固体与氯气反应:
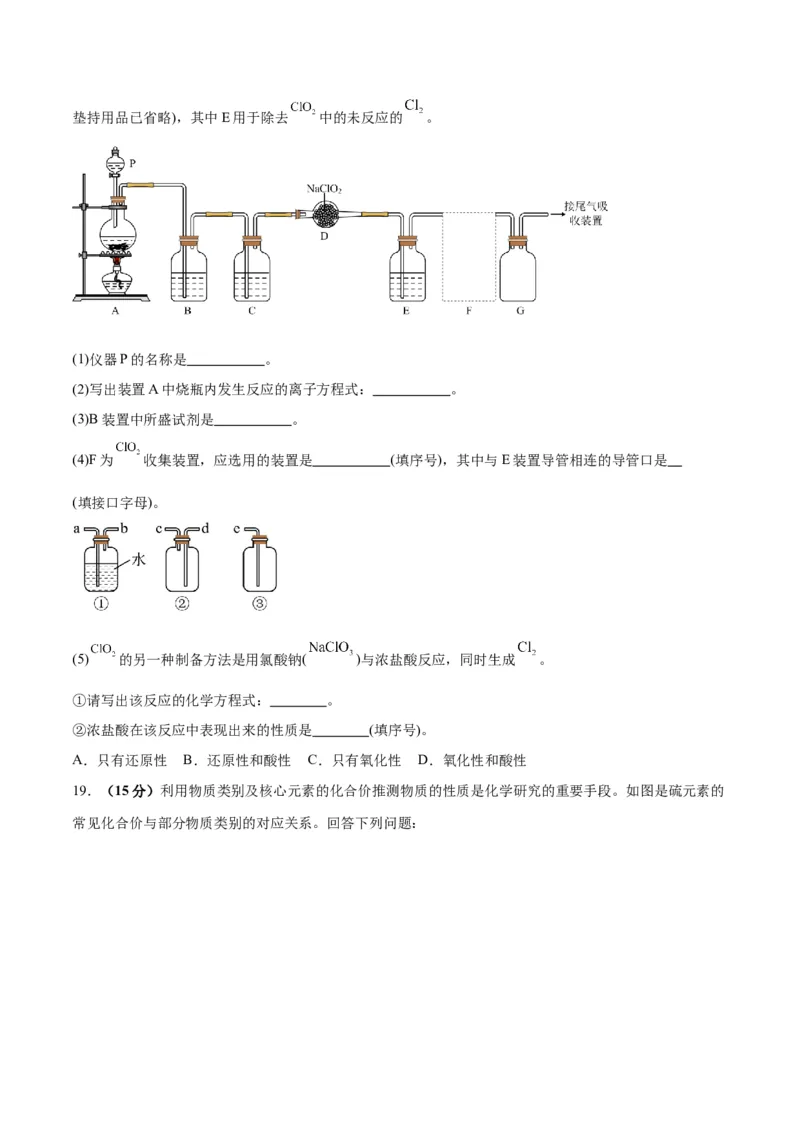
,下图是实验室用于制备和收集一定量纯净的 的装置(某些夹持装置和垫持用品已省略),其中E用于除去 中的未反应的 。
(1)仪器P的名称是 。
(2)写出装置A中烧瓶内发生反应的离子方程式: 。
(3)B装置中所盛试剂是 。
(4)F为 收集装置,应选用的装置是 (填序号),其中与E装置导管相连的导管口是
(填接口字母)。
(5) 的另一种制备方法是用氯酸钠( )与浓盐酸反应,同时生成 。
①请写出该反应的化学方程式: 。
②浓盐酸在该反应中表现出来的性质是 (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
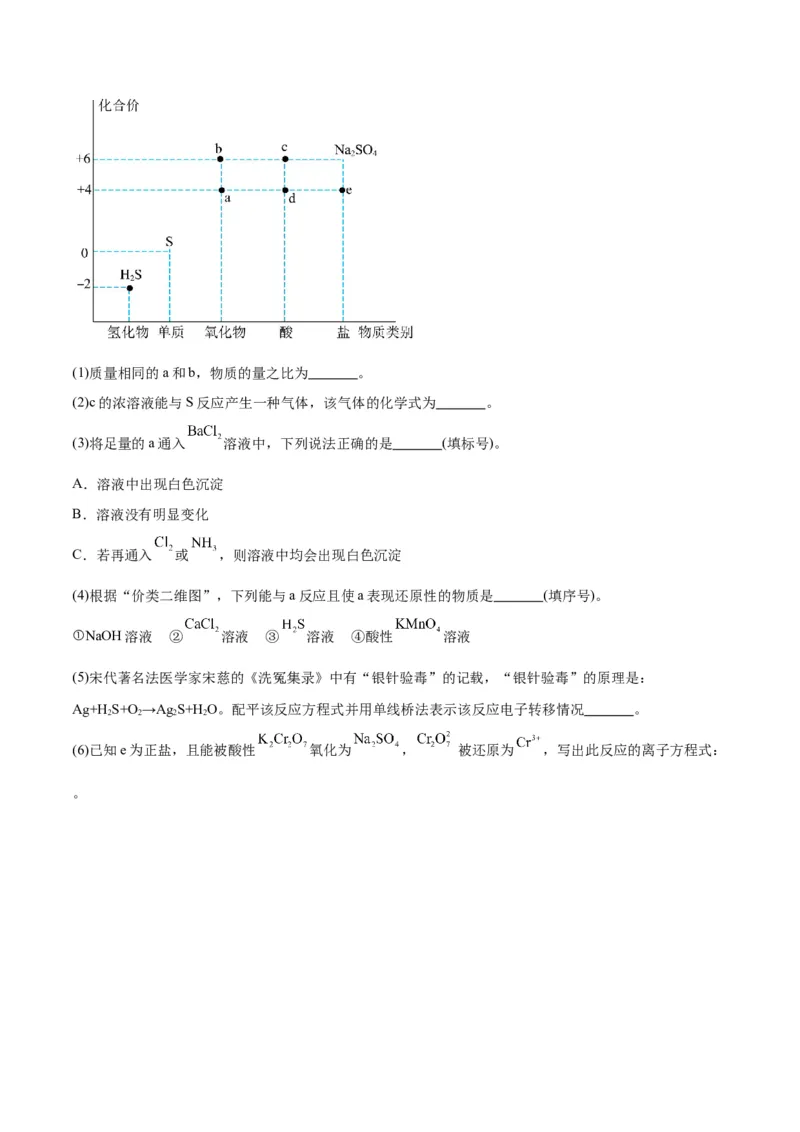
19.(15分)利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的
常见化合价与部分物质类别的对应关系。回答下列问题:(1)质量相同的a和b,物质的量之比为 。
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为 。
(3)将足量的a通入 溶液中,下列说法正确的是 (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或 ,则溶液中均会出现白色沉淀
(4)根据“价类二维图”,下列能与a反应且使a表现还原性的物质是 (填序号)。
①NaOH溶液 ② 溶液 ③ 溶液 ④酸性 溶液
(5)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是:
Ag+HS+O→Ag S+HO。配平该反应方程式并用单线桥法表示该反应电子转移情况 。
2 2 2 2
(6)已知e为正盐,且能被酸性 氧化为 , 被还原为 ,写出此反应的离子方程式:
。