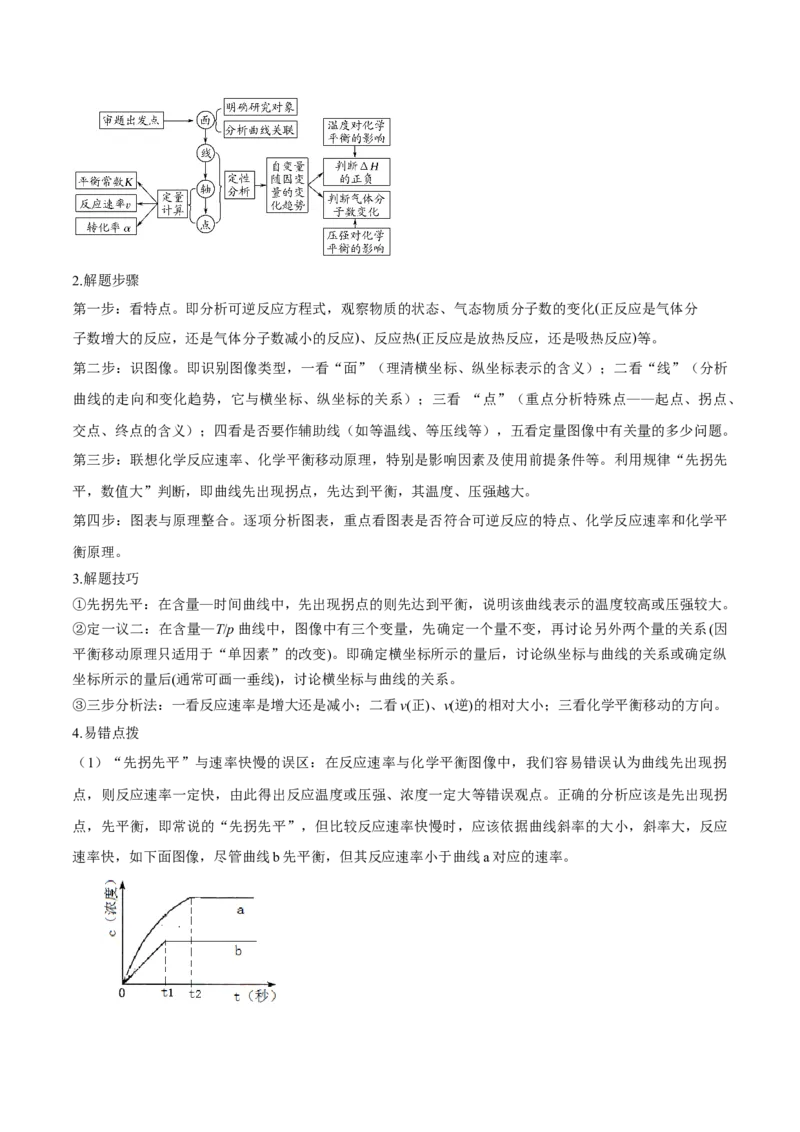
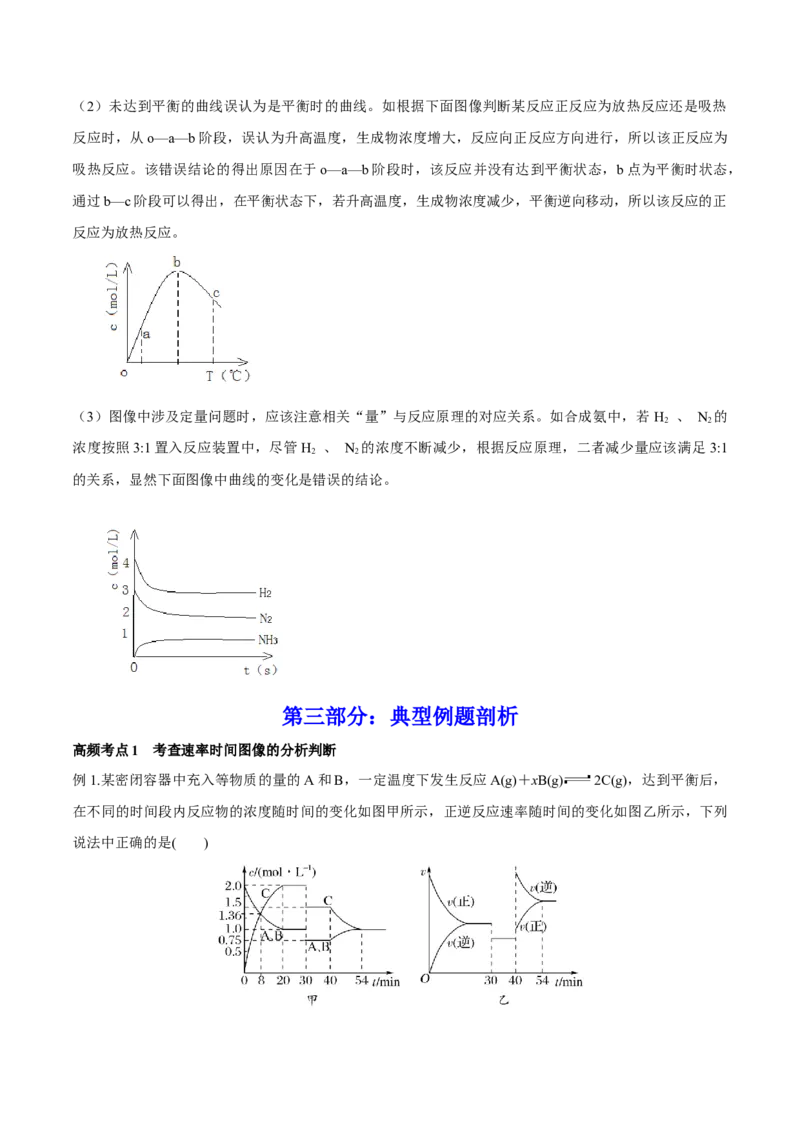
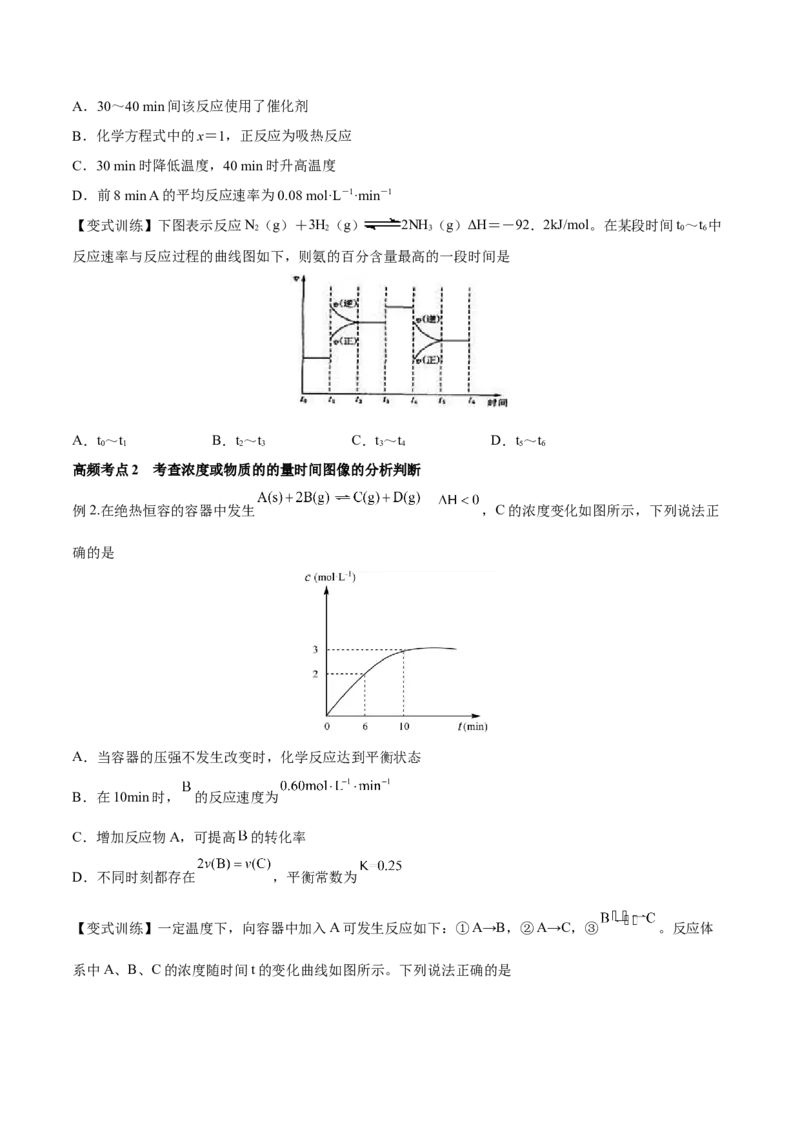
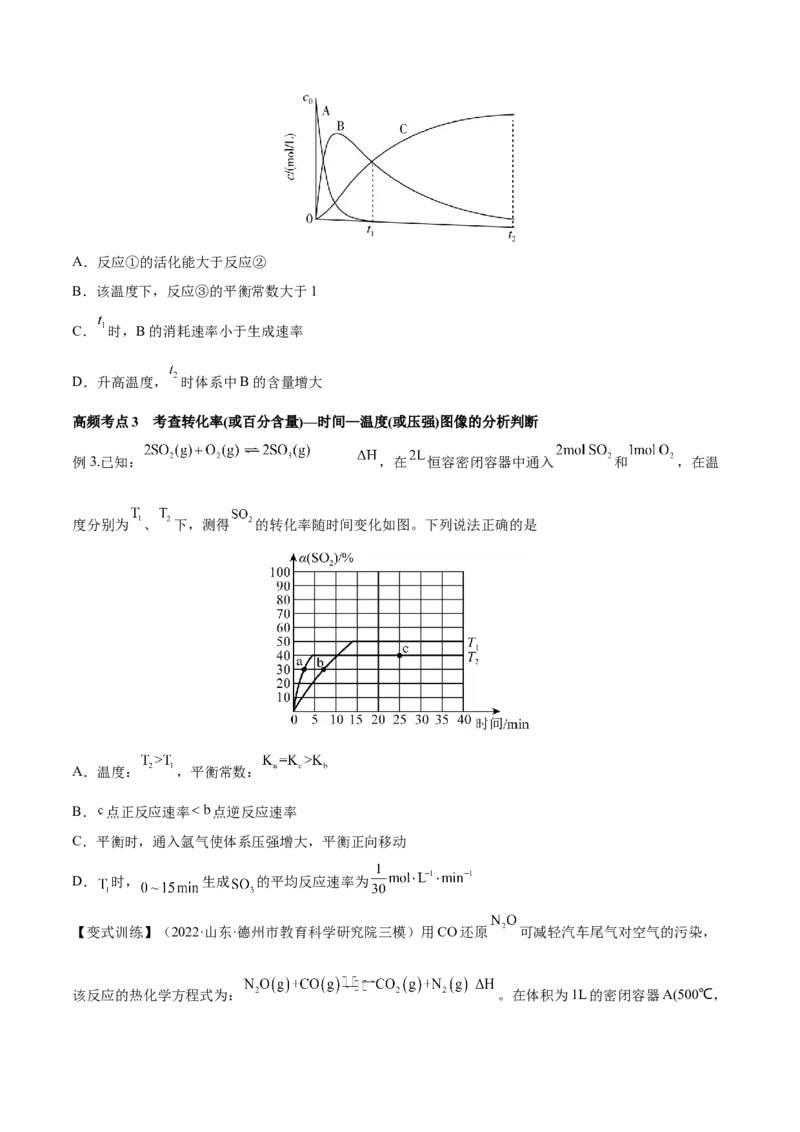
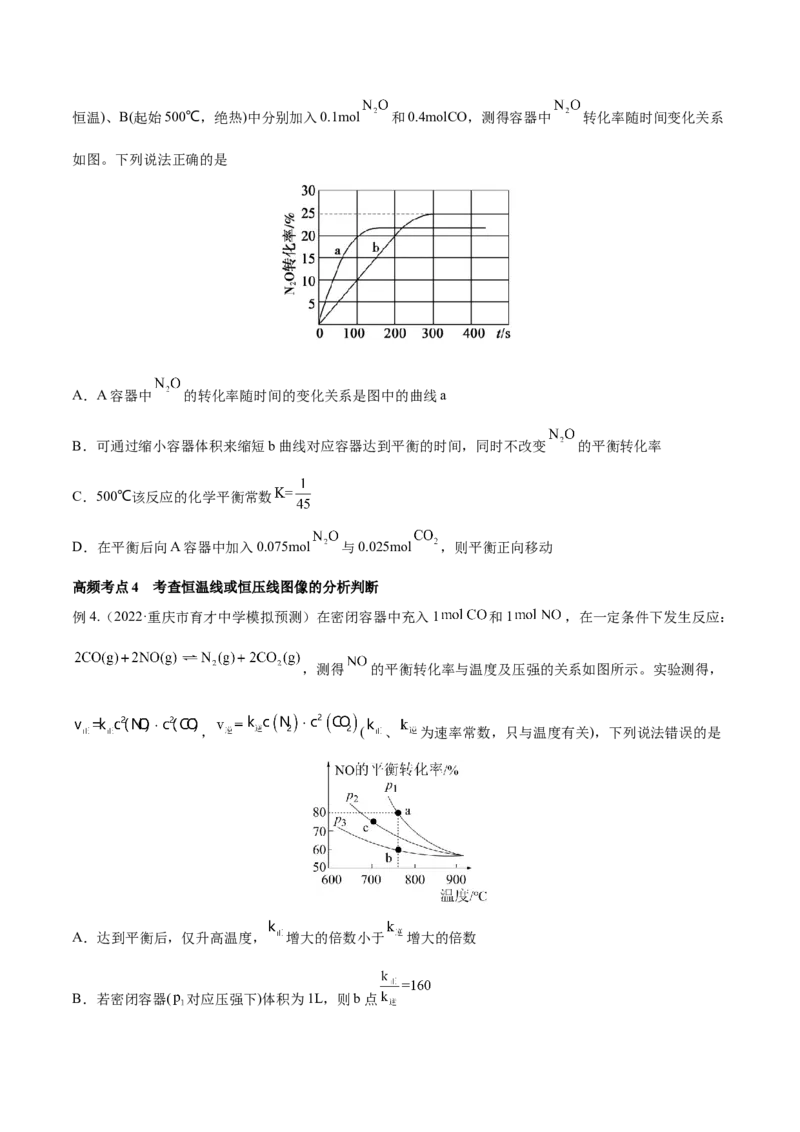
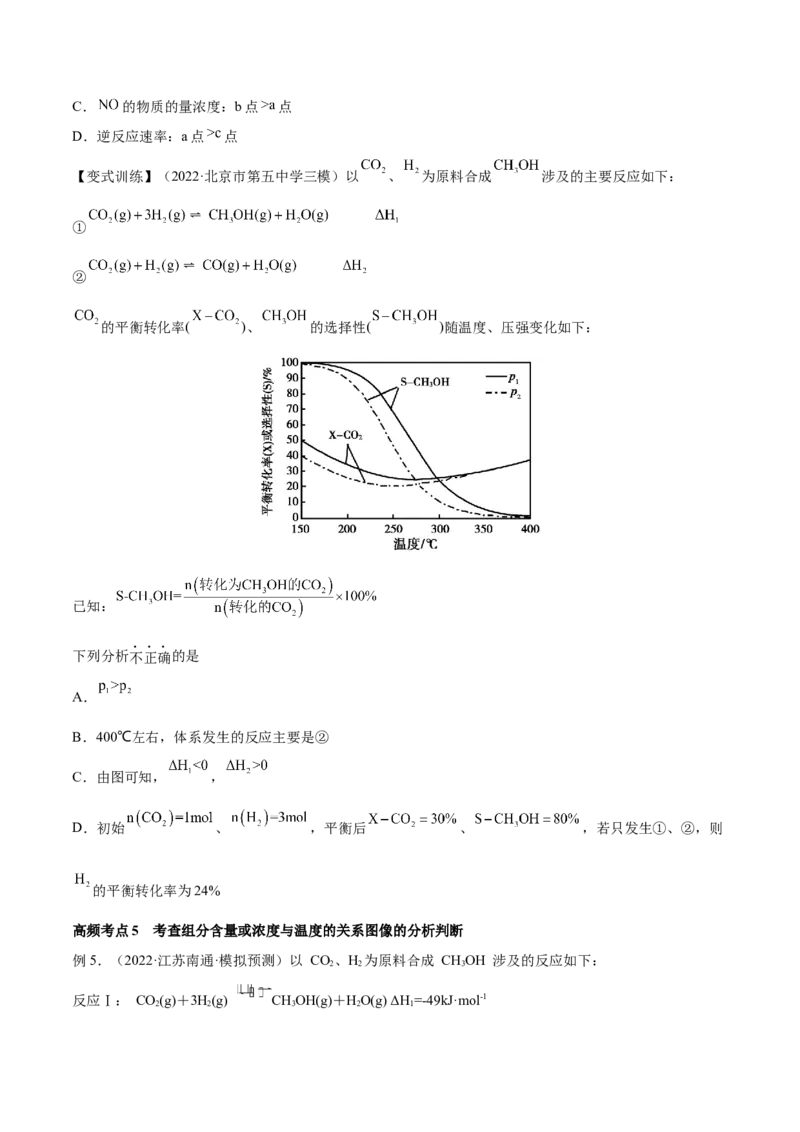
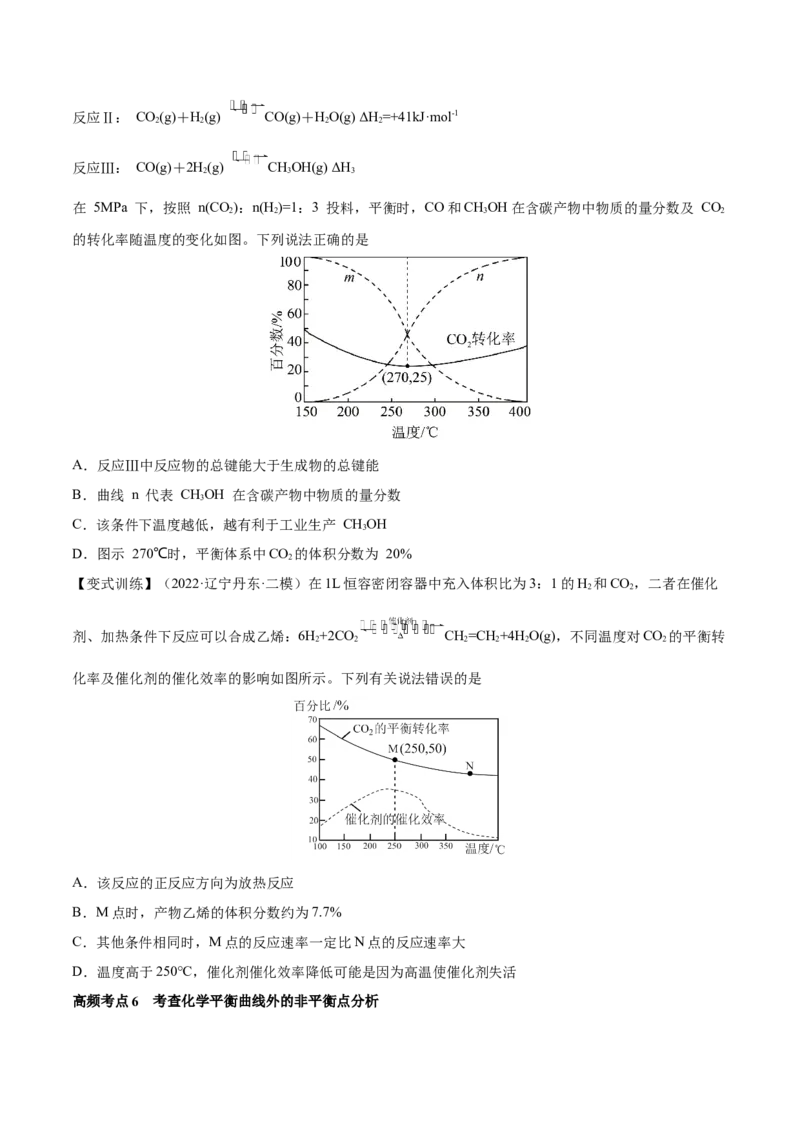
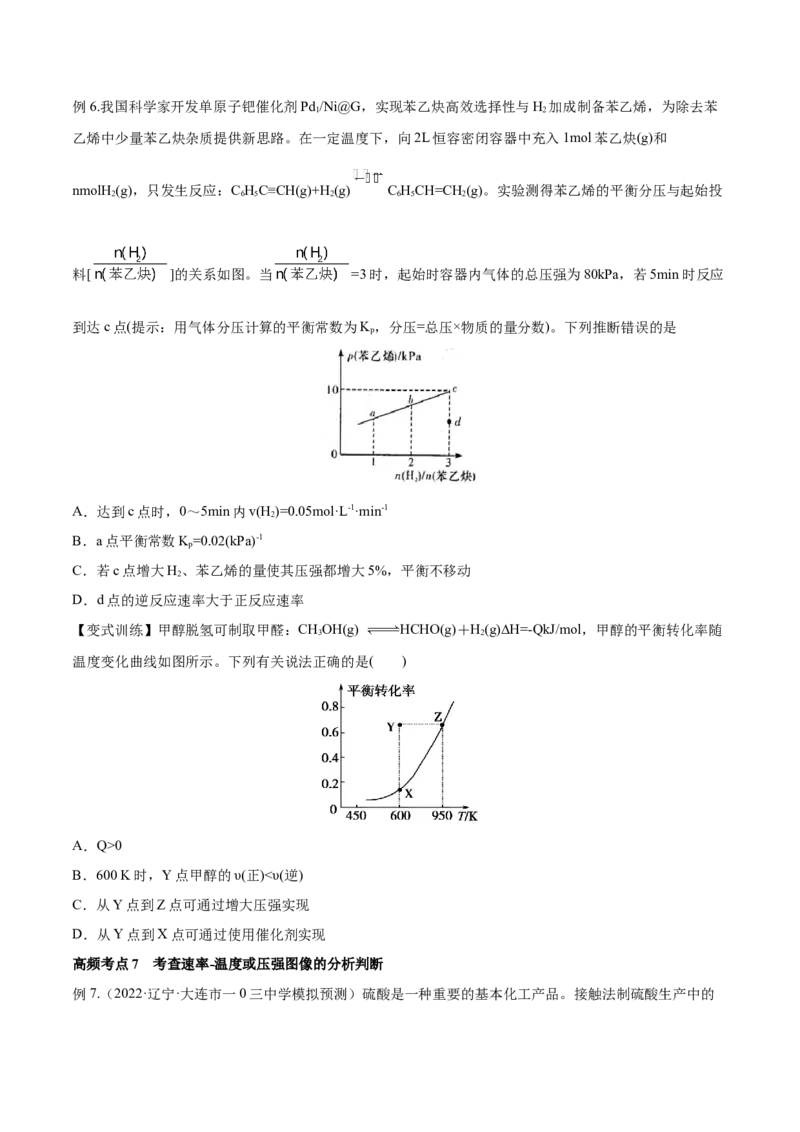
文档内容
专题讲座(七) 常考速率、平衡图像题解题策略
目录
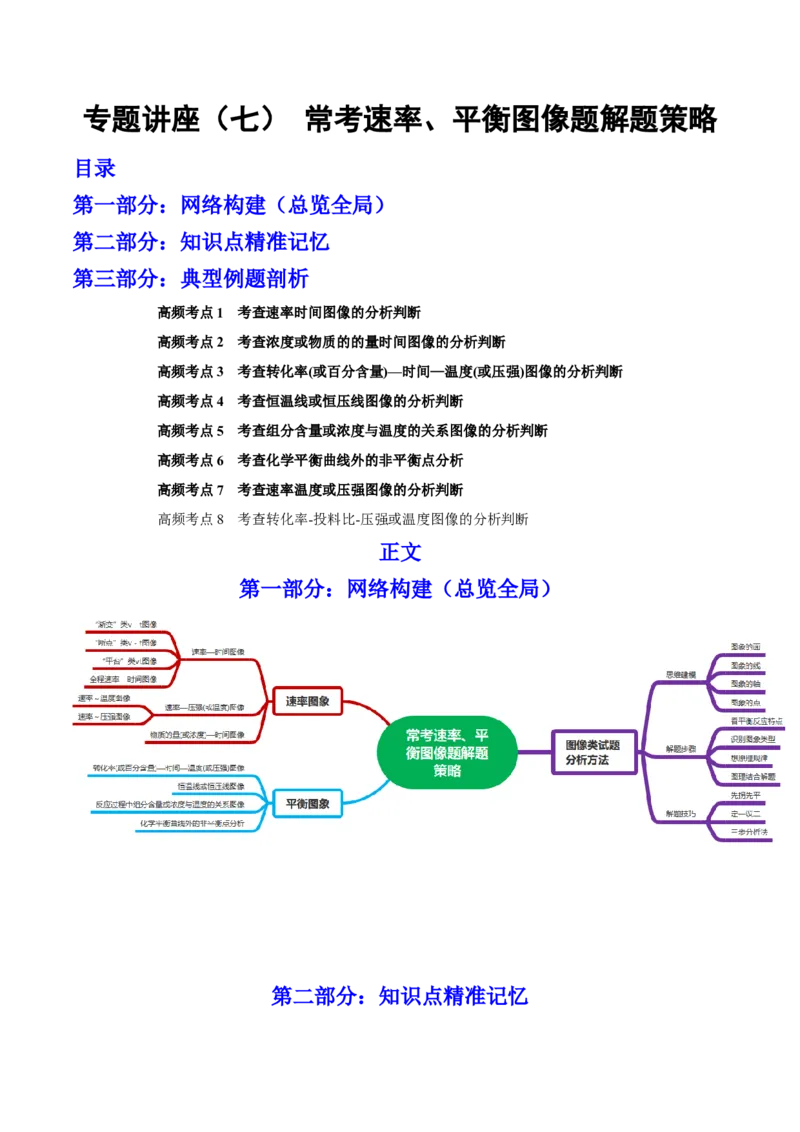
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查速率时间图像的分析判断
高频考点2 考查浓度或物质的的量时间图像的分析判断
高频考点3 考查转化率(或百分含量)—时间—温度(或压强)图像的分析判断
高频考点4 考查恒温线或恒压线图像的分析判断
高频考点5 考查组分含量或浓度与温度的关系图像的分析判断
高频考点6 考查化学平衡曲线外的非平衡点分析
高频考点7 考查速率温度或压强图像的分析判断
高频考点8 考查转化率-投料比-压强或温度图像的分析判断
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆知能点一 速率图像
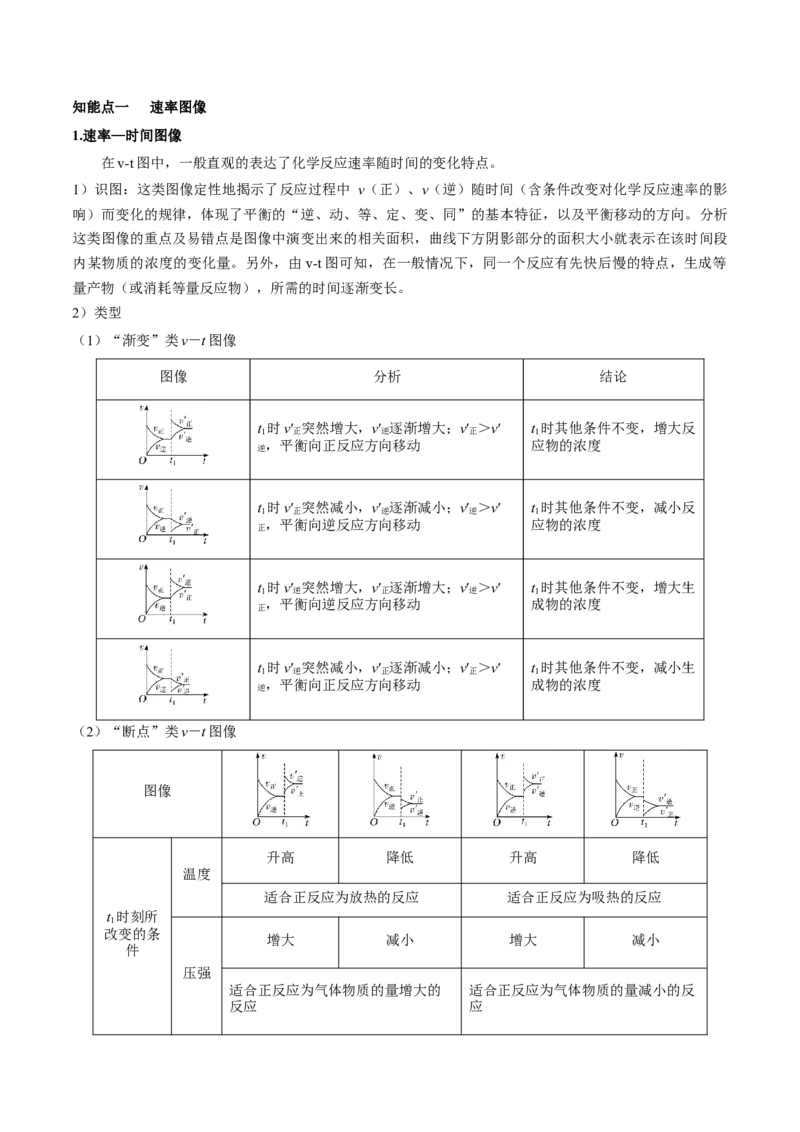
1.速率—时间图像
在v-t图中,一般直观的表达了化学反应速率随时间的变化特点。
1)识图:这类图像定性地揭示了反应过程中 v(正)、v(逆)随时间(含条件改变对化学反应速率的影
响)而变化的规律,体现了平衡的“逆、动、等、定、变、同”的基本特征,以及平衡移动的方向。分析
这类图像的重点及易错点是图像中演变出来的相关面积,曲线下方阴影部分的面积大小就表示在该时间段
内某物质的浓度的变化量。另外,由v-t图可知,在一般情况下,同一个反应有先快后慢的特点,生成等
量产物(或消耗等量反应物),所需的时间逐渐变长。
2)类型
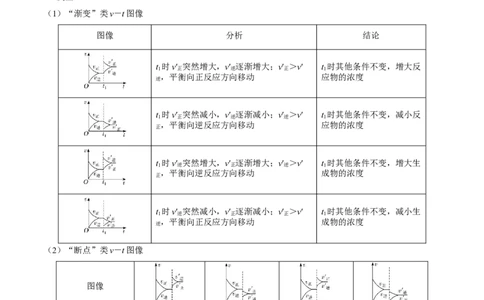
(1)“渐变”类v-t图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大反
1 正 逆 正 1
,平衡向正反应方向移动 应物的浓度
逆
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小反
1 正 逆 逆 1
,平衡向逆反应方向移动 应物的浓度
正
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大生
1 逆 正 逆 1
,平衡向逆反应方向移动 成物的浓度
正
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小生
1 逆 正 正 1
,平衡向正反应方向移动 成物的浓度
逆
(2)“断点”类v-t图像
图像
升高 降低 升高 降低
温度
适合正反应为放热的反应 适合正反应为吸热的反应
t 时刻所
1
改变的条
增大 减小 增大 减小
件
压强
适合正反应为气体物质的量增大的 适合正反应为气体物质的量减小的反
反应 应(3)“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 1 时v′ 正 、v′ 逆 均突然增大且v′ 正 t 时其他条件不变增大反应体
1
=v′
逆
,平衡不移动
系的压强且m+n=p+q(反应前后
气体体积无变化)
t 时其他条件不变,减小反应
t 时v′ 、v′ 均突然减小且v′ 1
1 正 逆 正 体系的压强且m+n=p+q(反应前
=v′ ,平衡不移动
逆 后气体体积无变化)
(4)全程速率—时间图像
例如:Zn与足量盐酸的反应,化学反应速率随时间的变化出现如图所示情况。
原因:(1)AB段(v增大), 反应放热,溶液温度逐渐升高, v 增大 。
(2)BC段(v减小), 溶液中 c (H + ) 逐渐减小, v 减小 。
3)常见v-t图像分析方法
(1)看图像中正、逆反应速率的变化趋势,看二者是同等程度的变化,还是不同程度的变化。同等程度的变化
一般从压强(反应前后气体体积不变的反应)和催化剂角度考虑;若是不同程度的变化,可从温度、浓度、压强
(反应前后气体体积改变的反应)角度考虑。
(2)对于反应速率变化程度不相等的反应,要注意观察改变某个条件瞬间,正、逆反应速率的大小关系及变化
趋势。同时要联系外界条件对反应速率的影响规律,加以筛选、验证、排除。
(3)改变条件判断v(正)、v(逆)的相对大小时,可以从平衡移动方向讨论,若平衡正移,v(正)>v(逆),若平衡逆移,
v(正)T。
2 1
②若为压强变化引起,压强较大时,反应达平衡所需时间短。如图乙中p>p。
1 2
③若为使用催化剂引起,使用适宜催化剂时,反应达平衡所需时间短。如图丙中a使用催化剂。
C.实例:正确掌握图像中反应规律的判断方法
[以mA(g)+nB(g) pC(g)中反应物A的转化率α 为例说明]
A
①图甲中,T>T,升高温度,α 降低,平衡逆向移动,正反应为放热反应。
2 1 A
②图乙中,p>p,增大压强,α 升高,平衡正向移动,则正反应为气体体积缩小的反应。
1 2 A
③若纵坐标表示A的百分含量,则甲中正反应为吸热反应,乙中正反应为气体体积增大的反应。
(2)恒温线或恒压线图像
该类图像的纵坐标为物质的平衡浓度(反应物或生成物)或反应物的转化率,横坐标为温度或压强。
A.识图:(α表示反应物的转化率,c表示反应物的平衡浓度)图①,若p>p>p ,则正反应为气体体积减小的反应,ΔH<0;图②,若T>T ,则正反应为放热反应。解
1 2 3 1 2
答此类图像问题,往往可作分析时可沿横轴作一条平行于纵轴的虚线——恒压线或恒温线,然后进行定一
议二,从而可解决问题。
B.规律:(1)“定一议二”原则:可通过分析相同温度下不同压强时反应物 A的转化率大小来判断平衡移动
的方向,从而确定反应方程式中反应物与产物气体物质间的系数的大小关系。如乙中任取两条压强曲线研
究,压强增大,α 增大,平衡正向移动,正反应为气体体积减小的反应,甲中任取一曲线,也能得出结论。
A
(2)通过分析相同压强下不同温度时反应物A的转化率的大小来判断平衡移动的方向,从而确定反应的热效
应。如利用上述分析方法,在甲中作垂直线,乙中任取一曲线,即能分析出正反应为放热反应。
(3)反应过程中组分含量或浓度与温度的关系图像
对于化学反应mA(g)+nB(g) pC(g)+qD(g),在相同时间段内,M点前,表示化学反应从反应物开
始,则v >v ,未达平衡;M点为刚达到的平衡点。M点后为平衡受温度的影响情况,即升温,A%增大
正 逆
(C%减小),平衡逆向移动,ΔH<0。
(4)化学平衡曲线外的非平衡点分析
对于化学反应mA(g)+nB(g) pC(g)+qD(g),L线上所有的点都是平衡点。
左上方(E点),A%大于此压强或温度时平衡体系中的A%,E点必须向正反应方
向移动才能达到平衡状态,所以,E点v >v ;则右下方(F点)v 0
B.600 K时,Y点甲醇的υ(正)<υ(逆)
C.从Y点到Z点可通过增大压强实现
D.从Y点到X点可通过使用催化剂实现
高频考点7 考查速率-温度或压强图像的分析判断
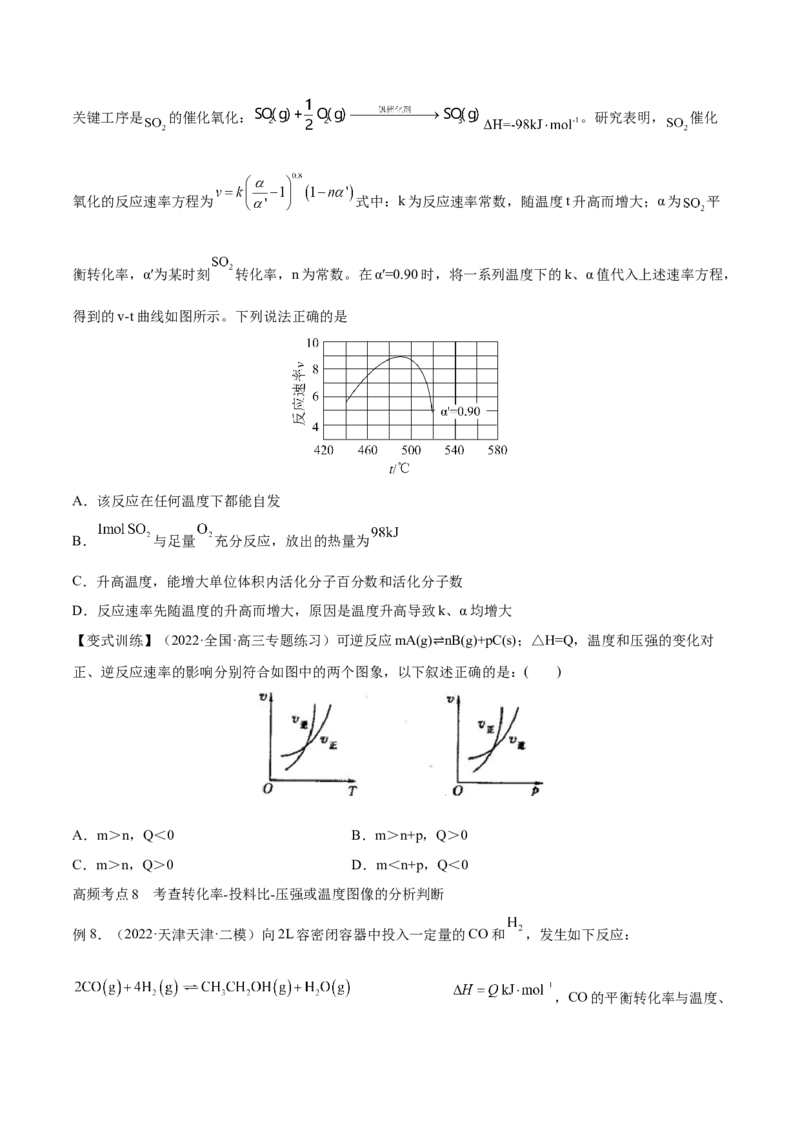
例7.(2022·辽宁·大连市一0三中学模拟预测)硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是 的催化氧化: 。研究表明, 催化
氧化的反应速率方程为 式中:k为反应速率常数,随温度t升高而增大;α为 平
衡转化率,α′为某时刻 转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,
得到的v-t曲线如图所示。下列说法正确的是
A.该反应在任何温度下都能自发
B. 与足量 充分反应,放出的热量为
C.升高温度,能增大单位体积内活化分子百分数和活化分子数
D.反应速率先随温度的升高而增大,原因是温度升高导致k、α均增大
【变式训练】(2022·全国·高三专题练习)可逆反应mA(g) nB(g)+pC(s);△H=Q,温度和压强的变化对
正、逆反应速率的影响分别符合如图中的两个图象,以下叙⇌述正确的是:( )
A.m>n,Q<0 B.m>n+p,Q>0
C.m>n,Q>0 D.m<n+p,Q<0
高频考点8 考查转化率-投料比-压强或温度图像的分析判断
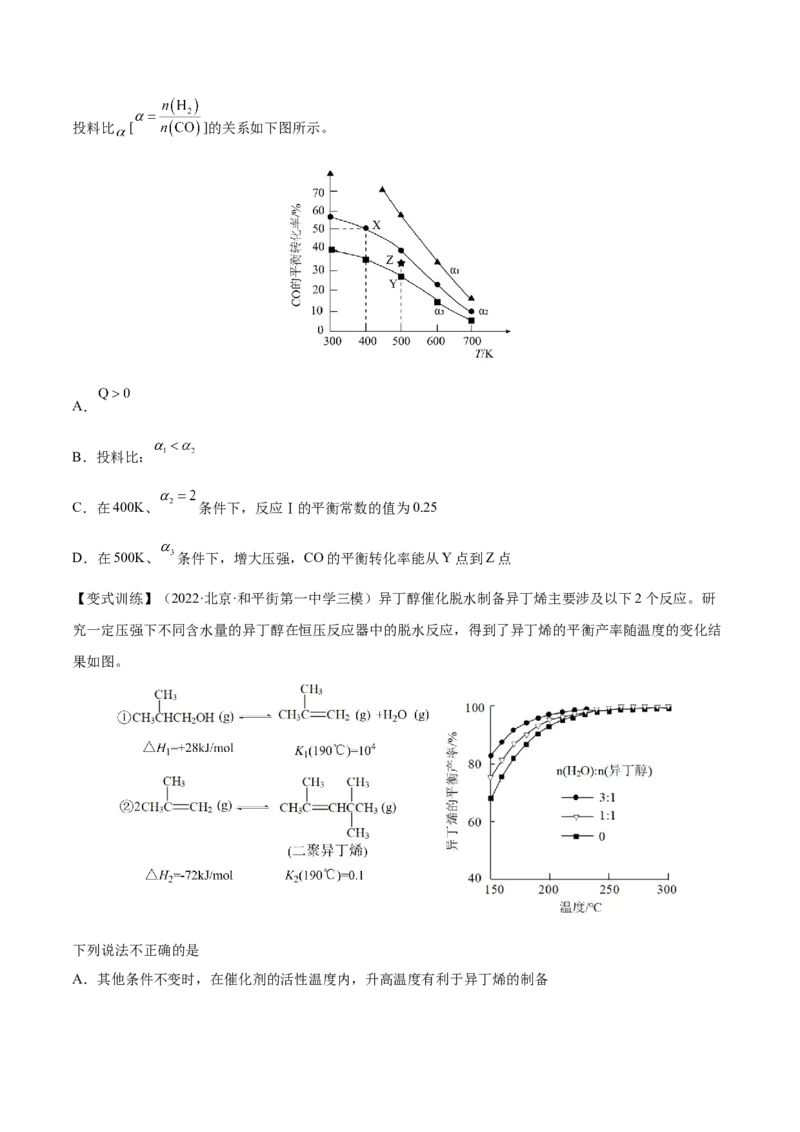
例8.(2022·天津天津·二模)向2L容密闭容器中投入一定量的CO和 ,发生如下反应:
,CO的平衡转化率与温度、投料比 [ ]的关系如下图所示。
A.
B.投料比:
C.在400K、 条件下,反应Ⅰ的平衡常数的值为0.25
D.在500K、 条件下,增大压强,CO的平衡转化率能从Y点到Z点
【变式训练】(2022·北京·和平街第一中学三模)异丁醇催化脱水制备异丁烯主要涉及以下2个反应。研
究一定压强下不同含水量的异丁醇在恒压反应器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结
果如图。
下列说法不正确的是
A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备B.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是 、
C.190℃时,增大 (异丁醇),不利于反应②的进行
D.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度 与流出物质浓度c之间存在: (异丁
醇)=c(异丁烯)+2c(二聚异丁烯)