文档内容
专题讲座(七)晶胞的分析与计算
【化学学科素养】
1.了解晶胞的概念,能根据晶胞确定晶体的组成并进行相关的计算。
【必备知识解读】
一、晶体结构与性质
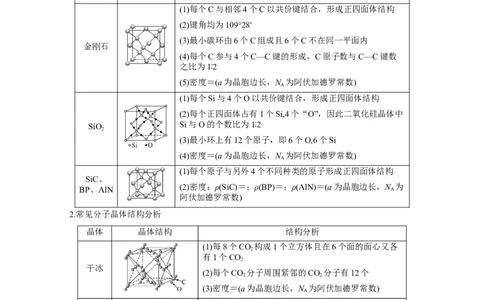
1.常见原子晶体结构分析
晶体 晶体结构 结构分析
(1)每个C与相邻4个C以共价键结合,形成正四面体结构
(2)键角均为109°28′
(3)最小碳环由6个C组成且6个C不在同一平面内
金刚石
(4)每个C参与4个C—C键的形成,C原子数与C—C键数
之比为1∶2
(5)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个Si与4个O以共价键结合,形成正四面体结构
(2)每个正四面体占有1个Si,4个“O”,因此二氧化硅晶体中
SiO
Si与O的个数比为1∶2
2
(3)最小环上有12个原子,即6个O,6个Si
(4)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个原子与另外4个不同种类的原子形成正四面体结构
SiC、
BP、AlN
(2)密度:ρ(SiC)=;ρ(BP)=;ρ(AlN)=(a为晶胞边长,N
A
为
阿伏加德罗常数)
2.常见分子晶体结构分析
晶体 晶体结构 结构分析
(1)每8个CO 构成1个立方体且在6个面的面心又各
2
有1个CO
2
干冰
(2)每个CO 分子周围紧邻的CO 分子有12个
2 2
(3)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)面心立方最密堆积
白磷
(2)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
3.常见金属晶体结构分析
(1)金属晶体的四种堆积模型分析
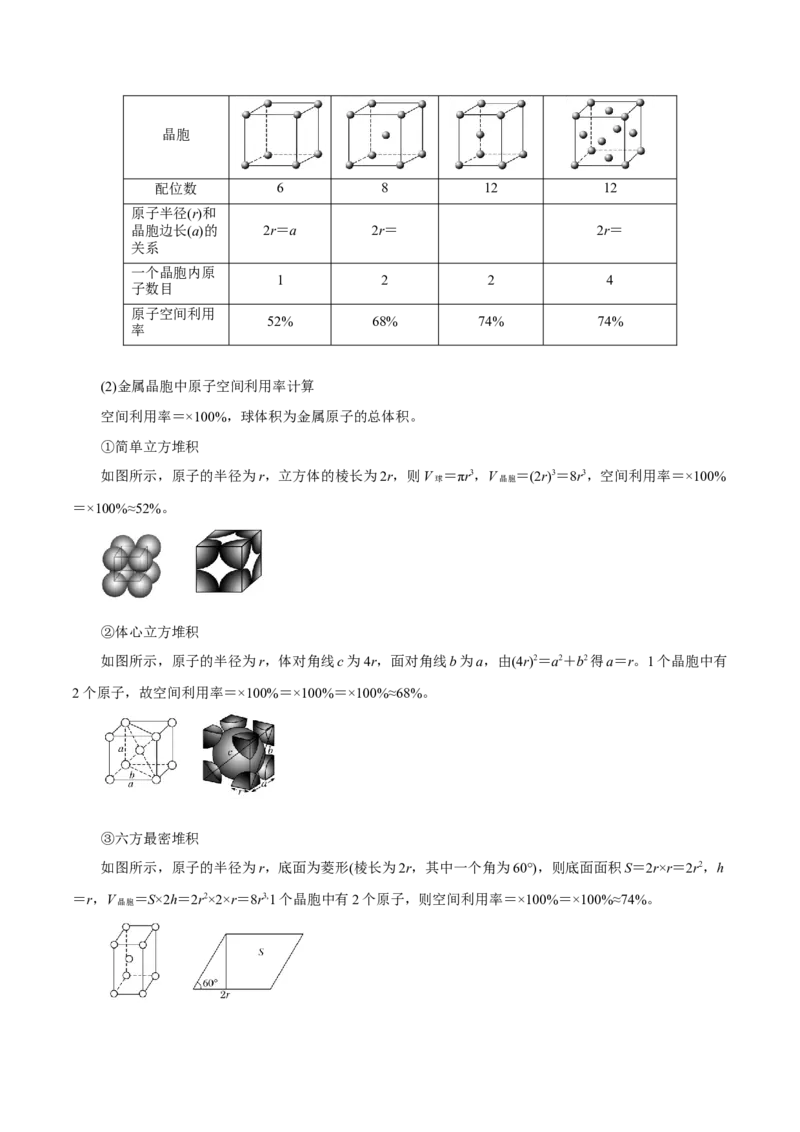
堆积模型 简单立方堆积 体心立方堆积 六方最密堆积 面心立方最密堆积晶胞
配位数 6 8 12 12
原子半径(r)和
晶胞边长(a)的 2r=a 2r= 2r=
关系
一个晶胞内原
1 2 2 4
子数目
原子空间利用
52% 68% 74% 74%
率
(2)金属晶胞中原子空间利用率计算
空间利用率=×100%,球体积为金属原子的总体积。
①简单立方堆积
如图所示,原子的半径为r,立方体的棱长为2r,则V =πr3,V =(2r)3=8r3,空间利用率=×100%
球 晶胞
=×100%≈52%。
②体心立方堆积
如图所示,原子的半径为r,体对角线c为4r,面对角线b为a,由(4r)2=a2+b2得a=r。1个晶胞中有
2个原子,故空间利用率=×100%=×100%=×100%≈68%。
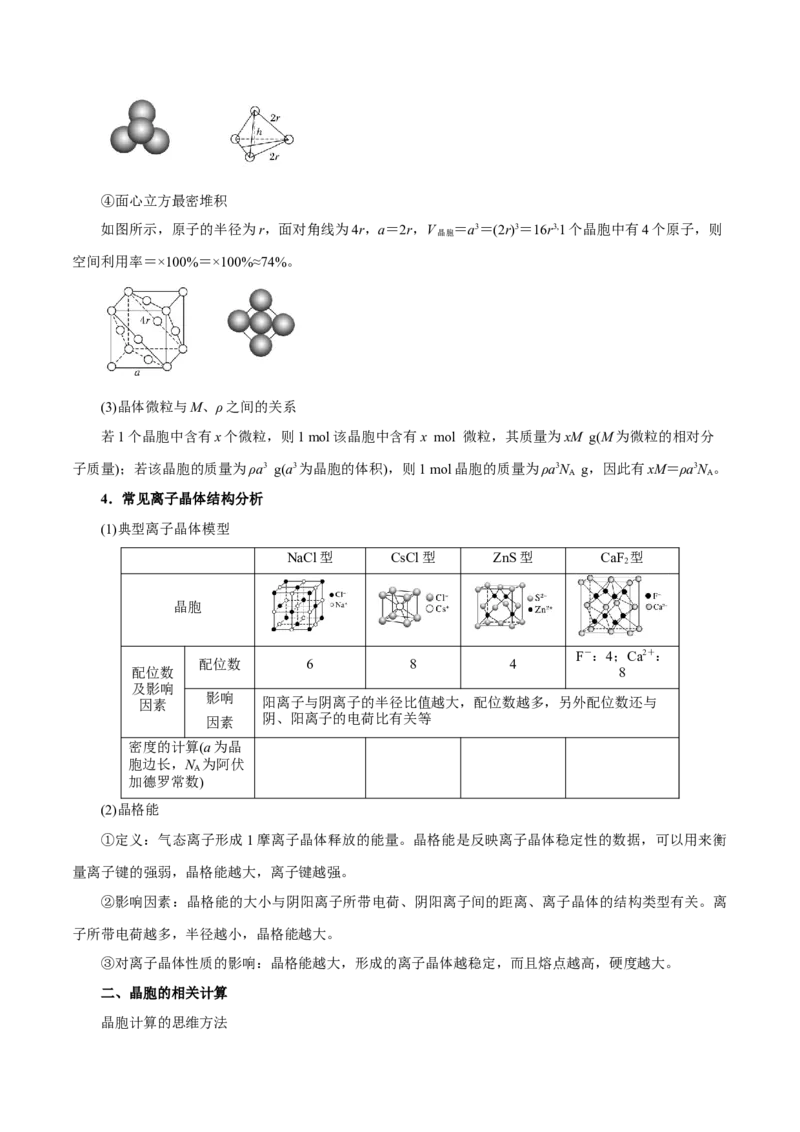
③六方最密堆积
如图所示,原子的半径为r,底面为菱形(棱长为2r,其中一个角为60°),则底面面积S=2r×r=2r2,h
=r,V =S×2h=2r2×2×r=8r3,1个晶胞中有2个原子,则空间利用率=×100%=×100%≈74%。
晶胞④面心立方最密堆积
如图所示,原子的半径为r,面对角线为4r,a=2r,V =a3=(2r)3=16r3,1个晶胞中有4个原子,则
晶胞
空间利用率=×100%=×100%≈74%。
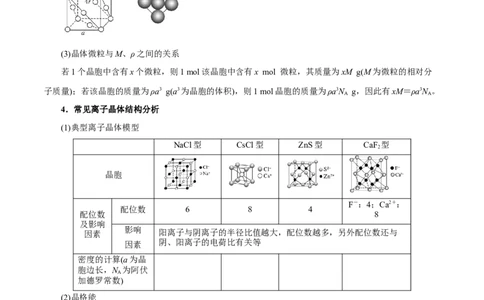
(3)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒的相对分
子质量);若该晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有xM=ρa3N 。
A A
4.常见离子晶体结构分析
(1)典型离子晶体模型
NaCl型 CsCl型 ZnS型 CaF 型
2
晶胞
F-:4;Ca2+:
配位数 6 8 4
配位数 8
及影响
因素 影响 阳离子与阴离子的半径比值越大,配位数越多,另外配位数还与
因素 阴、阳离子的电荷比有关等
密度的计算(a为晶
胞边长,N 为阿伏
A
加德罗常数)
(2)晶格能
①定义:气态离子形成1摩离子晶体释放的能量。晶格能是反映离子晶体稳定性的数据,可以用来衡
量离子键的强弱,晶格能越大,离子键越强。
②影响因素:晶格能的大小与阴阳离子所带电荷、阴阳离子间的距离、离子晶体的结构类型有关。离
子所带电荷越多,半径越小,晶格能越大。
③对离子晶体性质的影响:晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。
二、晶胞的相关计算
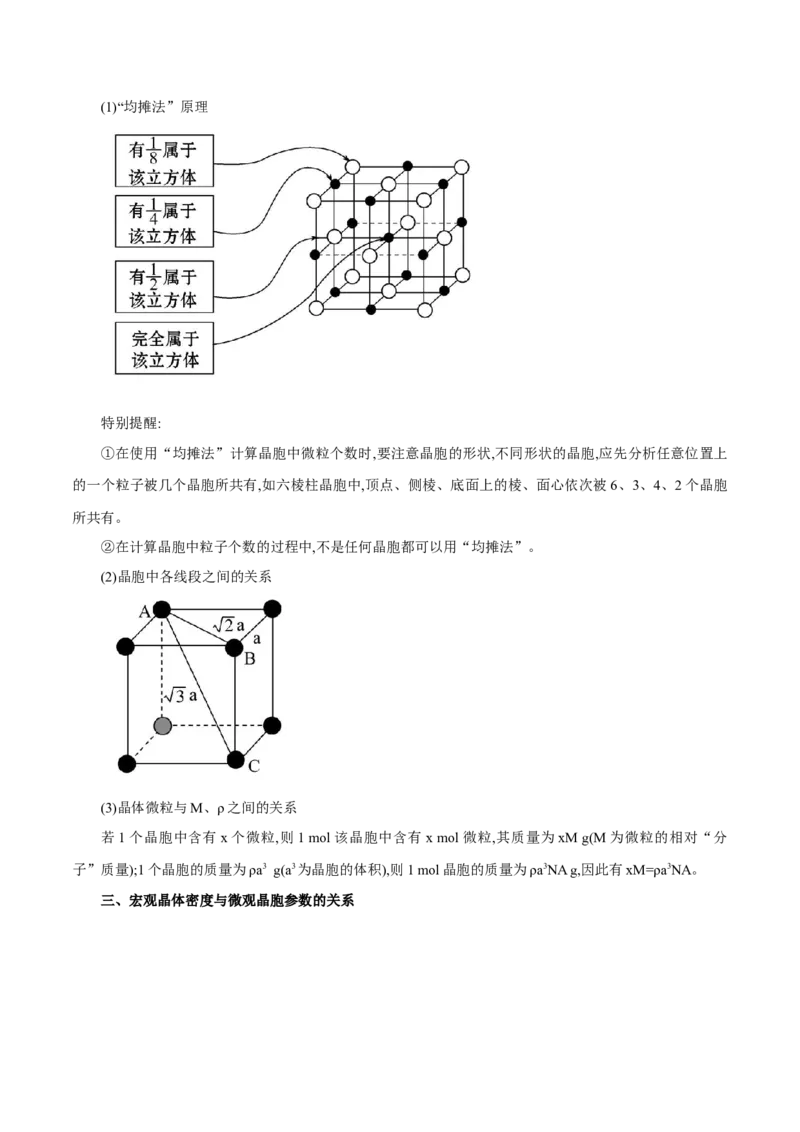
晶胞计算的思维方法(1)“均摊法”原理
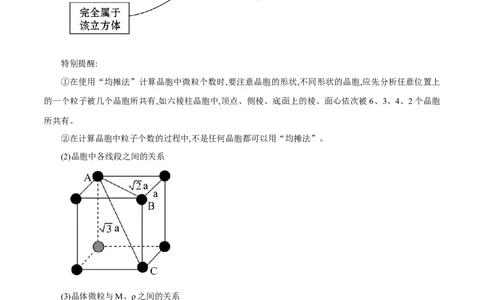
特别提醒:
①在使用“均摊法”计算晶胞中微粒个数时,要注意晶胞的形状,不同形状的晶胞,应先分析任意位置上
的一个粒子被几个晶胞所共有,如六棱柱晶胞中,顶点、侧棱、底面上的棱、面心依次被6、3、4、2个晶胞
所共有。
②在计算晶胞中粒子个数的过程中,不是任何晶胞都可以用“均摊法”。
(2)晶胞中各线段之间的关系
(3)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol该晶胞中含有x mol微粒,其质量为xM g(M为微粒的相对“分
子”质量);1个晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3NA g,因此有xM=ρa3NA。
三、宏观晶体密度与微观晶胞参数的关系【核心题型例解】
高频考点一 晶胞粒子和化学式的计算
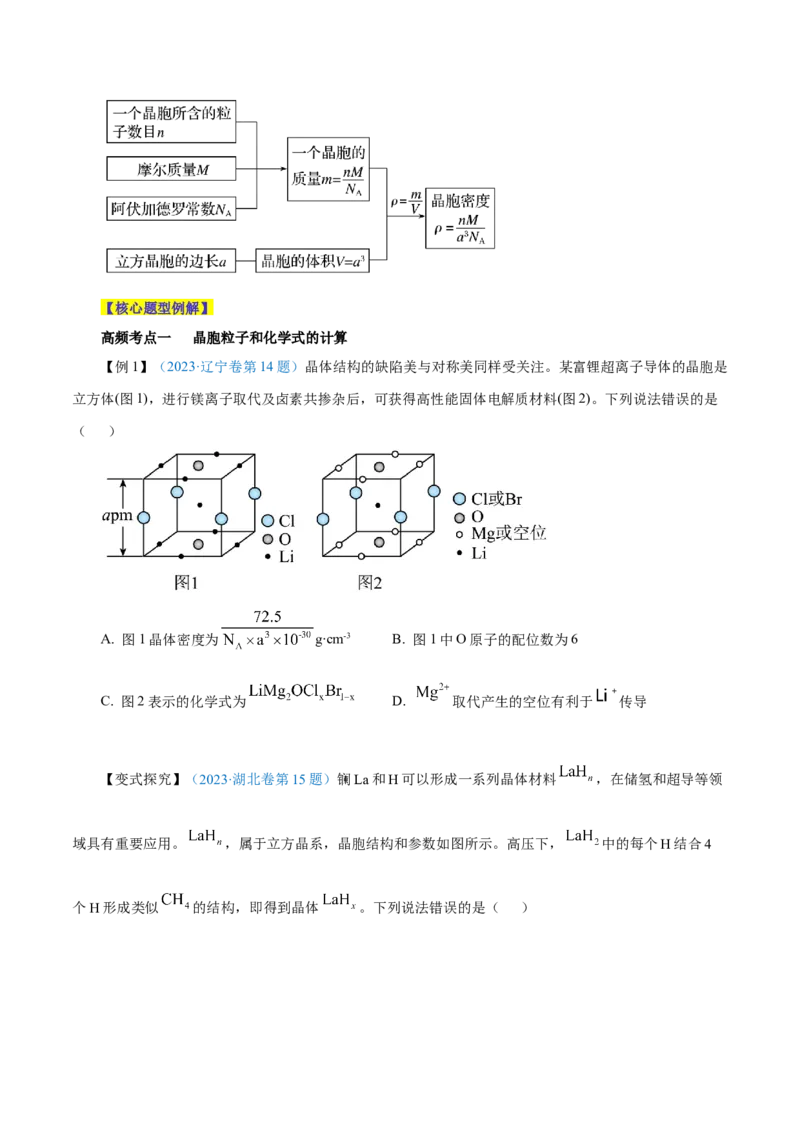
【例1】(2023·辽宁卷第14题)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是
立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
( )
A. 图1晶体密度为 g∙cm-3 B. 图1中O原子的配位数为6
C. 图2表示的化学式为 D. 取代产生的空位有利于 传导
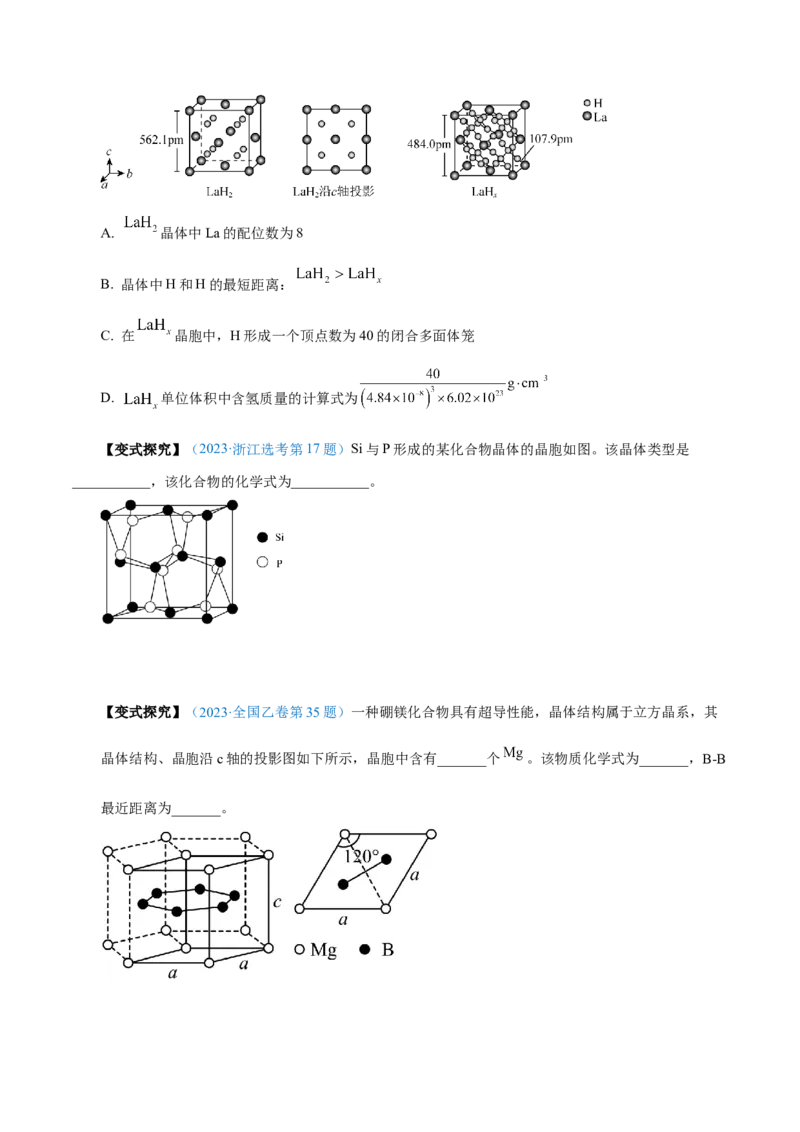
【变式探究】(2023·湖北卷第15题)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领
域具有重要应用。 ,属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4
个H形成类似 的结构,即得到晶体 。下列说法错误的是( )A. 晶体中La的配位数为8
B. 晶体中H和H的最短距离:
C. 在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
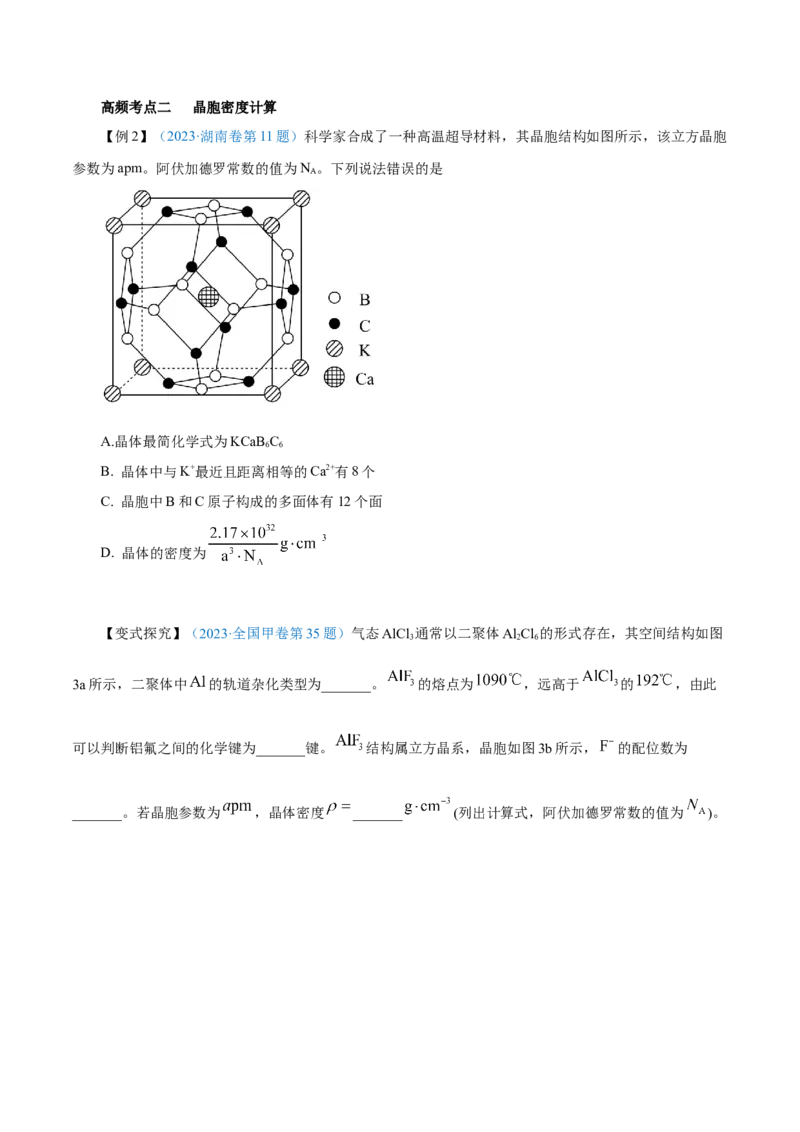
【变式探究】(2023·浙江选考第17题)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是
___________,该化合物的化学式为___________。
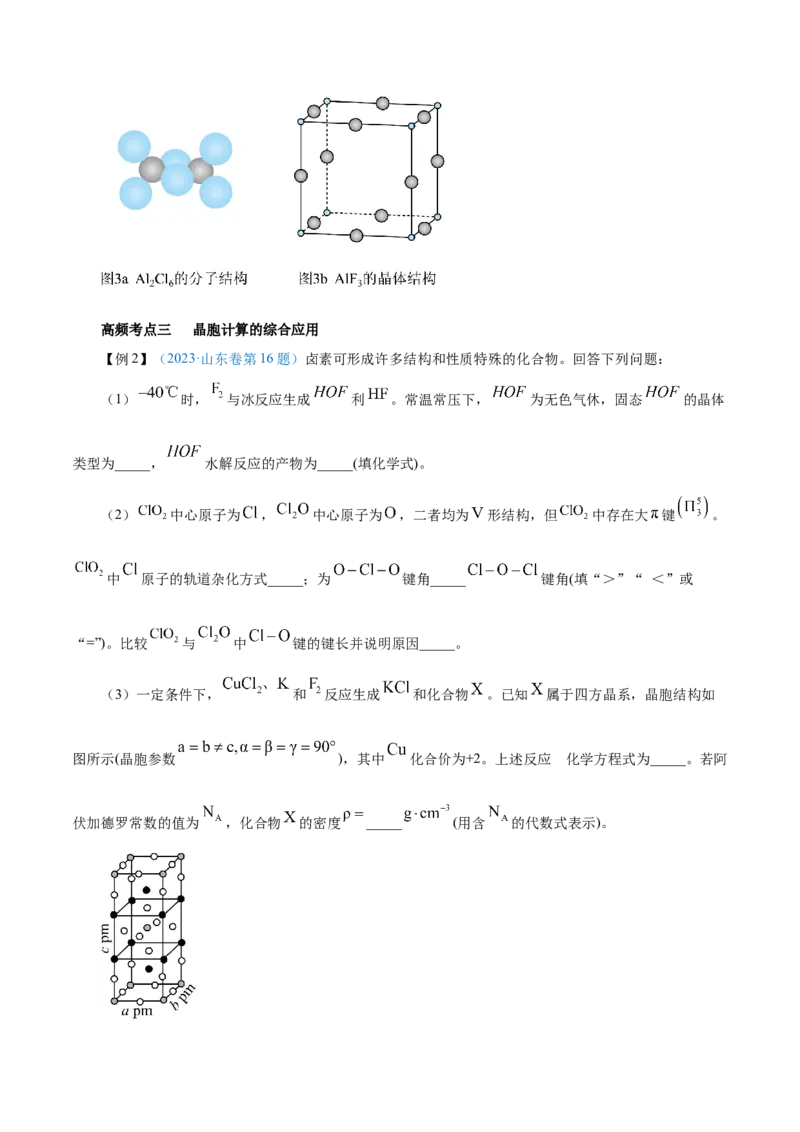
【变式探究】(2023·全国乙卷第35题)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其
晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有_______个 。该物质化学式为_______,B-B
最近距离为_______。高频考点二 晶胞密度计算
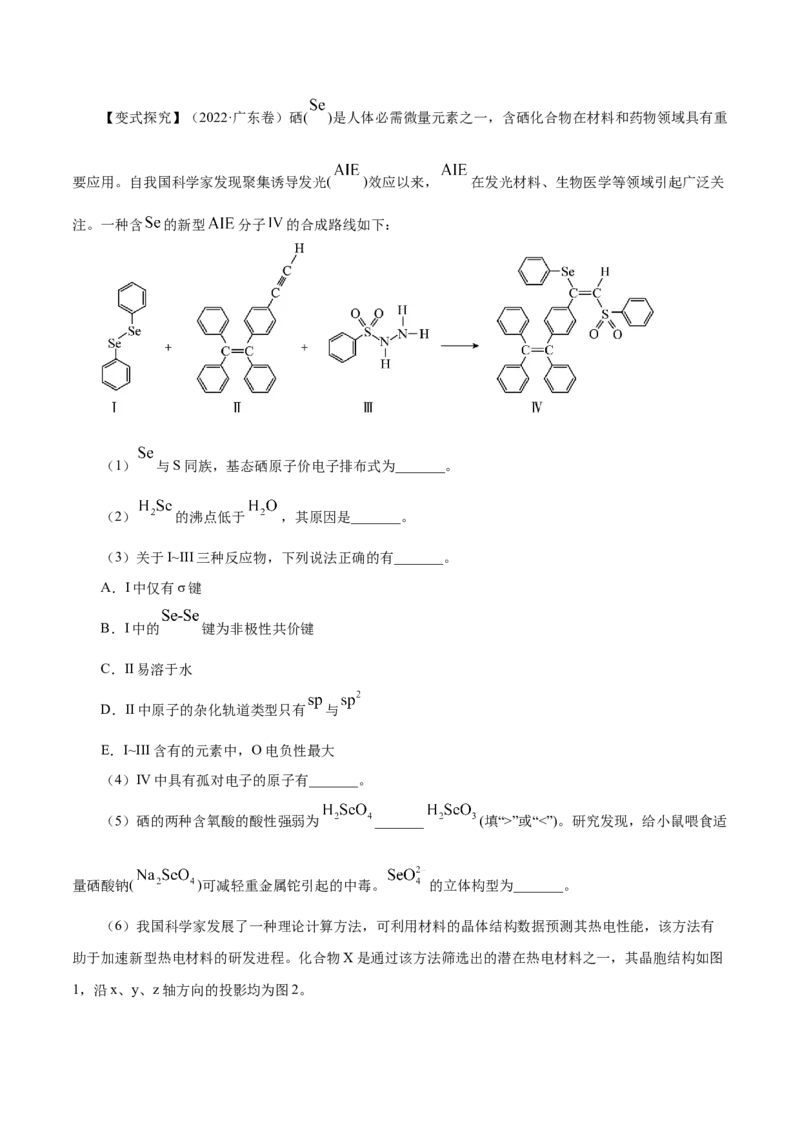
【例2】(2023·湖南卷第11题)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞
参数为apm。阿伏加德罗常数的值为N 。下列说法错误的是
A
A.晶体最简化学式为KCaB C
6 6
B. 晶体中与K+最近且距离相等的Ca2+有8个
C. 晶胞中B和C原子构成的多面体有12个面
D. 晶体的密度为
【变式探究】(2023·全国甲卷第35题)气态AlCl 通常以二聚体Al Cl 的形式存在,其空间结构如图
3 2 6
3a所示,二聚体中 的轨道杂化类型为_______。 的熔点为 ,远高于 的 ,由此
可以判断铝氟之间的化学键为_______键。 结构属立方晶系,晶胞如图3b所示, 的配位数为
_______。若晶胞参数为 ,晶体密度 _______ (列出计算式,阿伏加德罗常数的值为 )。高频考点三 晶胞计算的综合应用
【例2】(2023·山东卷第16题)卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1) 时, 与冰反应生成 利 。常温常压下, 为无色气休,固态 的晶体
类型为_____, 水解反应的产物为_____(填化学式)。
(2) 中心原子为 , 中心原子为 ,二者均为 形结构,但 中存在大 键 。
中 原子的轨道杂化方式_____;为 键角_____ 键角(填“>”“ <”或
“=”)。比较 与 中 键的键长并说明原因_____。
(3)一定条件下, 和 反应生成 和化合物 。已知 属于四方晶系,晶胞结构如
的
图所示(晶胞参数 ),其中 化合价为+2。上述反应 化学方程式为_____。若阿
伏加德罗常数的值为 ,化合物 的密度 _____ (用含 的代数式表示)。【变式探究】(2022·广东卷)硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重
要应用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关
注。一种含 的新型 分子 的合成路线如下:
(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有σ键
B.I中的 键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小鼠喂食适
量硒酸钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有
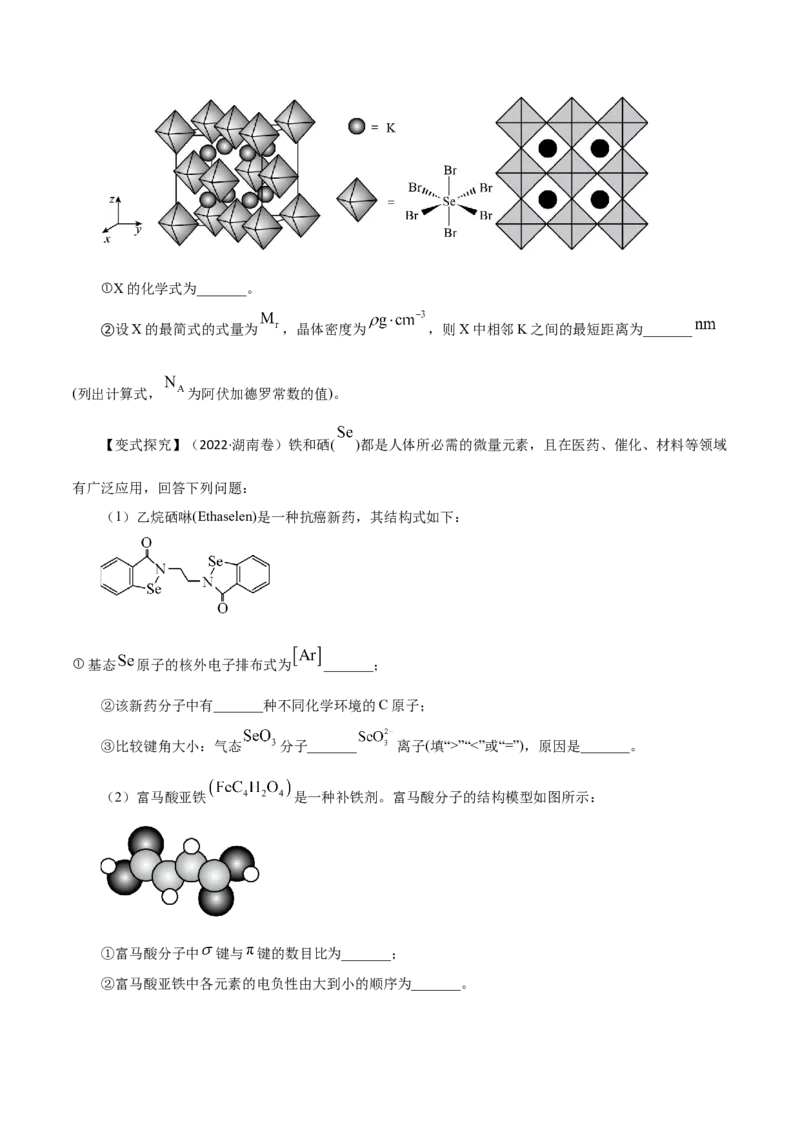
助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图
1,沿x、y、z轴方向的投影均为图2。①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______
(列出计算式, 为阿伏加德罗常数的值)。
【变式探究】(2022·湖南卷)铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域
有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态 原子的核外电子排布式为 _______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态 分子_______ 离子(填“>”“<”或“=”),原因是_______。
(2)富马酸亚铁 是一种补铁剂。富马酸分子的结构模型如图所示:
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将 转化
为
,反应过程如图所示:
①产物中N原子的杂化轨道类型为_______;
②与 互为等电子体的一种分子为_______(填化学式)。
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为 ,则该晶体的密度为_______
(列出计算式)。