文档内容
专题讲座(六) 介质和隔膜在电化学的作用
【考情分析】
在近几年高考中,涉及离子交换膜的应用及电解质溶液介质对电极反应影响的试题比较多,且常出常新,
离子交换膜的功能在于选择性地通过某些离子和阻止某些离子来隔离某些物质,电解质溶液中的电解质可能
与电极反应产物进行反应。通过分析、推理等方法认识原电池及电解池原理,明确电解质溶液中离子的移动
方向,两电极发生的反应,根据离子交换膜的种类确定通过哪些离子,判断交换膜的作用。
【核心素养分析】
1.证据推理与模型认知:建立介质和隔膜的认知模型,并能运用模型解释化学现象,揭示现象的本质和规律。
2.科学态度与社会责任:关注与电化学有关的社会热点问题,具有可持续发展意识和绿色化学观念,提升科学
态度与社会责任的化学核心素养。
【知识梳理】
智能点一 电化学中的隔膜
1.常见的离子交换膜
离子交换膜又叫隔膜,由高分子特殊材料制成。使离子选择性定向迁移(目的是平衡整个溶液的离子浓
度或电荷)。
2.离子交换膜的作用
(1)能将两极区隔离,阻止两极区产生的物质接触,防止副反应的发生,避免影响所制取产品的质量;防止
引发不安全因素。如在电解饱和食盐水中,利用阳离子交换膜,防止阳极产生的氯气进入阴极室与氢氧化钠
反应,导致所制产品不纯;防止氯气与阴极产生的氢气混合发生爆炸。
(2)能选择性的通过离子,起到平衡电荷、形成闭合回路的作用。
(3)用于物质的制备、分离、提纯等。
3.离子交换膜的类型
(1)阳离子交换膜 (只允许阳离子和水分子通过,阻止阴离子和气体通过)
以锌铜原电池为例,中间用阳离子交换膜隔开
①负极反应式:Zn-2e-===Zn2+
②正极反应式:Cu2++2e-===Cu
③Zn2+通过阳离子交换膜进入正极区
④阳离子→透过阳离子交换膜→原电池正极(或电解池的阴极)
(2)阴离子交换膜 (只允许阴离子和水分子通过,阻止阳离子和气体通过)
以Pt为电极电解淀粉KI溶液,中间用阴离子交换膜隔开
①阴极反应式:2HO+2e-===H↑+2OH-
2 2
②阳极反应式:2I--2e-===I
2
③阴极产生的OH-移向阳极与阳极产物反应:3I+6OH-===IO+5I-+3HO
2 2
④阴离子→透过阴离子交换膜→电解池阳极(或原电池的负极)(3)质子交换膜 (只允许H+和水分子通过)
在微生物作用下电解有机废水(含CHCOOH),可获得清洁能源H
3 2
①阴极反应式:2H++2e-===H↑
2
②阳极反应式:CHCOOH-8e-+2HO===2CO↑+8H+
3 2 2
③阳极产生的H+通过质子交换膜移向阴极
④H+→透过质子交换膜→原电池正极(或电解池的阴极)
(4)电渗析法
将含AB 的废水再生为HB和A(OH) 的原
n m n m
理:已知A为金属活动顺序表H之前的金
属,Bn-为含氧酸根离子
4.离子交换膜选择的依据:离子的定向移动。
5.离子交换膜类型的判断(根据电解质溶液呈中性的原则,判断交换膜的类型)
(1)首先写出阴、阳两极上的电极反应,依据电极反应确定该电极附近哪种离子剩余,
(2)根据溶液呈电中性,从而判断出离子移动的方向,进而确定离子交换膜的类型。
如电解饱和食盐水时,阴极反应为2H++2e- H↑,则阴极区域破坏水的电离平衡,OH-有剩余,阳极区域
2
的Na+穿过离子交换膜进入阴极室,与OH-形成NaOH溶液,故电解食盐水时的离子交换膜是阳离子交换膜。
6.“离子交换膜”电解池的解题思路
(1)分清隔膜类型:即交换膜属于阳膜、阴膜或质子膜中的哪一种,判断允许哪种离子通过隔膜;
(2)写出电极反应式:判断交换膜两侧离子变化,推断电荷变化,据电荷平衡判断离子迁移方向;
(3)分析隔膜作用:在产品制备中,隔膜作用主要是提高产品纯度,避免产物之间发生反应,或避免产物
因发生反应而造成危险;
(4)利用定量关系进行计算:外电路电子转移数=通过隔膜的阴、阳离子带的负或正电荷数。
智能点二 隔膜在多室电解池中的应用
多室电解池是利用离子交换膜的选择透过性,即允许带某种电荷的离子通过而限制带相反电荷的离子
通过,将电解池分为两室、三室、多室等,以达到浓缩、净化、提纯及电化学合成的目的。
(1)两室电解池
①制备原理:如工业上利用如图两室电解装置制备烧碱阳极室中电极反应:2Cl--2e-===Cl↑,阴极室中的电极反应:2HO+2e-===H↑+2OH-,阴极区H+放电,
2 2 2
破坏了水的电离平衡,使OH-浓度增大,阳极区Cl-放电,使溶液中的c(Cl-)减小,为保持电荷守恒,阳
极室中的Na+通过阳离子交换膜与阴极室中生成的OH-结合,得到浓的NaOH溶液。利用这种方法制备物质,
纯度较高,基本没有杂质。
②阳离子交换膜的作用:它只允许Na+通过,而阻止阴离子(Cl-)和气体(Cl)通过。这样既防止了两极产
2
生的H 和Cl 混合爆炸,又避免了Cl 和阴极产生的NaOH反应生成NaClO而影响烧碱的质量。
2 2 2
(2)三室电解池
利用三室电解装置制备NHNO,其工作原理如图所示。
4 3
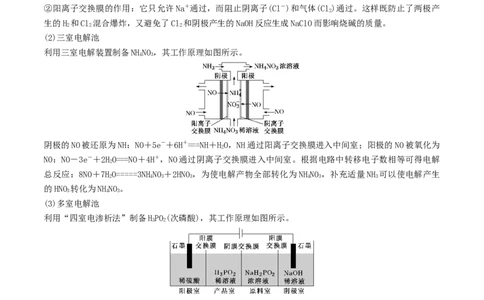
阴极的NO被还原为NH:NO+5e-+6H+===NH+HO,NH通过阳离子交换膜进入中间室;阳极的NO被氧化为
2
NO:NO-3e-+2HO===NO+4H+,NO通过阴离子交换膜进入中间室。根据电路中转移电子数相等可得电解
2
总反应:8NO+7HO=====3NHNO +2HNO ,为使电解产物全部转化为NHNO ,补充适量NH 可以使电解产生
2 4 3 3 4 3 3
的HNO 转化为NHNO。
3 4 3
(3)多室电解池
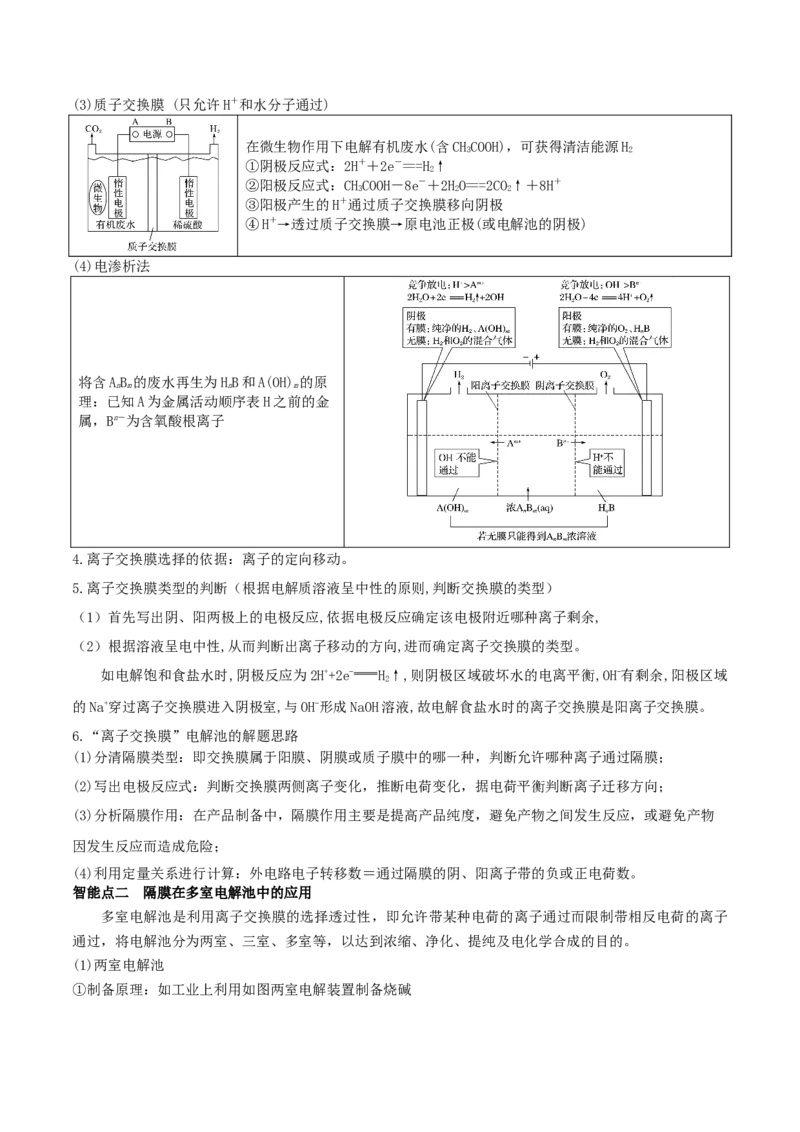
利用“四室电渗析法”制备HPO(次磷酸),其工作原理如图所示。
3 2
电解稀硫酸的阳极反应:2HO-4e-===O↑+4H+,产生的H+通过阳离子交换膜进入产品室,原料室中的
2 2
HPO穿过阴离子交换膜进入产品室,与H+结合生成弱电解质HPO ;电解NaOH稀溶液的阴极反应:4HO+
2 3 2 2
4e-===2H↑+4OH-,原料室中的Na+通过阳离子交换膜进入阴极室。
2
智能点三 电化学中的介质
1.不同介质下电极反应式、总反应式的书写方法
1)燃料电池总反应方程式的书写
因为燃料电池发生电化学反应的最终产物与燃料燃烧的产物相同,可根据燃料燃烧反应写出燃料电池
的总反应方程式,但要注意燃料的种类。若是氢氧燃料电池,其电池总反应方程式不随电解质的状态和电解质溶液的酸碱性变化而变化,即2H+O=2HO。若燃料是含碳元素的可燃物,其电池总反应方程式就与电
2 2 2
解质的状态和电解质溶液的酸碱性有关,如甲烷燃料电池在酸性电解质中生成CO 和HO,即
2 2
CH+2O=CO+2HO;在碱性电解质中生成CO2-离子和HO,即CH+2OH-+2O=CO2-+3HO。
4 2 2 2 3 2 4 2 3 2
2)燃料电池正极反应式的书写
因为燃料电池正极反应物一律是氧气,正极都是氧化剂氧气得到电子的还原反应,所以可先写出正极
反应式,正极反应的本质都是O 得电子生成O2-离子,故正极反应式的基础都是O+4e-=2O-。正极产生O2-
2 2 2
离子的存在形式与燃料电池的电解质的状态和电解质溶液的酸碱性有着密切的关系。这是非常重要的一
步。现将与电解质有关的五种情况归纳如下。
⑴电解质为酸性电解质溶液(如稀硫酸)
在酸性环境中,O2-离子不能单独存在,可供O2-离子结合的微粒有H+离子和HO,O2-离子优先结合H+离
2
子生成HO。这样,在酸性电解质溶液中,正极反应式为O+4H++4e-=2HO。
2 2 2
⑵电解质为中性或碱性电解质溶液(如氯化钠溶液或氢氧化钠溶液)
在中性或碱性环境中,O2-离子也不能单独存在,O2-离子只能结合HO生成OH-离子,故在中性或碱性
2
电解质溶液中,正极反应式为O+2HO +4e-=4OH-。
2 2
⑶电解质为熔融的碳酸盐(如LiCO 和NaCO 熔融盐混和物)
3 2 3
在熔融的碳酸盐环境中,O2-离子也不能单独存在,O2-离子可结合CO 生成CO2-离子,则其正极反应式
2 3
为O+2CO+4e-=2CO2-。
2 2 3
⑷电解质为固体电解质(如固体氧化锆—氧化钇)
该固体电解质在高温下可允许O2-离子在其间通过,故其正极反应式应为O+4e-=2O2-。
2
综上所述,燃料电池正极反应式本质都是O+4e-=2O2-,在不同电解质环境中,其正极反应式的书写形式有
2
所不同。因此在书写正极反应式时,要特别注意所给电解质的状态和电解质溶液的酸碱性。
3)燃料电池负极反应式的书写
燃料电池负极反应物种类比较繁多,可为氢气、水煤气、甲烷、丁烷、甲醇、乙醇等可燃性物质。不
同的可燃物有不同的书写方式,要想先写出负极反应式相当困难。一般燃料电池的负极反应式都是采用间
接方法书写,即按上述要求先正确写出燃料电池的总反应式和正极反应式,然后在电子守恒的基础上用总
反应式减去正极反应式即得负极反应式。
2.电化学中常见的六大介质(以CHOH、O 燃料电池为例)
3 2
(1)中性溶液(如KSO 溶液)。
2 4
总反应:2CHOH+3O 2CO+4HO
3 2 2 2
负极反应:2CHOH-12e-+2HO 2CO↑+12H+
3 2 2
正极反应:3O+12e-+6HO 12OH-
2 2(2)碱性介质(如KOH溶液)。
总反应:2CHOH+3O+4OH- 2C +6HO
3 2 O2− 2
3
负极反应:2CHOH-12e-+16OH- 2C +12HO
3 O2− 2
3
正极反应:3O+12e-+6HO 12OH-
2 2
(3)酸性介质(如HSO 溶液)。
2 4
总反应:2CHOH+3O 2CO+4HO
3 2 2 2
负极反应:2CHOH-12e-+2HO 2CO↑+12H+
3 2 2
正极反应:3O+12e-+12H+ 6HO
2 2
(4)熔融盐介质(如熔融的KCO)。
2 3
总反应:2CHOH+3O 2CO+4HO
3 2 2 2
负极反应:2CHOH-12e-+6C 8CO↑+4HO
3 O2− 2 2
3
正极反应:3O+12e-+6CO 6C
2 2 O2−
3
(5)在高温下能传导正极生成的O2-的介质(如掺杂YO 的ZrO 固体电解质)。
2 3 3
总反应:2CHOH+3O 2CO+4HO
3 2 2 2
负极反应:2CHOH-12e-+6O2- 2CO↑+4HO
3 2 2
正极反应:3O+12e- 6O2-
2
(6)在高温下能传导质子的固体介质
总反应:2CHOH+3O 2CO+4HO
3 2 2 2
负极反应:2CHOH-12e-+2HO 2CO↑+12H+
3 2 2
正极反应:3O+12e-+12H+ 6HO
2 2
【典例剖析】
高频考点1 考查离子交换膜在原电池中的应用
例1.(2021·平阴县第一中学高三月考)一种“全氢电池”的工作原理如图所示。下列说法不正确的是A.电子流向是从吸附层M通过导线到吸附层N
B.Na+从右边穿过离子交换膜向左边移动
C.离子交换膜可用质子交换膜
D.负极的电极反应是:H-2e-+2OH-=2HO
2 2
【解析】A.由工作原理图可知,左边吸附层M为负极,右边吸附层N为正极,则电子流向为从吸附层M通
过导线到吸附层N,故A正确;B.原电池中阳离子移向正极,阴离子移向负极,所以电解质溶液中Na+向
右边移动,故B错误;C.由工作原理图可知,左边溶液为碱性,右边溶液为酸性,所以离子交换膜可阻止
左边的碱性溶液和右边的酸性溶液发生中和,故C错误;D.左边吸附层M为负极极,发生了氧化反应,电
极反应是H-2e-+2OH-=2HO,故D正确;故选:BC。
2 2
【答案】BC
【名师点睛】(1)在原电池中,正极区的阴离子通过阴离子交换膜到负极区;负极区的阳离子通过阳离子
交换膜到正极区;
(2)相同时间内,外电路中通过电子所带电量等于内电路中通过离子交换膜的离子所带电量;
(3)如果为质子交换膜,一般负极反应要生成H+,正极反应要消耗H+。
【变式训练】(2021·湖北师范大学高三月考)我国科学家设计的一种光电催化高效脱硫,并同步制备
HO 的装置如图所示。其中双极膜是由阴离子交换膜和阳离子交换膜组成,两膜之间的催化剂可将水分子
2 2
离解成H+和OH-。下列说法错误的是
A.该装置将电能和太阳能转化为化学能
B.双极膜中的a膜是阳离子交换膜C.阴极区发生的电极反应为O+2e-+2H+=HO
2 2 2
D.0.5 mol SO 参与反应,生成HO 的数目为0.5N
2 2 2 A
【答案】B
【解析】A.该装置有电源,为电解池,装置中还有太阳光,所以是将电能和太阳能转化为化学能的装置,
A正确,不符合题意;B.左边上实现的是二氧化硫变成硫酸根离子,失去电子,电极反应为SO+4OH--2e-=
2
+2HO,为阳极,所以水电离出的氢氧根离子通过阴离子交换膜进入左侧,故a为阴离子交换膜,B
2
错误,不符合题意;C.右边为阴极,是氧气变成过氧化氢,电极反应为O+2e-+2H+=HO,C正确,不符合
2 2 2
题意;D.0.5 mol SO 参与反应,转移1mol电子,对应生成HO 的数目为0.5N,D正确,不符合题意;故
2 2 2 A
选B。
高频考点2 考查离子交换膜在电解池中的应用
例2.(2021·湖南高三)双极膜(BP)是阴、阳复合膜,在直流电作用下,阴、阳膜复合层间的HO解离成
2
H+和OH-。利用双极膜电渗析法和惰性电极电解食盐水可获得淡水、NaOH溶液和盐酸,其工作原理如下图
所示,M、N为离子交换膜。下列说法错误的是
A.M膜为阴离子交换膜
B.出口2的产物是盐酸
C.若去掉双极膜(BP),阳极室会有Cl 生成
2
D.电路中每转移1 mol电子,两极共得到0.5 mol气体
【解析】由题给示意图可知,该装置为电解池,左侧与电源负极相连的电极为电解池的阴极,BP双极膜解
离出的氢离子在阴极上得到电子发生还原反应生成氢气,解离出的氢氧根离子进入1室,使1室中溶液电
荷不守恒,促使盐室中的钠离子从阳离子交换膜进入1室,则M膜为阳离子交换膜,出口1的产物为氢氧
化钠溶液;右侧与电源正极相连的电极为阳极,BP双极膜解离出的氢氧根离子在阳极上失去电子发生氧化
反应生成氧气,解离出的氢离子进入2室,使2室中溶液电荷不守恒,促使盐室中的氯离子从阳离子交换
膜进入2室,则N膜为阴离子交换膜,出口2的产物为盐酸。A.由分析可知,M膜为阳离子交换膜,故A
错误;B.由分析可知,出口2的产物为盐酸,故B正确;C.若去掉双极膜,浓氯化钠溶液中的氯离子会在阳极上失去电子发生氧化反应生成氯气,则阳极室会有氯气生成,故C正确;D.由分析可知,氢离子在
阴极上得到电子发生还原反应生成氢气,氢氧根离子在阳极上失去电子发生氧化反应生成氧气,若电路中
每转移1 mol电子,由得失电子数目守恒可得两极共得到气体的物质的量为1 mol× +1 mol×
=0.75mol,故D错误;故选AD。
【答案】AD
【名师点睛】(1)在电解池中,各池中的阳离子向阴极移动,阴离子向阳极移动.
(2)各池中的阳离子只能透过阳膜向阴极移动而不能向阳极移动;各池中的阴离子只能透过阴膜向阳极移
动而不能向阴极移动.
(3)若某室中同时有阴、阳离子进入,二者结合的产物即为该室产品;若某室中同时有阴、阳离子移出(或
消耗),则二者结合的产物即为该室消耗的物质; 若某室中既有离子进入,又有离子移出(或消耗),进入
离子与原溶液中未移出(或消耗)的离子结合的产物即为该室产品.
(4)在同一电解池或串联的各个电解池中,相同时间内,通过各离子交换膜的离子所带电量与通过外电路
的电子所带电量相等.
(5)在电解池中,阳离子移向的方向为阴极,通过的交换膜为阳膜;阴离子移向的方向为阳极,通过的交
换膜为阴膜.
(6)若离子交换膜为单质子交换膜,一般阳极反应要生成H+,阴极反应要消耗H+.
【变式训练】(化学-学科网2021年高三3月大联考(新课标Ⅱ卷))利用双极膜制备磷酸和氢氧化钠
的原理如图所示。已知双极膜是一种复合膜,在直流电作用下,双极膜中间界面内水解离为H+和OH−,并
实现其定向通过。下列说法正确的是
A.若用铅蓄电池为电源,则X极与Pb电极相连
B.双极膜中a为H+,b为OH–
C.阴极区溶液pH减小
D.M膜为阴离子交换膜,N膜为阳离子交换膜
【解析】A.铅蓄电池中Pb为负极,PbO 电极为正极,X极应与PbO 相连,A项错误;B.电解池中阴离子
2 2
向阳极迁移,阳离子向阴极迁移,所以双极膜中a为OH−,b为H+,B项错误;C.阴极电极反应为2H+
+2e−=H↑,每转移1 mol电子,消耗1 mol H+,此时双极膜又产生1 mol H+,因阴极区电解液未知,无法
2确定阴极区溶液pH变化情况,C项错误;D.M膜为阴离子交换膜,原料室中 通过M膜进入产品室
1,与双极膜产生的H+结合生成HPO,N膜为阳离子交换膜,原料室中Na+通过N膜进入产品室2,与双极
3 4
膜产生的OH−结合生成NaOH,D项正确。故选D。
【答案】D
高频考点3 考查介质在燃烧电池中的应用
例3.目前,我们日常生活中使用的电能主要还是来自火力发电,火力发电是利用化石燃料燃烧,通过蒸
汽机将产生的能量转化为电能,能量利用率低;燃料电池可以将燃料的化学能直接转化为电能,能量利用
率高。
(1)火力发电厂利用燃煤发电,其能量转化形式为化学能→_______→_______→电能。
(2)磷酸盐燃料电池(PAFC)是当前商业化发展最快的一种燃料电池,以浓磷酸为电解质,以贵金属催化的
气体扩散电极为正、负电极。其优点为构造简单,稳定,电解质挥发度低。磷酸盐燃料电池正极的电极反
应式为_______。
(3)碱性燃料电池(AFC)是最早进入实用阶段的燃料电池之一,也是最早用于车辆的燃料电池,以KOH、
NaOH溶液之类的强碱性溶液为电解质溶液。其优点为性能可靠,具有较高的效率。甲烷碱性燃料电池正极
的电极反应式为_______。
(4)固体氧化物型燃料电池(SOFC),其效率更高,可用于航空航天。如图1所示的装置中,以稀土金属材料
作惰性电极,在电极上分别通入甲烷和空气,其中固体电解质是掺杂了YO 和ZrO 的固体,它在高温下能
2 3 2
穿到O2-;A通入的气体为_______,d电极上的电极反应式为_______。
(5)熔融碳酸盐燃料电池是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔陶瓷阳极、金属极板构成的,电
解质通常为锂和钾的混合碳酸盐,工作温度为650 ℃,其工作原理如图2所示,M为电池的_______(填
“正极”或“负极”),N极的电极反应式为_______。
【解析】(1) 火力发电的原理是发电时,利用燃料加热水产生蒸汽,利用蒸汽推动汽轮机,然后由汽轮机
带动发电机发电,其能量转化关系为化学能→热能→机械能→电能,故填热能、机械能;(2)根据题意,参与磷酸盐燃料电池正极的为空气中的氧气,氧气在正极得电子被还原,其在酸性环境下
的电极反应为 ,故填 ;
(3)甲烷碱性燃料电池的正极为O 参与,氧气在正极得电子被还原,其电极反应式为
2
,故填 ;
(4)原电池中,电子的移动方向为:经外电路有负极流向正极,电流流向与电子流向相反,图中电流由c经
外电路流向d,故c为正极,d为负极,所以A为氧气,B为甲烷,电解质为固体电解质是掺杂了YO 和
2 3
ZrO 的固体,在高温下能穿到O2-,则负极电极反应式为 ,故填O、
2 2
;
(5)根据图示,N极通入的是氧气,其化合价只能降低作正极,则M极为负极,电解质为熔融碳酸盐,则正
极的电极反应式为 ,故填负极、 。
【答案】(1)热能 机械能
(2)
(3)
(4)O
2
(5)负极
【名师点睛】书写燃料电池电极反应式一般分为三步:第一步,根据介质性质先写出燃料电池的总反应方
程式;第二步,根据介质性质再写出燃料电池的正极反应式;第三步,在电子守恒的基础上用燃料电池的
总反应式减去正极反应式即得到负极反应式。
【变式训练】如图为原电池的装置示意图。(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成原电池,这两个原电
池中,作负极的分别是_______(填字母)。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____。
(2)若A、B均为铂片,电解质溶液为NaOH溶液,分别从A、B两极通入H 和O,该电池即为氢氧燃料电池,
2 2
写出A电极反应式:____。该电池在工作一段时间后,溶液的碱性将____(填“增强”、“减弱”或“不
变”)
(3)若A、B均为铂片,电解质溶液为HSO 溶液,分别从A、B两极通入CH 和O,该电池即为甲烷燃料电池,
2 4 4 2
写出A电极反应式:___。若该电池反应消耗了6.4gCH,则转移电子的数目为____。
4
【解析】(1)铝片和铜片用导线相连,插入浓硝酸中,金属铝钝化,Cu作负极、Al作正极;铝片和铜片用
导线相连,插入烧碱溶液中,铝和氢氧化钠溶液反应,Al作负极、Cu为正极,Al元素失去电子在碱性溶
液中以AlO 存在,故电极反应为Al-3e-+4OH-=AlO +2HO,故答案为:B;Al-3e-+4OH-=AlO +2HO;
2 2
(2)若A、B均为铂片,电解质为NaOH溶液,分别从A、B两极通入H 和O,该电池即为氢氧燃料电池,A
2 2
为负极,负极电极反应式为H+2OH--2e-=2HO;该电池在工作一段时间后,NaOH溶液的浓度减小,溶液的
2 2
碱性将减弱,故答案为:H+2OH--2e-=2HO;减弱;
2 2
(3)若A、B均为铂片,电解质溶液为HSO 溶液,分别从A、B两极通入CH 和O,该电池即为甲烷燃料电池,
2 4 4 2
A电极为负极,负极反应式为CH-8e-+2HO=CO+8H+;若该电池反应消耗了6.4gCH,甲烷的物质的量是
4 2 2
6.4g÷16g/mol=0.4mol,则转移电子的数目为0.4×8×N=3.2N,故答案为:CH-8e-+2HO=CO+8H+;
A A 4 2 2
3.2N。
A
【答案】(1)B Al-3e-+4OH-=AlO +2HO
2
(2)H+2OH--2e-=2HO 减弱
2 2
(3)CH-8e-+2HO=CO+8H+ 3.2N
4 2 2 A