文档内容
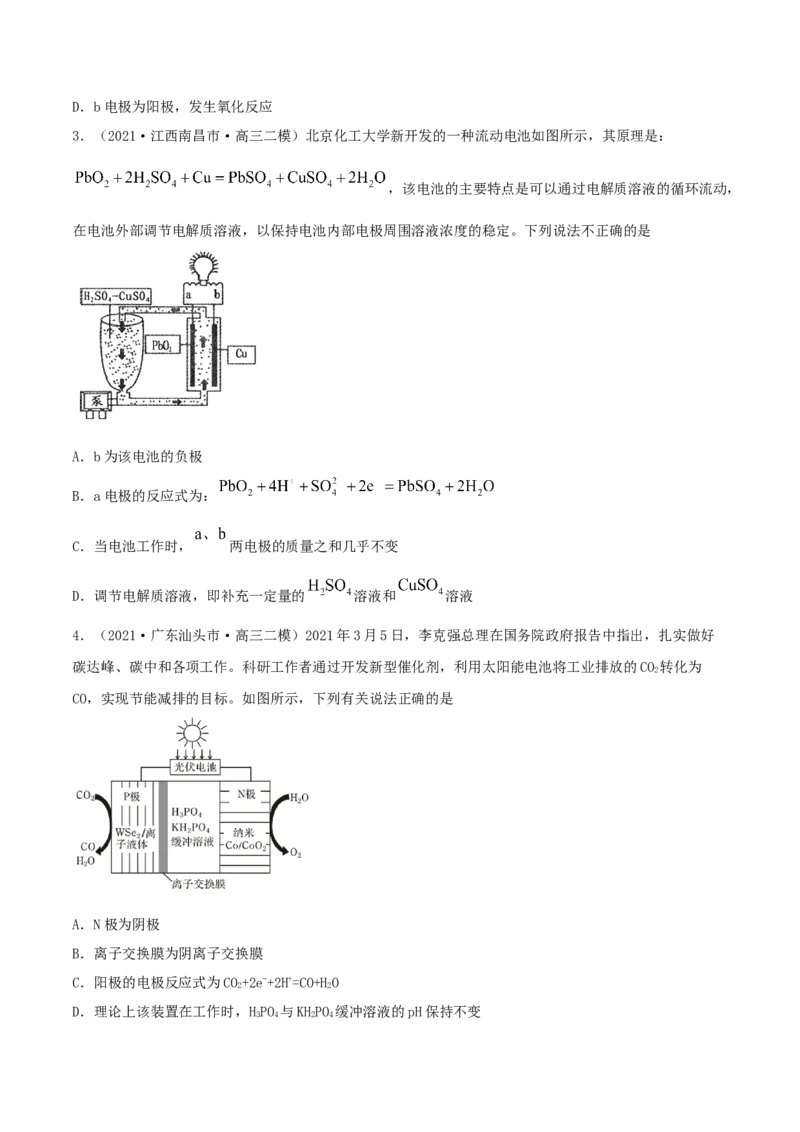
第六章 化学反应与能量
第19讲 电解池 金属的电化学腐蚀与防护(精练)
完卷时间:50分钟
可能用到的相对原子质量:H1 N14 O16 Na23 S32 Cl35.5 K39 Cu64
一、选择题(每小题只有一个正确选项,共12*5分)
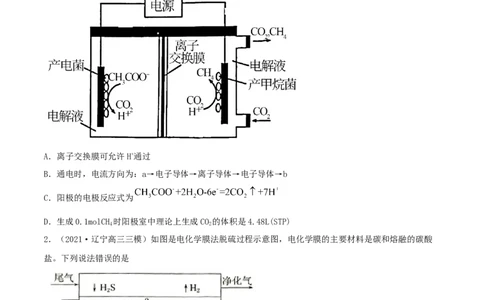
1.(2021·山东潍坊市·高三三模)将电化学法和生物还原法有机结合,利用微生物电化学方法生产甲
烷,装置如图所示。下列说法错误的是
A.离子交换膜可允许H+通过
B.通电时,电流方向为:a→电子导体→离子导体→电子导体→b
C.阳极的电极反应式为
D.生成0.1molCH 时阳极室中理论上生成CO 的体积是4.48L(STP)
4 2
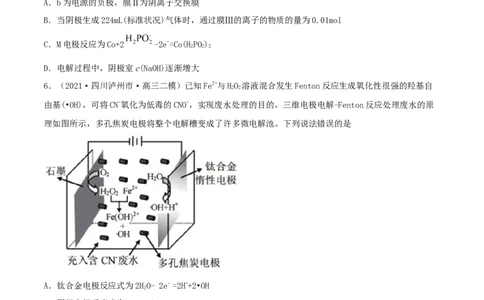
2.(2021·辽宁高三三模)如图是电化学膜法脱硫过程示意图,电化学膜的主要材料是碳和熔融的碳酸
盐。下列说法错误的是
A.工作一段时间后,生成H 和S 的物质的量之比为2:1
2 2
B.净化气中CO 含量明显增加,是电化学膜中的碳被氧化
2
C.阴极反应式为HS+2e-=S2-+H↑
2 2D.b电极为阳极,发生氧化反应
3.(2021·江西南昌市·高三二模)北京化工大学新开发的一种流动电池如图所示,其原理是:
,该电池的主要特点是可以通过电解质溶液的循环流动,
在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。下列说法不正确的是
A.b为该电池的负极
B.a电极的反应式为:
C.当电池工作时, 两电极的质量之和几乎不变
D.调节电解质溶液,即补充一定量的 溶液和 溶液
4.(2021·广东汕头市·高三二模)2021年3月5日,李克强总理在国务院政府报告中指出,扎实做好
碳达峰、碳中和各项工作。科研工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为
2
CO,实现节能减排的目标。如图所示,下列有关说法正确的是
A.N极为阴极
B.离子交换膜为阴离子交换膜
C.阳极的电极反应式为CO+2e-+2H+=CO+HO
2 2
D.理论上该装置在工作时,HPO 与KHPO 缓冲溶液的pH保持不变
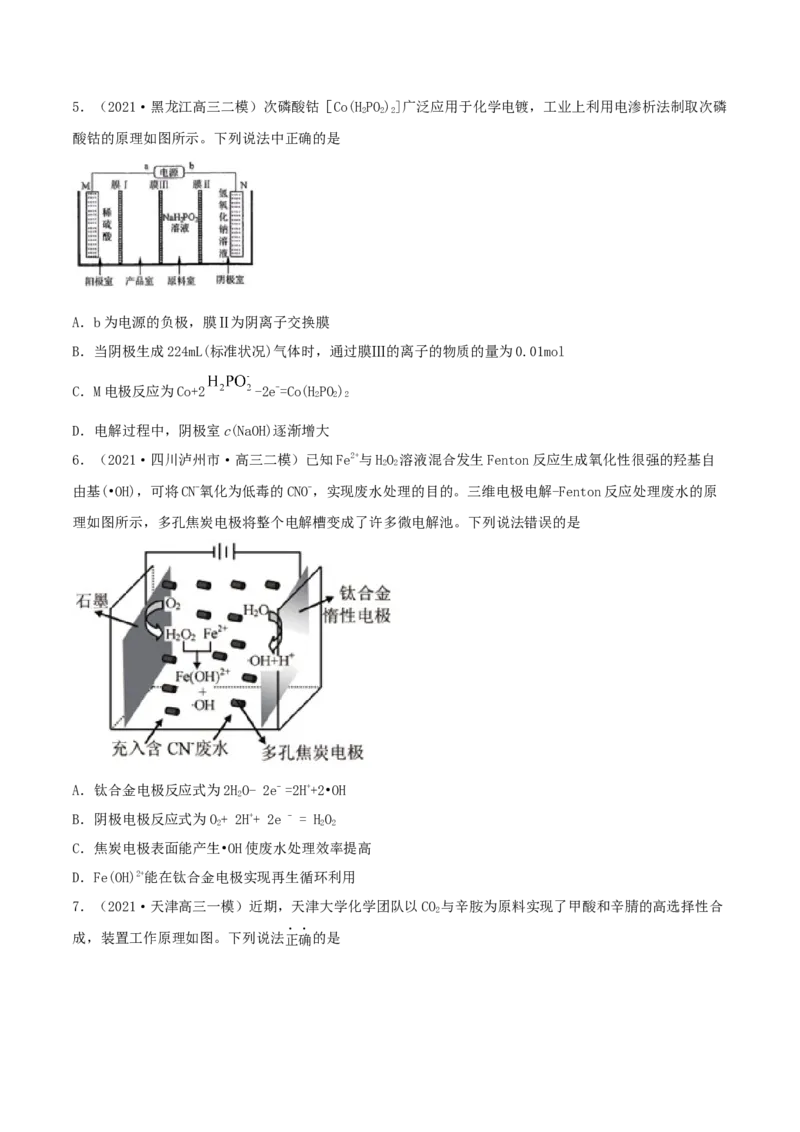
3 4 2 45.(2021·黑龙江高三二模)次磷酸钴[Co(HPO)]广泛应用于化学电镀,工业上利用电渗析法制取次磷
2 2 2
酸钴的原理如图所示。下列说法中正确的是
A.b为电源的负极,膜Ⅱ为阴离子交换膜
B.当阴极生成224mL(标准状况)气体时,通过膜Ⅲ的离子的物质的量为0.01mol
C.M电极反应为Co+2 -2e-=Co(HPO)
2 2 2
D.电解过程中,阴极室c(NaOH)逐渐增大
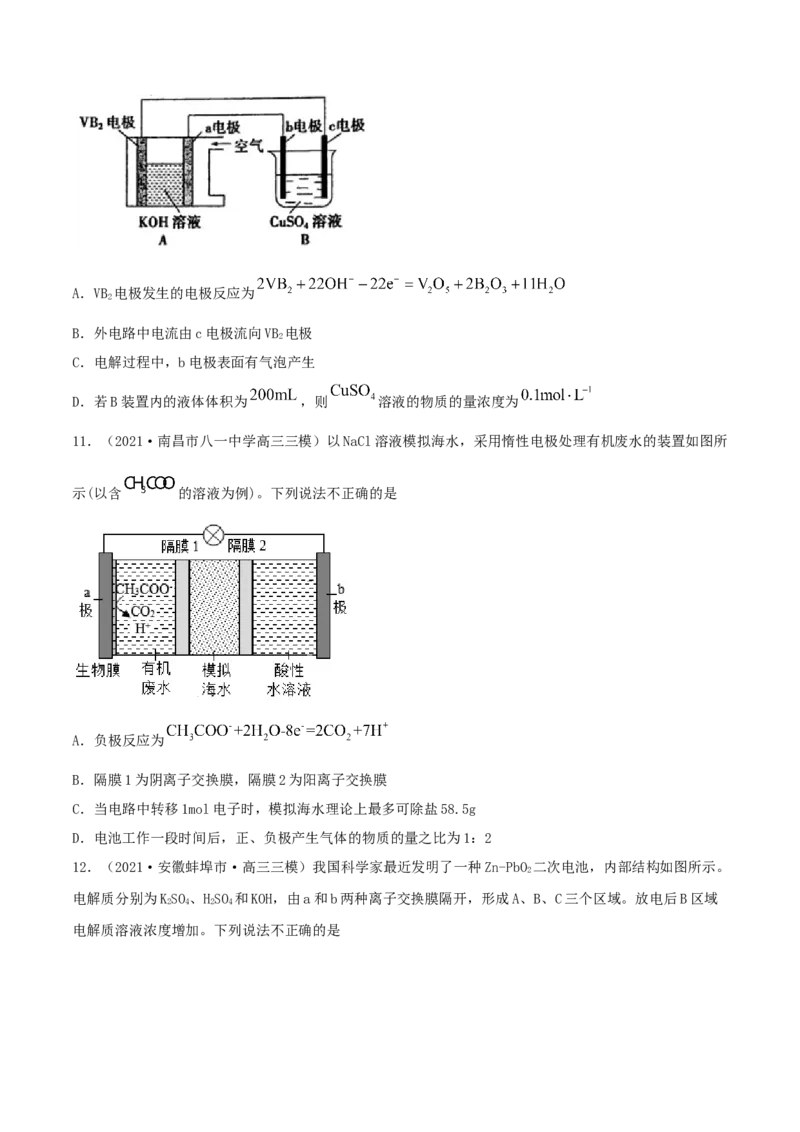
6.(2021·四川泸州市·高三二模)已知Fe2+与HO 溶液混合发生Fenton反应生成氧化性很强的羟基自
2 2
由基(•OH),可将CN-氧化为低毒的CNO-,实现废水处理的目的。三维电极电解-Fenton反应处理废水的原
理如图所示,多孔焦炭电极将整个电解槽变成了许多微电解池。下列说法错误的是
A.钛合金电极反应式为2HO- 2e- =2H++2•OH
2
B.阴极电极反应式为O+ 2H++ 2e - = HO
2 2 2
C.焦炭电极表面能产生•OH使废水处理效率提高
D.Fe(OH)2+能在钛合金电极实现再生循环利用
7.(2021·天津高三一模)近期,天津大学化学团队以CO 与辛胺为原料实现了甲酸和辛腈的高选择性合
2
成,装置工作原理如图。下列说法正确的是A.NiP电极与电源负极相连
2
B.辛胺转化为辛腈发生了还原反应
C.In/InO 电极上可能有副产物H 生成
2 3-x 2
D.在In/InO 电极上发生的反应为CO+HO-2e-=HCOO-+OH-
2 3-x 2 2
8.(2020·吉林长春市·东北师大附中高三二模)为了抵御海水的侵蚀,往往会在船体上安装大型的锌
块,利用原电池反应:2Zn+2HO+O=2Zn(OH),下列说法正确的是
2 2 2
A.锌块发生还原反应而被腐蚀
B.船体与海水中的NaCl等发生反应
C.正极的电极反应式为:2HO+2e-=H↑+2OH-
2 2
D.该抵御措施称为牺牲阳极的阴极保护法
9.(2020·辽宁高三二模)青钢的出现是人类从石器时代走向新时代的里程碑,中国古代的青铜器铸造
工艺、造型艺术,在世界上享有极高的声誉。下列说法错误的是
A.“曾青得铁则化为铜”描述的是一个置换反应
B.我国已知最大的青铜器后母戊鼎,是一种铜合金制品
C.青铜器中含有锡、铅,发生电化学腐蚀时铜为正极
D.出土的古代青铜器表面的铜绿是一种铜的氧化物
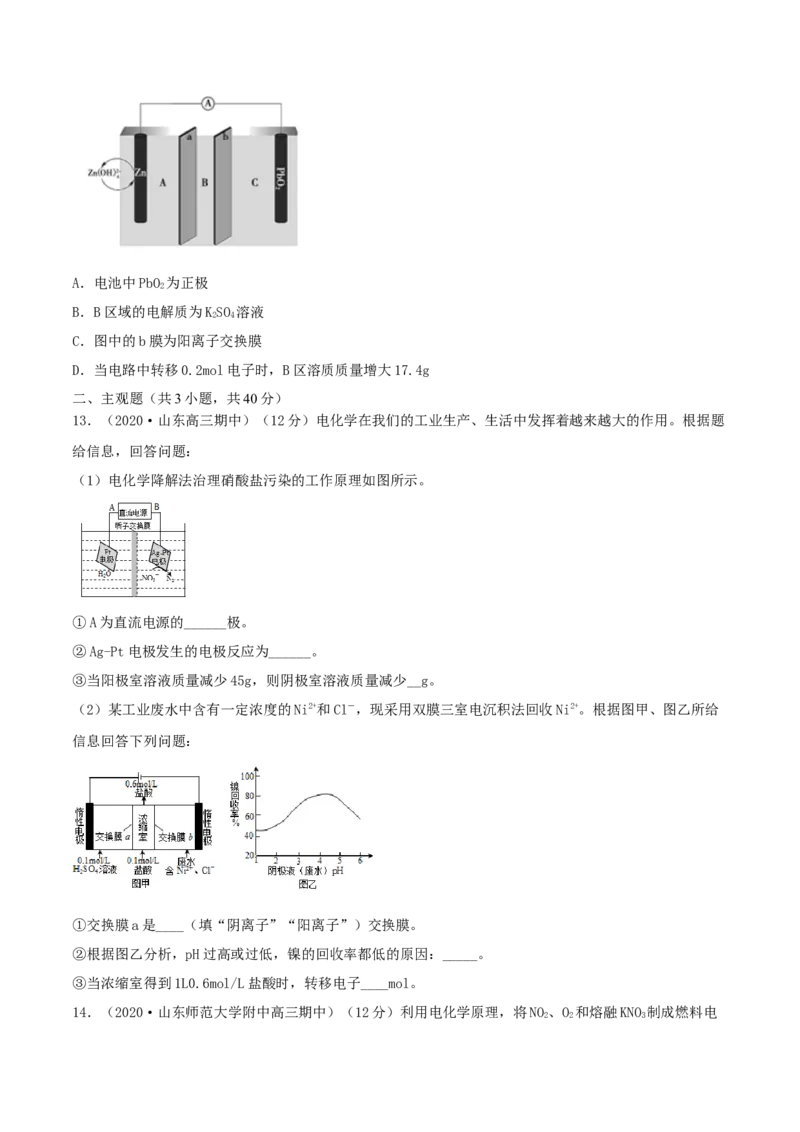
10.(2021·江西鹰潭市·高三一模)碱性硼化钒(VB)一空气电池工作时反应为
2
。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。
当外电路中通过 电子时,B装置内共收集到 气体(标准状况下),则下列说法不正确的是A.VB 电极发生的电极反应为
2
B.外电路中电流由c电极流向VB 电极
2
C.电解过程中,b电极表面有气泡产生
D.若B装置内的液体体积为 ,则 溶液的物质的量浓度为
11.(2021·南昌市八一中学高三三模)以NaCl溶液模拟海水,采用惰性电极处理有机废水的装置如图所
示(以含 的溶液为例)。下列说法不正确的是
A.负极反应为
B.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上最多可除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为1:2
12.(2021·安徽蚌埠市·高三三模)我国科学家最近发明了一种Zn-PbO 二次电池,内部结构如图所示。
2
电解质分别为KSO、HSO 和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个区域。放电后B区域
2 4 2 4
电解质溶液浓度增加。下列说法不正确的是A.电池中PbO 为正极
2
B.B区域的电解质为KSO 溶液
2 4
C.图中的b膜为阳离子交换膜
D.当电路中转移0.2mol电子时,B区溶质质量增大17.4g
二、主观题(共3小题,共40分)
13.(2020·山东高三期中)(12分)电化学在我们的工业生产、生活中发挥着越来越大的作用。根据题
给信息,回答问题:
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。
①A为直流电源的______极。
②Ag-Pt电极发生的电极反应为______。
③当阳极室溶液质量减少45g,则阴极室溶液质量减少__g。
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给
信息回答下列问题:
①交换膜a是____(填“阴离子”“阳离子”)交换膜。
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:_____。
③当浓缩室得到1L0.6mol/L盐酸时,转移电子____mol。
14.(2020·山东师范大学附中高三期中)(12分)利用电化学原理,将NO、O 和熔融KNO 制成燃料电
2 2 3池,模拟工业电解法来处理含CrO 废水,如下图所示;电解过程中溶液发生反应:CrO +6Fe2++14H+
2 2
===2Cr3++6Fe3++7HO。
2
(1)甲池工作时,NO 转变成绿色硝化剂Y,Y是NO,可循环使用。则石墨Ⅰ是电池的________极;石墨
2 2 5
Ⅰ附近发生的电极反应式为___________________。
(2)工作时,甲池内的NO 向___________极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的
O 和NO 的体积比为____________。
2 2
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为_________________________________。
(4)若溶液中减少了0.01 mol CrO ,则电路中至少转移了___________mol电子。
2
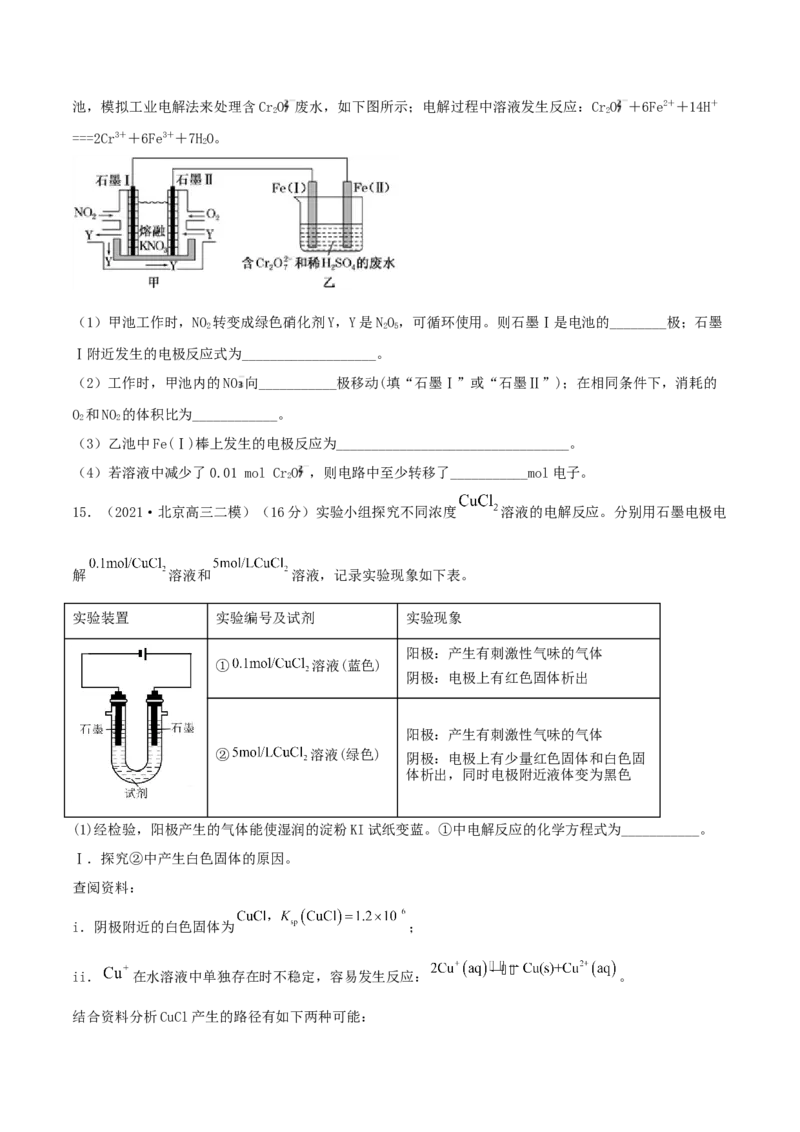
15.(2021·北京高三二模)(16分)实验小组探究不同浓度 溶液的电解反应。分别用石墨电极电
解 溶液和 溶液,记录实验现象如下表。
实验装置 实验编号及试剂 实验现象
阳极:产生有刺激性气味的气体
① 溶液(蓝色)
阴极:电极上有红色固体析出
阳极:产生有刺激性气味的气体
② 溶液(绿色) 阴极:电极上有少量红色固体和白色固
体析出,同时电极附近液体变为黑色
(1)经检验,阳极产生的气体能使湿润的淀粉KI试纸变蓝。①中电解反应的化学方程式为___________。
Ⅰ.探究②中产生白色固体的原因。
查阅资料:
i.阴极附近的白色固体为 ;
ii. 在水溶液中单独存在时不稳定,容易发生反应: 。
结合资料分析CuCl产生的路径有如下两种可能:(2)路径1:阴极发生电极反应分两步:
i.___________
ⅱ. ,同时伴随反应 ,生成白色沉淀。
(3)路径2:阴极发生电极反应 ,而后发生反应a:___________(写出离子方程式),生成白色
沉淀。同学们通过实验证明反应a可以发生,其实验操作和现象是___________。
Ⅱ.探究②中阴极区液体中黑色物质的成分。
进一步查阅资料,提出以下猜想。
猜想1.生成氢氧化铜,进而转化为极细小的氧化铜;
猜想2.生成铜的速率快,形成黑色纳米铜;
猜想3.发生反应 (棕黑色)。
(4)若猜想1成立,则阴极一定还存在的电极反应是___________。
取2mL黑色液体于试管中,分别加入不同试剂,记录实验现象如下表。
实验编号 ③ ④ ⑤
加入试剂 4mL浓 4mL浓HCl
溶液变澄清,呈绿
溶液变澄清,呈绿色,试管口有浅
实验现象 黑色液体颜色变深 色,同时出现少量白
红棕色气体生成
色沉淀
(5)甲同学根据实验③产生的现象得出结论:黑色液体中一定有纳米铜。乙同学认为甲同学的结论不合理,
他做出判断的依据是___________。
(6)由上述实验可得到的关于黑色物质成分的结论是___________。