文档内容
专题 05 化学能与电能的转化
1.钢铁在中性条件下发生电化学腐蚀时,正极上的电极反应式为
A. B.
C. D.
2.下列有关工业生产的叙述正确的是
A.工业上通常采用电解熔融的MgO制得金属Mg
B.空气吹出法是海水提溴的常用方法,其中用到氯气作还原剂
C.电解饱和食盐水制烧碱采用阳离子交换膜法,可防止阴极室产生的OH-进入阳极室
D.电解精炼铜时,同一时间内阳极减少的质量一定等于阴极增加的质量
3.海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A.M极发生的电极反应:
B.隔膜和玻璃陶瓷只具有传导离子的功能,不具有防水的功能
C.海水中的 或者海水中溶解的 等物质在N极反应
D.该锂―海水电池属于一次电池
4.用下图所示装置电解饱和碳酸钠溶液,实验如下:
装置 X电极材料 现象
两极均有气泡产生;
石墨
5min后澄清石灰水变浑浊
两极均有气泡产生;
铂(Pt)
30min后澄清石灰水不变浑浊下列判断正确的是A.X电极为阴极
B.左侧电极附近溶液 增大
C.X为石墨时,石灰水变浑浊的主要原因是阳极产生的 与 反应生成了
D.电解过程中,溶液里一直存在
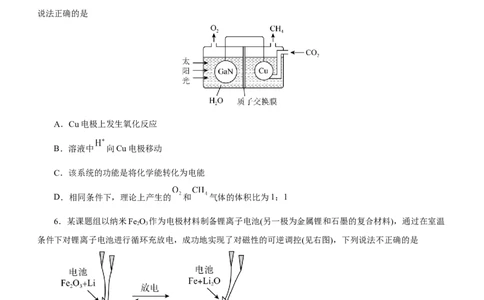
5.氮化镓(GaN)与Cu可组成如下图所示的人工光合系统,该装置能以 和 为原料合成 。下列
说法正确的是
A.Cu电极上发生氧化反应
B.溶液中 向Cu电极移动
C.该系统的功能是将化学能转化为电能
D.相同条件下,理论上产生的 和 气体的体积比为1:1
6.某课题组以纳米Fe O 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温
2 3
条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(见右图),下列说法不正确的是
A.充电时,Fe O 对应电极连接充电电源的负极
2 3
B.该电池的正极的电极反应式:Fe O+6Li++6e−=3Li O+2Fe
2 3 2
C.该电池不能使用氢氧化钠溶液作为电解液
D.该电池工作的原理:放电时,Fe O 作为电池正极被还原为Fe,电池被磁铁吸引
2 3
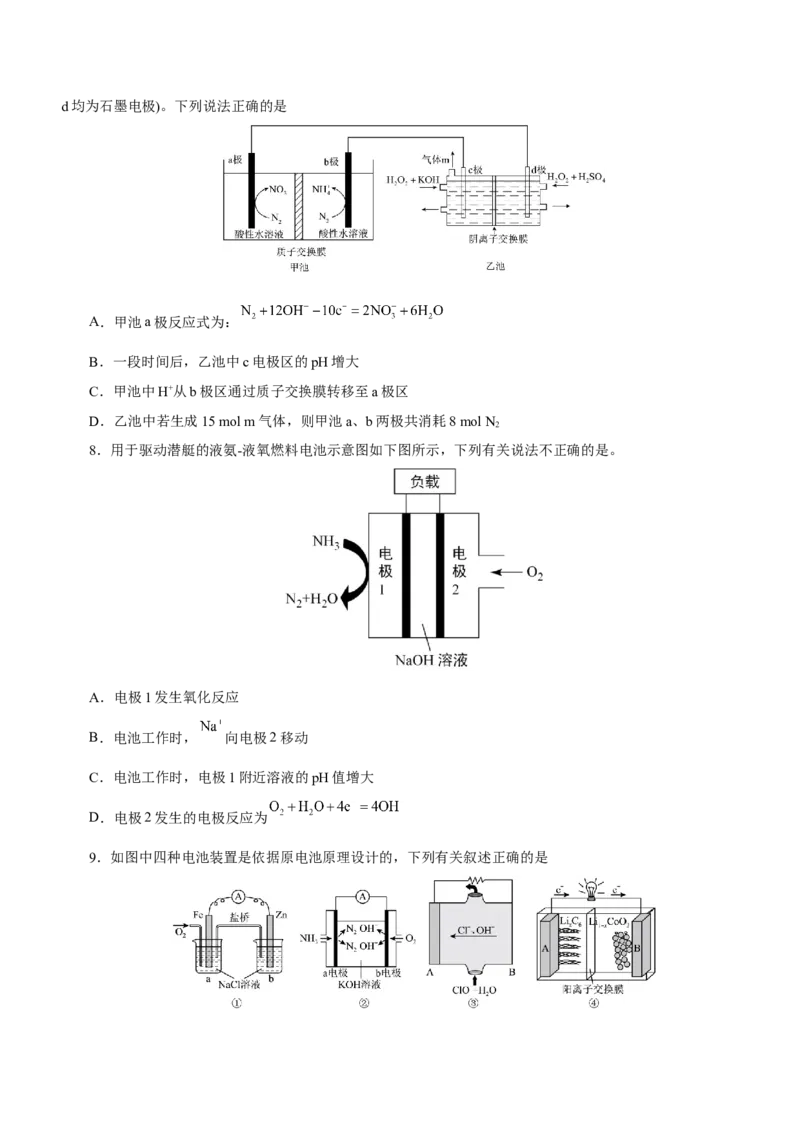
7.用一种新型HO 液态燃料电池(乙池)电解催化氮气制备铵盐和硝酸盐(甲池)的工作原理示意图如下(c、
2 2d均为石墨电极)。下列说法正确的是
A.甲池a极反应式为:
B.一段时间后,乙池中c电极区的pH增大
C.甲池中H+从b极区通过质子交换膜转移至a极区
D.乙池中若生成15 mol m气体,则甲池a、b两极共消耗8 mol N
2
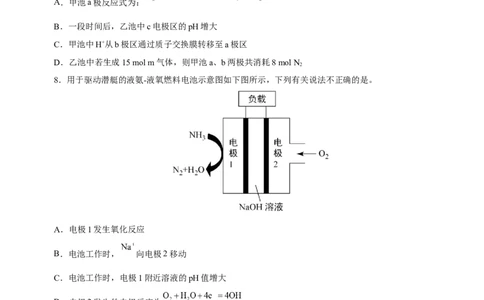
8.用于驱动潜艇的液氨-液氧燃料电池示意图如下图所示,下列有关说法不正确的是。
A.电极1发生氧化反应
B.电池工作时, 向电极2移动
C.电池工作时,电极1附近溶液的pH值增大
D.电极2发生的电极反应为
9.如图中四种电池装置是依据原电池原理设计的,下列有关叙述正确的是A.①中铁电极做负极
B.②中电子由a电极经溶液流向b电极
C.③中外电路中电流由A电极流向B电极
D.④中锂电池工作时,会有Li+从LiC 中脱落下来
x 6
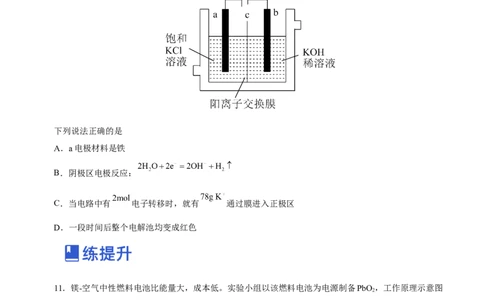
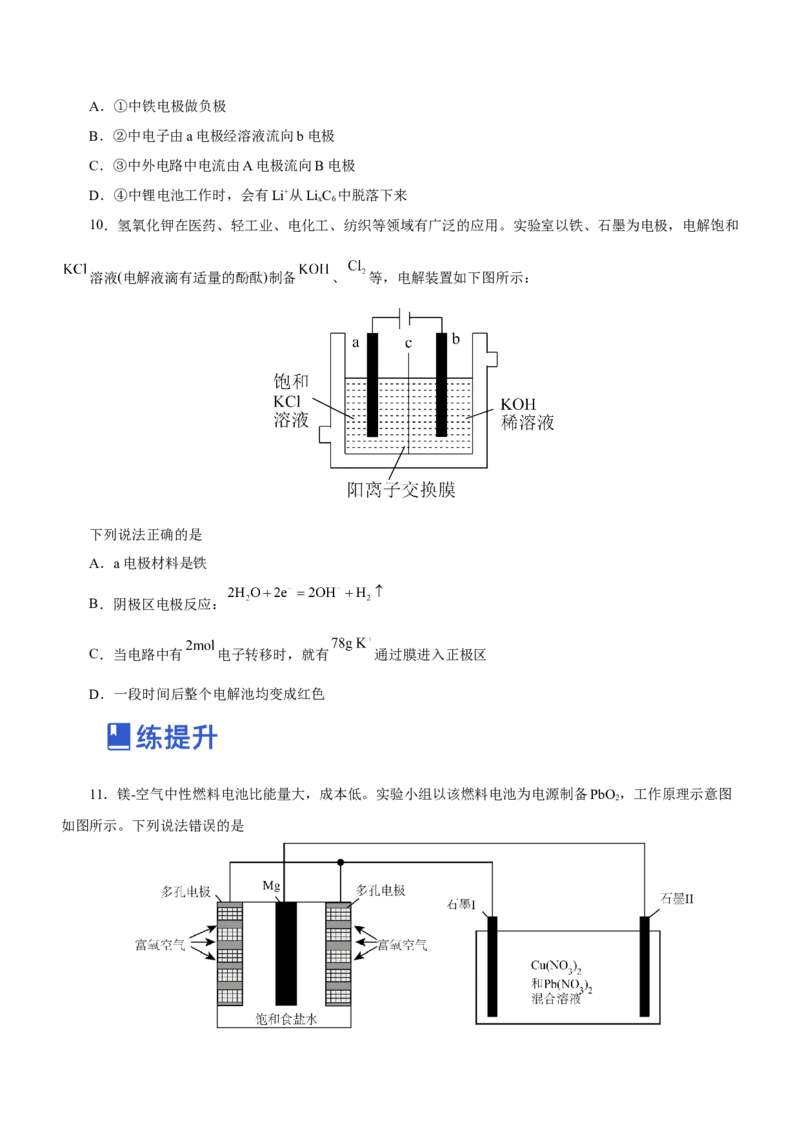
10.氢氧化钾在医药、轻工业、电化工、纺织等领域有广泛的应用。实验室以铁、石墨为电极,电解饱和
溶液(电解液滴有适量的酚酞)制备 、 等,电解装置如下图所示:
下列说法正确的是
A.a电极材料是铁
B.阴极区电极反应:
C.当电路中有 电子转移时,就有 通过膜进入正极区
D.一段时间后整个电解池均变成红色
11.镁-空气中性燃料电池比能量大,成本低。实验小组以该燃料电池为电源制备PbO ,工作原理示意图
2
如图所示。下列说法错误的是A.采用多孔电极有利于增大接触面积和氧气扩散
B.工作时,电源的正极反应式为
C.工作时,Pb2+在石墨II电极上失去电子
D.外电路中流过2mole-,理论上生成1molPbO
2
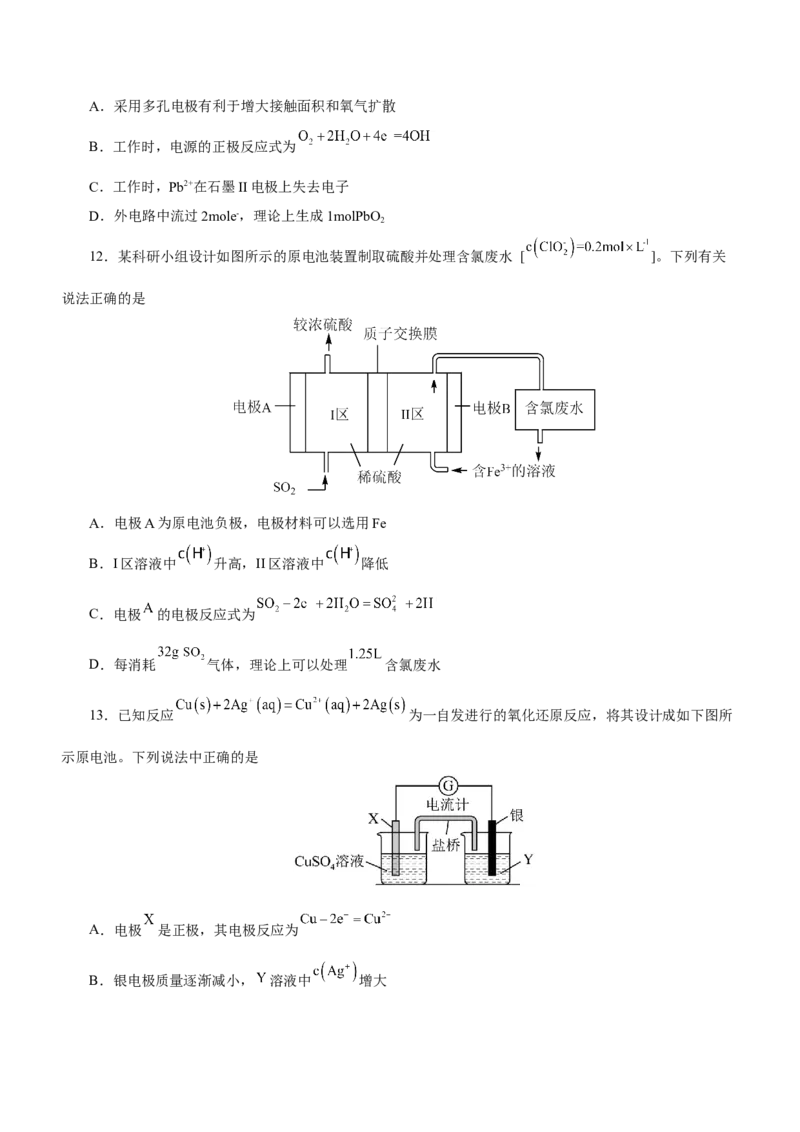
12.某科研小组设计如图所示的原电池装置制取硫酸并处理含氯废水 [ ]。下列有关
说法正确的是
A.电极A为原电池负极,电极材料可以选用Fe
B.I区溶液中 升高,II区溶液中 降低
C.电极 的电极反应式为
D.每消耗 气体,理论上可以处理 含氯废水
13.已知反应 为一自发进行的氧化还原反应,将其设计成如下图所
示原电池。下列说法中正确的是
A.电极 是正极,其电极反应为
B.银电极质量逐渐减小, 溶液中 增大C. 电极减少 时,电解质溶液中有 电子转移
D.外电路中电流计的指针有偏转
14.低温非水溶剂铝硫电池是一种新型的二次电池,相比锂电池具有原料来源广泛,电容量大等优点。如
下图所示电池以EtNH+Cl-和AlCl 混合物形成的离子液体作电解质,该电解质中Al元素只以 和 离
3 3
子形态存在,下列说法正确的是
A.放电时,S/Al S 电极为负极
2 3
B.放电时,Al电极的电极反应为
C.充电时,Al电极电势较高
D.充电时,每有1 mol电子转移,S/Al S 电极减轻9 g
2 3
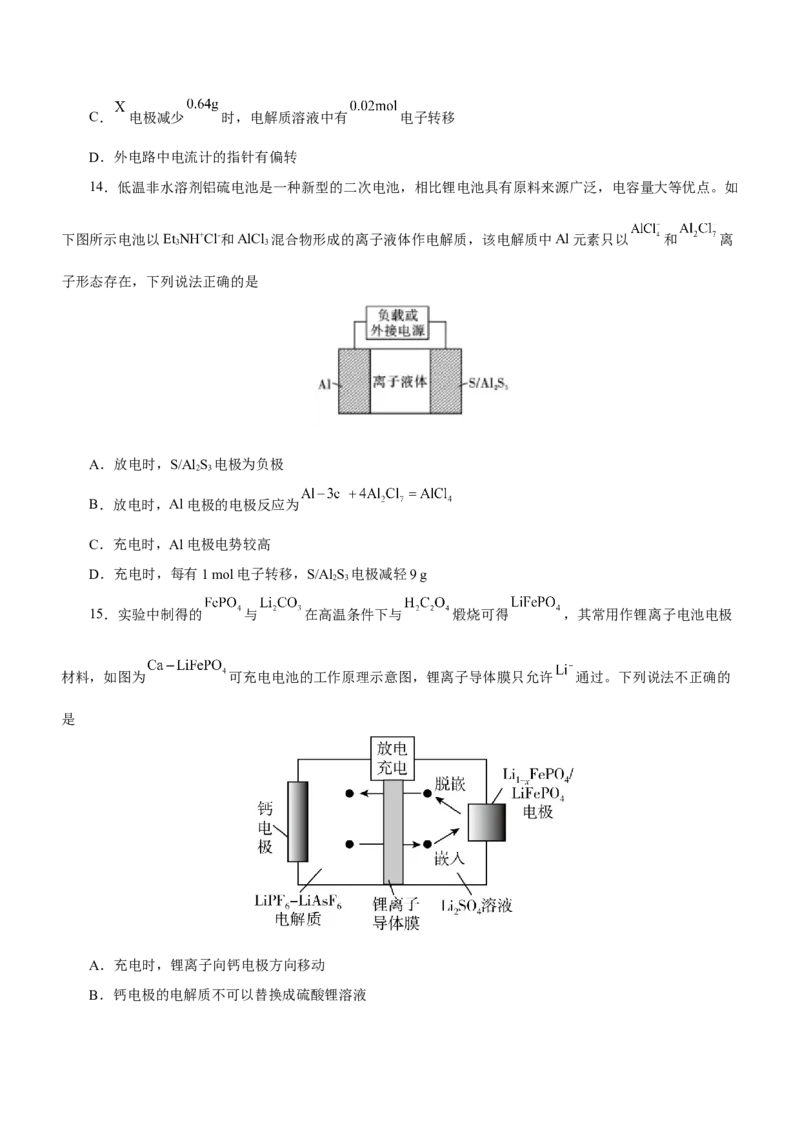
15.实验中制得的 与 在高温条件下与 煅烧可得 ,其常用作锂离子电池电极
材料,如图为 可充电电池的工作原理示意图,锂离子导体膜只允许 通过。下列说法不正确的
是
A.充电时,锂离子向钙电极方向移动
B.钙电极的电解质不可以替换成硫酸锂溶液C.理论上,每消耗x mol Ca,可生成1mol
D.放电时,电极上发生 的嵌入,
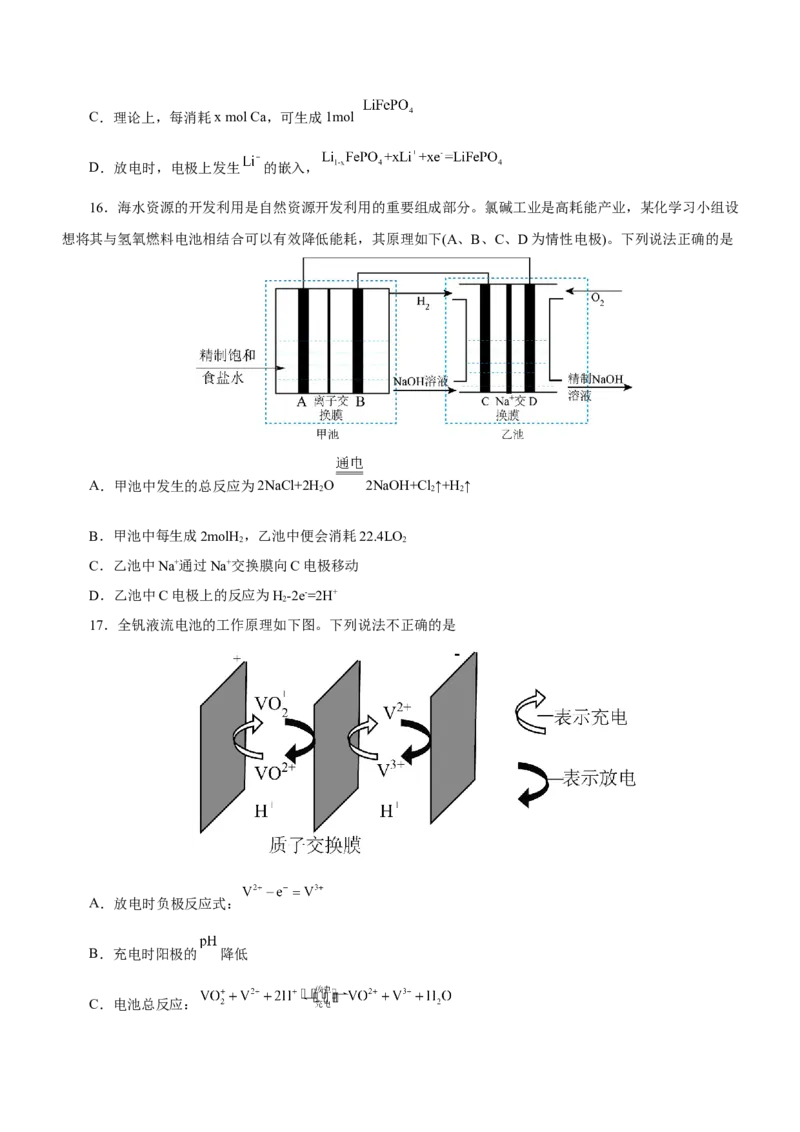
16.海水资源的开发利用是自然资源开发利用的重要组成部分。氯碱工业是高耗能产业,某化学习小组设
想将其与氢氧燃料电池相结合可以有效降低能耗,其原理如下(A、B、C、D为情性电极)。下列说法正确的是
A.甲池中发生的总反应为2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
B.甲池中每生成2molH ,乙池中便会消耗22.4LO
2 2
C.乙池中Na+通过Na+交换膜向C电极移动
D.乙池中C电极上的反应为H-2e-=2H+
2
17.全钒液流电池的工作原理如下图。下列说法不正确的是
A.放电时负极反应式:
B.充电时阳极的 降低
C.电池总反应:D.放电时正极每消耗2mol ,负极区便有2mol 通过质子交换膜移向正极区
\s\do9(放电)
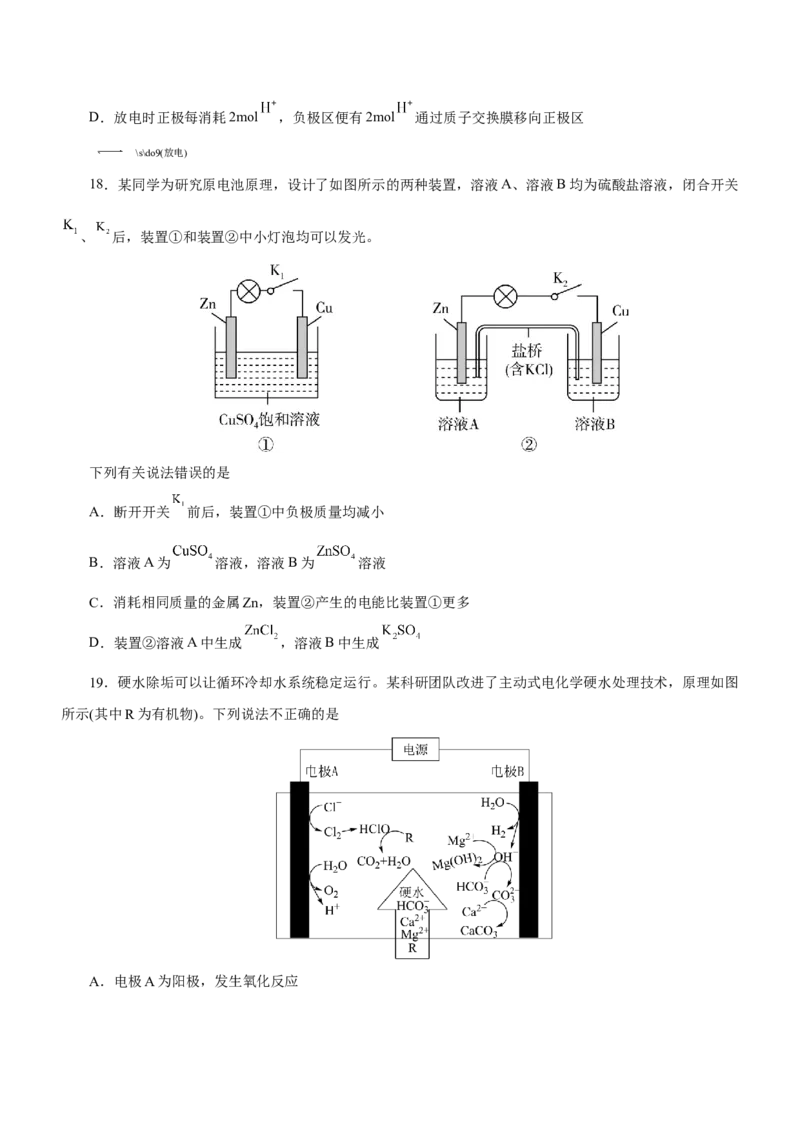
18.某同学为研究原电池原理,设计了如图所示的两种装置,溶液A、溶液B均为硫酸盐溶液,闭合开关
、 后,装置①和装置②中小灯泡均可以发光。
下列有关说法错误的是
A.断开开关 前后,装置①中负极质量均减小
B.溶液A为 溶液,溶液B为 溶液
C.消耗相同质量的金属Zn,装置②产生的电能比装置①更多
D.装置②溶液A中生成 ,溶液B中生成
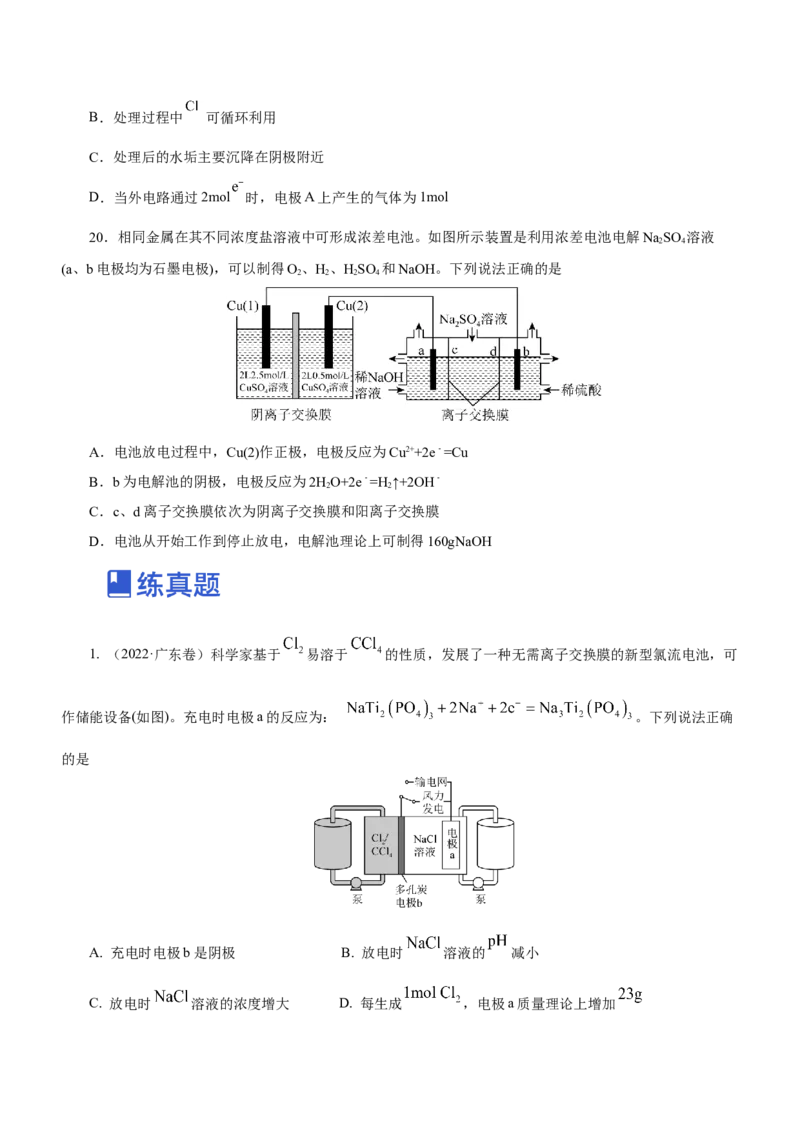
19.硬水除垢可以让循环冷却水系统稳定运行。某科研团队改进了主动式电化学硬水处理技术,原理如图
所示(其中R为有机物)。下列说法不正确的是
A.电极A为阳极,发生氧化反应B.处理过程中 可循环利用
C.处理后的水垢主要沉降在阴极附近
D.当外电路通过2mol 时,电极A上产生的气体为1mol
20.相同金属在其不同浓度盐溶液中可形成浓差电池。如图所示装置是利用浓差电池电解NaSO 溶液
2 4
(a、b电极均为石墨电极),可以制得O、H、HSO 和NaOH。下列说法正确的是
2 2 2 4
A.电池放电过程中,Cu(2)作正极,电极反应为Cu2++2e﹣=Cu
B.b为电解池的阴极,电极反应为2HO+2e﹣=H ↑+2OH﹣
2 2
C.c、d离子交换膜依次为阴离子交换膜和阳离子交换膜
D.电池从开始工作到停止放电,电解池理论上可制得160gNaOH
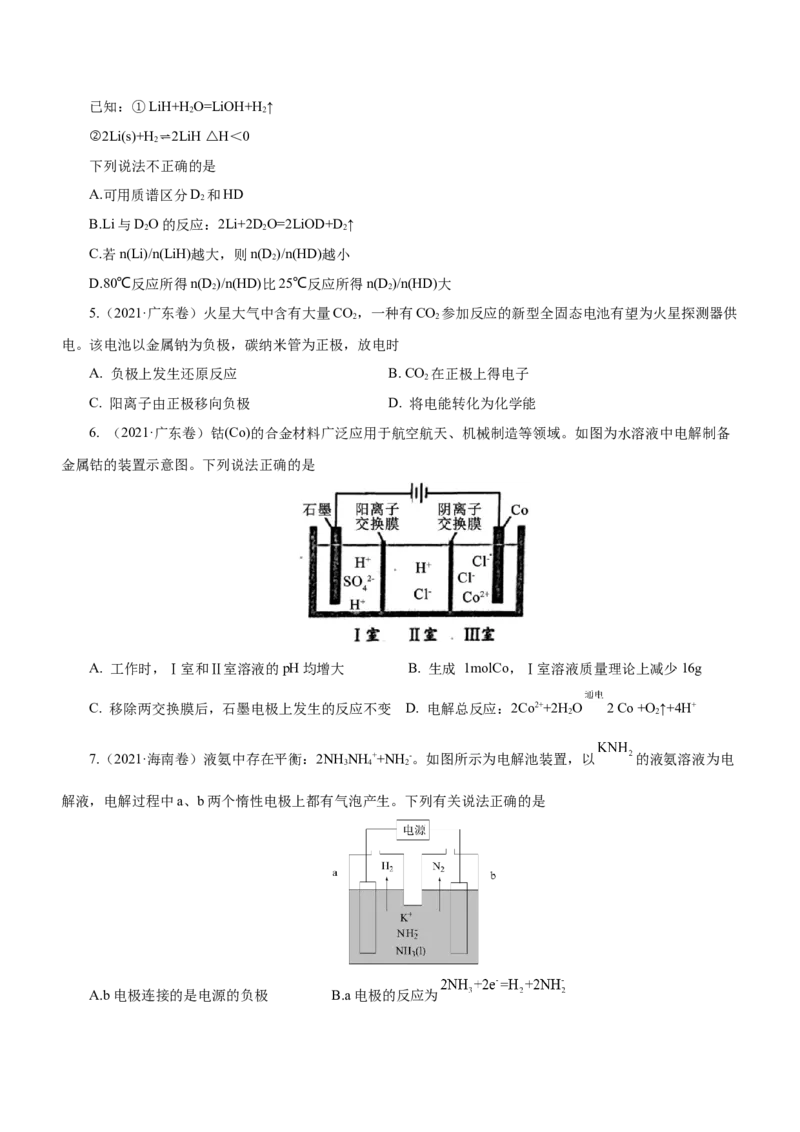
1. (2022·广东卷)科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电池,可
作储能设备(如图)。充电时电极a的反应为: 。下列说法正确
的是
A. 充电时电极b是阴极 B. 放电时 溶液的 减小
C. 放电时 溶液的浓度增大 D. 每生成 ,电极a质量理论上增加2. (2022·北京卷)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间后阴
① 极表面有红色固体,气体减少。经检
验电解液中有
阴极表面未观察到气体,一段时间后
② 阴极表面有致密红色固体。经检验电
解液中无 元素
下列说法不正确的是
A. ①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B. ①中检测到 ,推测可能发生反应:
C. 随阴极析出 ,推测②中溶液 减少, 平衡逆移
D. ②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
3.(2022·浙江卷)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电极(在特制玻璃
薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测溶液中组成电池,
pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
4.(2021·北京卷)有科学研究提出:锂电池负极材料(Li)由于生成LH而不利于电池容量的保持。一定温度
下,利用足量重水(D O)与含LiH的Li负极材料反应,通过测定n(D )/n(HD)可以获知 n(Li)/n(LiH)。
2 2已知:①LiH+H O=LiOH+H ↑
2 2
②2Li(s)+H 2⇌2LiH △H<0
下列说法不正确的是
A.可用质谱区分D 和HD
2
B.Li与DO的反应:2Li+2DO=2LiOD+D ↑
2 2 2
C.若n(Li)/n(LiH)越大,则n(D )/n(HD)越小
2
D.80℃反应所得n(D )/n(HD)比25℃反应所得n(D )/n(HD)大
2 2
5.(2021·广东卷)火星大气中含有大量CO,一种有CO 参加反应的新型全固态电池有望为火星探测器供
2 2
电。该电池以金属钠为负极,碳纳米管为正极,放电时
A. 负极上发生还原反应 B. CO 在正极上得电子
2
C. 阳离子由正极移向负极 D. 将电能转化为化学能
6. (2021·广东卷)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备
金属钴的装置示意图。下列说法正确的是
A. 工作时,Ⅰ室和Ⅱ室溶液的pH均增大 B. 生成 1molCo,Ⅰ室溶液质量理论上减少16g
C. 移除两交换膜后,石墨电极上发生的反应不变 D. 电解总反应:2Co2++2H O 2 Co +O ↑+4H+
2 2
7.(2021·海南卷)液氨中存在平衡:2NH NH ++NH-。如图所示为电解池装置,以 的液氨溶液为电
3 4 2
解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
A.b电极连接的是电源的负极 B.a电极的反应为C.电解过程中,阴极附近K+浓度减小 D.理论上两极产生的气体物质的量之比为1:1
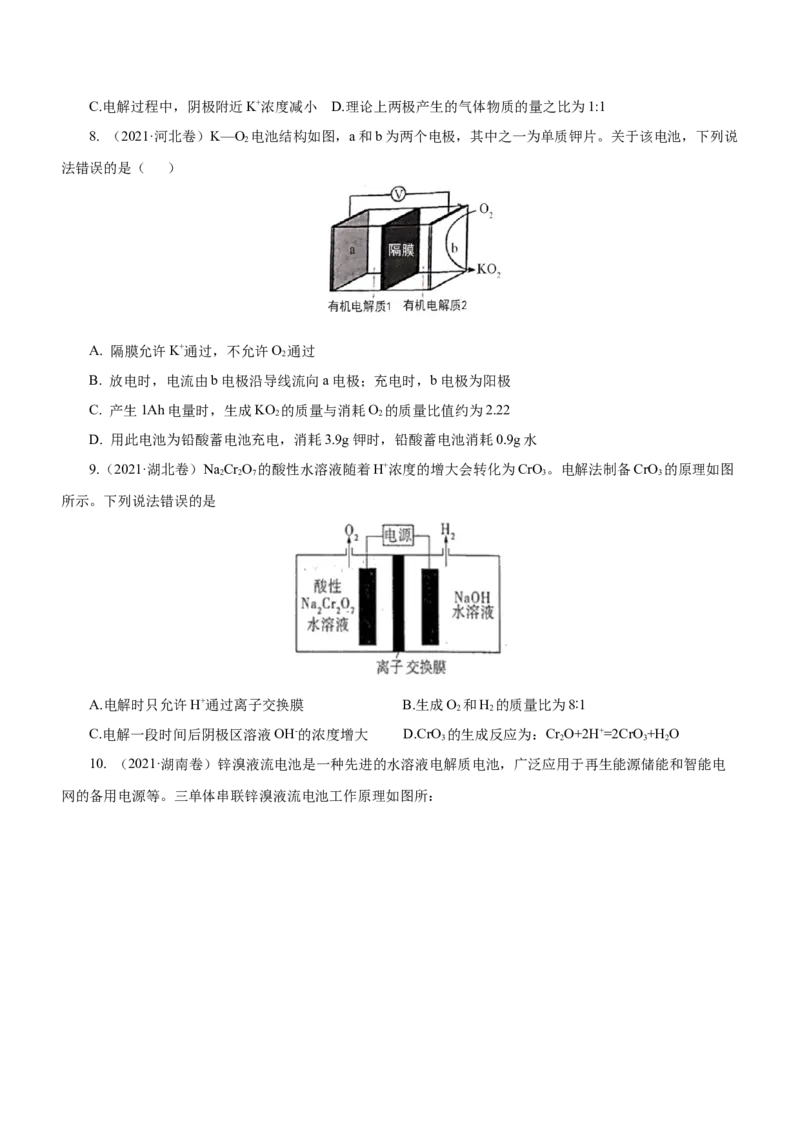
8. (2021·河北卷)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下列说
2
法错误的是( )
A. 隔膜允许K+通过,不允许O 通过
2
B. 放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C. 产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D. 用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
9.(2021·湖北卷)NaCr O 的酸性水溶液随着H+浓度的增大会转化为CrO。电解法制备CrO 的原理如图
2 2 7 3 3
所示。下列说法错误的是
A.电解时只允许H+通过离子交换膜 B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大 D.CrO 的生成反应为:Cr O+2H+=2CrO +H O
3 2 3 2
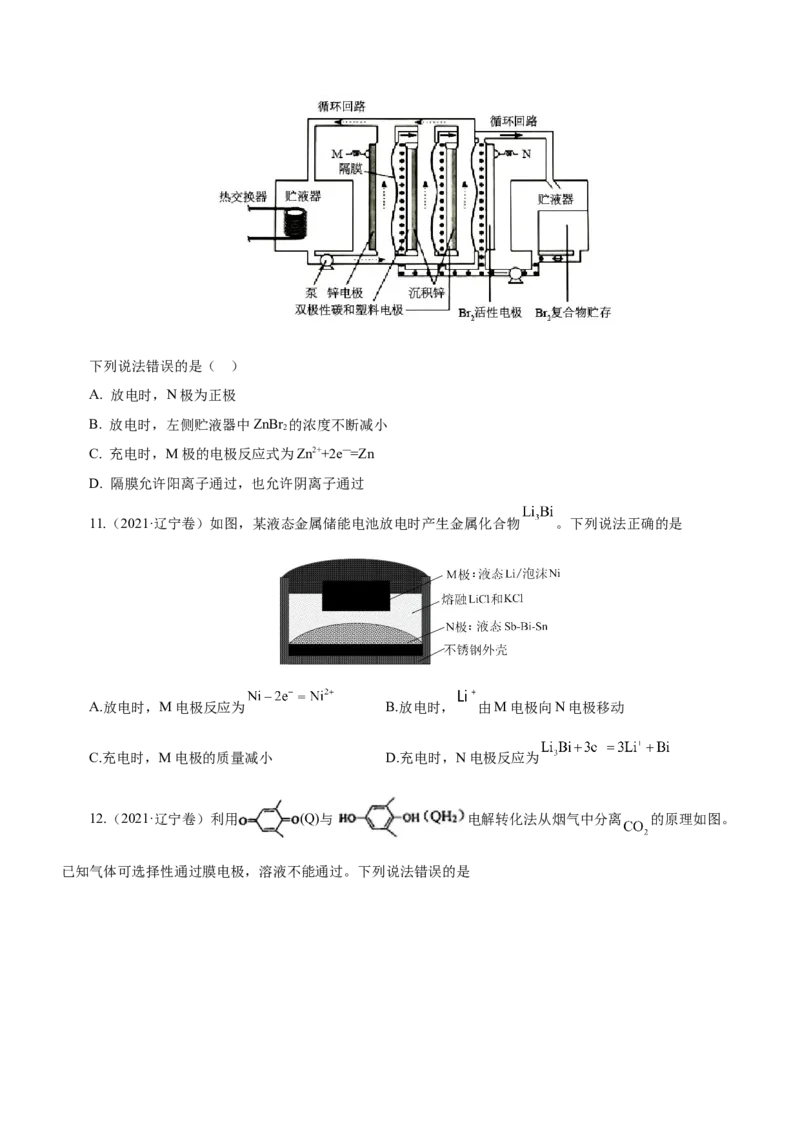
10. (2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电
网的备用电源等。三单体串联锌溴液流电池工作原理如图所:下列说法错误的是( )
A. 放电时,N极为正极
B. 放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C. 充电时,M极的电极反应式为Zn2++2e—=Zn
D. 隔膜允许阳离子通过,也允许阴离子通过
11.(2021·辽宁卷)如图,某液态金属储能电池放电时产生金属化合物 。下列说法正确的是
A.放电时,M电极反应为 B.放电时, 由M电极向N电极移动
C.充电时,M电极的质量减小 D.充电时,N电极反应为
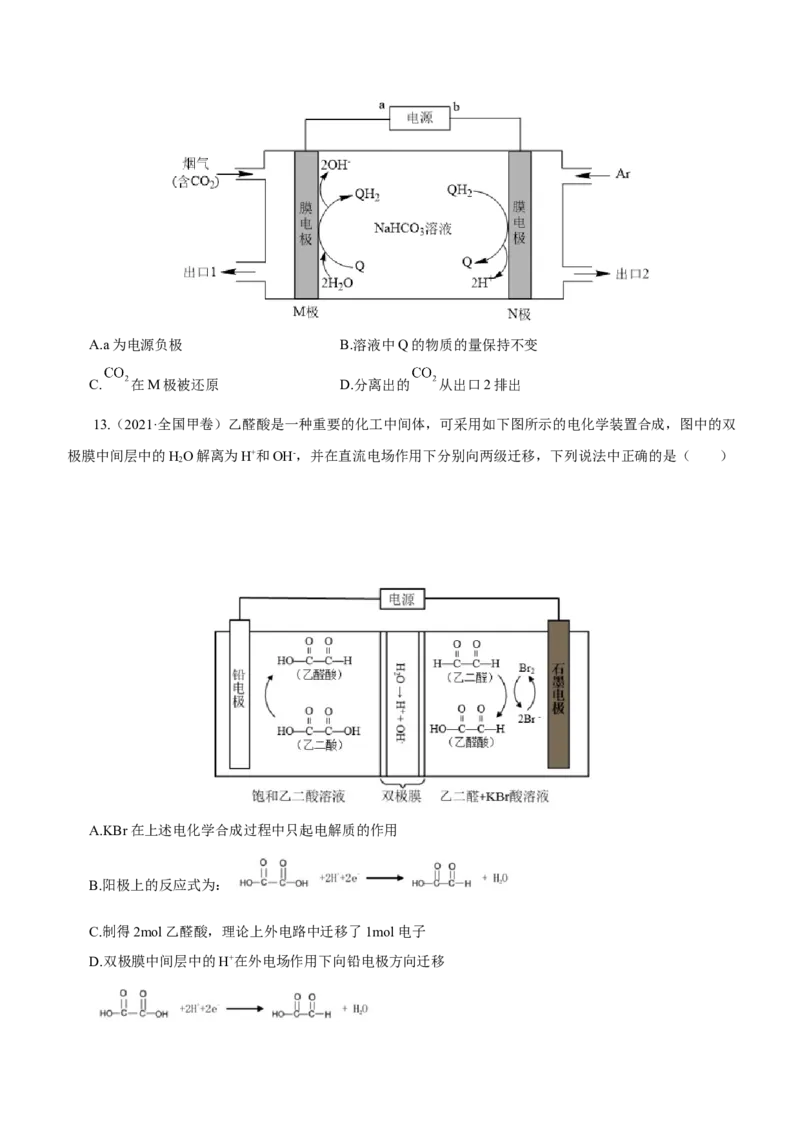
12.(2021·辽宁卷)利用 (Q)与 电解转化法从烟气中分离 的原理如图。
已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的是A.a为电源负极 B.溶液中Q的物质的量保持不变
C. 在M极被还原 D.分离出的 从出口2排出
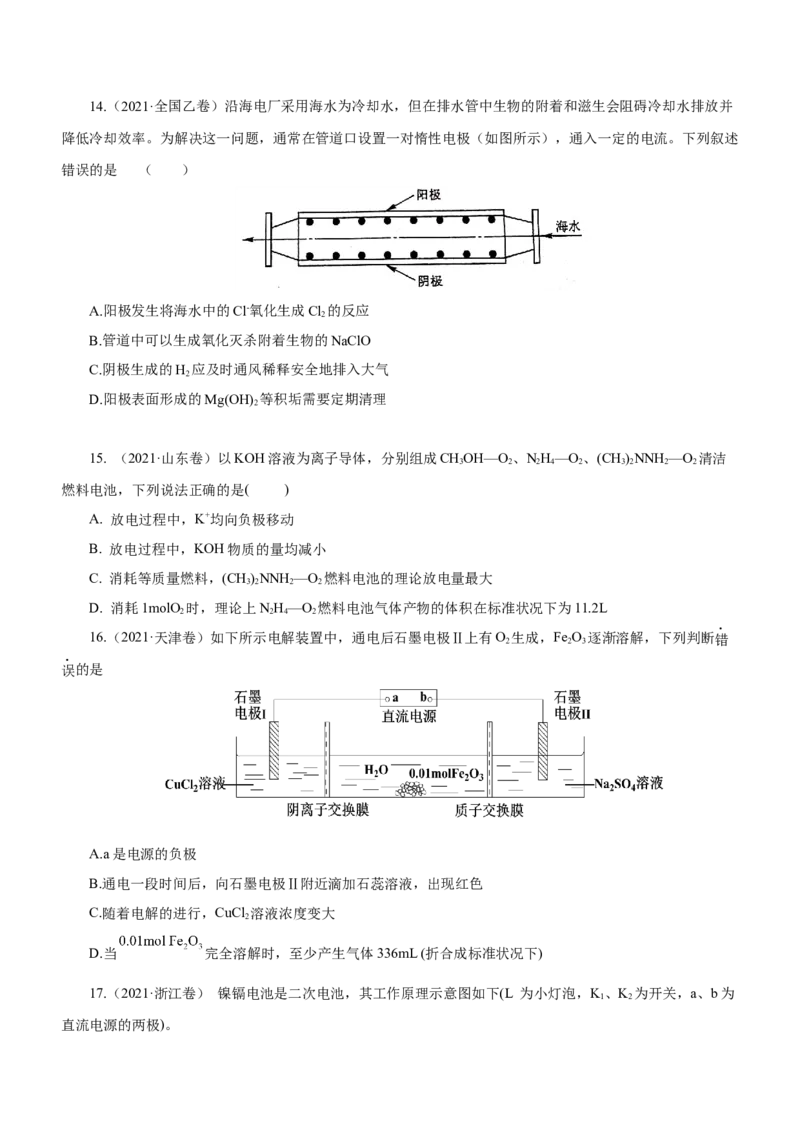
13.(2021·全国甲卷)乙醛酸是一种重要的化工中间体,可采用如下图所示的电化学装置合成,图中的双
极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别向两级迁移,下列说法中正确的是( )
2
A.KBr在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为:
C.制得2mol乙醛酸,理论上外电路中迁移了1mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移14.(2021·全国乙卷)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并
降低冷却效率。为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。下列叙述
错误的是 ( )
A.阳极发生将海水中的Cl-氧化生成Cl 的反应
2
B.管道中可以生成氧化灭杀附着生物的NaClO
C.阴极生成的H 应及时通风稀释安全地排入大气
2
D.阳极表面形成的Mg(OH) 等积垢需要定期清理
2
15. (2021·山东卷)以KOH溶液为离子导体,分别组成CHOH—O、NH—O、(CH)NNH—O 清洁
3 2 2 4 2 3 2 2 2
燃料电池,下列说法正确的是( )
A. 放电过程中,K+均向负极移动
B. 放电过程中,KOH物质的量均减小
C. 消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D. 消耗1molO 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
16.(2021·天津卷)如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列判断错
2 2 3
误的是
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当 完全溶解时,至少产生气体336mL (折合成标准状况下)
17.(2021·浙江卷) 镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开关,a、b为
1 2
直流电源的两极)。下列说法不正确的是
A. 断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B. 断开K、合上K,电极A为阴极,发生还原反应
1 2
C. 电极B发生氧化反应过程中,溶液中KOH浓度不变
D. 镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
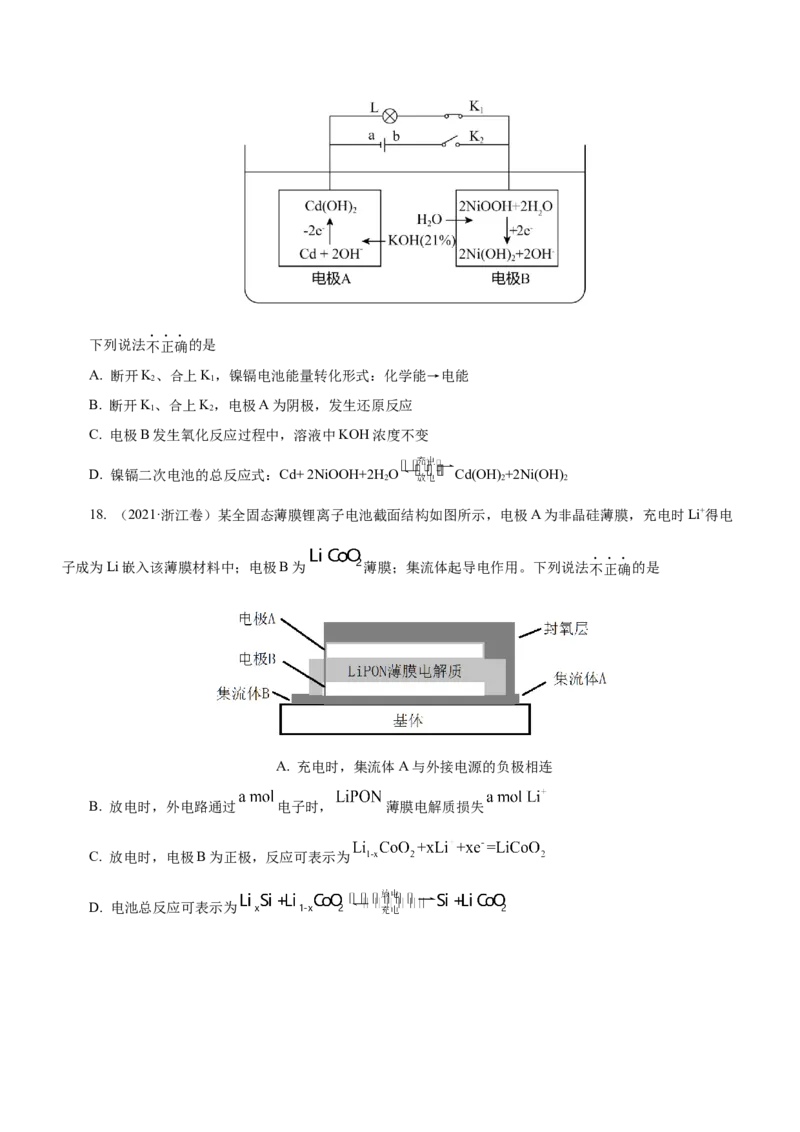
18. (2021·浙江卷)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时Li+得电
子成为Li嵌入该薄膜材料中;电极B为 薄膜;集流体起导电作用。下列说法不正确的是
A. 充电时,集流体A与外接电源的负极相连
B. 放电时,外电路通过 电子时, 薄膜电解质损失
C. 放电时,电极B为正极,反应可表示为
D. 电池总反应可表示为