文档内容
专题讲座(六) 介质和隔膜在电化学的作用
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
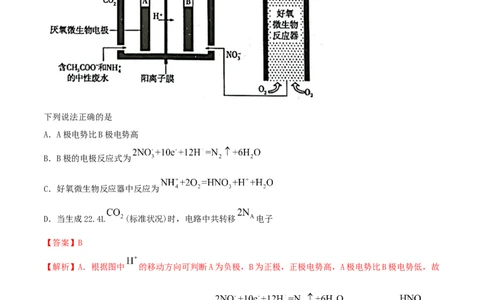
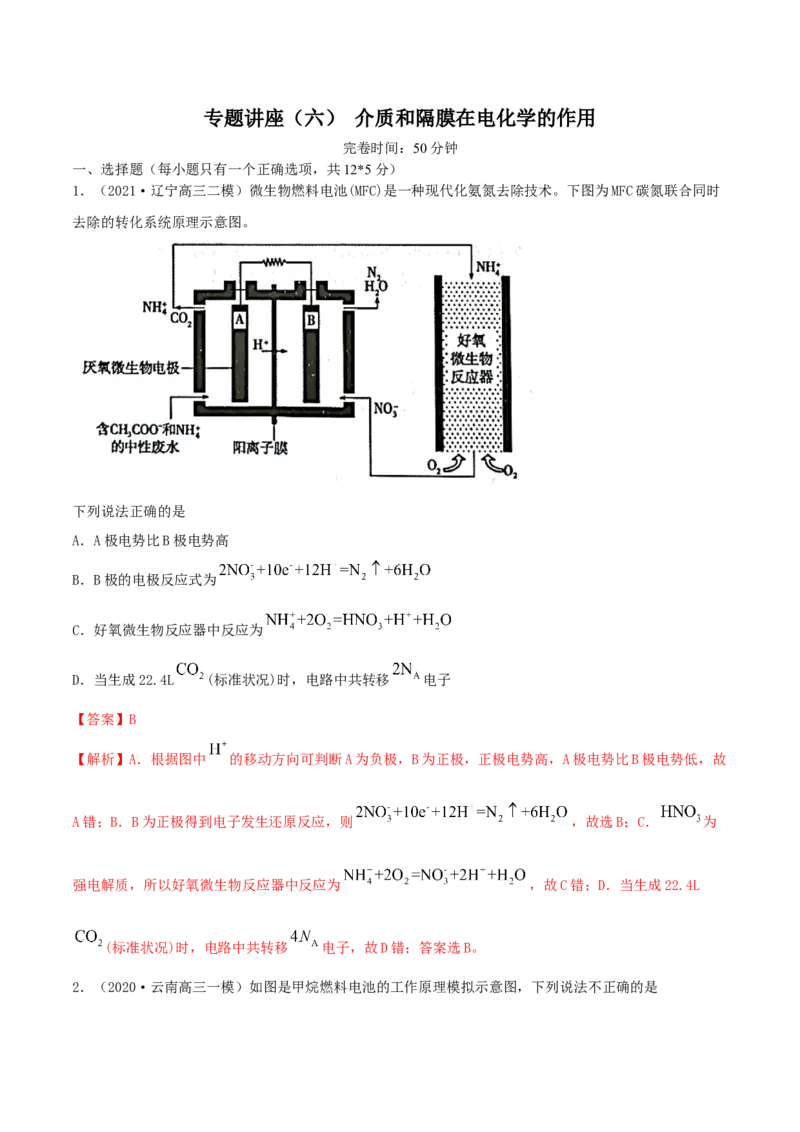
1.(2021·辽宁高三二模)微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时
去除的转化系统原理示意图。
下列说法正确的是
A.A极电势比B极电势高
B.B极的电极反应式为
C.好氧微生物反应器中反应为
D.当生成22.4L (标准状况)时,电路中共转移 电子
【答案】B
【解析】A.根据图中 的移动方向可判断A为负极,B为正极,正极电势高,A极电势比B极电势低,故
A错;B.B为正极得到电子发生还原反应,则 ,故选B;C. 为
强电解质,所以好氧微生物反应器中反应为 ,故C错;D.当生成22.4L
(标准状况)时,电路中共转移 电子,故D错;答案选B。
2.(2020·云南高三一模)如图是甲烷燃料电池的工作原理模拟示意图,下列说法不正确的是A.电极B为正极
B. 在电极A上发生氧化反应
C.电极A区发生反应:
D.当有 通过外电路时,有 通过阴离子交换膜
【答案】D
【解析】电极A是负极,甲烷( )燃料电池的反应原理是 与 反应生成 和 ,但该甲烷
燃料电池的电解质溶液为 溶液,生成的 还要与 反应生成 ,所以总反应为
,负极反应为 ;电极B是正极,
发生还原反应,当有 通过外电路时,有 通过阴离子交换膜。A. 电极B发生还原反应
为正极,故A正确;B.A是负极, 在电极A上发生氧化反应,故B正确;C. 甲烷( )燃料电池
的反应原理是 与 反应生成 和 ,但该甲烷燃料电池的电解质溶液为 溶液,生成的
还要与 反应生成 ,电极A区发生反应: ,故C正确;D.
当有 通过外电路时,有 通过阴离子交换膜,故D错误;故选D。
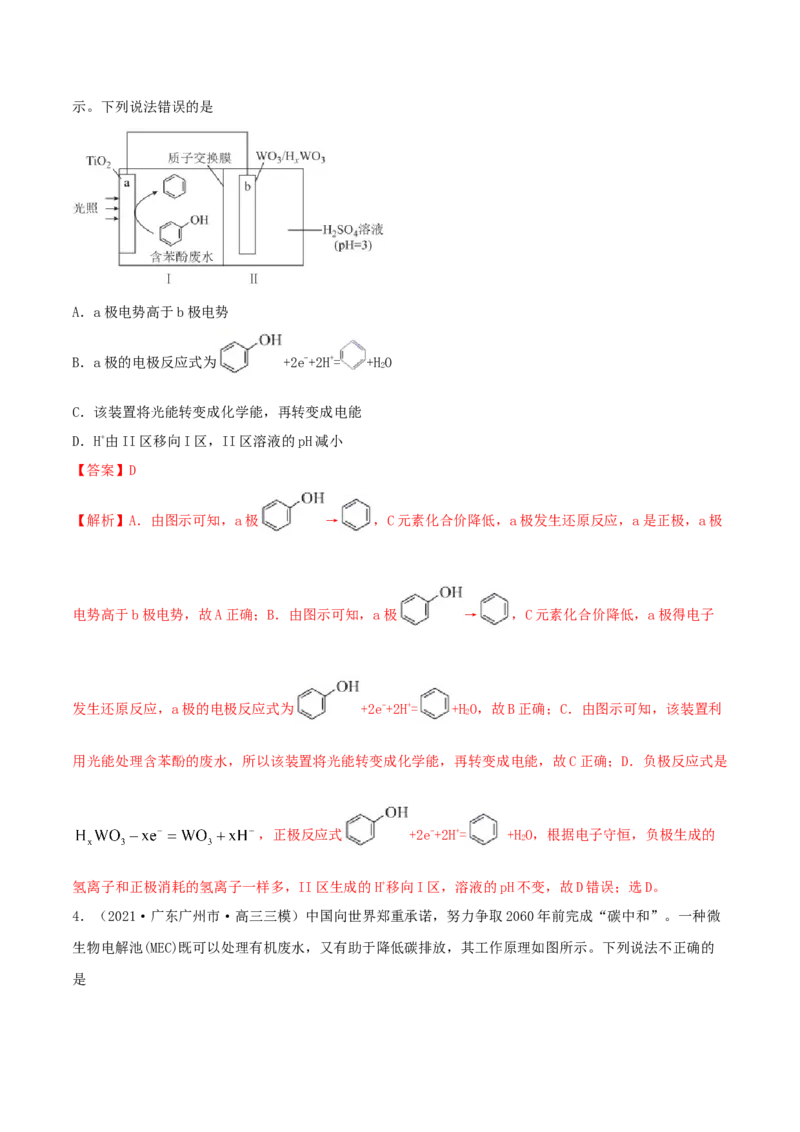
3.(2021·南昌市·江西师大附中高三三模)我国科学家利用光能处理含苯酚( )废水,装置如图所示。下列说法错误的是
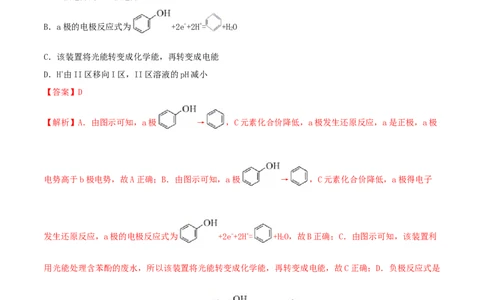
A.a极电势高于b极电势
B.a极的电极反应式为 +2e-+2H+= +HO
2
C.该装置将光能转变成化学能,再转变成电能
D.H+由II区移向I区,II区溶液的pH减小
【答案】D
【解析】A.由图示可知,a极 → ,C元素化合价降低,a极发生还原反应,a是正极,a极
电势高于b极电势,故A正确;B.由图示可知,a极 → ,C元素化合价降低,a极得电子
发生还原反应,a极的电极反应式为 +2e-+2H+= +HO,故B正确;C.由图示可知,该装置利
2
用光能处理含苯酚的废水,所以该装置将光能转变成化学能,再转变成电能,故C正确;D.负极反应式是
,正极反应式 +2e-+2H+= +HO,根据电子守恒,负极生成的
2
氢离子和正极消耗的氢离子一样多,II区生成的H+移向I区,溶液的pH不变,故D错误;选D。
4.(2021·广东广州市·高三三模)中国向世界郑重承诺,努力争取2060年前完成“碳中和”。一种微
生物电解池(MEC)既可以处理有机废水,又有助于降低碳排放,其工作原理如图所示。下列说法不正确的
是A.a电极为MEC的阳极
B.MEC工作时,质子将从a电极室向b电极室迁移
C.b电极的电极反应式为CO+8e-+8H+=CH+2HO
2 4 2
D.a电极室产生的CO 与b电极室消耗的CO 相等
2 2
【答案】D
【解析】电极a上有机质转化为CO,发生氧化反应,所以a为阳极,电极b上CO 转化为CH,发生还原反
2 2 4
应,所以b为阴极。A.电极a上有机质转化为CO,发生氧化反应,所以a为阳极,A正确;B.工作时为
2
电解池,电解池中阳离子由阳极向阴极迁移,所以质子将从a电极室向b电极室迁移,B正确;C.电极b
上CO 得电子被还原,结合迁移过来的氢离子生成CH 和HO,根据电子守恒和元素守恒可得电极反应式为
2 4 2
CO+8e-+8H+=CH+2HO,C正确;D.有机质中C元素的化合价不一定和甲烷中C元素的化合价相同,所以a
2 4 2
电极室产生的CO 与b电极室消耗的CO 不一定相等,D错误;综上所述答案为D。
2 2
5.(2021·江苏盐城市·高三三模)辉铜矿(主要成分CuS)可以用FeCl 溶液漫泡提取铜,反应的离子方
2 3
程式为CuS+4Fe3+=2Cu2++4Fe2++S。CuS可由黄铜矿(主要成分CuFeS)通过电化学反应转变而成,其工作原
2 2 2
理如图所示。下列有关电解CuFeS 的说法正确的是
2
A.a为电源的负极
B.该装置将化学能转化为电能
C.离子交换膜为阴离子交换膜
D.b电极上的反应为:2CuFeS+6H++2e—=CuS+2Fe2++3HS↑
2 2 2【答案】D
【解析】由图可知,该装置为电解池,a电极为电解池的阳极,在硫化氢作用下,铜在阳极失去电子发生
氧化反应生成硫化亚铜和氢离子,电极反应式为2Cu—2e—+HS= CuS+2H+,b电极是阴极,CuFeS 在阴极得
2 2 2
到电子发生还原反应CuS、Fe2+、HS,电极反应式为2CuFeS+6H++2e—=CuS+2Fe2++3HS↑,氢离子通过阳离
2 2 2 2 2
子交换膜,由左室向右室移动。A.由分析可知,该装置为电解池,a电极为电解池的阳极,故A错误;
B.由分析可知,该装置为将电能转化为化学能的电解池,故B错误;C.由分析可知,该装置为电解池,
工作时氢离子通过阳离子交换膜,由左室向右室移动,故C错误;D.由分析可知,该装置为电解池,a电
极为电解池的阳极,在硫化氢作用下,铜在阳极失去电子发生氧化反应生成硫化亚铜和氢离子,电极反应
式为2Cu—2e—+HS= CuS+2H+,故D正确;故选D。
2 2
6.(2021·宁夏吴忠市·高三二模)向如图所示电池中加入稀HSO 酸化,若充电时m侧溶液颜色由蓝色
2 4
变为黄色,则下列叙述正确的是
A.放电时,装置中n电极做正极
B.充电过程中,m极附近pH增大
C.充电过程中,n极发生的电极反应式为V3++e-=V2+
D.放电时,H+从左槽迁移进入右槽
【答案】C
【解析】根据题干信息:充电时m侧溶液颜色由蓝色变为黄色,m侧电极反应式为
,发生氧化反应,m级为电解池的阳极,n级为电解池的阴极,发生的电
极反应为 。A.根据上述分析,m级在电解池中为阳极,放电时为原电池的正极,n电极做原
电池的负极,故A错误;B.充电过程中,m极的电极反应为 ,所以m极附
近pH减小,故B错误;C.充电过程中,n级为电解池的阴极,发生的电极反应为 ,故C正确;D.放电时,H+从负极移动到正极,所以从右槽迁移进入左槽,故D错误;综上答案为C。
7.(2021·广东珠海市·高三二模)2020年7月10日正式上市的比亚迪“汉”汽车,让电动汽车安全达
到一个新高度,其配置磷酸铁锂“刀片电池”放电时的总反应: ,
工作原理如图所示。下列说法正确的是
A.放电时,铝箔作负极
B.放电时,Li+通过隔膜移向负极
C.用充电桩给汽车电池充电的过程中,阴极质量减小
D.充电时的阳极反应式为
【答案】D
【解析】放电时的总反应: ,放电时,铜箔上 失电子为负极,
铝箔上 得电子做正极。A.放电时,铜箔上 失电子为负极,铝箔上 得电子
做正极,A错误;B.放电时,阳离子移向正极,所以Li+通过隔膜移向正极,B错误;C.用充电桩给汽车
电池充电的过程中,阴极反应为: ,质量增加,C错误;D.充电时的阳极反应式
为 ,D正确;答案选D。
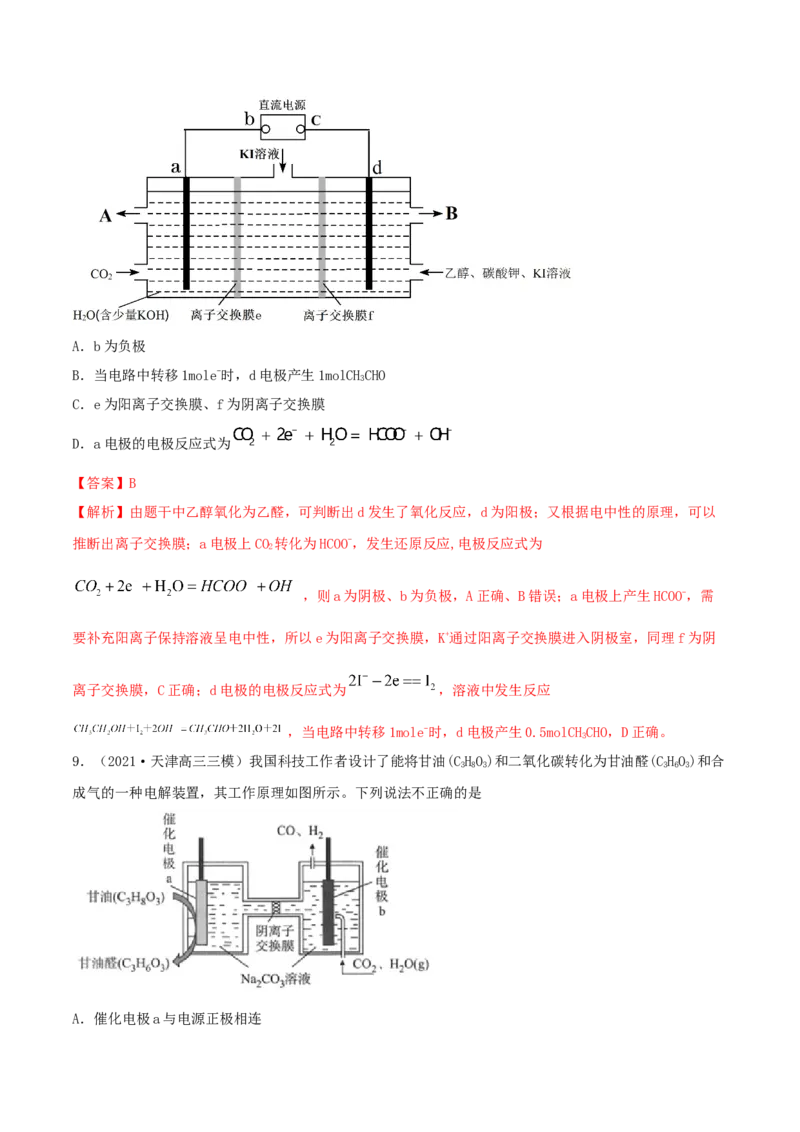
8.(2021·湖北高三二模)科学家设计利用电化学原理回收CO 达到节能减排的目的,实验装置如图所示。
2
已知在碱性条件下,卤素单质可以将乙醇氧化为乙醛,一段时间后测得a电极有HCOO-生成,下列说法不正
确的是A.b为负极
B.当电路中转移1mole-时,d电极产生1molCHCHO
3
C.e为阳离子交换膜、f为阴离子交换膜
D.a电极的电极反应式为
【答案】B
【解析】由题干中乙醇氧化为乙醛,可判断出d发生了氧化反应,d为阳极;又根据电中性的原理,可以
推断出离子交换膜;a电极上CO 转化为HCOO-,发生还原反应,电极反应式为
2
,则a为阴极、b为负极,A正确、B错误;a电极上产生HCOO-,需
要补充阳离子保持溶液呈电中性,所以e为阳离子交换膜,K+通过阳离子交换膜进入阴极室,同理f为阴
离子交换膜,C正确;d电极的电极反应式为 ,溶液中发生反应
,当电路中转移1mole-时,d电极产生0.5molCHCHO,D正确。
3
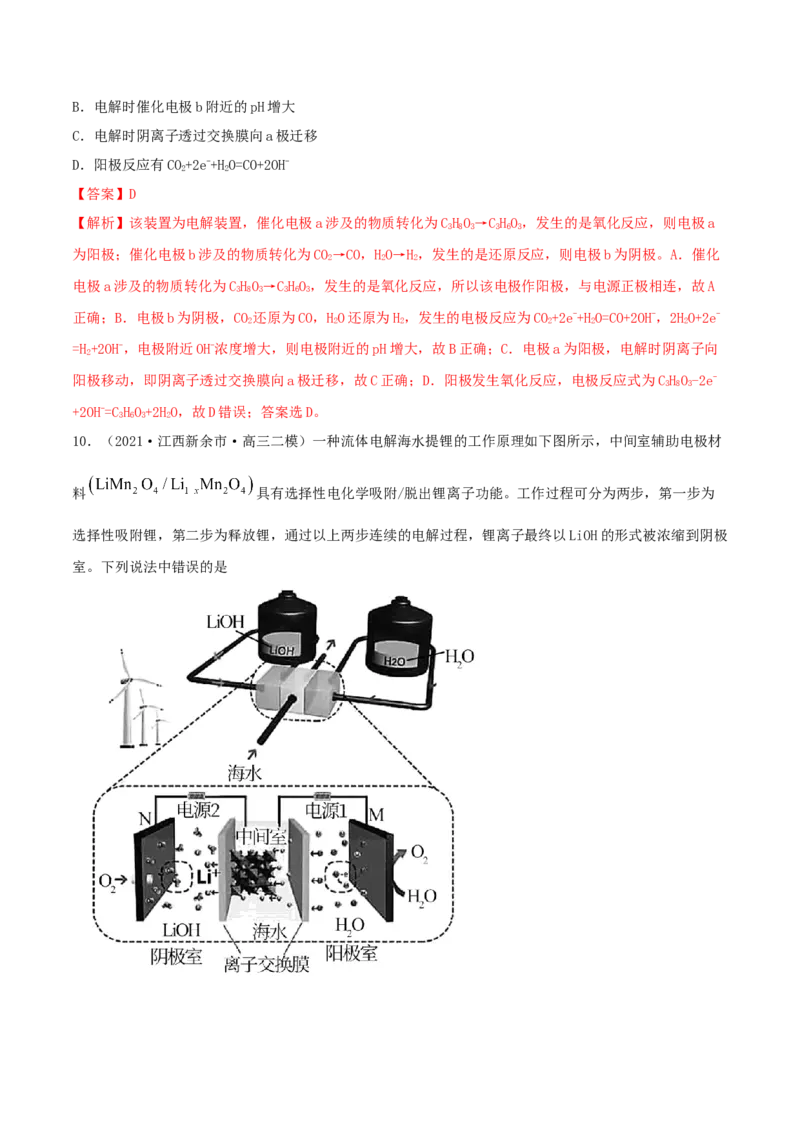
9.(2021·天津高三三模)我国科技工作者设计了能将甘油(CHO)和二氧化碳转化为甘油醛(CHO)和合
3 8 3 3 6 3
成气的一种电解装置,其工作原理如图所示。下列说法不正确的是
A.催化电极a与电源正极相连B.电解时催化电极b附近的pH增大
C.电解时阴离子透过交换膜向a极迁移
D.阳极反应有CO+2e-+HO=CO+2OH-
2 2
【答案】D
【解析】该装置为电解装置,催化电极a涉及的物质转化为CHO→CHO,发生的是氧化反应,则电极a
3 8 3 3 6 3
为阳极;催化电极b涉及的物质转化为CO→CO,HO→H,发生的是还原反应,则电极b为阴极。A.催化
2 2 2
电极a涉及的物质转化为CHO→CHO,发生的是氧化反应,所以该电极作阳极,与电源正极相连,故A
3 8 3 3 6 3
正确;B.电极b为阴极,CO 还原为CO,HO还原为H,发生的电极反应为CO+2e-+HO=CO+2OH-,2HO+2e-
2 2 2 2 2 2
=H+2OH-,电极附近OH-浓度增大,则电极附近的pH增大,故B正确;C.电极a为阳极,电解时阴离子向
2
阳极移动,即阴离子透过交换膜向a极迁移,故C正确;D.阳极发生氧化反应,电极反应式为CHO-2e-
3 8 3
+2OH-=CHO+2HO,故D错误;答案选D。
3 6 3 2
10.(2021·江西新余市·高三二模)一种流体电解海水提锂的工作原理如下图所示,中间室辅助电极材
料 具有选择性电化学吸附/脱出锂离子功能。工作过程可分为两步,第一步为
选择性吸附锂,第二步为释放锂,通过以上两步连续的电解过程,锂离子最终以LiOH的形式被浓缩到阴极
室。下列说法中错误的是A.第一步接通电源1选择性提取锂:第二步接通电源2释放锂
B.释放锂过程中,中间室材料应接电源负极,发生的电极反应式为
C.中间室两侧的离子交换膜选用阳离子交换膜
D.当阴极室得到4.8gLiOH时,理论上阳极室产生1.12L气体(标准状态下)
【答案】B
【解析】A. 第一步接通电源1,中间室为阴极,发生反应 ,选择
性提取锂,第二步接通电源2,中间室为阴极,发生反应 释放锂,
故A正确;B. 释放锂过程中,中间室材料应接电源正极,发生的电极反应式为
,故B错误;C. 根据图示,第一步为选择性吸附锂过程中阳极室中的离子
向中间室移动,第二步为释放锂的过程中锂离子移向阴极室,所以中间室两侧的离子交换膜选用阳离子交
换膜,故C正确;D.当阴极室得到4.8gLiOH时,电路中转移0.2mol电子,阳极室电极反应式是
,产生氧气的体积是 1.12L气体(标准状态下),故D正确;选B。
11.(2021·四川南充市·高三三模)科学家最近设计出了质子膜HS电池,实现了HS废气变废为宝,电
2 2
池结构原理如图,下列相关说法正确的是
A.电极a为正极,发生还原反应
B.H+经过固体电解质膜向a电极移动
C.电极b的反应为:O+4e-+4H+=2HO
2 2
D.用该电池进行粗铜的精炼,当电路中转移2 mol e-时,阳极减轻64g
【答案】C
【解析】由图可知HS在电极a发生氧化反应转化为S,因此电极a为负极,电极b为正极。A.由分析可
2 2知电极a为负极,发生氧化反应,A错误;B.电解质中阳离子移向正极,因此H+经过固体电解质膜向b电
极移动,B错误;C.电极b为正极,氧气在正极得电子,发生还原反应,电极反应式为O+4e-+4H+
2
=2HO,C正确;D.电解精炼铜时,粗铜作阳极,粗铜中比铜活泼的金属先失电子,因此当电路中转移2
2
mol e-时,阳极减轻的质量不为1molCu的质量,即64g,D错误;答案选C。
12.(2021·江西九江市·高三一模)结合 溶液,可利用微生物电化学技术实现将含乙醛的废水
有效处理,其工作原理如图所示,下列有关说法正确的是
A.该反应在高温下,反应速率加快
B.右侧电极为负极,发生还原反应
C.当有 通过电解质溶液,将有 生成
D.左侧电极反应式为:
【答案】D
【解析】A.该反应是利用微生物电化学技术,微生物在高温下活性会降低,高温下,反应速率反而会减
慢,故A说法错误;B.根据工作原理图,右侧是Cr元素的粒子从电极上得到电子,故右侧电极为正极,
发生还原反应,故B说法错误;C.电子只能从负极沿外接线路到达正极,不能通过电解质溶液,故C说法
错误;D.左侧是乙醛在微生物上失去电子被氧化成CO,失去电子就使左侧电极反应式左边整体上带正电
2
荷,则电极反应式右边也必然带正电荷,带正电荷的必然是H+,结合质量守恒定律,则整个电极反应式为
,故D正确;本题答案D。
二、主观题(共3小题,共40分)
13.(2020·陕西西安市·交大附中高三三模)(10分)(1)全固态锂离子电池的结构如图所示,放电
时电池反应为 2Li+MgH=Mg+2LiH。放电时,X 极作_________极。充电时,Y 极反应式为___________。
2(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳
酸根离子)。
①阳极的电极反应式为 ________________
②简述浓缩室中得到浓乳酸的原理:________________
③电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的OH-可忽略不计。400
mL 10 g∙L −1 乳酸溶液通电一段时间后,浓度上升为 145 g∙L −1 (溶液体积变化忽略不计),阴极上产生的
H 在标准状况下的体积约为_____________L。(乳酸的摩尔质量为90 g•mol-1)
2
【答案】(每空2分)(1)正 LiH + e- = Li +H-
⑵①4OH- − 4e- = O↑+ 2HO
2 2
②阳极室中的H+穿过阳离子交换膜与阴极室中穿过阴离子交换膜的A-离子在浓缩室结合生成HA
③6.72
【解析】⑴全固态锂离子电池的结构如图所示,放电时电池反应为 2Li+MgH = Mg+2LiH。Li化合价升高
2
失去电子,放电时,作负极,MgH 作正极,因此放电时,X极作正极,充电时,Y极为阴极,其电极反应式
2
为LiH + e- = Li +H-,故答案为:正;LiH + e- = Li +H-;
⑵①阳极上阴离子得到电子,即水中的氢氧根得到电子,其电极反应式为4OH- − 4e- = O↑+ 2HO,故
2 2
答案为:4OH- − 4e- = O↑+ 2HO;
2 2
②简述浓缩室中得到浓乳酸的原理:阳极室中的H+穿过阳离子交换膜与阴极室中穿过阴离子交换膜的A-离
子在浓缩室结合生成HA,故答案为:阳极室中的H+穿过阳离子交换膜与阴极室中穿过阴离子交换膜的A-
离子在浓缩室结合生成HA;
③400 mL 10 g∙L −1 乳酸溶液通电一段时间后,浓度上升为 145 g∙L −1 (溶液体积变化忽略不计),则增加
的乳酸的质量为(145 g∙L −1−10 g∙L −1)×0.4L=54g,增加的乳酸的物质的量为,根据2HA —2A-—H 关系得到阴极上产生的 H 的物质的量为
2 2
,在标准状况下的体积约为0.3mol×22.4 L∙mol −1 = 6.72L,故答案
为:6.72。
14.(12分)二氧化硫在生产和生活中有着广泛的用途。
(1)用足量NaOH溶液吸收尾气中的SO,反应的离子方程式为______;吸收后的浓溶液可用图1的装置再
2
生循环脱硫,并制得硫酸,电极a的电极反应为_____,乙是____。
(2)可设计二氧化硫空气质子交换膜燃料电池处理尾气中的二氧化硫,原理如图2所示。其能量转化的主
要形式是______,c电极是__极,移动的离子及方向是____。
【答案】(每空2分)(1)SO+2OH-=SO2-+HO 2HO+2e-= H↑+2OH-(或2H++2e-=H↑) 浓度较大的
2 4 2 2 2 2
HSO 溶液
2 4
(2)化学能转化成电能 负 H+由c电极通过质子交换膜向d电极移动
【解析】(1)用足量NaOH溶液吸收尾气中的SO,反应生成亚硫酸钠,反应的离子方程式为SO+2OH-=SO2-
2 2 3
+HO;吸收后的浓溶液可再生循环脱硫,并制得硫酸,根据图示,电极a为阴极,溶液中的氢离子放电发
2
生还原反应,电极反应为2HO+2e-= H↑+2OH-(或2H++2e-=H↑),电极b为阳极,SO2-在阳极发生氧化反应
2 2 2 3
生成硫酸,因此乙是浓度较大的HSO 溶液,故答案为SO+2OH-=SO2-+HO;2HO+2e-= H↑+2OH-(或2H++2e-
2 4 2 3 2 2 2
=H↑);浓度较大的HSO 溶液;
2 2 4
(2)二氧化硫空气质子交换膜燃料电池属于原电池,原电池的能量转化是化学能转化成电能,二氧化硫为
燃料,在负极上发生氧化反应,通入空气的电极为正极,因此c电极是负极,溶液中的氢离子由c电极通
过质子交换膜向d电极移动,故答案为化学能转化成电能;负;H+由c电极通过质子交换膜向d电极移动。
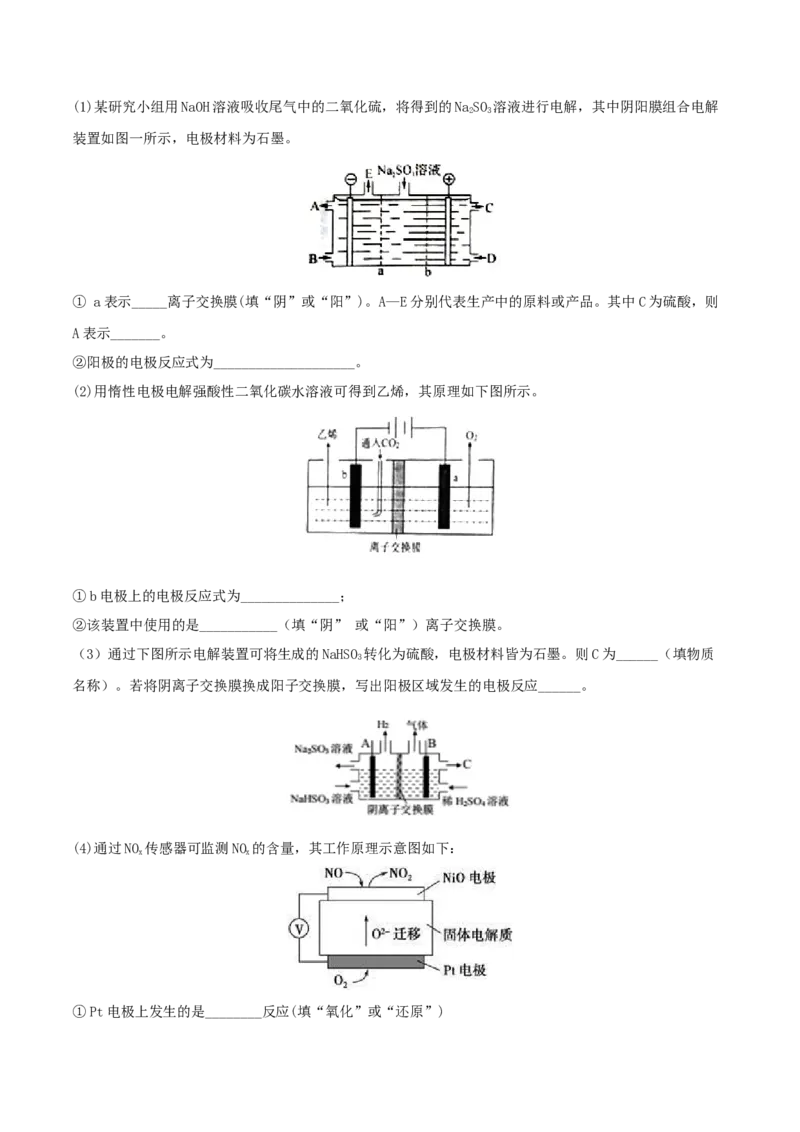
15.(18分)电化学在工业生产中有重要作用(1)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的NaSO 溶液进行电解,其中阴阳膜组合电解
2 3
装置如图一所示,电极材料为石墨。
① a表示_____离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品。其中C为硫酸,则
A表示_______。
②阳极的电极反应式为____________________。
(2)用惰性电极电解强酸性二氧化碳水溶液可得到乙烯,其原理如下图所示。
①b电极上的电极反应式为______________;
②该装置中使用的是___________(填“阴” 或“阳”)离子交换膜。
(3)通过下图所示电解装置可将生成的NaHSO 转化为硫酸,电极材料皆为石墨。则C为______(填物质
3
名称)。若将阴离子交换膜换成阳子交换膜,写出阳极区域发生的电极反应______。
(4)通过NO 传感器可监测NO 的含量,其工作原理示意图如下:
x x
①Pt电极上发生的是________反应(填“氧化”或“还原”)②写出NiO电极的电极反应式:______________________________________。
【答案】(每空2分)(1)①阳 NaOH溶液 ②SO2--2e-+HO=2H++SO2-
3 2 4
(2)①2CO+12e-+12H+=CH+HO ②阳
2 2 4 2
(3)较浓的硫酸溶液 4OH--4e-=O +2HO或2HO-4e-=O +4H+
2 2 2 2
(4)①还原 ②NO+O2--2e-=NO
2
【解析】(1)①从C为硫酸可知,硫酸根来源于亚硫酸根放电.故b为阴离子交换膜,a为阳离子交换膜,
在阴极区应为水放电生成氢气和氢氧根离子,故A为氢氧化钠,E为氢气,故答案为阳;NaOH溶液;
②阳极应为亚硫酸根放电生成硫酸根,反应的离子方程式为SO2--2e-+HO=2H++SO2-,故答案为SO2--2e-
3 2 4 3
+HO=2H++SO2- ;
2 4
(2)①b电极与电源的负极相连,作阴极,溶液中的CO 得到电子转化为乙烯,溶液显酸性,因此阴极上的
2
电极反应式为2CO+12e-+12H+=CH+HO;②为了防止氢氧根离子与CO 反应,因此该装置中使用的是阳离子
2 2 4 2 2
交换膜。
(3)电解时,由HSO-转变成SO2-的过程中S元素失去电子被氧化,该反应在阳极发生。反应原理为 HSO-
3 4 3
-2e-+HO=SO2-+3H+,生成的H+使阳极区域酸性增强,部分HSO-与H+反应生成SO 气体。阴极2H++2e-=H↑,
2 4 3 2 2
所以A是电解池的阴极,B是阳极。从阴极通入的NaHSO 的HSO-通过阴离子交换膜进入阳极,放电生成
3 3
SO2-,使得阳极区域通入的稀硫酸转变成较浓的硫酸后导出,所以C导出的是较浓的硫酸。如果将阴离子
4
交换膜改成阳离子交换膜,则HSO-离子不能进入阳极区域,则阳极区域OH-放电生成O ,即4OH--4e-=O
3 2 2
+2HO。
2
(4)①铂电极上氧气得电子生成氧离子而被还原,答案为:还原;②NiO电极上NO失电子和氧离子反应
生成二氧化氮,所以电极反应式为:NO+O2--2e-=NO,答案为:NO+O2--2e-=NO.
2 2