文档内容
第六章 化学反应与能量
第19讲 电解池 金属的电化学腐蚀与防护(精练)
完卷时间:50分钟
可能用到的相对原子质量:H1 N14 O16 Na23 S32 Cl35.5 K39 Cu64
一、选择题(每小题只有一个正确选项,共12*5分)
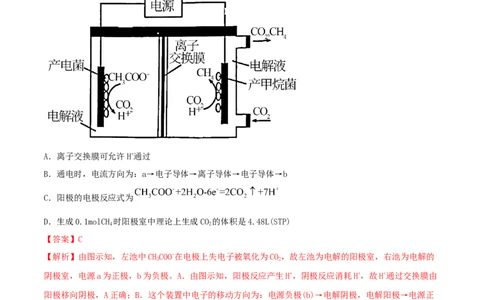
1.(2021·山东潍坊市·高三三模)将电化学法和生物还原法有机结合,利用微生物电化学方法生产甲
烷,装置如图所示。下列说法错误的是
A.离子交换膜可允许H+通过
B.通电时,电流方向为:a→电子导体→离子导体→电子导体→b
C.阳极的电极反应式为
D.生成0.1molCH 时阳极室中理论上生成CO 的体积是4.48L(STP)
4 2
【答案】C
【解析】由图示知,左池中CHCOO-在电极上失电子被氧化为CO,故左池为电解的阳极室,右池为电解的
3 2
阴极室,电源a为正极,b为负极。A.由图示知,阳极反应产生H+,阴极反应消耗H+,故H+通过交换膜由
阳极移向阴极,A正确;B.这个装置中电子的移动方向为:电源负极(b)→电解阴极,电解阳极→电源正
极(a),故电流方向为:电源正极(a)→外电路(电子导体)→电解质溶液(离子导体,阳极→阴极)→外电路
(电子导体)→电源负极(b),形成闭合回路,B正确;C.由分析知,左池为阳极,初步确定电极反应为:
CHCOO--8e-→2CO↑,根据图示知可添加H+配平电荷守恒,添加HO配平元素守恒,得完整方程式为:
3 2 2
CHCOO--8e-+2HO→2CO↑+7H+,C错误;D.由图示知,右池生成CO 转化为CH,根据转移电子关系
3 2 2 2 4
CH~8e-,0.1 mol CH 生成转移0.8 mol电子,由C选项知:CO~4e-,故生成CO 的n(CO)=
4 4 2 2 2,故V(CO)=0.2 mol×22.4 L/mol=4.48 L,D正确;故答案选C。
2
2.(2021·辽宁高三三模)如图是电化学膜法脱硫过程示意图,电化学膜的主要材料是碳和熔融的碳酸
盐。下列说法错误的是
A.工作一段时间后,生成H 和S 的物质的量之比为2:1
2 2
B.净化气中CO 含量明显增加,是电化学膜中的碳被氧化
2
C.阴极反应式为HS+2e-=S2-+H↑
2 2
D.b电极为阳极,发生氧化反应
【答案】B
【解析】由图示可知,该装置为电解池,HS发生反应生成S2-和H,可知a电极为阴极,电极反应式为
2 2
HS+2e-=S2-+H↑,则b电极为阳极,S2-在阳极失去电子发生氧化反应生成S,电极反应式为2 S2--4e-=
2 2 2
S。A.根据得失电子守恒可知,电解池上作一段时间后,转移相同物质的量的电子时,生成H 和S 的物
2 2 2
质的量之比为2:1,故A正确;B.HS是酸性气体,能够和熔融碳酸盐反应生成CO,所以净化气中CO 含
2 2 2
量明显增加,故B错误;C.由上述分析可知,阴极的电极反应式为HS+2e-=S2-+H↑,故C正确;D.由上
2 2
述分析可知,b电极为阳极,阳极上发生的是氧化反应,故D正确;故选B。
3.(2021·江西南昌市·高三二模)北京化工大学新开发的一种流动电池如图所示,其原理是:
,该电池的主要特点是可以通过电解质溶液的循环流动,
在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。下列说法不正确的是A.b为该电池的负极
B.a电极的反应式为:
C.当电池工作时, 两电极的质量之和几乎不变
D.调节电解质溶液,即补充一定量的 溶液和 溶液
【答案】D
【解析】A.根据 分析铜化合价升高,是原电池的负极,
因此b为该电池的负极,故A正确;B.根据总反应方程式a极是PbO 得到电子,因此a电极的反应式为:
2
,故B正确;. ,当
电池工作时,a极由1mol PbO 变为1mol PbSO,质量相当增加了1mol SO 即64g,b极减少1mol Cu即
2 4 2
64g,因此 两电极的质量之和几乎不变,故C正确;D. 在不断消耗,因此调节电解质溶液,
即补充一定量的 溶液,故D错误。综上所述,答案为D。
4.(2021·广东汕头市·高三二模)2021年3月5日,李克强总理在国务院政府报告中指出,扎实做好
碳达峰、碳中和各项工作。科研工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为
2
CO,实现节能减排的目标。如图所示,下列有关说法正确的是A.N极为阴极
B.离子交换膜为阴离子交换膜
C.阳极的电极反应式为CO+2e-+2H+=CO+HO
2 2
D.理论上该装置在工作时,HPO 与KHPO 缓冲溶液的pH保持不变
3 4 2 4
【答案】D
【解析】由图示知,该装置外电路有光伏电池(将太阳能转化为电能),故为电解池装置,在P极上,CO
2
得电子转化为CO,故P极为阴极,N极为阳极,阴极电极反应为:CO+2H++2e-=CO+HO,需要缓冲溶液提供
2 2
H+,故离子交换膜为阳离子交换膜,阳极电极反应为:2HO-4e-=O↑+4H+。A.由分析知,N极为阳极,A错
2 2
误;B.由分析知,离子交换膜为阳离子交换膜,B错误;C.由分子知,CO 在阴极转化为CO,故选项所写
2
电极反应为阴极电极反应,C错误;D.根据得失电子守恒和阴阳极电极反应知,缓冲溶液流入阴极的H+和
阳极流入缓冲溶液的H+数目相等,故缓冲溶液中c(H+)保持不变,故pH保持不变,D正确;故答案选D。
5.(2021·黑龙江高三二模)次磷酸钴[Co(HPO)]广泛应用于化学电镀,工业上利用电渗析法制取次磷
2 2 2
酸钴的原理如图所示。下列说法中正确的是
A.b为电源的负极,膜Ⅱ为阴离子交换膜
B.当阴极生成224mL(标准状况)气体时,通过膜Ⅲ的离子的物质的量为0.01mol
C.M电极反应为Co+2 -2e-=Co(HPO)
2 2 2
D.电解过程中,阴极室c(NaOH)逐渐增大
【答案】D【解析】膜Ⅰ和膜Ⅲ之间为产品室, 经膜Ⅲ进入产品室,膜Ⅲ为阴离子交换膜,Co2+经膜Ⅰ进入产
品室,则M为Co,为电解池的阳极,则a为电源的正极,N为阴极,b为电源的负极,膜Ⅱ为阳离子交换膜,
防止OH-进入原料室消耗 。A.根据分析,b为电源的负极,膜Ⅱ为阳离子交换膜,故A不符合题意;
B.b为电源的负极,N为阴极,电极反应为:2HO+2e-=H↑+2OH-,当阴极生成224mL(标准状况)气体时,
2 2
n(H)= = =0.01mol,转移的电子的物质的量为0.02mol, 带一个单位的负电荷,故
2
通过膜Ⅲ的离子的物质的量为0.02mol,故B不符合题意;C.M为Co,为电解池的阳极,M电极产生
Co2+,反应为Co-2e-=Co2+,故C不符合题意;D.电解过程中,阴极反应为:2HO+2e-=H↑+2OH-,产生了
2 2
OH-,膜Ⅱ为阳离子交换膜,Na+进入阴极,阴极室c(NaOH)逐渐增大,故D符合题意;答案选D。
6.(2021·四川泸州市·高三二模)已知Fe2+与HO 溶液混合发生Fenton反应生成氧化性很强的羟基自
2 2
由基(•OH),可将CN-氧化为低毒的CNO-,实现废水处理的目的。三维电极电解-Fenton反应处理废水的原
理如图所示,多孔焦炭电极将整个电解槽变成了许多微电解池。下列说法错误的是
A.钛合金电极反应式为2HO- 2e- =2H++2•OH
2
B.阴极电极反应式为O+ 2H++ 2e - = HO
2 2 2
C.焦炭电极表面能产生•OH使废水处理效率提高
D.Fe(OH)2+能在钛合金电极实现再生循环利用
【答案】D
【解析】由图示知,钛合金电极连接电源正极,作电解的阳极,HO在电极表面放电生成·OH和H+,电极
2
反应为:2HO-2e- =2H++2·OH,石墨电极为电解的阴极,O 在电极表面得电子生成HO,电极反应为:
2 2 2 2
O+2e-+2H+=HO。A.由分析知,A正确;B.由分析知,B正确;C.多孔焦炭电极将整个电解槽变成许多微
2 2 2电解池,其作阳极的部分对应电极反应与钛合金电极相同,也可产生·OH,使废水处理效率提高,C正确;
D.Fe(OH)2+中Fe元素为+3价,变回Fe2+需得电子,故可在石墨电极(阴极)上再生循环,D错误;故答案
选D。
7.(2021·天津高三一模)近期,天津大学化学团队以CO 与辛胺为原料实现了甲酸和辛腈的高选择性合
2
成,装置工作原理如图。下列说法正确的是
A.NiP电极与电源负极相连
2
B.辛胺转化为辛腈发生了还原反应
C.In/InO 电极上可能有副产物H 生成
2 3-x 2
D.在In/InO 电极上发生的反应为CO+HO-2e-=HCOO-+OH-
2 3-x 2 2
【答案】C
【解析】A.根据电解质“异性相吸”原理,氢氧根向NiP电极移动,说明NiP电极为阳极,与电源正极
2 2
相连,故A错误;B.左侧CO 变为HCOO-,化合价降低,发生还原反应,则辛胺在阳极转化为辛腈发生了
2
氧化反应,故B错误;C.In/InO 电极为阴极,阴极可能有氢离子得到电子,因此可能有副产物H 生成,
2 3-x 2
故C正确;D.In/InO 电极为阴极,根据图中信息,阴极上发生的反应为CO+HO+2e-=HCOO-+OH-,故D
2 3-x 2 2
错误。综上所述,答案为C。
8.(2020·吉林长春市·东北师大附中高三二模)为了抵御海水的侵蚀,往往会在船体上安装大型的锌
块,利用原电池反应:2Zn+2HO+O=2Zn(OH),下列说法正确的是
2 2 2
A.锌块发生还原反应而被腐蚀
B.船体与海水中的NaCl等发生反应
C.正极的电极反应式为:2HO+2e-=H↑+2OH-
2 2
D.该抵御措施称为牺牲阳极的阴极保护法
【答案】D
【解析】A.在船体上安装大型的锌块可以构成锌铁海水原电池,锌的金属性强于铁,锌做负极,失去电子发生氧化反应而被腐蚀,故A错误;B.在船体上安装大型的锌块可以构成锌铁海水原电池,反应的实质是
锌与海水中溶解的氧气反应,不与海水中的NaCl等发生反应,故B错误;C.在船体上安装大型的锌块可以
构成锌铁海水原电池,氧气在正极上得到电子发生还原反应,电极反应式为O+4e-+2HO =4OH-,故C错误;
2 2
D.在船体上安装大型的锌块可以构成锌铁海水原电池保护船体的措施为牺牲阳极的阴极保护法,故D正确;
故选D。
9.(2020·辽宁高三二模)青钢的出现是人类从石器时代走向新时代的里程碑,中国古代的青铜器铸造
工艺、造型艺术,在世界上享有极高的声誉。下列说法错误的是
A.“曾青得铁则化为铜”描述的是一个置换反应
B.我国已知最大的青铜器后母戊鼎,是一种铜合金制品
C.青铜器中含有锡、铅,发生电化学腐蚀时铜为正极
D.出土的古代青铜器表面的铜绿是一种铜的氧化物
【答案】D
【解析】A.“曾青得铁则化为铜”描述的是铁与硫酸铜反应生成铜和硫酸亚铁的反应,是置换反应故A正
确;B.青铜是铜、锡、铅按一定比例铸造而成的,是一种铜合金,故B正确;C.锡、铅比铜活泼,在发生
电化学腐蚀时,铜为正极,故C正确;D.铜绿的化学成分是碱式碳酸铜,不是氧化物,故D错误。故答案
为D
10.(2021·江西鹰潭市·高三一模)碱性硼化钒(VB)一空气电池工作时反应为
2
。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。
当外电路中通过 电子时,B装置内共收集到 气体(标准状况下),则下列说法不正确的是
A.VB 电极发生的电极反应为
2
B.外电路中电流由c电极流向VB 电极
2
C.电解过程中,b电极表面有气泡产生
D.若B装置内的液体体积为 ,则 溶液的物质的量浓度为【答案】D
【解析】A.根据碱性硼化钒(VB)一空气电池工作时反应为 得到VB 是原
2 2
电池的正极,其电极发生的电极反应为 ,故A正确;
B.外电路中电流由a极流向b极,再从c电极流向VB 电极,故B正确;C.根据图中信息得到B为电解池,
2
因此在电解过程中,b为阳极,b电极表面有氧气产生,故C正确;D.当外电路中通过 电子时,
B装置内共收集到 气体(标准状况下),则阴极产生氢气根据2HO-4e-=O↑+4H+,因此生成
2 2
0.01mol氢气即标准状况下0.224L,说明阴极生成了氢气,则先发生Cu2++2e-=Cu,再发生2HO+2e-=
2
H↑+2OH-,由于共生成0.448L气体,说明产生了0.224L氢气即0.01mol,转移电子0.02mol,根据转移
2
电子数目相等,因此铜离子得到0.02mol电子,即n(Cu2+)=0.01mol,若B装置内的液体体积为 ,
则 溶液的物质的量浓度大于等于 ,故D错误。综上所述,答案为D。
11.(2021·南昌市八一中学高三三模)以NaCl溶液模拟海水,采用惰性电极处理有机废水的装置如图所
示(以含 的溶液为例)。下列说法不正确的是
A.负极反应为
B.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上最多可除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为1:2
【答案】D
【解析】该装置为原电池,有机废水中的CHCOO-发生失电子的氧化反应生成CO,则a极为负极,电极反
3 2
应式为CHCOO-+2HO-8e-═2CO↑+7H+,b极为正极,酸性条件下,H+得电子生成H,反应式为2H++2e-
3 2 2 2
═H↑,原电池工作时,阴离子移向负极、阳离子移向正极,即模拟海水NaCl溶液中的Na+通过阳离子交
2换膜移向b极、Cl-通过阴离子交换膜移向a极,则隔膜1为阴离子交换膜,隔膜2为阳离子交换膜。A.该
原电池中a极为负极,b极为正极,有机废水中的CHCOO-在负极失电子生成CO,电极反应式为CHCOO-
3 2 3
+2HO-8e-═2CO↑+7H+,故A正确;B.原电池工作时,阴离子移向负极、阳离子移向正极,即NaCl溶液
2 2
中的Na+通过阳离子交换膜移向b极、Cl-通过阴离子交换膜移向a极,达到海水淡化目的,所以隔膜1为
阴离子交换膜,隔膜2为阳离子交换膜,故B正确;C.由于电子与Na+、Cl-所带电荷数相等,所以电路中
转移1mol电子时,通过离子交换膜的Na+、Cl-物质的量均为1mol,质量为1mol×58.5g/mol=58.5g,即模
拟海水理论上除盐58.5g,故C正确;D.负极反应式为CHCOO-+2HO-8e-═2CO↑+7H+,正极反应式为2H+
3 2 2
+2e-═H↑,若转移8mole-电子时正极得到4molH、负极得到2molCO,即正、负极产生气体的物质的量之
2 2 2
比为2:1,故D错误;故选:D。
12.(2021·安徽蚌埠市·高三三模)我国科学家最近发明了一种Zn-PbO 二次电池,内部结构如图所示。
2
电解质分别为KSO、HSO 和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个区域。放电后B区域
2 4 2 4
电解质溶液浓度增加。下列说法不正确的是
A.电池中PbO 为正极
2
B.B区域的电解质为KSO 溶液
2 4
C.图中的b膜为阳离子交换膜
D.当电路中转移0.2mol电子时,B区溶质质量增大17.4g
【答案】C
【解析】A.Zn与PbO 构成原电池,Zn Zn(OH)2-,Zn失电子为负极,则PbO 为正极,故A正确;B.A
2 4 2
区域发生反应:Zn Zn(OH)2-,A为碱性区域,故A为KOH,C中应为酸性条件,故C为HSO,故B为
4 2 4
KSO 溶液,故B正确;C.B为KSO,B中的SO2-是由C中硫酸溶液提供,b需要能使阴离子通过,故b为
2 4 2 4 4
阴离子交换膜,故C错误;D.闭合回路中电荷转移守恒可知,0.2mol电子转移时,溶液中应该有
0.2molK+和0.1molSO2-,B区域中KSO 物质的量增加0.1mol,质量增加17.4g,故D正确;故选C。
4 2 4
二、主观题(共3小题,共40分)
13.(2020·山东高三期中)(12分)电化学在我们的工业生产、生活中发挥着越来越大的作用。根据题
给信息,回答问题:(1)电化学降解法治理硝酸盐污染的工作原理如图所示。
①A为直流电源的______极。
②Ag-Pt电极发生的电极反应为______。
③当阳极室溶液质量减少45g,则阴极室溶液质量减少__g。
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给
信息回答下列问题:
①交换膜a是____(填“阴离子”“阳离子”)交换膜。
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:_____。
③当浓缩室得到1L0.6mol/L盐酸时,转移电子____mol。
【答案】(每空2分)(1)①正 ②2NO +10e-+12H+=N↑+6HO ③9
2 2
(2)①阳离子 ②pH过高,Ni2+可能转变为Ni(OH) 沉淀,pH过低,溶液中H+浓度较大,氢离子在阴
2
极放电,Ni2+被还原的量减少,所以镍的回收率都低 ③0.5
【解析】(1)①由题给示意图可知,硝酸根离子中氮元素化合价降低,说明硝酸根离子得电子发生还原
反应生成氮气,则Ag-Pt电极为电解池的阴极,Pt电极为电解池的阳极,则与Pt电极相连的直流电源的A
电极为正极,故答案为:正;
②由分析可知,Ag-Pt电极为电解池的阴极,硝酸根离子在阴极得电子发生还原反应生成氮气,电极反应
式为2 +10e-+12H+=N↑+6HO,故答案为:2 +10e-+12H+=N↑+6HO;
2 2 2 2
③阳极反应式为2HO-4e-=O +4H+,若阳极转移2mol电子,阳极消耗1mol水,同时生成2mol氢离子通过
2 2
质子交换膜进入阴极区,减少质量为18g,阴极室放出0.2mol氮气,同时有2mol氢离子进入,阴极室质
量减少为0.2mol 28g/mol-2mol 1g/mol=3.6g,则当阳极室溶液质量减少45g,则阴极室溶液质量减少g=9g,故答案为:9;
(2)阳极区域是稀硫酸,阳极氢氧根离子失电子生成氧气,氢离子通过交换膜a进入浓缩室,所以交换膜
a为阳离子交换膜,阴极发生还原反应,酸性强时主要氢离子发生还原反应生成氢气,酸性弱时主要
Ni2+发生还原反应生成Ni。①由分析可知,交换膜a为阳离子交换膜,故答案为:阳离子;②根据图乙可
知,若溶液pH过高,Ni2+可能转变为Ni(OH) 沉淀,若pH过低,溶液中H+浓度较大,氢离子在阴极放电,
2
Ni2+被还原的量减少,所以镍的回收率都低,故答案为:pH过高,Ni2+可能转变为Ni(OH) 沉淀,pH过低,
2
溶液中H+浓度较大,氢离子在阴极放电,Ni2+被还原的量减少,所以镍的回收率都低;③当浓缩室得到
1L0.6mol/L盐酸时,溶液中氢离子增大的物质的量为0.5mol,则转移电子的物质的量0.5mol,故答案为:
0.5。
14.(2020·山东师范大学附中高三期中)(12分)利用电化学原理,将NO、O 和熔融KNO 制成燃料电
2 2 3
池,模拟工业电解法来处理含CrO 废水,如下图所示;电解过程中溶液发生反应:CrO +6Fe2++14H+
2 2
===2Cr3++6Fe3++7HO。
2
(1)甲池工作时,NO 转变成绿色硝化剂Y,Y是NO,可循环使用。则石墨Ⅰ是电池的________极;石墨
2 2 5
Ⅰ附近发生的电极反应式为___________________。
(2)工作时,甲池内的NO 向___________极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的
O 和NO 的体积比为____________。
2 2
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为_________________________________。
(4)若溶液中减少了0.01 mol CrO ,则电路中至少转移了___________mol电子。
2
【答案】(每空2分)(1)负 NO+NO -e-===NO
2 2 5
(2)石墨Ⅰ 1∶4
(3) Fe-2e-===Fe2+
(4)0.12
【解析】(1)甲池工作时,NO 转变成NO,说明氮元素的化合价升高,石墨Ⅰ为负极,电极反应式为
2 2 5
NO+NO--e-=NO,石墨Ⅱ为正极,故答案为负;NO+NO--e-=NO;
2 3 2 5 2 3 2 5
(2)由于石墨Ⅰ为负极,原电池中阴离子向负极移动,根据得失电子守恒计算1molO 反应中转移4mol电子,
24molNO 转变成NO,转移4mol电子,相同状况下气体的体积比等于物质的量之比,故O 和NO 的体积比为
2 2 5 2 2
1:4,故答案为石墨Ⅰ;1:4;
(3)由于石墨Ⅰ为负极,故Fe(Ⅰ)为阳极,铁失去电子生成亚铁离子,电极反应为Fe-2e-=Fe2+,故答案为
Fe-2e-=Fe2+;
(4) 根据CrO2-+6Fe2++14H+===2Cr3++6Fe3++7HO,0.01mol CrO2-能够氧化0.06mol Fe2+,即电解
2 7 2 2 7
过程中需要生成0.06mol Fe2+,Fe(I)为阳极,电极反应式为Fe-2e-= Fe2+,故转移电子的物质的量为
0.06mol×2= 0.12mol,故答案为0.12。
点睛:本题考查原电池与电解原理,明确各个电极上发生的反应、物质之间的转化是解本题关键。本题的
难点是(4)的计算,需要根据CrO2-+6Fe2++14H+===2Cr3++6Fe3++7HO计算出电解过程中生成的Fe2+,
2 7 2
再根据电极反应式进行计算,注意电路中转移的电子与CrO2-+6Fe2++14H+===2Cr3++6Fe3++7HO中转
2 7 2
移的电子是不一样的。
15.(2021·北京高三二模)(16分)实验小组探究不同浓度 溶液的电解反应。分别用石墨电极电
解 溶液和 溶液,记录实验现象如下表。
实验装置 实验编号及试剂 实验现象
阳极:产生有刺激性气味的气体
① 溶液(蓝色)
阴极:电极上有红色固体析出
阳极:产生有刺激性气味的气体
② 溶液(绿色) 阴极:电极上有少量红色固体和白色固
体析出,同时电极附近液体变为黑色
(1)经检验,阳极产生的气体能使湿润的淀粉KI试纸变蓝。①中电解反应的化学方程式为___________。
Ⅰ.探究②中产生白色固体的原因。
查阅资料:
i.阴极附近的白色固体为 ;
ii. 在水溶液中单独存在时不稳定,容易发生反应: 。
结合资料分析CuCl产生的路径有如下两种可能:
(2)路径1:阴极发生电极反应分两步:
i.___________ⅱ. ,同时伴随反应 ,生成白色沉淀。
(3)路径2:阴极发生电极反应 ,而后发生反应a:___________(写出离子方程式),生成白色
沉淀。同学们通过实验证明反应a可以发生,其实验操作和现象是___________。
Ⅱ.探究②中阴极区液体中黑色物质的成分。
进一步查阅资料,提出以下猜想。
猜想1.生成氢氧化铜,进而转化为极细小的氧化铜;
猜想2.生成铜的速率快,形成黑色纳米铜;
猜想3.发生反应 (棕黑色)。
(4)若猜想1成立,则阴极一定还存在的电极反应是___________。
取2mL黑色液体于试管中,分别加入不同试剂,记录实验现象如下表。
实验编号 ③ ④ ⑤
加入试剂 4mL浓 4mL浓HCl
溶液变澄清,呈绿
溶液变澄清,呈绿色,试管口有浅
实验现象 黑色液体颜色变深 色,同时出现少量白
红棕色气体生成
色沉淀
(5)甲同学根据实验③产生的现象得出结论:黑色液体中一定有纳米铜。乙同学认为甲同学的结论不合理,
他做出判断的依据是___________。
(6)由上述实验可得到的关于黑色物质成分的结论是___________。
【答案】(除标注外,每空2分)(1)CuCl Cu+Cl↑
2 2
(2)Cu2++e-=Cu+
(3)Cu+Cu2++2Cl-=2CuCl↓ 在5mol/LCuCl 溶液中加入少量铜粉(或打磨过的铜片),观察到有白色固体
2
生成(3分)
(4)2HO+2e-=H↑+2OH-
2 2
(5)若猜想3成立,[Cu(II)Cu(I)Cl(HO)]-中+1价铜具有还原性,也可与硝酸反应产生类似的现象(3
4 2
分)
(6)黑色物质中一定含[Cu(II)Cu(I)Cl(HO)]-,可能含纳米铜粉
4 2
【解析】(1)电解 溶液,阳极产生的气体能使湿润的淀粉KI试纸变蓝,是氯气,阴极上有红
色固体析出,固体为铜,则电解反应的化学方程式为CuCl Cu+Cl↑。
2 2Ⅰ.(2)若阴极电极反应分两步,第二步是 ,则第一步是生成Cu+,则电极反应为Cu2++e-=Cu+。
(3)若阴极先发生电极反应 ,而后发生资料ⅱ中可逆反应的逆反应,即铜和铜离子的归中反应,
生成的Cu+和溶液中的Cl-生成CuCl白色沉淀:Cu+Cu2++2Cl-=2CuCl↓。要通过实验证明反应a能发生,可
以在5mol/LCuCl 溶液中加入少量铜粉(或打磨过的铜片),观察到有白色固体生成。
2
Ⅱ.(4)若猜想1成立,需要生成OH-,所以阴极一定还存在的电极反应是2HO+2e-=H↑+2OH-。
2 2
(5)实验③发生了氧化还原反应,铜被氧化生成Cu2+,硝酸被还原生成NO,但不一定是单质铜被氧化,也
可能是 中的+1价铜被氧化,所以乙同学认为甲同学的结论不合理。
(6)由上述实验可知猜想1不成立,因为阴极没有气体产生,根据实验④,加入浓盐酸,增大了Cl-的浓度,
使 平衡正向移动,黑色液体颜色加深,根据实验⑤,加
水, 平衡逆向移动,溶液变澄清,呈绿色,同时出现少
量白色沉淀CuCl,所以黑色物质一定有 ,根据实验③,也可能含有纳米铜粉。