文档内容
绝密★启用前
2025 年高考考前信息必刷卷 02(江苏专用)
化 学
考情速递
高考·新动向:试卷的题目设计体现了高考化学命题的综合性和应用性趋势。例如,选择题中涉及的元
素周期表、化学键、反应机理等内容,不仅考查了学生对基础知识的掌握,还要求他们能够灵活运用
这些知识解决实际问题。此外,题目中还融入了跨学科的内容,如物理、生物等学科的知识点,体现
了高考命题的跨学科融合趋势。题目呈现方式的变化:试卷中大量使用了图表、反应机理图、实验装
置图等,考查学生的信息提取和分析能力。例如,第13题通过图表展示了含氮元素占比随时间的变
化,要求学生根据图表信息推导反应机理和平衡常数。这种题目呈现方式的变化,要求学生不仅要掌
握化学知识,还要具备较强的数据分析能力。
高考·新考法:常规考点的新设问:试卷中对常规考点进行了创新性设问。例如,第4题考查了离子半
径、电离能、沸点、键角等常规知识点,但通过对比分析的方式设问,要求学生不仅要记住这些知识
点,还要能够进行比较和推理。这种设问方式增加了题目的难度和深度,考查了学生的综合分析能
力。
非常规考点的创新糅合:试卷中还涉及了一些非常规考点,如第8题考查了有机物的合成路线和对映
异构体,第9题考查了电解法的应用。这些题目不仅考查了学生对基础知识的掌握,还要求他们能够
理解并应用化学反应的实际应用,体现了高考命题的创新性和实用性。
高考·新情境:情境题目的创新性:试卷中设置了多个实际应用情境,如第14题利用锰银矿制备硫酸锰
和银的实验流程,第16题利用废定影液制备硝酸银的实验流程。这些题目不仅考查了学生的化学知
识,还要求他们能够理解并应用化学实验的实际操作,体现了高考命题的实践性和创新性。
跨学科的融合性:试卷中部分题目涉及了物理、生物等学科的知识点,如第17题考查了氢能的制备方
法,涉及了电化学、热力学等内容。这种跨学科的融合考查了学生的综合学科素养,符合高考命题的
跨学科融合趋势。
命题·大预测:趋势性预测:从本试卷的命题特点来看,未来的高考化学试题将继续保持综合性、应用
性和创新性的趋势。题目将更加注重实际应用情境的考查,要求学生能够将化学知识应用于解决实际
问题。同时,跨学科融合的题目将会增多,考查学生的综合学科素养。
• 备考方向:学生在备考时应注重基础知识的扎实掌握,同时要加强对实际应用情境的理解和分析能
力。此外,学生还应注意跨学科知识的积累,特别是物理、生物等学科中与化学相关的内容。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共13小题,每小题3分,共39分。每小题只有一个选项符合题目要求。
1. 我国科学家在月壤中发现一种新矿物——嫦娥石[ ],探月工程取得重大进展。下列元
素属于非金属元素的是
A. 磷(P) B. 钙(Ca) C. 铁(Fe) D. 钇(Y)
【答案】A
【解析】钙(Ca)、铁(Fe)、钇(Y)均为金属元素,而磷为非金属元素;
故选A。
2. 过氧化钠用于呼吸面罩的供氧剂,其反应原理为 下列说法正确
的是
A. NaO 中含极性共价键 B. CO 的电子式为
2 2 2
C. 的空间构型为正四面体形 D. O原子结构示意图为
【答案】B
【解析】A.NaO 中O和O之间存在非极性共价键,A错误;
2 2
B.CO 的电子式为 ,B正确;
2
C. 的中心原子的价层电子对数为 ,无孤对电子,空间构型为平面三角形,C
错误;
D.O原子的核外电子数为8,结构示意图为 ,D错误;
故选B。
3. 实验室进行炭与浓硫酸反应的实验。下列装置和操作能达到实验目的是A. 用装置甲进行炭与浓硫酸的反应 B. 用装置乙检验
C. 用装置丙检验 D. 用装置丁检验
【答案】C
【解析】A.炭与浓硫酸需要在加热条件下反应,在装置甲中缺少酒精灯,A错误;
B.检验HO(g)应该用无水硫酸铜,而不能用无水氯化钙,B错误;
2
C.利用 的漂白性,用品红溶液检验 和 混合气体中 ,C正确;
D.由装置丙导出的气体中仍然混有 ,而 也能与澄清石灰水反应出现浑浊,不能检验炭与浓硫
酸反应生成的 ,D错误;
故选C。
4. 摩尔盐 可用于治疗缺铁性贫血。下列说法正确的是
.
A 半径: B. 第一电离能:
C. 沸点: D. 键角:
【答案】D
【解析】A.O2-的核外电子数为10,电子层数为2,S2-的核外电子数为18,电子层数为3,电子层数越
多离子半径越大,则离子半径: ,故A错误;
B.N、O为同周期元素,同周期元素第一电离能从左到右呈增大趋势,但N最外层2p能级中电子为半
满稳定结构,其第一电离能大于O,故B错误;
C. 均是由分子构成的物质,两者均能形成氢键,但水分子间可形成氢键数目比氨气多,
水分子之间的分子间作用力更大,因此水的沸点高,故沸点: ,故C错误;
D. 中中心原子价电子对数都是4,均是sp3杂化,N原子无孤电子对、O原子有2个孤电
子对,孤电子对对成键电子对的斥力较大,所以键角: ,故D正确;故选D。
阅读下列材料,回答5-7题。
人类对酸碱的认识经历了漫长的时间。最早的酸碱概念由Robert Boyle于1663年提出,1887年
Arrhenius提出了酸碱电离理论,1923年J.N.Bronsted和Lowry提出了酸碱质子理论。酸碱质子理论认
为:凡是能够给出质子的物质都是酸;凡是能够接受质子的物质都是碱。酸碱的概念不断更新,逐渐
完善,其他重要的酸碱理论还有酸碱溶剂理论和酸碱电子理论等。
5. 下列物质的性质与用途具有对应关系的是
A. 硫酸可电离出 和 ,可用作铅蓄电池的电解质
B. 盐酸易挥发,可用作金属表面除锈剂
C. 微溶于水,可用于改良酸性土壤
D. 为两性氢氧化物,其胶体可用于净水
6. 下列涉及酸或碱的化学反应表示正确的是
A. Al粉和NaOH溶液反应制取少量 :
B. 室温下用稀 溶解Cu:
C. 室温下用NaOH溶液吸收 :
D. 向 溶液中加入稀 :
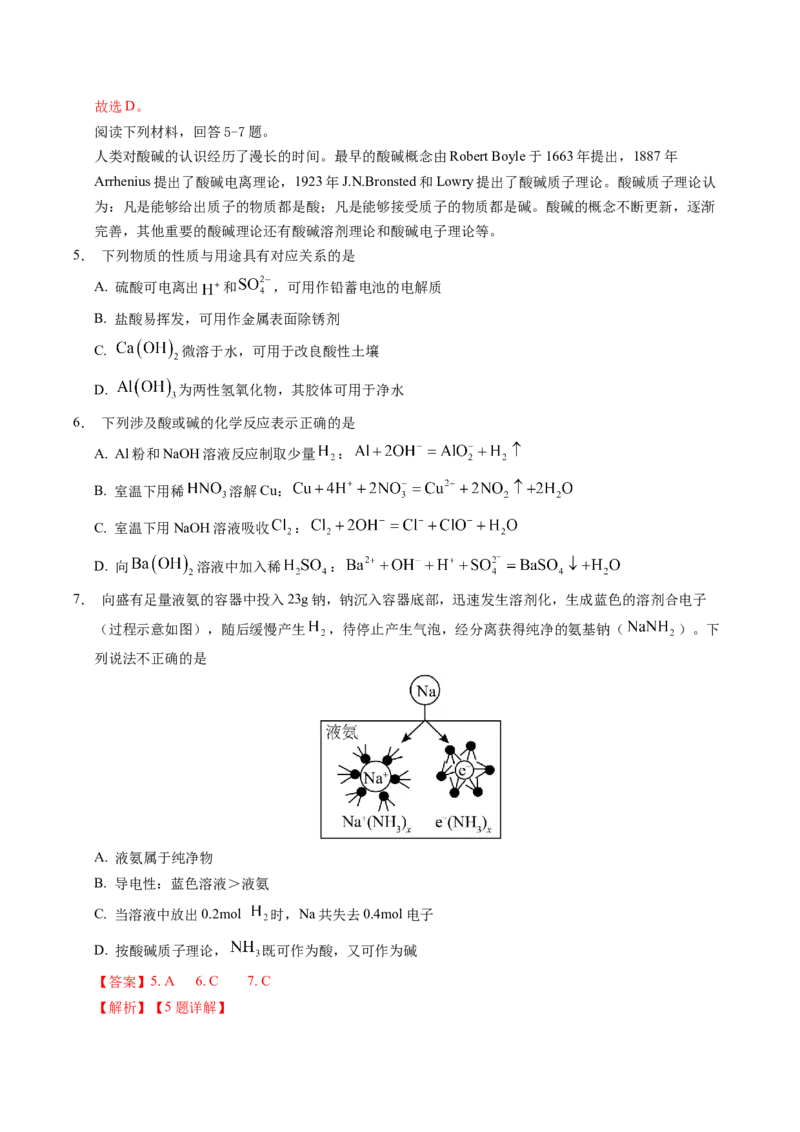
7. 向盛有足量液氨的容器中投入23g钠,钠沉入容器底部,迅速发生溶剂化,生成蓝色的溶剂合电子
(过程示意如图),随后缓慢产生 ,待停止产生气泡,经分离获得纯净的氨基钠( )。下
列说法不正确的是
A. 液氨属于纯净物
B. 导电性:蓝色溶液>液氨
C. 当溶液中放出0.2mol 时,Na共失去0.4mol电子
D. 按酸碱质子理论, 既可作为酸,又可作为碱
【答案】5. A 6. C 7. C
【解析】【5题详解】A.硫酸为强酸,水溶液中可电离出 和 ,可用作铅蓄电池的电解质,A正确;
B.盐酸具有酸性,能和氧化铁、氧化铝等金属氧化物反应,可用作金属表面除锈剂,与挥发性无关,
B错误;
C. 能和酸反应,可用于改良酸性土壤,与溶解性无关,C错误;
D. 形成胶体能加速悬浮颗粒沉淀,故其胶体可用于净水,与其是两性氧化物无关,D错
误;
故选A;
【6题详解】
A.Al粉和NaOH溶液反应制取少量 反应为: ,A错
误;
B.室温下用稀 溶解Cu生成硝酸铜和NO、水: ,B
错误;
C.室温下用NaOH溶液吸收 生成氯化钠和次氯酸钠、水,C正确;
D.向 溶液中加入稀 反应为: ,D错
误;
故选C;
【7题详解】
A.液氨为氨的液态,属于纯净物,A正确;
B.溶液或熔融电解质导电的原因是存在自由移动的离子,由图,钠沉入容器底部,迅速发生溶剂化,
生成蓝色的溶剂合电子、氨合钠离子,能导电,而液氨中无自由移动离子不导电,故导电性:蓝色溶
液>液氨,B正确;
C.当溶液中放出0.2mol 时,H得到0.4mol电子,但是钠迅速发生溶剂化,生成蓝色的溶剂合电子
过程中也会失去电子,故Na共失去电子大于0.4mol,C错误;
D.按酸碱质子理论, 可接受质子形成铵根离子,又可以给出质子形成 ,故既可作为酸,又
可作为碱,D正确;
故选C。
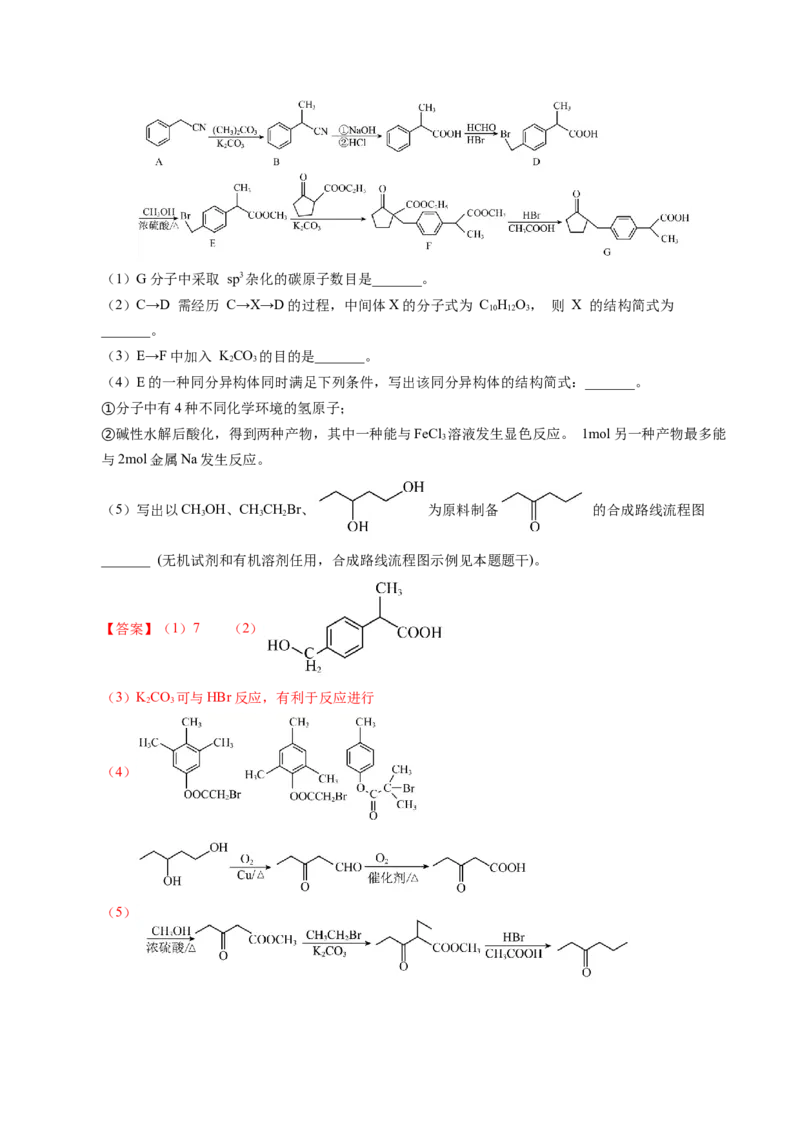
8. 有机物 合的成路线如下,下列说法不正确的是
A. 的酸性比乙酸强 B. 、 都有相同的产物生成C. 最多可以消耗 D. 具有对映异构体
【答案】C
【解析】A.羰基为吸电子基团,使得 中羧基上的H更易电离,故酸性比乙酸强,A正确;
B. 、 都是取代反应,都生成了氯化氢,所以都有相同的产物生成,B正确;
C.Z中含有酚酯基, 水解会消耗 ,C错误;
D. 中含手性碳原子,具有对映异构体,D正确;
故选C。
9. 利用电解法可使 Fe (SO ) 转化成FeSO , 加入甲醇能提高FeSO 产率, 装置如图所示。下列有关说
2 4 3 4 4
法不正确的是
A. 电解时 Fe3+在阴极放电
B. 可用 KMnO 溶液检验有 Fe2+生成
4
C. 反应中每生成 1mol HCHO,转移电子数约为1.204×1024
D. 生成的 HCHO 具有还原性,能防止 Fe2+被氧化
【答案】B
【解析】根据电解装置示意图可知: 失电子变成 ,因此生成 这一极为电解池
的阳极,电极反应式为 ; 得电子变成 ,因此生成 这一极为
电解池的阴极,电极反应式为: ,据此分析回答问题;
A.电解时 得电子变成 ,因此Fe3+在阴极放电,A正确;
B.电解液中有甲醇,甲醇也会使KMnO 溶液褪色,因此不能用KMnO 溶液检验有 Fe2+生成,B错
4 4
误;
C.生成 这一极的电极反应式为 ,根据电极反应式可知每生成
1mol HCHO,转移电子数为 ,约为 ,C正确;
D. 易被氧化,生成的 HCHO 具有还原性,能防止 Fe2+被氧化,D正确;
故选B。
10.在给定条件下,下列制备过程涉及的物质转化不能实现的是
.
A 金属铝制备:B. 锅炉除垢:
C. 酸雨形成:
D. 检验葡萄糖:
【答案】A
【解析】A. 和盐酸反应生成 溶液,电解 溶液的过程中,阳离子Al3+不放电,不能
生成Al,A符合题意;
B. 的溶解度小于 , 和碳酸钠溶液反应生成 , 和盐酸反应生成
氯化钙溶液,B不符合题意;
C.酸雨形成过程中, 和水反应生成 , 被空气中的氧气氧化为 ,C不符合题
意;
D.检验葡萄糖过程中, 溶液和过量NaOH溶液反应得到 悬浊液,加入葡萄糖溶液
反应生成砖红色的 ,D不符合题意;
故选A。
11.室温下,根据下列实验过程及现象,能验证相应实验结论的是
选
实验过程及现象 实验结论
项
A 测定等物质的量浓度的NaCO 和 NaSO 溶液的pH, 前者的pH大 非金属性: S>C
2 3 2 3
向 Fe(NO ) 和KSCN的混合溶液中滴入酸化的AgNO 溶液, 溶液出
B 3 2 3 氧化性:Ag+>Fe3+
现血红色
用pH计分别测定0.1mol·L⁻¹ NaClO 溶液和0.1 mol·L⁻¹CH COONa溶 结合 H+能力:ClO⁻>
3
C
液pH,NaClO 溶液 pH大 CHCOO⁻
3
向 BaSO 固体中加入饱和NaCO 溶液,充分搅拌后, 取沉淀洗 溶度积常数: K (BaSO)>
D 4 2 3 sp 4
净, 加入盐酸有气泡产生 K (BaCO)
sp 3
【答案】C
【解析】A.测定等物质的量浓度的NaCO 和 NaSO 溶液的pH,前者的pH大,则表明 的水
2 3 2 3
解能力大于 ,酸性HCO<HSO ,但由于HSO 不属于S的最高价氧化物对应的水化物,所以
2 3 2 3 2 3
不能得出结论:非金属性S>C,A不正确;
B.向 Fe(NO ) 和KSCN的混合溶液中滴入酸化的AgNO 溶液,溶液出现血红色,表明发生反应生成
3 2 3
了Fe3+,Fe3+可能是由Ag+氧化Fe2+生成,也可能是由酸性条件下 氧化Fe2+生成,所以不能得出结
论:氧化性Ag+>Fe3+,B不正确;C.用pH计分别测定0.1mol·L⁻¹ NaClO 溶液和0.1 mol·L⁻¹CH COONa溶液pH,NaClO 溶液 pH大,
3
表明ClO-的水解能力强于CHCOO-,则结合 H+能力:ClO⁻>CHCOO⁻,C正确;
3 3
D.向 BaSO 固体中加入饱和NaCO 溶液,充分搅拌后, 取沉淀洗净,加入盐酸有气泡产生,表明
4 2 3
有BaCO 生成,由于BaSO 难溶于水,其饱和溶液中c( )很小,而NaCO 饱和溶液中c( )
3 4 2 3
较大,所以不能得出结论:溶度积常数K (BaSO)>K (BaCO),D不正确;
sp 4 sp 3
故选C。
12.某实验室回收废水中苯酚的过程如下图所示。已知:苯酚的电离常数 ,HCO 的电离
2 3
常数 , 。
下列有关说法不正确的是
A. 操作1、操作2 均为分液
B. NaHCO 溶液中存在:c(HCO)+c(H+)=c(OH-)+c( )
3 2 3
C. 若反应1后溶液中存在c(Na+)=2 c(C HO-)+2 c(C HOH),此时c(C HO-)>c( )
6 5 6 5 6 5
D. 反应2 中通入CO 至溶液 pH=10时, 此时溶液中存在: c(C HO-)= c(C HOH)
2 6 5 6 5
【答案】C
【解析】据流程图可知,将苯酚废水用有机溶剂苯先进行萃取分液,得到苯酚的苯溶液,接着加入碳
酸钠溶液,使苯酚转化成苯酚钠进入水溶液中,再通过分液分离有机层苯,随后往苯酚钠溶液中通入
二氧化碳,苯酚在水中溶解度小,析出后过滤即可得到苯酚。
A.结合流程分析,操作1、操作2均溶液分层,采取分液的方法进行分离,A正确;
B. NaHCO 溶液中存在质子守恒:c(HCO)+c(H+)=c(OH-)+c( ),B正确;
3 2 3
C.苯酚酸性小于碳酸,因此反应1苯酚与碳酸钠溶液混合生成碳酸氢钠和苯酚钠,根据电离常数可
知,苯酚钠的水解能力大于碳酸氢钠,故c(C HO-)<c( ),C错误;
6 5
D.反应2 中通入 CO 至溶液 pH=10时,此时溶液中存在:
2
,故 (C HO-) (C HOH),D正确;
6 5 6 5
故选C。
13.基于单簇催化剂(SCC)的NO还原反应(NORR)的主要反应如下:
(Ⅰ)
(Ⅱ)(Ⅲ)
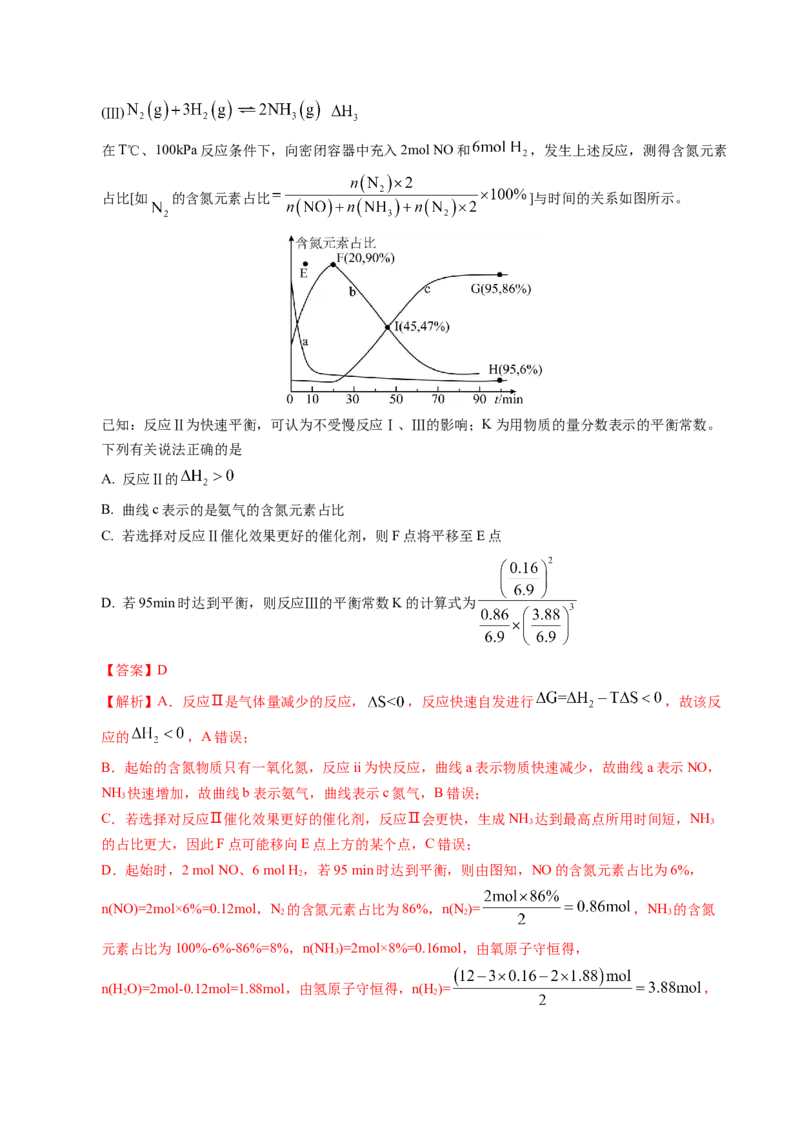
在T℃、100kPa反应条件下,向密闭容器中充入2mol NO和 ,发生上述反应,测得含氮元素
占比[如 的含氮元素占比 ]与时间的关系如图所示。
已知:反应Ⅱ为快速平衡,可认为不受慢反应Ⅰ、Ⅲ的影响;K为用物质的量分数表示的平衡常数。
下列有关说法正确的是
A. 反应Ⅱ的
B. 曲线c表示的是氨气的含氮元素占比
C. 若选择对反应Ⅱ催化效果更好的催化剂,则F点将平移至E点
D. 若95min时达到平衡,则反应Ⅲ的平衡常数K的计算式为
【答案】D
【解析】A.反应Ⅱ是气体量减少的反应, ,反应快速自发进行 ,故该反
应的 ,A错误;
B.起始的含氮物质只有一氧化氮,反应ii为快反应,曲线a表示物质快速减少,故曲线a表示NO,
NH 快速增加,故曲线b表示氨气,曲线表示c氮气,B错误;
3
C.若选择对反应Ⅱ催化效果更好的催化剂,反应Ⅱ会更快,生成NH 达到最高点所用时间短,NH
3 3
的占比更大,因此F点可能移向E点上方的某个点,C错误;
D.起始时,2 mol NO、6 mol H ,若95 min时达到平衡,则由图知,NO的含氮元素占比为6%,
2
n(NO)=2mol×6%=0.12mol,N 的含氮元素占比为86%,n(N )= ,NH 的含氮
2 2 3
元素占比为100%-6%-86%=8%,n(NH )=2mol×8%=0.16mol,由氧原子守恒得,
3
n(H O)=2mol-0.12mol=1.88mol,由氢原子守恒得,n(H )= ,
2 2此时总物质的量为(0.12+0.86+0.16+1.88+3.88)=6.9mol,N 的物质的量分数为 ,H 的物质的量分
2 2
数为: ,NH 的物质的量分数为: ,则反应Ⅲ的平衡常数Kx= ,D正确;
3
故选D。
二、非选择题:本题共4小题,共61分。
14.利用锰银矿(主要成分为MnO 、Ag和少量SiO 等杂质)制备硫酸锰和银。
2 2
(1)用蔗糖(C H O )、水和浓硫酸浸取锰银矿,过滤得硫酸锰溶液和含银滤渣。
12 22 11
①提高锰元素浸出率的措施___________(任写—条)。
②蔗糖还原 MnO 生成硫酸锰和CO 的化学方程式为___________。
2 2
③其它条件相同,酸矿比0.33∶1,糖矿比0.04∶1时,酸浸过程中随着水矿比的增大,锰的浸出率如图
所示:
水矿比大于2∶1时,锰的浸出率逐渐减小的原因为___________。
(2)在空气中用 NaCN 溶液浸取含银滤渣,得到含[Ag(CN) ]⁻的浸出液, 再用锌粉置换得银。
2
①浸出反应的离子方程式:___________。
②如图所示,pH小于10.5时,随pH的减小,银的浸出率降低的原因:___________。
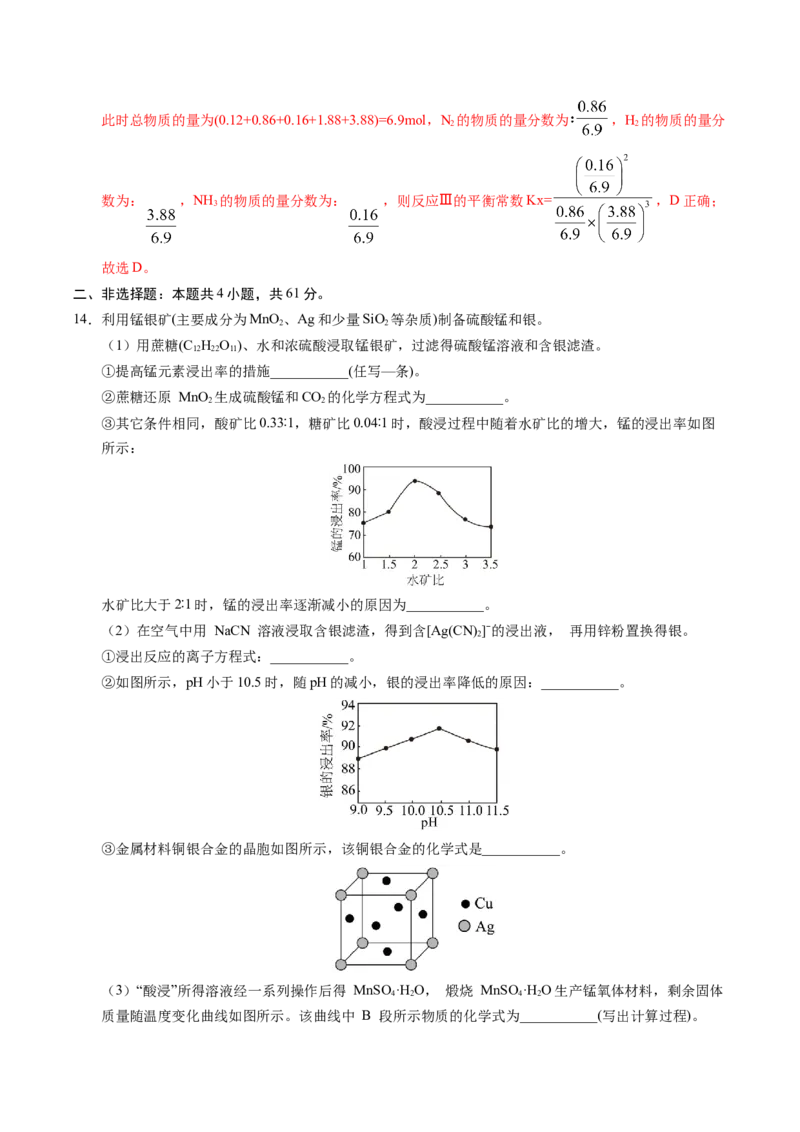
③金属材料铜银合金的晶胞如图所示,该铜银合金的化学式是___________。
(3)“酸浸”所得溶液经一系列操作后得 MnSO ·H O, 煅烧 MnSO ·H O生产锰氧体材料,剩余固体
4 2 4 2
质量随温度变化曲线如图所示。该曲线中 B 段所示物质的化学式为___________(写出计算过程)。【答案】(1) ①. 加热或粉碎、充分搅拌等 ②.
③. 水矿比大于2:1时硫酸(或
蔗糖)的浓度降低,化学反应速率降低,浸出率下降
(2) ①. ②. 随 较低, 水解程度增
大,浓度减小,银的浸出率降低 ③.
(3)
【解析】(1)①提高锰元素浸出率的措施有加热或粉碎、充分搅拌等;
②二氧化锰将蔗糖氧化为二氧化碳,自身被还原为二价锰,化学方程式为
;
③水矿比大于2∶1时,水较多,反应物被稀释,故锰的浸出率逐渐减小的原因为硫酸(或蔗糖)的浓度降
低,化学反应速率降低,浸出率下降;
(2)①Ag与NaCN 溶液形成配合物[Ag(CN) ]⁻,Ag的化合价由0价升高到+1价,则氧气做氧化
2
剂,离子方程式为 ;
②由上一问可知,银的浸出需要与CN-形成配合物,CN-是弱酸的阴离子,易水解,则pH的减小,银
的浸出率降低的原因是随 较低, 水解程度增大,浓度减小,银的浸出率降低;
③根据均摊法可知,晶胞中含有Ag的个数为 ,含有Cu的个数是 ,则晶胞的化学式
为 ;
(3)n(Mn) = n(MnSO ·H O) = = 0.9mol;
4 2
m(Mn)= n(Mn)·M(Mn) = 0.9mol×55g·mol-1 = 49.5g;
n(O)= =1.2mol,n(Mn):n(O)=0.9:1.2=3:4,化学式为 。
15.化合物G是一种药物中间体,其一种合成路线如下:(1)G分子中采取 sp3杂化的碳原子数目是_______。
(2)C→D 需经历 C→X→D的过程,中间体X的分子式为 C H O, 则 X 的结构简式为
10 12 3
_______。
(3)E→F中加入 KCO 的目的是_______。
2 3
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中有4种不同化学环境的氢原子;
②碱性水解后酸化,得到两种产物,其中一种能与FeCl 溶液发生显色反应。 1mol另一种产物最多能
3
与2mol金属Na发生反应。
(5)写出以CHOH、CHCHBr、 为原料制备 的合成路线流程图
3 3 2
_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
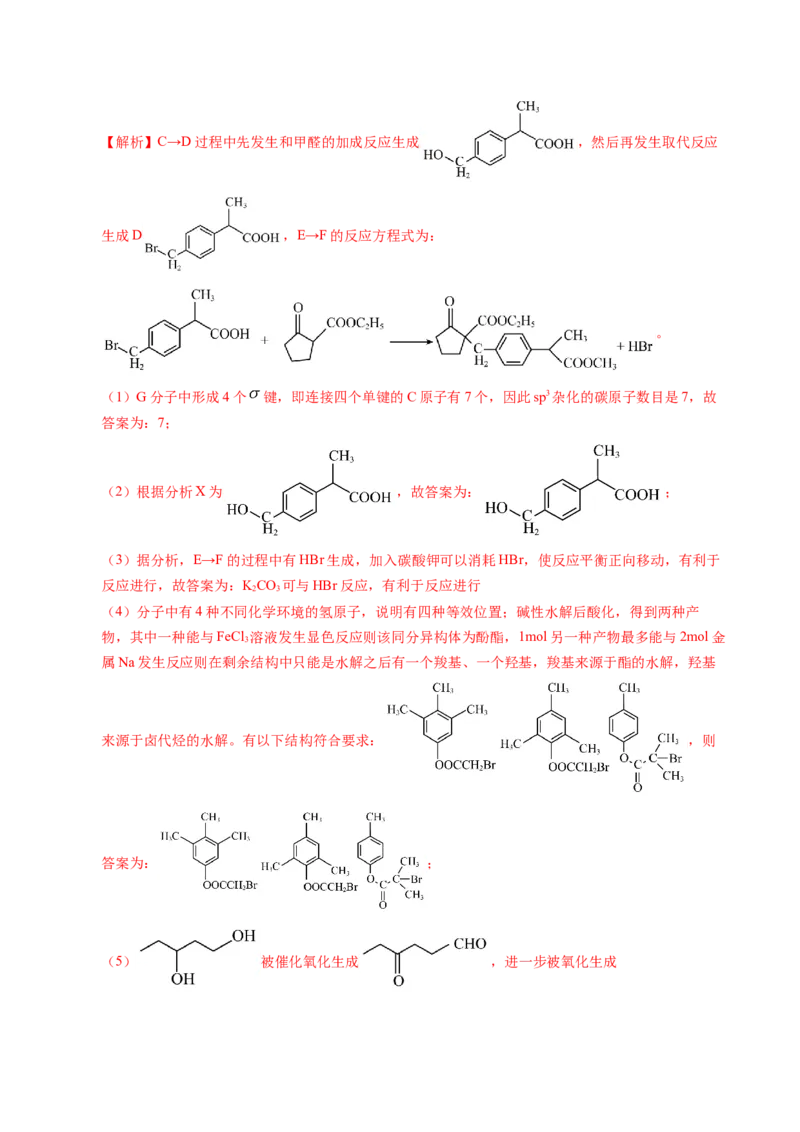
【答案】(1)7 (2)
(3)KCO 可与HBr反应,有利于反应进行
2 3
(4)
(5)【解析】C→D过程中先发生和甲醛的加成反应生成 ,然后再发生取代反应
生成D ,E→F的反应方程式为:
。
(1)G分子中形成4个 键,即连接四个单键的C原子有7个,因此sp3杂化的碳原子数目是7,故
答案为:7;
(2)根据分析X为 ,故答案为: ;
(3)据分析,E→F的过程中有HBr生成,加入碳酸钾可以消耗HBr,使反应平衡正向移动,有利于
反应进行,故答案为:KCO 可与HBr反应,有利于反应进行
2 3
(4)分子中有4种不同化学环境的氢原子,说明有四种等效位置;碱性水解后酸化,得到两种产
物,其中一种能与FeCl 溶液发生显色反应则该同分异构体为酚酯,1mol另一种产物最多能与2mol金
3
属Na发生反应则在剩余结构中只能是水解之后有一个羧基、一个羟基,羧基来源于酯的水解,羟基
来源于卤代烃的水解。有以下结构符合要求: ,则
答案为: ;
(5) 被催化氧化生成 ,进一步被氧化生成, 通过酯化反应得到 ,利用E→F的反
应机理可以得到: ,最终利用F→G的机理得到目标产物: ,故
答案为: 。
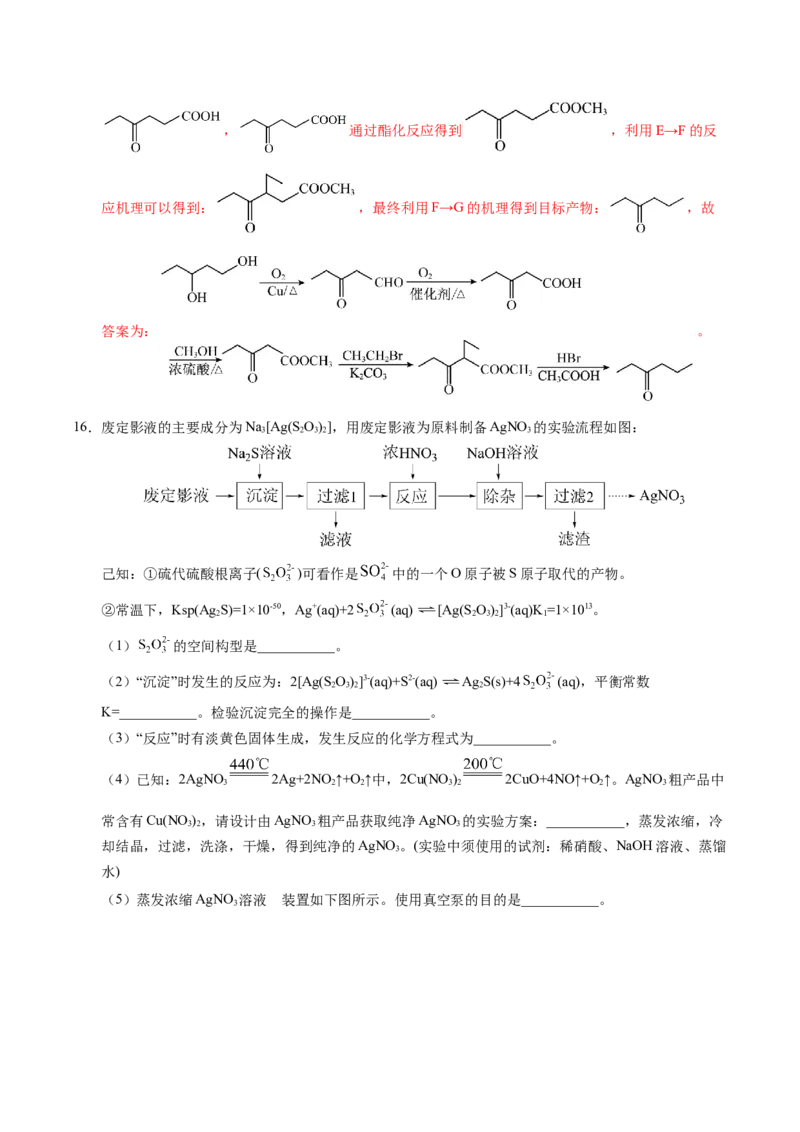
16.废定影液的主要成分为Na[Ag(S O)],用废定影液为原料制备AgNO 的实验流程如图:
3 2 3 2 3
己知:①硫代硫酸根离子( )可看作是 中的一个О原子被S原子取代的产物。
②常温下,Ksp(Ag S)=1×10-50,Ag+(aq)+2 (aq) [Ag(S O)]3-(aq)K=1×1013。
2 2 3 2 1
(1) 的空间构型是___________。
(2)“沉淀”时发生的反应为:2[Ag(S O)]3-(aq)+S2-(aq) Ag S(s)+4 (aq),平衡常数
2 3 2 2
K=___________。检验沉淀完全的操作是___________。
(3)“反应”时有淡黄色固体生成,发生反应的化学方程式为___________。
(4)已知:2AgNO 2Ag+2NO ↑+O ↑中,2Cu(NO ) 2CuO+4NO↑+O ↑。AgNO 粗产品中
3 2 2 3 2 2 3
常含有Cu(NO ),请设计由AgNO 粗产品获取纯净AgNO 的实验方案:___________,蒸发浓缩,冷
3 2 3 3
却结晶,过滤,洗涤,干燥,得到纯净的AgNO。(实验中须使用的试剂:稀硝酸、NaOH溶液、蒸馏
3
水)
(5)蒸发浓缩AgNO 溶液 的装置如下图所示。使用真空泵的目的是___________。
3【答案】(1)四面体形
(2) ①. 1×1024 ②. 静置,向上层清液中继续滴加NaS溶液,若不再有沉淀生成,则沉淀完
2
全
(3)Ag S+4HNO (浓)=2AgNO +2NO↑+2H O+S
2 3 3 2 2
(4)将AgNO 粗产品加热并维持温度在200℃至恒重,同时用足量NaOH溶液吸收产生的气体;待
3
固体冷却后加入蒸馏水,充分溶解、过滤、洗涤,并将洗涤液与滤液合并,再加入适量稀HNO
3
(5)防止AgNO 分解;减小压强,利于水分在较低温度下蒸发
3
【解析】废定影液 (主要含Na[Ag(S O)] ),加入硫化钠溶液,可生成硫化银,经过滤1,所得滤渣
3 2 3 2
含有硫化银,洗涤干净后加入浓硝酸溶解Ag S得到硝酸银、硫单质与二氧化氮;用氢氧化钠除杂、
2
经过滤2后得到硝酸银溶液,蒸发浓缩、冷却结晶得到硝酸银晶体,据此分析作答。
(1) 与 属于等电子体,二者的空间构型类似, 的中心原子S原子价层电子对为4,
属于四面体形结构;
(2)根据平衡常数、硫化银的溶度积,可计算“沉淀”时发生的反应2[Ag(S O)]3-(aq)+S2-
2 3 2
(aq) Ag S(s)+4S (aq)的平衡常数:K= = =
⇋ 2 2
=1.0×1024;“沉淀”时Na[Ag(S O)]与NaS反应制得Ag S,则检验沉淀
3 2 3 2 2 2
完全的操作是:静置,向上层清液中继续滴加NaS溶液,若不再有沉淀生成,则沉淀完全;
2
(3)“反应”时有淡黄色固体即S生成,根据原子守恒可知,则为硫离子被氧化生成硫单质,则浓
HNO 被还原为NO 气体,则发生反应的化学方程式为:
3 2
Ag S+4HNO (浓)=2AgNO +2NO↑+2H O+S;
2 3 3 2 2
(4)根据给定的已知信息可知,硝酸铜的分解温度为200℃,硝酸银的分解温度在440℃,则可设计
除去硝酸铜的方法为:将AgNO 粗产品加热并维持温度在200℃至恒重,同时用足量NaOH溶液吸收
3
产生的气体,待固体残留物冷却后,加入蒸馏水,充分溶解、过滤、洗涤,并将洗涤液与滤液合并,
再加入适量稀硝酸;
(5)考虑硝酸银易分解,而实验装置中真空泵可以形成负压,有利于水分在较低温度下蒸发,同时
可防止AgNO3分解,则使用真空泉的目的是:防止AgNO3分解;减小压强,利于水分在较低温度下
蒸发。
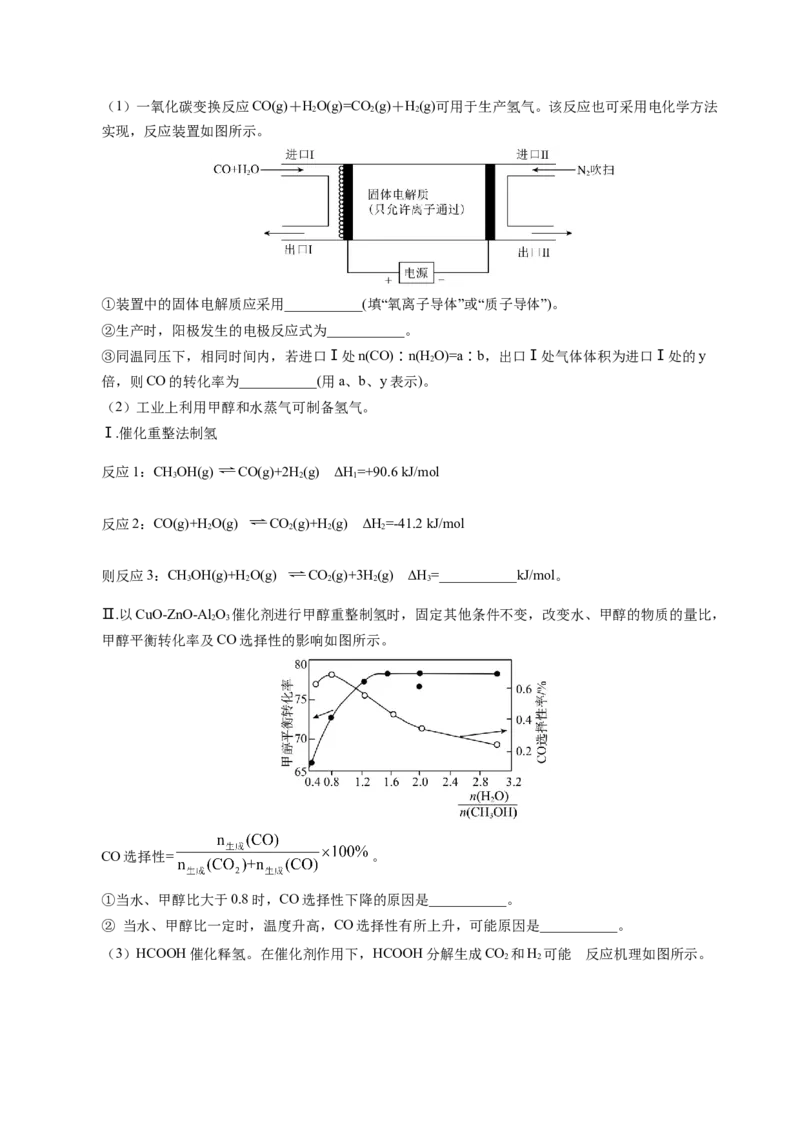
17.氢能是一种极具发展潜力的清洁能源,目前有以下制取氢气的方法:(1)一氧化碳变换反应CO(g)+HO(g)=CO(g)+H(g)可用于生产氢气。该反应也可采用电化学方法
2 2 2
实现,反应装置如图所示。
①装置中的固体电解质应采用___________(填“氧离子导体”或“质子导体”)。
②生产时,阳极发生的电极反应式为___________。
③同温同压下,相同时间内,若进口Ⅰ处n(CO)∶n(H O)=a∶b,出口Ⅰ处气体体积为进口Ⅰ处的y
2
倍,则CO的转化率为___________(用a、b、y表示)。
(2)工业上利用甲醇和水蒸气可制备氢气。
Ⅰ.催化重整法制氢
反应1:CHOH(g) CO(g)+2H(g) ΔH=+90.6 kJ/mol
3 2 1
反应2:CO(g)+HO(g) CO(g)+H(g) ΔH=-41.2 kJ/mol
2 2 2 2
则反应3:CHOH(g)+H O(g) CO(g)+3H(g) ΔH=___________kJ/mol。
3 2 2 2 3
Ⅱ.以CuO-ZnO-Al O 催化剂进行甲醇重整制氢时,固定其他条件不变,改变水、甲醇的物质的量比,
2 3
甲醇平衡转化率及CO选择性的影响如图所示。
CO选择性= 。
①当水、甲醇比大于0.8时,CO选择性下降的原因是___________。
② 当水、甲醇比一定时,温度升高,CO选择性有所上升,可能原因是___________。
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO 和H 可能 的反应机理如图所示。
2 2①HCOOD催化释氢反应除生成CO 外,还生成___________(填化学式)。
2
②研究发现:其他条件不变时,以 HCOOK溶液代替 HCOOH催化释氢的效果更佳,其具体优点是
___________。
【答案】(1) ①. 质子导体 ②. CO+HO-2e-=CO +2H+ ③.
2 2
(2) ①. +49.4 ②. 增加水蒸气的用量,有利于反应2正向进行,反应3中更多的CHOH转
3
化为CO ,都使CO选择性下降 ③. 升高温度,反应1的ΔH>0,K增大,反应正向进行程度增
2 1
大,反应2的ΔH<0,K减小,反应正向进行程度减小,都使CO选择性上升;反应3的ΔH>0,温度
2 3
升高,K增大,反应正向进行程度增大,使更多的甲醇转化为CO ,使CO 选择性上升,但此影响程
2 2
度小于前两者使CO选择性上升的影响,故CO选择性仍然随温度的升高而上升
(3) ①. HD ②. 提高释放氢气的速率,提高释放出氢气的纯度(HCOOK是强电解质,更容
易产生HCOOˉ和K+,更快的产生KH,KH可以与水反应生成H 和KOH,生成的KOH可以吸收分解
2
产生的CO,从而使氢气更纯净)
2
【解析】(1)①电解时,阳极上CO被氧化生成CO,则氢气要在阴极产生,即阳极产生CO 的同时
2 2
产生氢离子,氢离子通过固体电解质在阴极附近得电子生成H,所以装置中的固体电解质应采用质子
2
导体;
②电解时,阳极上CO被氧化生成CO,同时产生氢离子,则阳极发生的电极反应式为:
2
;
③同温同压下,相同时间内,若进口Ⅰ处n(CO)∶n(H O)=a∶b,则设n(CO)=amol,n(H O)=bmol,根
2 2
据阳极的电极反应式( )可知,阳极上每消耗1molCO,气体物质的量减少
1mol,当出口Ⅰ处气体体积为进口Ⅰ处的y倍时,气体物质的量减少(a+b)-y(a+b)=(1-y)(a+b),则消耗
CO物质的量为(1-y)(a+b),所以CO的转化率为 ;
(2)反应3=反应1+反应2,则根据盖斯定律可知,∆H=∆H +∆H =+90.6kJ/mol+(-41.2)kJ/
3 1 2
mol=+49.4kJ/mol;
Ⅱ①可以从水蒸气浓度对平衡移动的角度分析,当水、甲醇比大于0.8时,CO选择性下降的原因是:
增加水蒸气的用量,有利于反应2正向进行,反应3中更多的CHOH转化为CO,都使CO选择性下
3 2降;
②可以从温度对平衡移动的角度分析,当水、甲醇比一定时,温度升高,CO选择性有所上升,可能
原因是:升高温度,反应1的ΔH>0,K增大,反应正向进行程度增大,反应2的ΔH<0,K减小,
1 2
反应正向进行程度减小,都使CO选择性上升;反应3的ΔH>0,温度升高,K增大,反应正向进行
3
程度增大,使更多的甲醇转化为CO,使CO 选择性上升,但此影响程度小于前两者使CO选择性上
2 2
升的影响,故CO选择性仍然随温度的升高而上升;
(3)①由反应机理图可知,HCOOH催化分解生成CO 和H,则HCOOD催化释氢反应除生成CO
2 2 2
外,还生成HD;
②HCOOK是强电解质,更容易产生 HCOO-和K+,更快的产生KH,KH可以与水反应生成 H 和
2
KOH,生成的KOH可以吸收分解产生的CO ,从而使氢气更纯净,所以具体优点是:提高释放氢气
2
的速率,提高释放出氢气的纯度(HCOOK是强电解质,更容易产生HCOOˉ和K+,更快的产生KH,
KH可以与水反应生成H 和KOH,生成的KOH可以吸收分解产生的CO,从而使氢气更纯净)。
2 2