文档内容
微专题32 电化学中的交换膜
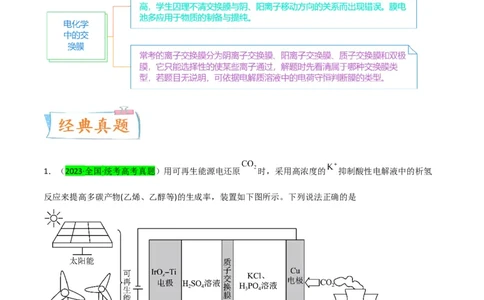
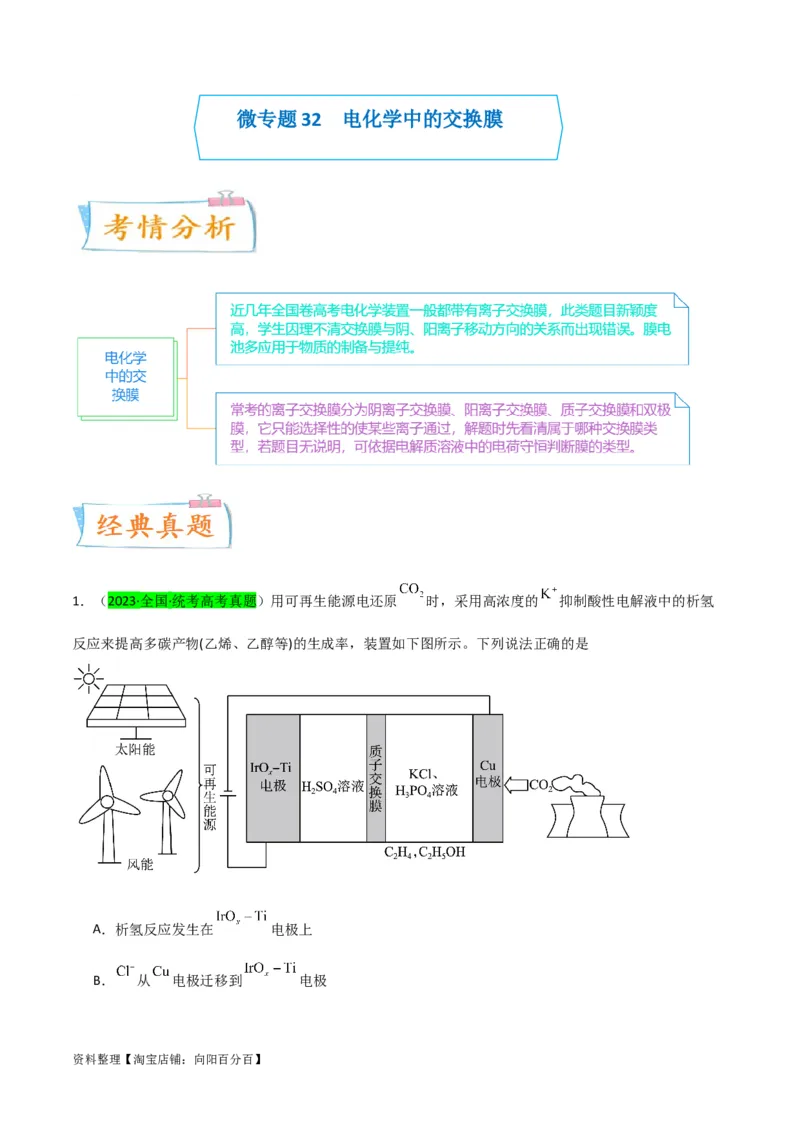
1.(2023·全国·统考高考真题)用可再生能源电还原 时,采用高浓度的 抑制酸性电解液中的析氢
反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
A.析氢反应发生在 电极上
B. 从 电极迁移到 电极
资料整理【淘宝店铺:向阳百分百】C.阴极发生的反应有:
D.每转移 电子,阳极生成 气体(标准状况)
【答案】C
【解析】由图可知,该装置为电解池,与直流电源正极相连的IrO-Ti电极为电解池的阳极,水在阳极失去
x
电子发生氧化反应生成氧气和氢离子,电极反应式为2H O-4e—=O ↑+4H+,铜电极为阴极,酸性条件下二氧
2 2
化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式为2CO +12H++12e−=C H +4H O、
2 2 4 2
2CO +12H++12e−=C H OH+3H O,电解池工作时,氢离子通过质子交换膜由阳极室进入阴极室。
2 2 5 2
A.析氢反应为还原反应,应在阴极发生,即在铜电极上发生,故A错误;
B.离子交换膜为质子交换膜,只允许氢离子通过,Cl-不能通过,故B错误;
C.由分析可知,铜电极为阴极,酸性条件下二氧化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,
电极反应式有2CO +12H++12e−=C H +4H O,故C正确;
2 2 4 2
D.水在阳极失去电子发生氧化反应生成氧气和氢离子,电极反应式为2H O-4e—=O ↑+4H+,每转移1mol
2 2
电子,生成0.25molO ,在标况下体积为5.6L,故D错误;
2
答案选C。
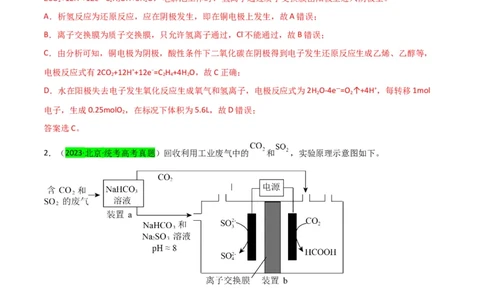
2.(2023·北京·统考高考真题)回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和
资料整理【淘宝店铺:向阳百分百】D.装置 中的总反应为
【答案】C
【解析】A. 是酸性氧化物,废气中 排放到空气中会形成硫酸型酸雨,故A正确;
B.装置a中溶液的溶质为 ,溶液显碱性,说明 的水解程度大于电离程度,故B正确;
C.装置a中 溶液的作用是吸收 气体, 与 溶液不反应,不能吸收 ,故C错误;
D.由电解池阴极和阳极反应式可知,装置b中总反应为 ,故D正确;
选C。
1.解答步骤
第一步,分清隔膜类型。即交换膜属于阳膜、阴膜、质子膜中的哪一种,判断允许哪种离子通过隔膜。
第二步,写出电极反应式。判断交换膜两侧离子变化,推断电荷变化,根据电荷平衡判断离子迁移方向。
第三步,分析隔膜作用。在产品制备中,隔膜作用主要是提高产品纯度,避免产物之间发生反应,或避免
产物因发生反应而造成危险。
2.离子交换膜类型的判断方法
依据电解质溶液呈电中性的原理,判断膜的类型,判断时首先要写出阴、阳两极上的电极反应,依据电极
反应式确定该电极附近哪种离子剩余;依据该电极附近电解质溶液满足电荷守恒原则,判断出离子移动的
方向、进而确定离子交换膜的类型。
1.离子交换膜的功能
使离子选择性定向迁移(目的是平衡整个溶液的离子浓度或电荷)。
2.离子交换膜在电化学中的作用
(1)隔离某些物质防止发生反应。
(2)用于物质的制备。
(3)物质分离、提纯等。
资料整理【淘宝店铺:向阳百分百】3.离子交换膜的类型
离子交换膜是由高分子特殊材料制成。离子交换膜分四类:
①阳离子交换膜,简称阳膜,只允许阳离子通过,即允许H+和其他阳离子通过,不允许阴离子通过。
②阴离子交换膜,简称阴膜,只允许阴离子通过,不允许阳离子通过。
③质子交换膜,只允许H+通过,不允许其他阳离子和阴离子通过。
④双极膜,由一张阳膜和一张阴膜复合制成的阴、阳复合膜。该膜特点是在直流电的作用下,阴、阳膜复
合层间的HO解离成H+和OH-并分别通过阴膜和阳膜,作为H+和OH-的离子源。
2
4.应用原理
(1)阳(阴)离子交换膜有很多微孔,孔道上有许多带负(正)电荷的基团,阳(阴)离子可以自由通
过孔道,而阴(阳)离子移动到孔道处,受到孔道带负(正)电荷基团的排斥而不能进入孔道中,因而不
能通过交换膜。
质子交换膜是阳离子交换膜的特例,仅允许质子(H+)通过,其他离子不能通过。
(2)交换膜隔离两种电解质溶液,避免负极材料与能发生反应的电解质溶液直接接触,能提高电流效率。
在这种装置中,交换膜起到盐桥作用,且优于盐桥(盐桥需要定时替换或再生)。通过限制离子迁移,使指
定离子在溶液中定向移动形成闭合回路,完成氧化剂和还原剂在不接触条件下发生氧化还原反应。
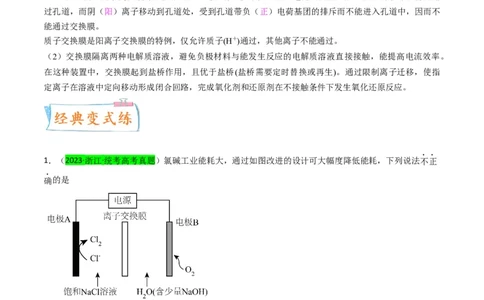
1.(2023·浙江·统考高考真题)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正
确的是
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
【答案】B
【解析】A.电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接电源正极,
资料整理【淘宝店铺:向阳百分百】发生氧化反应,故A正确;
B.电极B为阴极,通入氧气,氧气得到电子,其电极反应式为: ,故B错误;
C.右室生成氢氧根,应选用阳离子交换膜,左边的钠离子进入到右边,在右室获得浓度较高的 溶
液,故C正确;
D.改进设计中增大了氧气的量,提高了电极B处的氧化性,通过反应物的氧化性来降低电解电压,减少
能耗,故D正确。
综上所述,答案为B。
2.(2022·全国·高考真题)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O
2 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于两
2 2 2
个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可
以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,生成
资料整理【淘宝店铺:向阳百分百】Zn(OH) ,Ⅱ区的SO 向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。
3.(2022·山东·高考真题)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生
成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
【答案】BD
【解析】A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,同时生成H+,电极
2
反应式为CH COO--8 e-+2 H O =2CO ↑+7 H+,H+通过阳膜进入阴极室,甲室的电极反应式为Co2++2e-=Co,因
3 2 2
此,甲室溶液pH逐渐减小,A错误;
B.对于乙室,正极上LiCoO 得到电子,被还原为C o2+,同时得到Li+,其中的O2-与溶液中的H+结合
2
资料整理【淘宝店铺:向阳百分百】H O,电极反应式为2LiCoO +2e-+8H+=2Li++2Co2++4H O,负极发生的反应为CH COO--8 e-+2 H O =2CO ↑+7
2 2 2 3 2 2
H+,负极产生的H+通过阳膜进入正极室,但是乙室的H+浓度仍然是减小的,因此电池工作一段时间后应该
补充盐酸,B正确;
C.电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO +e-+4H+=Li++Co2++2H O,C错误;
2 2
D.若甲室Co2+减少200 mg,则电子转移物质的量为n(e-)= ;若乙室Co2+增加300
mg,则转移电子的物质的量为n(e-)= ,由于电子转移的物质的量不等,说明此时已
进行过溶液转移,即将乙室部分溶液转移至甲室,D正确;
故合理选项是BD。
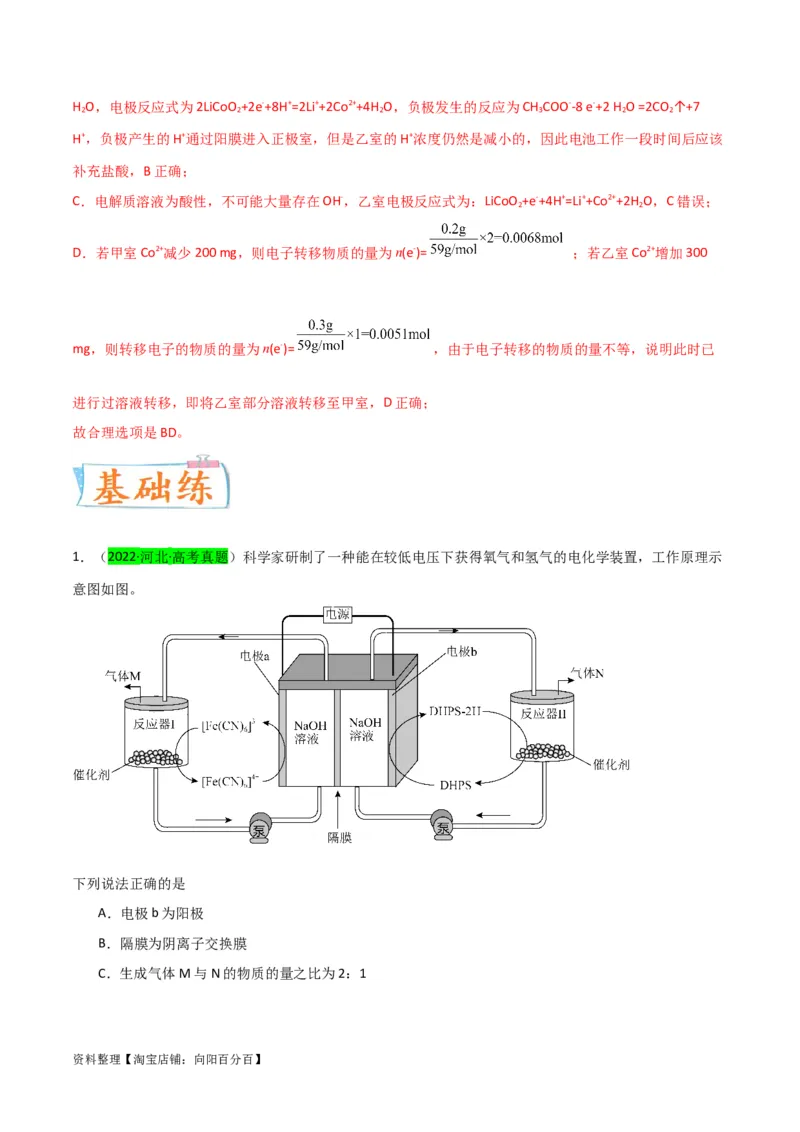
1.(2022·河北·高考真题)科学家研制了一种能在较低电压下获得氧气和氢气的电化学装置,工作原理示
意图如图。
下列说法正确的是
A.电极b为阳极
B.隔膜为阴离子交换膜
C.生成气体M与N的物质的量之比为2:1
资料整理【淘宝店铺:向阳百分百】D.反应器I中反应的离子方程式为4[Fe(CN) ]3—+4OH— 4[Fe(CN) ]4—+O ↑+2H O
6 6 2 2
【答案】BD
【解析】由图可知,a电极为阳极,碱性条件下[Fe(CN) ]4—离子在阳极失去电子发生氧化反应生成[Fe(CN) ]3
6 6
—离子,催化剂作用下,[Fe(CN) ]3—离子与氢氧根离子反应生成[Fe(CN) ]4—离子、氧气和水,b电极为阴极,
6 6
水分子作用下DHPS在阴极得到电子发生还原反应生成DHPS—2H和氢氧根离子,催化剂作用下,DHPS—
2H与水反应生成DHPS和氢气,氢氧根离子通过阴离子交换膜由阴极室向阳极室移动,则M为氧气、N为
氢气。
A.由分析可知,b电极为电解池的阴极,故A错误;
B.由分析可知,氢氧根离子通过阴离子交换膜由阴极室向阳极室移动,则隔膜为阴离子交换膜,故B正
确;
C.由分析可知,M为氧气、N为氢气,由得失电子数目守恒可知,氧气和氢气的的物质的量之比为1:
2,故C错误;
D.由分析可知,反应器I中发生的反应为催化剂作用下,[Fe(CN) ]3—离子与氢氧根离子反应生成[Fe(CN) ]4—
6 6
离子、氧气和水,反应的离子方程式为4[Fe(CN) ]3—+4OH— 4[Fe(CN) ]4—+O ↑+2H O,故D正确;
6 6 2 2
故选BD。
2.(2023·全国·高三统考专题练习)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法
不正确的是
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
资料整理【淘宝店铺:向阳百分百】D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
【答案】B
【解析】A.电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接电源正极,
发生氧化反应,故A正确;
B.电极B为阴极,通入氧气,氧气得到电子,其电极反应式为: ,故B错误;
C.右室生成氢氧根,应选用阳离子交换膜,左边的钠离子进入到右边,在右室获得浓度较高的 溶
液,故C正确;
D.改进设计中增大了氧气的量,提高了电极B处的氧化性,通过反应物的氧化性来降低电解电压,减少
能耗,故D正确。
综上所述,答案为B。
3.(2023·北京·高三统考专题练习)回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和
D.装置 中的总反应为
【答案】C
【解析】A. 是酸性氧化物,废气中 排放到空气中会形成硫酸型酸雨,故A正确;
资料整理【淘宝店铺:向阳百分百】B.装置a中溶液的溶质为 ,溶液显碱性,说明 的水解程度大于电离程度,故B正确;
C.装置a中 溶液的作用是吸收 气体, 与 溶液不反应,不能吸收 ,故C错误;
D.由电解池阴极和阳极反应式可知,装置b中总反应为 ,故D正确;
选C。
4.(2023·全国·高三统考专题练习)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
【答案】B
【解析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳电极为正极,正极
4
上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO 电极为阴极,PbSO 得
4 4
电子生成Pb和硫酸。
A.放电时负极上Pb失电子结合硫酸根离子生成PbSO 附着在负极上,负极质量增大,A错误;
4
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错误;
D.充电时,总反应为PbSO +2Fe2+=Pb+ +2Fe3+,D错误;
4
故答案选B。
5.(2023·江西上饶·校联考二模)Li-O 电池比能最高,在汽车、航天等领域具有良好的应用前景。近年
2
科学来家研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动
2
阴极反应(Li+ +e-= Li)和阳极反应Li O +2h+=2Li++O )对电池进行充电,下列叙述错误的是
2 2 2
资料整理【淘宝店铺:向阳百分百】A.放电时,电池的总反应2Li+O =Li O
2 2 2
B.充电时,Li+从锂电极穿过离子交换膜向光催化电极迁移
C.放电时,每转移2mol电子,消耗标况下的O 体积为22.4L
2
D.充电效率与光照产生的电子和空穴量有关
【答案】B
【解析】A.由题意可知,充电时总反应为Li O =2Li+O ,则放电时,电池的总反应2Li+O =Li O ,故A正确;
2 2 2 2 2 2
B.由题意可知,充电时,锂电极为阴极、光催化电极为阳极,则阳离子锂离子向锂电极迁移,故B错误;
C.由分析可知,放电时,光催化电极为正极,锂离子作用下氧气在正极得到电子发生还原反应生成过氧
化锂,电极反应式为O +2Li++2e—=Li O ,则每转移2mol电子,消耗标况下氧气的体积为2mol× ×22.4L/
2 2 2
mol=22.4L,故C正确;
D.由题意可知,充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,
则充电效率与光照产生的电子和空穴量有关,故D正确;
故选B。
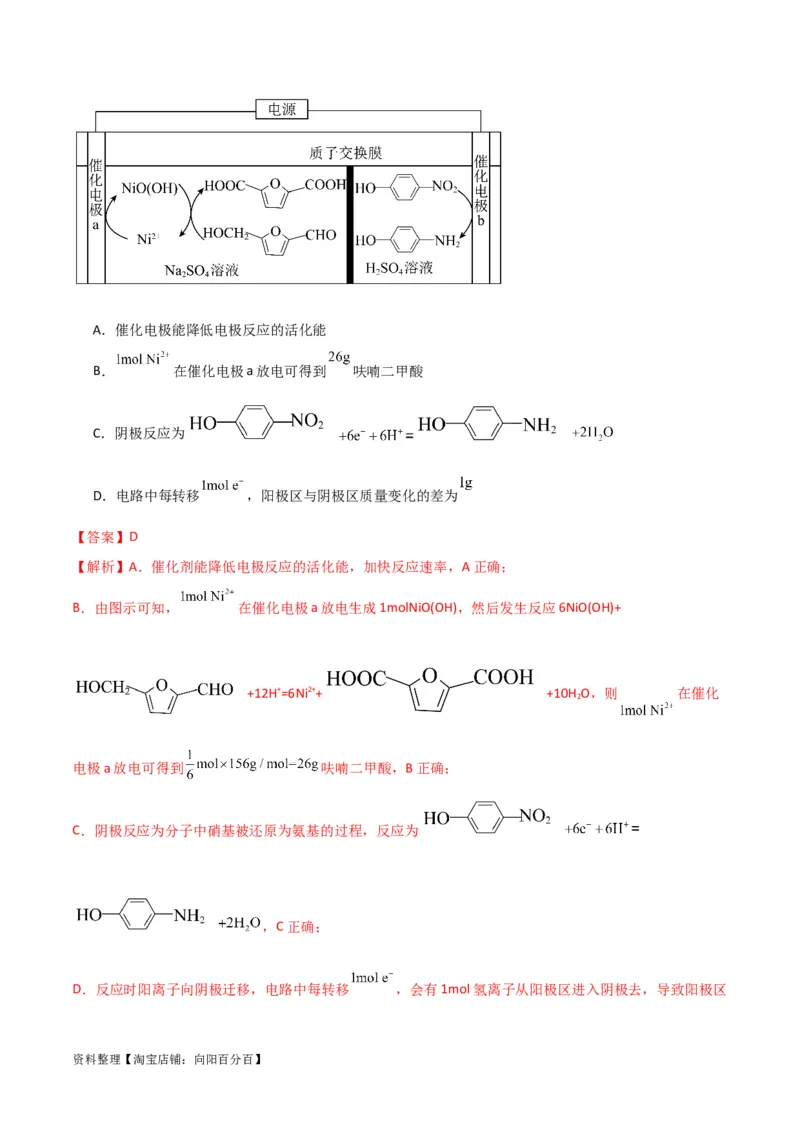
6.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)电有机合成相对于传统有机合成具有显著优势,利用如
图所示装置实现电催化合成呋喃二甲酸。下列说法错误的是
资料整理【淘宝店铺:向阳百分百】A.催化电极能降低电极反应的活化能
B. 在催化电极a放电可得到 呋喃二甲酸
C.阴极反应为
D.电路中每转移 ,阳极区与阴极区质量变化的差为
【答案】D
【解析】A.催化剂能降低电极反应的活化能,加快反应速率,A正确;
B.由图示可知, 在催化电极a放电生成1molNiO(OH),然后发生反应6NiO(OH)+
+12H+=6Ni2++ +10H O,则 在催化
2
电极a放电可得到 呋喃二甲酸,B正确;
C.阴极反应为分子中硝基被还原为氨基的过程,反应为
,C正确;
D.反应时阳离子向阴极迁移,电路中每转移 ,会有1mol氢离子从阳极区进入阴极去,导致阳极区
资料整理【淘宝店铺:向阳百分百】减小1g、阴极区增加1g,质量变化的差为2g,D错误;
故选D。
7.(2023·陕西西安·统考一模)高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
A.放电时,负极反应式为Zn-2e-+4OH-=Zn(OH)
B.充电时,电路中转移2mole-,中性电解质NaCl的物质的量增多2mol
C.放电时,1molFQ转化为FQH 转移2mol电子
2
D.充电时,m接外接电源的负极,n接外接电源的正极
【答案】B
【解析】高电压水系锌-有机混合液流电池工作原理为:放电时为原电池,金属Zn发生失电子的氧化反应
生成Zn2+,为负极,则FQ所在电极为正极,正极反应式为2FQ+2e-+2H+═FQH ,负极反应式为Zn-2e-+4OH-
2
=Zn(OH) ;充电时电解池,原电池的正负极连接电源的正负极,阴阳极的电极反应与原电池的负正极的反
应式相反,电解质中阳离子移向阴极、阴离子移向阳极,因此充电时,m接外接电源的负极,n接外接电
源的正极。
A.放电时为原电池,金属Zn为负极,负极反应式为 ,选项A正确;
B.充电时装置为电解池,电解质中阳离子移向阴极、阴离子移向阳极,NaCl溶液中的钠离子和氯离子分
别发生定向移动,即电解质NaCl的浓度减小,选项B错误;
C.充电时电解池,阳极反应为FQH -2e-=2FQ+2e-+2H+,则1molFQH 转化为FQ时转移2mol电子,选项C正
2 2
确;
D.根据上述分析可知,充电时,m接外接电源的负极,n接外接电源的正极,选项D正确;
故答案选B。
8.(2023·辽宁沈阳·东北育才学校校考模拟预测)一种氯离子介导的电化学合成方法,能将乙烯高效清洁、
选择性地转化为环氧乙烷,电化学反应的具体过程如图所示。在电解结束后,将阴、阳极电解液输出混合,
资料整理【淘宝店铺:向阳百分百】便可反应生成环氧乙烷。下列说法错误的是
A.Ni电极与电源负极相连
B.阴极生成标况下22.4L气体,最终可制得2mol
C.工作过程中阴极附近pH增大
D.在电解液混合过程中会发生反应:HCl+KOH=KCl+H O
2
【答案】B
【解析】根据题给信息得乙烯在左室与HClO发生氧化还原反应,HClO由Cl 与H O反应生成,而由 转
2 2
化生成 应发生在Pt电极上,即Pt电极为阳极,连接电源正极,Ni为阴极,连接电源负极。
A.根据分析知,Ni为阴极,与电源负极相连,A正确;
B.阴极电极反应式为: ,阴极生成标况下22.4L气体时,电路上转移的电子为
2mol;阳极对应生成1molCl ,Cl 与水反应为可逆反应,生成的HClO小于1mol,被氧化的CH =CH 小于
2 2 2 2
1mol,因此可制得的环氧乙烷小于1mol,B错误;
C.工作过程中,阴极上水被电解生成氢气和氢氧根离子,因此阴极附近pH增大,C正确;
D.电解过程中,阳极生成的Cl 与水反应时生成HCl,阴极反应生成KOH,电解液混合时会发生以下反应:
2
HCl+KOH=KCl+H O,D正确;
2
故选B。
9.(2023春·山东烟台·高三统考期中)据2022年1月统计,我国光伏发电并网装机容量突破3亿千瓦,
连续七年稳居全球首位。已知四甲基氢氧化铵 常用作电子工业清洗剂,以四甲基氯化铵
资料整理【淘宝店铺:向阳百分百】为原料,采用电渗析法合成[ , ],工作原理如图。下列说法错误
的是
A.光伏并网发电装置中N型半导体为负极,P型半导体为正极
B.c为阳离子交换膜,d、e均为阴离子交换膜
C.a电极反应式为
D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况)
【答案】B
【解析】A.a极发生还原反应,为阴极,其连接的N型半导体为负极,b极发生氧化反应,为阳极,其连
接的M型半导体为正极,A项正确;
B.(CH ) N+通过c膜,通过Na+通过e膜,c、e为阳离子交换膜,Cl-通过d膜,d为阴离子交换膜,B项错
3 4
误;
C.a极为阴极,发生还原反应,电极反应式为 2(CH ) N++2H O+2e−=2(CH ) NOH+H ↑,C项正确;
3 4 2 3 4 2
D.制备182g四甲基氢氧化铵则转移2mole-,阴极产生1molH ,阳极产生0.5molO (电极反应式为4OH
2 2
--4e-=O ↑+2H O),共产生1.5mol气体(标准状况下为33.6L),D项正确。
2 2
答案选B。
10.(2023春·山东烟台·高三统考期中)电催化NO合成氨技术凭借其低能耗、绿色环保等优势成为化工
行业关注的热点。某科研团队设计的Zn-NO电池装置及在不同电压下 的单位时间产量如下图所示,已
知:①双极膜中 电离出的 和 在电场作用下可以向两极迁移;②法拉第效率
。下列说法错误的是
资料整理【淘宝店铺:向阳百分百】A.双极膜中的 移向X极
B.Y极电极反应式为
C.当外电路通过 时,双极膜中有 发生解离
D.0.5V电压下连续放电10小时,外电路通过 ,法拉第效率为93.5%
【答案】D
【解析】A.双极膜中的 移向负极即X极,A正确;
B.Y极NO得电子变成氨气,且氢离子移向正极即Y极,电极反应式为 ,B正
确;
C.由B可知,当外电路通过 时消耗1molH+,故双极膜中有 发生解离得到1molH+,C正确;
D.由图可知当电压为0.5V时,氨气产量为 ,则10h产生氨气为 ,由
可知,当电路中通过 时,理论上氨气的质量为
,法拉第效率为 ,D错误。
故选D。
1.(2023·山东·统考高考真题)利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,
资料整理【淘宝店铺:向阳百分百】甲、乙两室均预加相同的 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
【答案】CD
【解析】A. 向甲室加入足量氨水后电池开始工作,则甲室 电极溶解,变为铜离子与氨气形成
,因此甲室 电极为负极,故A错误;
B. 再原电池内电路中阳离子向正极移动,若隔膜为阳离子膜,电极溶解生成的铜离子要向右侧移动,通入
氨气要消耗铜离子,显然左侧阳离子不断减小,明显不利于电池反应正常进行,故B错误;
C. 左侧负极是 ,正极是 ,则电池总反应为:
,故C正确;
D. 扩散到乙室会与铜离子反应生成 ,铜离子浓度降低,铜离子得电子能力减弱,因此
将对电池电动势产生影响,故D正确。
综上所述,答案为CD。
2.(2023·全国·高三统考专题练习)电解质浓度不同形成的浓差电池,称为离子浓差电池。以浓差电池为
电源,以石墨为电极将NH 转化为高纯H 的装置如图所示。下列说法正确的是
3 2
资料整理【淘宝店铺:向阳百分百】A.Cu(1)的电势低于Cu(2)的电势
B.C(1)极电极反应式为2NH -6e-+6OH-=N +6H O
3 2 2
C.工作时,左池 从左侧经膜Ⅰ移向右侧,右池OH-从左侧经膜Ⅱ移向右侧
D.当浓差电池停止放电时,理论上可得到22.4L标准状况下的H (忽略溶液体积变化)
2
【答案】B
【解析】以浓差电池为电源,以石墨为电极将NH 转化为高纯H ,C(1)电极上,NH 转化为N ,N元素化合
3 2 3 2
价升高,发生氧化反应,C(1)电极为阳极,则C(2)电极为阴极,Cu(1)为正极,Cu(2)为负极。
A.由分析知,Cu(1)为正极,Cu(1)的电势高于Cu(2)的电势,A项错误;
B.C(1)极电极上NH 失电子被氧化为N ,电极反应式为2NH -6e-+6OH-=N +6H O,B项正确;
3 2 3 2 2
C.原电池中阴离子向负极迁移,则SO 向电池负极移动,故SO 经过阴离子交换膜Ⅰ从右侧移向左侧;
电解池在阴离子向阳极迁移,故OH-经过阴离子交换膜Ⅱ由右侧移向左侧,C项错误;
D.当浓差电池左右浓度相等时则停止放电,设负极放电使溶液中增加x mol Cu2+,则正极减少x mol
Cu2+,当浓差电池停止放电时有:x+2L×0.5mol/L=2L×2.5mol/L-x,解得x=2mol,则此时电路中转移电子
2×2mol=4mol,右池阴极反应为:2H O+2e-=H ↑+2OH-,则此时生成H 物质的量4mol× =2mol,标准状况
2 2 2
下其体积为2mol×22.4L/mol=44.8L,D项错误;
答案选B。
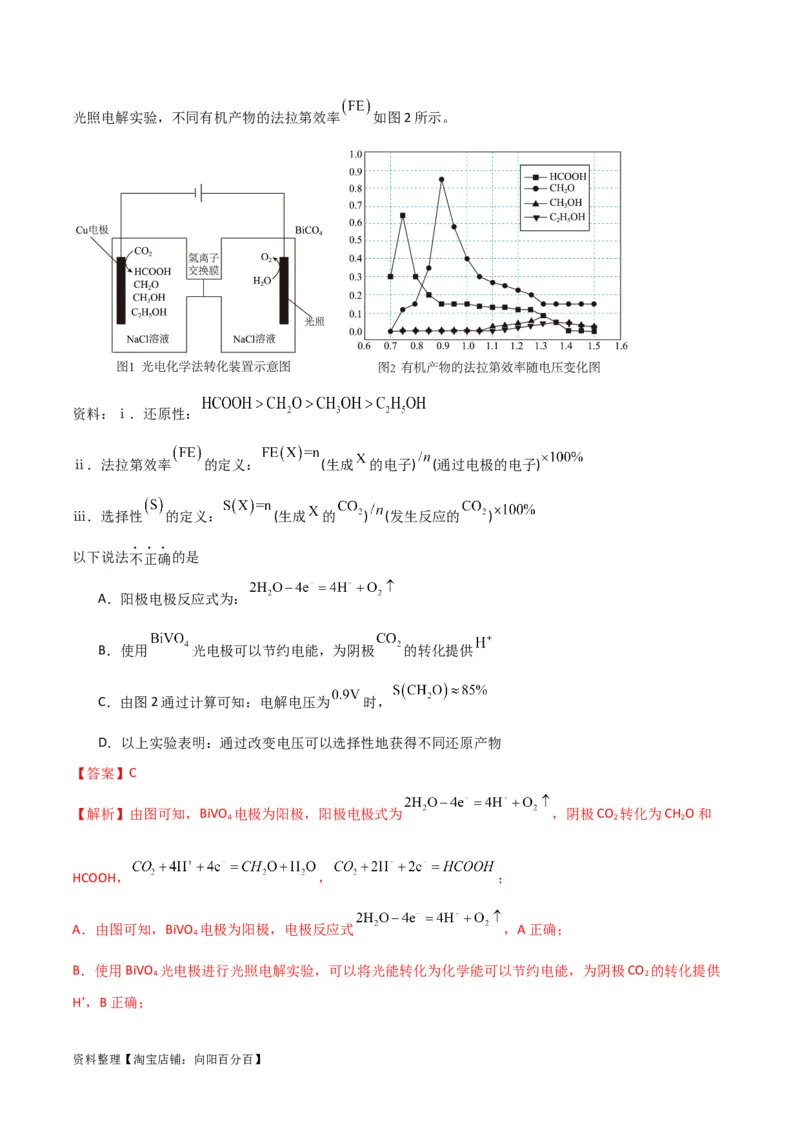
3.(2023·北京西城·北师大实验中学校考三模)光电化学装置可以将 还原为有机物,实现碳资源的再
生利用。图1是光电化学法实现 转化的 电解装置示意图。在不同电压条件下进行
资料整理【淘宝店铺:向阳百分百】光照电解实验,不同有机产物的法拉第效率 如图2所示。
资料:ⅰ.还原性:
ⅱ.法拉第效率 的定义: (生成 的电子) (通过电极的电子)
ⅲ.选择性 的定义: (生成 的 ) (发生反应的 )
以下说法不正确的是
A.阳极电极反应式为:
B.使用 光电极可以节约电能,为阴极 的转化提供
C.由图2通过计算可知:电解电压为 时,
D.以上实验表明:通过改变电压可以选择性地获得不同还原产物
【答案】C
【解析】由图可知,BiVO 电极为阳极,阳极电极式为 ,阴极CO 转化为CH O和
4 2 2
HCOOH, , ;
A.由图可知,BiVO 电极为阳极,电极反应式 ,A正确;
4
B.使用BiVO 光电极进行光照电解实验,可以将光能转化为化学能可以节约电能,为阴极CO 的转化提供
4 2
H+,B正确;
资料整理【淘宝店铺:向阳百分百】C.由分析可知,生成等物质的量的CH O或HCOOH等产物时转移的电子不同,由法拉第效率的定义,
2
,选择性(S)的定义, ,故由
图2可知,电解电压为0.9V 时,则 ,则 ,C错误;
D.由图2可知,通过改变电压可以选择性地获得不同还原产物,D正确;
故答案为:C。
4.(2023春·河北石家庄·高三校联考阶段练习)我国科学家设计了一种利用废水中的 将苯酚氧化为
和 的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基( )的氧
化性仅次于氟气。下列说法正确的是
A.电子转移方向:c电极→导线→b电极
B.d电极的电极反应为
C.右侧装置中,c、d两电极产生气体的体积比(相同条件下)为
D.若a电极上有 参与反应,理论上 溶液中有 通过阴离子膜进入a电极区溶液
【答案】C
资料整理【淘宝店铺:向阳百分百】【解析】
该装置是利用废水中的 将苯酚氧化为 和 的原电池—电解池组合装置,左侧为原电池,右侧
为电解池,a电极发生还原反应,为正极,b电极发生氧化反应,为负极,则c电极为阴极,d电极为阳极。
A.左侧装置是原电池,右侧装置是电解池,原电池中,a电极是正极,b电极为负极。电解池中,c电极
是阴极,d电极是阳极。电子转移方向:b电极→导线→c电极,故A错误;
B.根据图示可知,d电极的电极反应为 ,故B错误;
C.c电极的电极反应为 ,每转移 电子,c电极上产生 气体。d电极的电
极反应为 ,羟基自由基( )的氧化性仅次于氟气,苯酚被羟基自由基氧化的化学方程
式为 ,每转移 电子,d电极上产生 气体。c、d
两电极产生气体的体积比(相同条件下)为 ,故C正确;
D.a电极的电极反应为 ,若a电极上有 参与反应,理
论上有 从a电极区溶液通过阴离子膜进入 溶液,故D错误;
故选C。
5.(2023·陕西咸阳·统考三模)最近科学家研发了“全氢电池”,工作原理如图所示。下列说法正确的是
资料整理【淘宝店铺:向阳百分百】A.吸附层a发生的电极反应为:
B.NaClO 的作用是传导离子并参与电极反应
4
C.电解质溶液中Na+向左移动,ClO 向右移动
D.全氢电池的总反应为:2H +O =2H O
2 2 2
【答案】A
【解析】A.电子由吸附层a流出且氢气在吸附层a上与氢氧根结合生成水,则吸附层a发生的电极反应为:
,故A正确;
B. 的作用是离子的定向移动而形成电流,,但不参与电极反应,故B错误;
C.由分析可知,吸附层a为负极、吸附层b为正极;阳离子( )向正极移动(向右移);阴离子
( )移向负极(即向左移动),故C错误;
D.吸附层a上氢气失去电子与氢氧根结合生成水;吸附层b上氢离子得到电子生成氢气可知,“全氢电
池”工作时,将酸与碱反应的化学能转化为电能,则其总反应为: ,故D错误;
答案选A。
6.(2023·浙江·校联考模拟预测)直接 燃料电池是一种新型化学电源,其工作原理如图所示。
电池放电时,下列说法不正确的是
资料整理【淘宝店铺:向阳百分百】A.电池工作时,电极I电势低
B.电极Ⅱ的反应式为:
C.电池总反应为:
D.当电路中转移0.1mol电子时,通过阳离子交换膜的 为3.9g
【答案】C
【解析】电池工作时,电势低的是负极,电子从负极流向正极,故电极I为负极,电极Ⅱ为正极,负极:
H O -2e-+2OH-=O +2H O,正极: 。
2 2 2 2
A.电池工作时,电势低的是负极,电子从负极流向正极,故电极I电势低,A正确;
B.电极Ⅱ为正极,电极反应式为: ,B正确;
C.该电池放电过程中,负极区的OH-来自KOH,正极区的 来自H SO ,K+通过阳离子交换膜进入正极区
2 4
与硫酸根结合生成K SO ,因此电池总反应为: ,C错误;
2 4
D.当电路中转移0.1mol电子时,通过阳离子交换膜的 为0.1mol,即3.9g,D正确;
故选C。
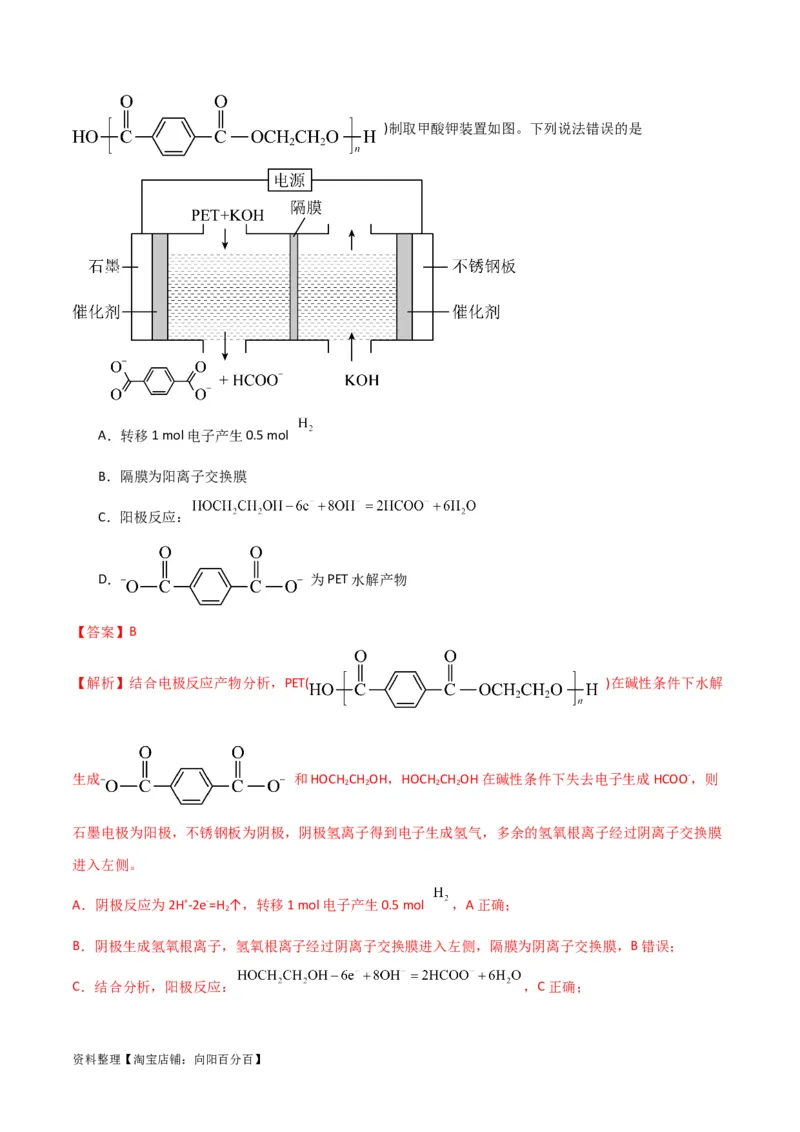
7.(2023秋·福建龙岩·高三校联考期末)某温度下,应用电化学原理处理废旧塑料PET(
资料整理【淘宝店铺:向阳百分百】)制取甲酸钾装置如图。下列说法错误的是
A.转移1 mol电子产生0.5 mol
B.隔膜为阳离子交换膜
C.阳极反应:
D. 为PET水解产物
【答案】B
【解析】结合电极反应产物分析,PET( )在碱性条件下水解
生成 和HOCH CH OH,HOCH CH OH在碱性条件下失去电子生成HCOO-,则
2 2 2 2
石墨电极为阳极,不锈钢板为阴极,阴极氢离子得到电子生成氢气,多余的氢氧根离子经过阴离子交换膜
进入左侧。
A.阴极反应为2H+-2e-=H ↑,转移1 mol电子产生0.5 mol ,A正确;
2
B.阴极生成氢氧根离子,氢氧根离子经过阴离子交换膜进入左侧,隔膜为阴离子交换膜,B错误;
C.结合分析,阳极反应: ,C正确;
资料整理【淘宝店铺:向阳百分百】D. PET( )在碱性条件下水解生成
和HOCH CH OH,D正确;
2 2
故选B。
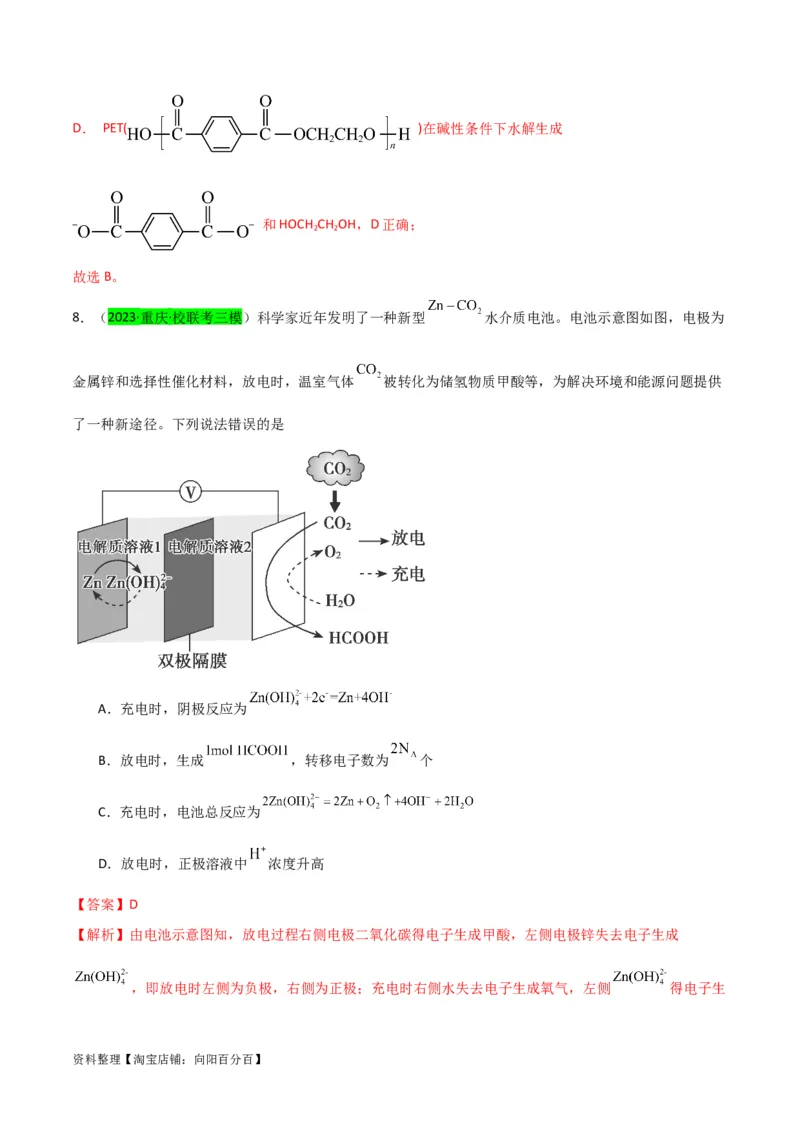
8.(2023·重庆·校联考三模)科学家近年发明了一种新型 水介质电池。电池示意图如图,电极为
金属锌和选择性催化材料,放电时,温室气体 被转化为储氢物质甲酸等,为解决环境和能源问题提供
了一种新途径。下列说法错误的是
A.充电时,阴极反应为
B.放电时,生成 ,转移电子数为 个
C.充电时,电池总反应为
D.放电时,正极溶液中 浓度升高
【答案】D
【解析】由电池示意图知,放电过程右侧电极二氧化碳得电子生成甲酸,左侧电极锌失去电子生成
,即放电时左侧为负极,右侧为正极;充电时右侧水失去电子生成氧气,左侧 得电子生
资料整理【淘宝店铺:向阳百分百】成锌单质,即充电时左侧为阴极,右侧为阳极。
A.充电时阴极发生还原反应,元素化合价降低,即是 ,A正确;
B.二氧化碳中碳元素+4价,甲酸中碳元素+2价,即放电时生成 转移电子数为 个,B正
确;
C.充电时阴极反应为 ;阳极反应为 ,故总反应为
,C正确;
D.放电时正极反应为 ,即正极溶液中 浓度降低,D错误;
故选D。
9.(2023·全国·高三专题练习)按照要求回答下列问题:
(1)用NaOH溶液吸收烟气中的SO ,将所得的Na SO 溶液进行电解,可循环再生NaOH,同时得到H SO ,
2 2 3 2 4
其原理如图所示(电极材料均为石墨)。
①图中A口产生的气体为 ,B口流出的物质是 。
②b电极表面发生的电极反应式为 。
(2)Co是磁性合金的重要材料,也是维生素的重要组成元素。工业上可用如图装置制取单质Co并获得副产
品盐酸(A、B均为离子交换膜)。
资料整理【淘宝店铺:向阳百分百】①A为 (填“阳”或“阴”)离子交换膜。
②该电解池的总反应离子方程式为 。
③若产品室中阴极质量增加11.8g,则产品室增加的HCl的物质的量为 。
【答案】(1) 氢气 氢氧化钠
(2) 阳 0.4mol
【解析】依据电解质溶液中阴阳离子的移动方向判断电极,阳离子移向阴极,a为阴极,b为阳极,
在阳极失去电子变成 ,可能伴有氢氧根离子放电生成氧气,所以C口流出的物质是H SO ,阴极区放
2 4
电离子为氢离子生成氢气;由图可知,Co为阴极,电极反应式为Co2++2e-=Co,石墨为阳极,电极反应式为
2H O-4e-=O ↑+4H+。
2 2
(1)①电解池中阳离子向阴极移动,由图可知,a为阴极,水放电生成氢气和氢氧根离子,图中A口产生
的气体为氢气,B口流出的物质是氢氧化钠;
②b电极为阳极,亚硫酸根离子失去电子发生氧化反应生成硫酸根离子,表面发生的电极反应式为
;
(2)①工业上可用如图装置制取单质Co并获得副产品盐酸,Co2+在阴极发生还原反应生成Co单质,阳极
水放电生成氧气和氢离子,阳极室中氢离子通过A膜、阴极室中氯离子通过B膜向产品室迁移得到HCl,
故A为阳离子交换膜;
②由①分析可知,该电解池的总反应离子方程式为 ;
资料整理【淘宝店铺:向阳百分百】③若产品室中阴极质量增加11.8g,则生成0.2mol Co,根据电子守恒可知, ,产品室增加
的HCl的物质的量为0.4mol。
资料整理【淘宝店铺:向阳百分百】