文档内容
微专题33 四步敲定高考新情景电池电极反应式的书写
1.(2023·全国·统考高考真题)一种以 和 为电极、 水溶液为电解质的电池,其示意
图如下所示。放电时, 可插入 层间形成 。下列说法错误的是
A.放电时 为正极
B.放电时 由负极向正极迁移C.充电总反应:
D.充电阳极反应:
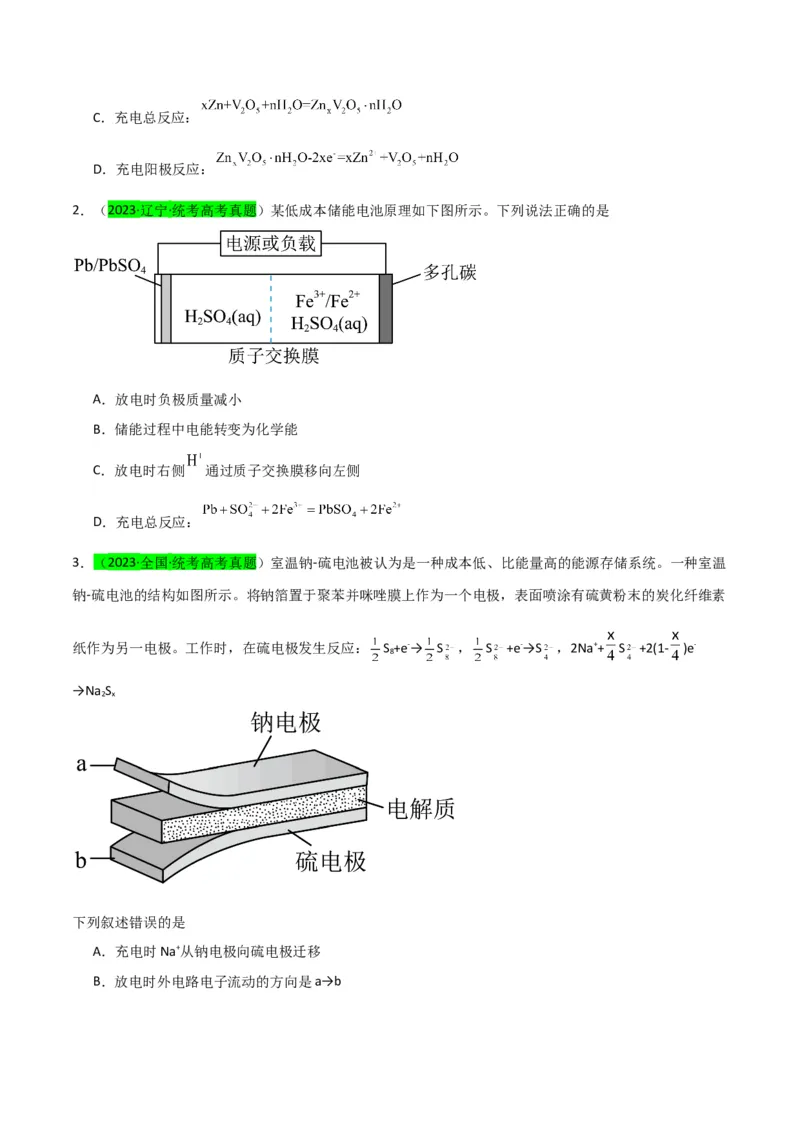
2.(2023·辽宁·统考高考真题)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
3.(2023·全国·统考高考真题)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温
钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素
纸作为另一电极。工作时,在硫电极发生反应: S +e-→ S , S +e-→S ,2Na++ S +2(1- )e-
8
→Na S
2 x
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→bC.放电时正极反应为:2Na++ S +2e-→Na S
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
1.原电池电极反应书写时的注意事项
(1)负失氧、正得还。
(2)注意溶液的酸碱性,视情况在电极反应方程式两边添加H+、OH-、H O等,使其符合电荷守恒和质量守恒。
2
(3)注意电极反应产物是否与电解质溶液反应。
(4)活泼金属不一定为负极,如镁、铝和氢氧化钠溶液组成的电池中,铝为负极。
1.“四步法”书写电极反应式的步骤如下:
第一步:书写负极(阳极),还原性微粒—ne-→氧化性产物;正极(阴极):氧化性微粒+ne-→还原性产
物。
第二步:标变价算n值,n=(高价—低价)×变价原子个数。
第三步:根据电池情景用H+、OH-、O2-、CO2-
等阴、阳离子配平电荷。
3
第四步:用H O等小分子配平原子。
2
2.用总反应式书写电极反应式
(1)书写三步骤
步骤一:写出电池总反应式,标出电子转移的方向和数目(ne-)。
步骤二:找出正、负极,失电子的电极为负极;确定溶液的酸碱性。
步骤三:写电极反应式。
负极反应:还原剂-ne-===氧化产物
正极反应:氧化剂+ne-===还原产物
(2)书写技巧
若某电极反应式较难写出时,可先写出较易的电极反应式,然后根据得失电子守恒,用总反应式减去较易
的电极反应式,即可得出较难写的电极反应式。
3.燃料电池中电极反应式的书写
第一步:写出电池总反应式
燃料电池的总反应与燃料的燃烧反应一致,若产物能和电解质反应则总反应为加和后的反应。
如甲烷燃料电池(电解质为NaOH溶液)的反应式为CH+2O===CO +2HO ①
4 2 2 2
CO+2NaOH===Na CO+HO ②
2 2 3 2
①式+②式得燃料电池总反应式为CH+2O+2NaOH===Na CO+3HO。
4 2 2 3 2
第二步:写出电池的正极反应式
根据燃料电池的特点,一般在正极上发生还原反应的物质是O ,随着电解质溶液的不同,其电极反应式有
2
所不同,大致有以下四种情况:
(1)酸性电解质溶液环境下电极反应式:
O+4H++4e-===2H O。
2 2
(2)碱性电解质溶液环境下电极反应式:
O+2HO+4e-===4OH-。
2 2
(3)固体电解质(高温下能传导O2-)环境下电极反应式:
O+4e-===2O2-。
2
(4)熔融碳酸盐(如熔融KCO)环境下电极反应式:
2 3
O+2CO+4e-===2CO。
2 2
第三步:根据电池总反应式和正极反应式写出负极反应式
电池反应的总反应式-电池正极反应式=电池负极反应式。因为O 不是负极反应物,因此两个反应式相减
2
时要彻底消除O。
2
(5)常见介质
常见介质 注意事项
中性溶液 反应物若是H+得电子或OH-失电子,则H+或OH-均来自于水的电离
酸性溶液 反应物或生成物中均没有OH-
碱性溶液 反应物或生成物中均没有H+
水溶液 不能出现O2-
1.(2022·辽宁·统考高考真题)某储能电池原理如图。下列说法正确的是A.放电时负极反应:
B.放电时 透过多孔活性炭电极向 中迁移
C.放电时每转移 电子,理论上 吸收
D.充电过程中, 溶液浓度增大
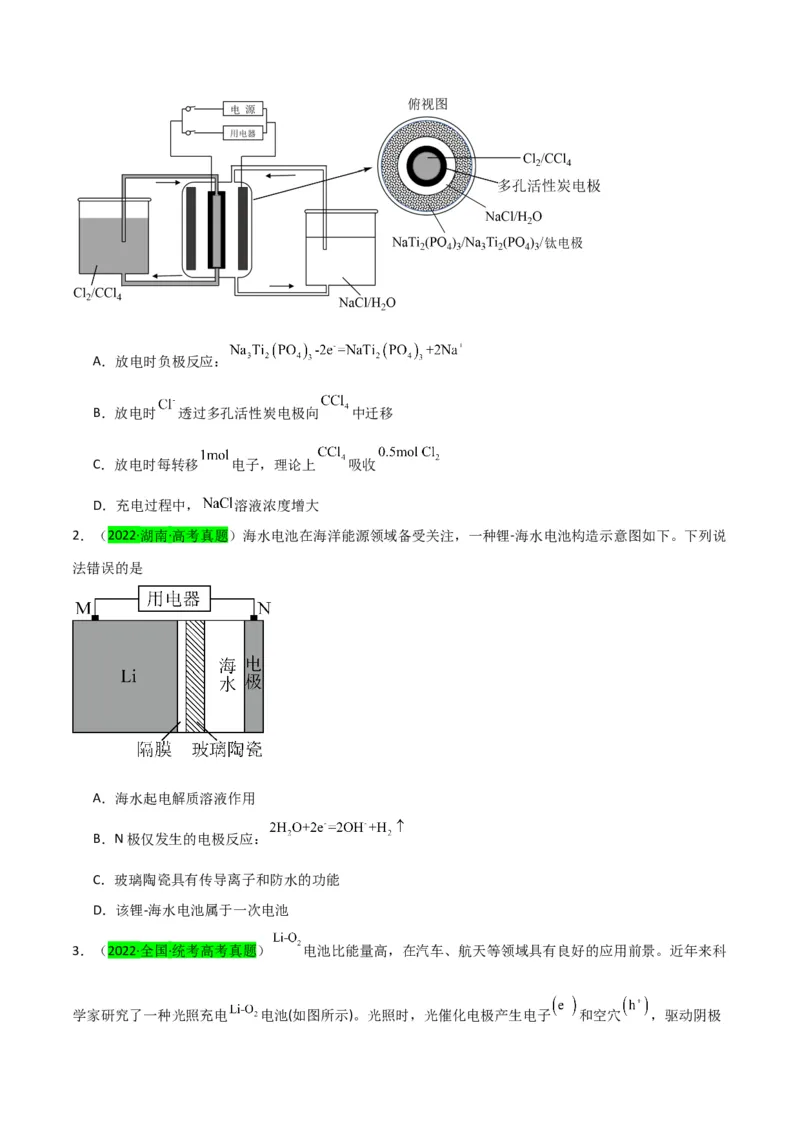
2.(2022·湖南·高考真题)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说
法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
3.(2022·全国·统考高考真题) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科
学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极反应 和阳极反应(Li O +2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
1.(2023·江苏扬州·扬州中学校考模拟预测)一种新型AC/LiMn O 电池体系,在快速启动、电动车等领域
2 4
具有广阔应用前景。其采用尖晶石结构的LiMn O 作正极(可由Li CO 和MnO 按物质的量比1:2反应合成),
2 4 2 3 2
高比表面积活性炭AC(石墨颗粒组成)作负极。充电、放电的过程如图所示:
下列说法正确的是
A.合成LiMn O 的过程中可能有H 产生
2 4 2
B.放电时正极的电极反应式为:LiMn O +xe-=Li xMn O +xLi+
2 4 (1- ) 2 4
C.充电时AC极应与电源负极相连
D.可以用Li SO 水溶液做电解液
2 42.(2023·河南·校联考模拟预测)我国科学家最近合成的ZnO@SnO 微米花作为负极材料提高锌镍二次电
2
池的循环性能,工作原理如图所示。已知:正极材料为NiOOH/Ni(OH) 。
2
下列叙述错误的是
A.放电时,上述装置主要将化学能转化成电能
B.放电时,负极表面副反应可能是Zn+2OH-= +H ↑
2
C.充电时,阴极附近电解质溶液pH降低
D.充电时,1molOH-向阳极迁移时理论上转移1mol电子
3.(2023春·河北沧州·高三泊头市第一中学校联考阶段练习)微生物电池是指在微生物的作用下将化学能
转化为电能的装置,其工作原理如图所示,下列有关微生物电池的说法错误的是
A.a极为负极,可选择导电性高、易于附着微生物的石墨
B.b极的电极反应式为
C.在b极涂覆的催化剂有利于氧气的还原
D.该电池在任何温度下均可发电
4.(2023·陕西西安·统考一模)高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是A.放电时,负极反应式为Zn-2e-+4OH-=Zn(OH)
B.充电时,电路中转移2mole-,中性电解质NaCl的物质的量增多2mol
C.放电时,1molFQ转化为FQH 转移2mol电子
2
D.充电时,m接外接电源的负极,n接外接电源的正极
5.(2023·甘肃·统考三模)以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图
2
所示。下列说法正确的是
A.镍电极上发生氧化反应
B.NO 是该电池的氧化剂
C.固体电解质只起到离子导体的作用
D.M的电极反应为2Na++O +2e-=Na O
2 2 2
6.(2023·辽宁·校联考模拟预测)未来的某一天,我们开着一辆电动汽车,当电池能量即将耗尽时,只需
将汽车开到附近的加氨站,5分钟内就能加满一桶液态氨,电池表便显示满格,加满后汽车能开1000公里
以上,且加氨价格低廉。随着“氨—氢”燃料电池的推出,这样的场景很快就要变成现实。我国某大学设
计的间接氨燃料固体氧化物燃料电池的工作原理如图所示,氨首先经过重整装置在催化剂(未标出)表面分
解生成 与 。下列说法错误的是A.电池工作时,a极的电极反应式为
B.电池工作时,b极发生还原反应
C. 的键角小于 的键角
D.大面积推广“氨—氢”燃料电池,有利于减少碳的排放量
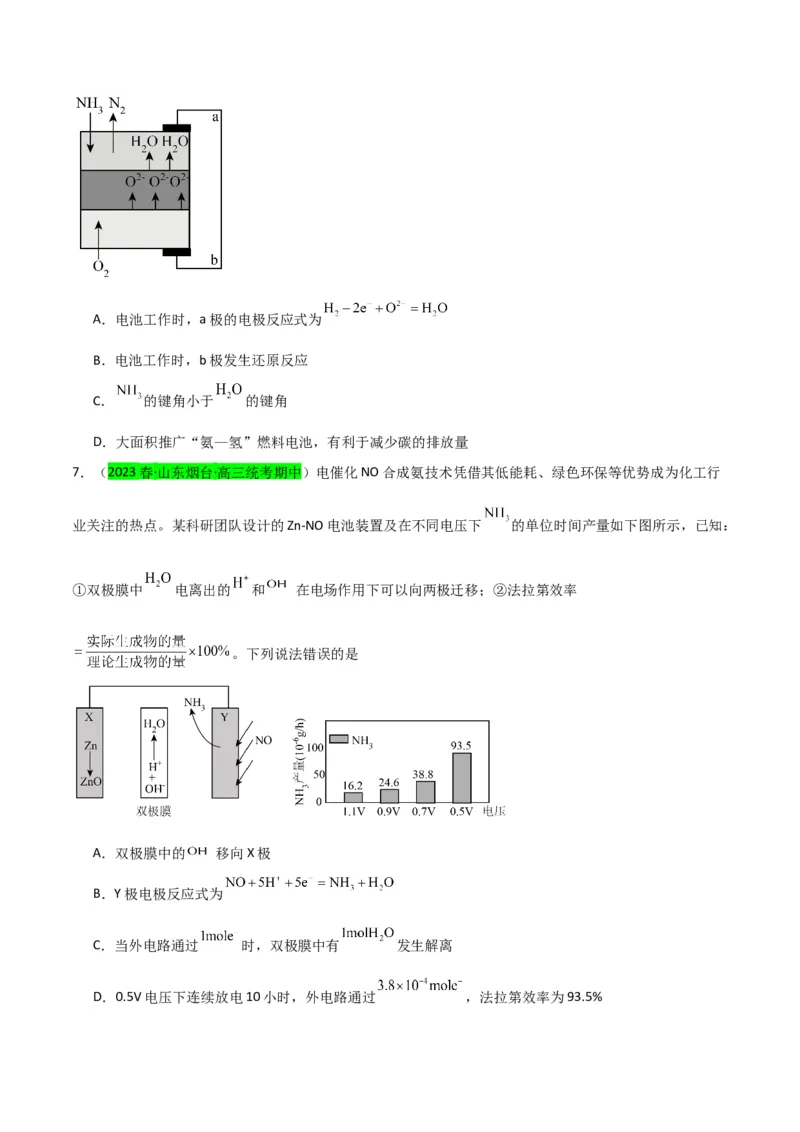
7.(2023春·山东烟台·高三统考期中)电催化NO合成氨技术凭借其低能耗、绿色环保等优势成为化工行
业关注的热点。某科研团队设计的Zn-NO电池装置及在不同电压下 的单位时间产量如下图所示,已知:
①双极膜中 电离出的 和 在电场作用下可以向两极迁移;②法拉第效率
。下列说法错误的是
A.双极膜中的 移向X极
B.Y极电极反应式为
C.当外电路通过 时,双极膜中有 发生解离
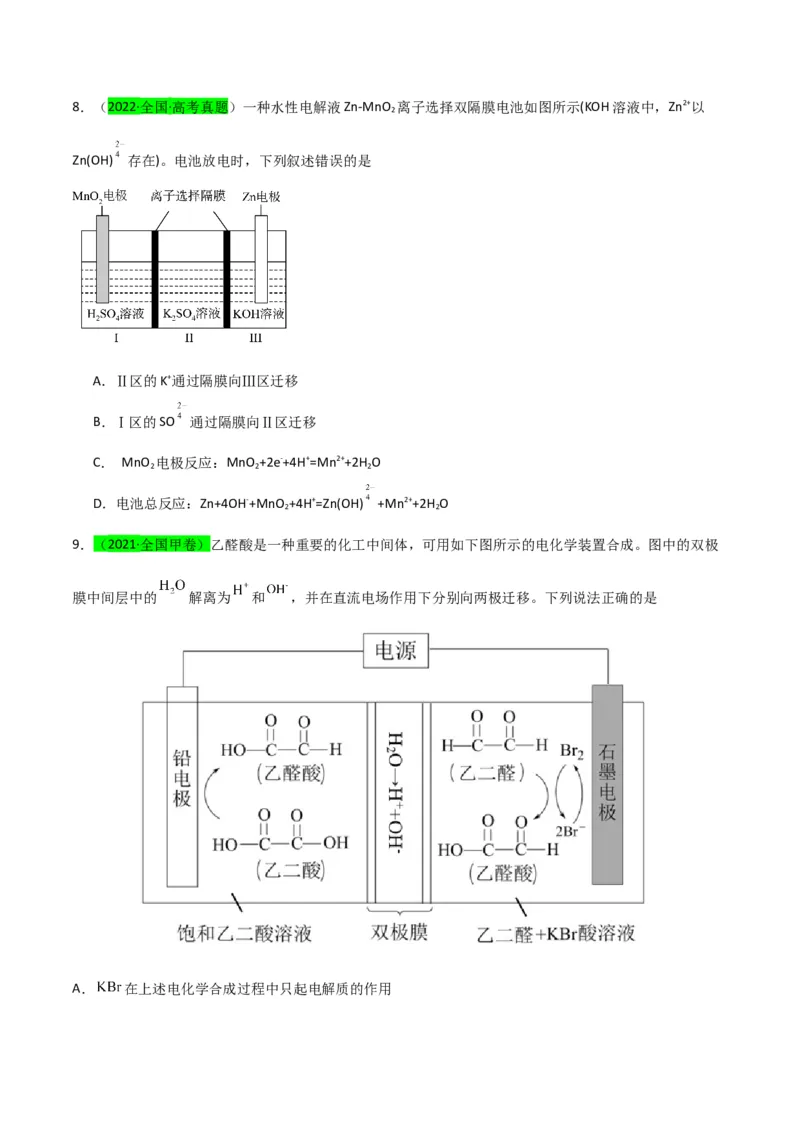
D.0.5V电压下连续放电10小时,外电路通过 ,法拉第效率为93.5%8.(2022·全国·高考真题)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O
2 2
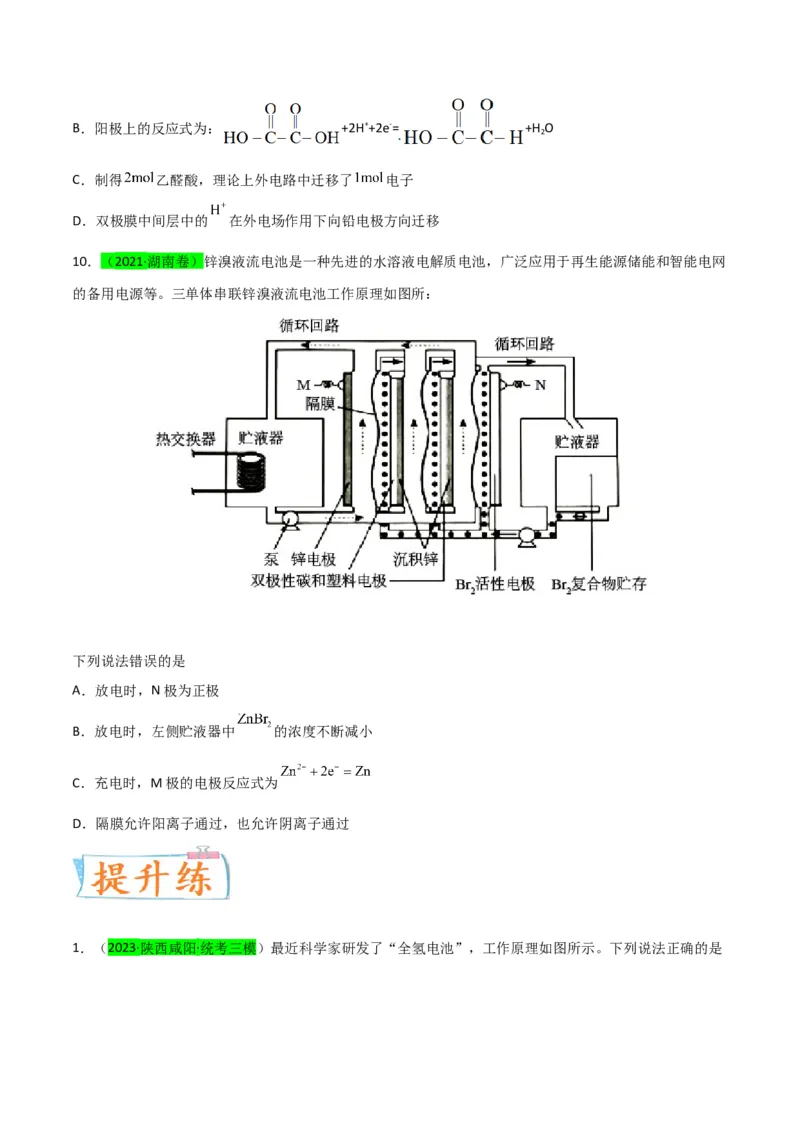
9.(2021·全国甲卷)乙醛酸是一种重要的化工中间体,可用如下图所示的电化学装置合成。图中的双极
膜中间层中的 解离为 和 ,并在直流电场作用下分别向两极迁移。下列说法正确的是
A. 在上述电化学合成过程中只起电解质的作用B.阳极上的反应式为: +2H++2e-= +H O
2
C.制得 乙醛酸,理论上外电路中迁移了 电子
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
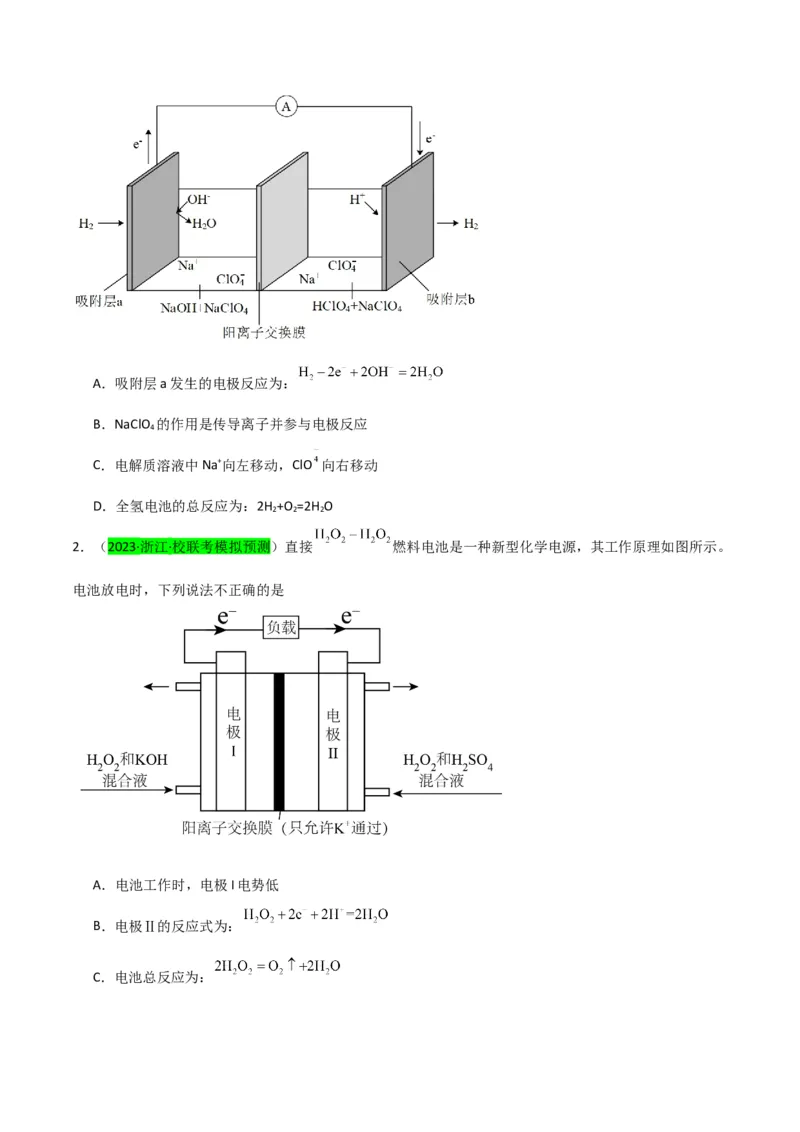
10.(2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网
的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中 的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
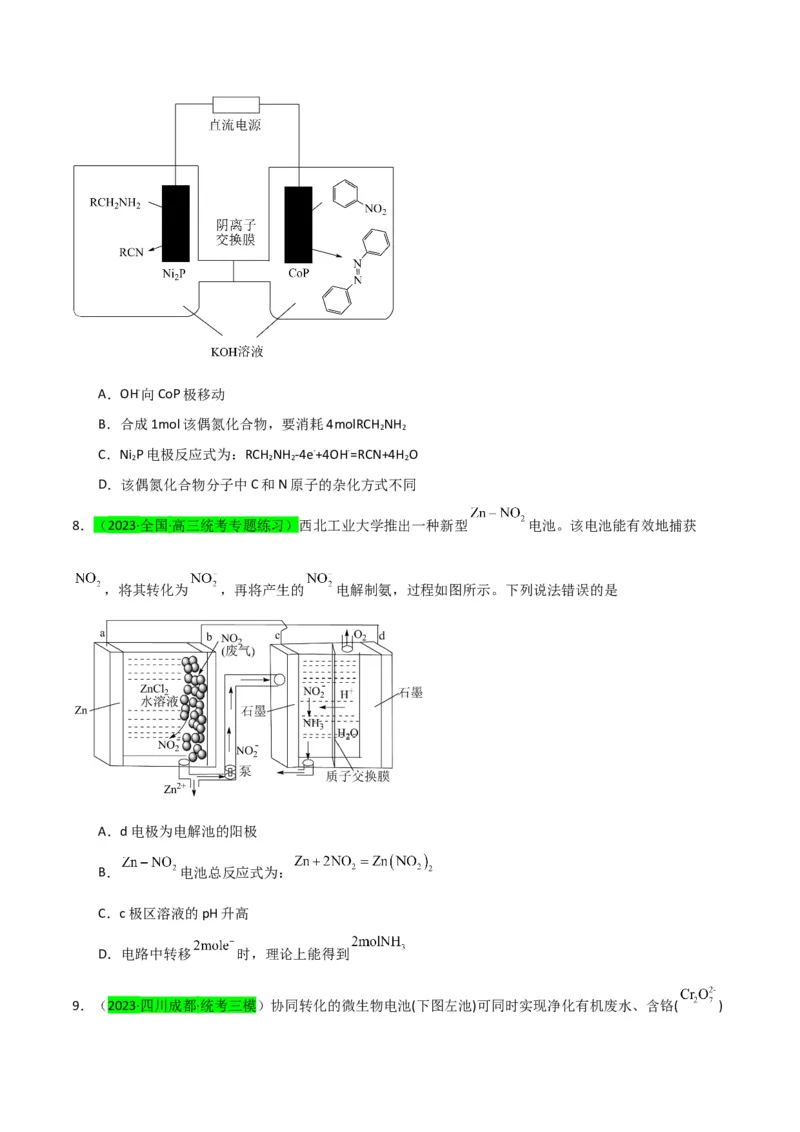
1.(2023·陕西咸阳·统考三模)最近科学家研发了“全氢电池”,工作原理如图所示。下列说法正确的是A.吸附层a发生的电极反应为:
B.NaClO 的作用是传导离子并参与电极反应
4
C.电解质溶液中Na+向左移动,ClO 向右移动
D.全氢电池的总反应为:2H +O =2H O
2 2 2
2.(2023·浙江·校联考模拟预测)直接 燃料电池是一种新型化学电源,其工作原理如图所示。
电池放电时,下列说法不正确的是
A.电池工作时,电极I电势低
B.电极Ⅱ的反应式为:
C.电池总反应为:D.当电路中转移0.1mol电子时,通过阳离子交换膜的 为3.9g
3.(2023·广西·统考三模)高效储能电池——锂硫电池具有价格低廉、环境友好等特点,已经用于某些飞
机,其原电池模型以及充、放电过程如图所示。下列说法错误的是
A.放电时,化学能转化为电能
B.碳添加剂是为了增强电极的导电性
C.充电时,阳极的总的电极反应式是8Li S-16e- = S + 16Li+
2 8
D.放电时,1 mol Li S 转化为Li S 得到2 mol电子
2 8 2 6
4.(2023秋·内蒙古赤峰·高三校联考期末)海水电池在海洋能源领域备受关注,一种锂——海水电池构造
示意图(图1),一种镁——海水电池装置示意图(如图2)。下列说法错误的是
A.玻璃陶瓷具有传导离子和防水的功能
B.N极发生的电极反应:O +4e-+2H O=4OH-
2 2
C.X为正极,可用铜、石墨等做电极材料
D.如图2外电路中每通过2mol电子,溶液中2molH+由阳离子交换膜左侧向右侧迁移
5.(2023春·河北沧州·高三校考阶段练习)某课题组提出了一种基于 自循环的生物杂化光
电化学池,通过在单室内协同耦合光电化学 生成和生物电化学 消耗,实现了直接和可持续的
“太阳能—燃料—电能”转化。实验装置如图,下列说法错误的是A.电极 : 是电池负极,有电子流出
B.消耗 “燃料”的电极反应式为
C.两电极附近 变化情况相同
D.该光电化学池无需外加燃料,简单、安全且经济高效
6.(2023·江西·校联考二模)水系可充电电池因其成本低、高离子电导率、高安全性和环境友好性等优势
而备受关注。一种 新型无隔膜Zn/MnO 液流电池的工作原理如图所示。电池以锌箔、石墨毡为集流体,
2
ZnSO 和MnSO 的混合液作电解质溶液,下列叙述正确的是
4 4
A.过程Ⅱ为放电过程,石墨毡电极的电极反应为MnO -2e-+4H+=Mn2++2H O
2 2
B.放电时,当外电路转移2mole-时,两电极质量变化的差值为22g
C.过程I为锌沉积过程,B连电源的正极,电极附近pH增大
D.将电解质溶液换成强酸或强碱性溶液都可延长电池的使用寿命
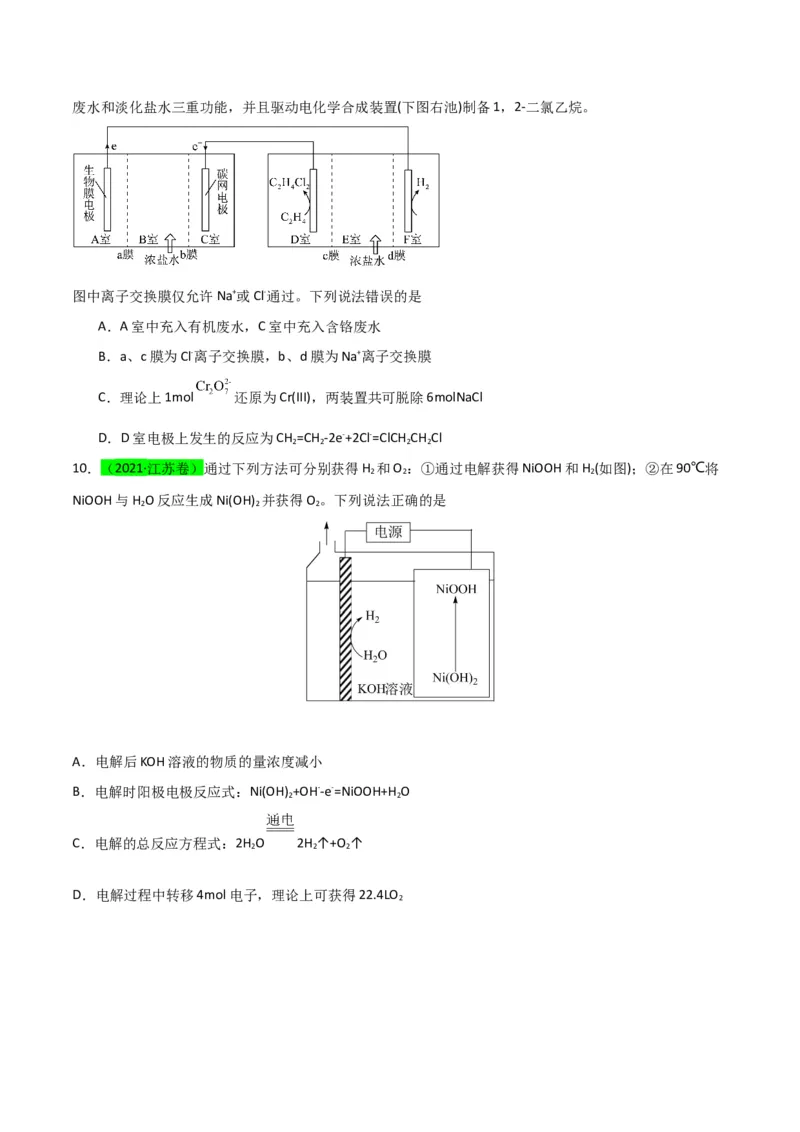
7.(2023·安徽芜湖·统考二模)下图为合成偶氮化合物 的电化学装置,有关说法正确的是A.OH-向CoP极移动
B.合成1mol该偶氮化合物,要消耗4molRCH NH
2 2
C.Ni P电极反应式为:RCH NH -4e-+4OH-=RCN+4H O
2 2 2 2
D.该偶氮化合物分子中C和N原子的杂化方式不同
8.(2023·全国·高三统考专题练习)西北工业大学推出一种新型 电池。该电池能有效地捕获
,将其转化为 ,再将产生的 电解制氨,过程如图所示。下列说法错误的是
A.d电极为电解池的阳极
B. 电池总反应式为:
C.c极区溶液的pH升高
D.电路中转移 时,理论上能得到
9.(2023·四川成都·统考三模)协同转化的微生物电池(下图左池)可同时实现净化有机废水、含铬( )废水和淡化盐水三重功能,并且驱动电化学合成装置(下图右池)制备1,2-二氯乙烷。
图中离子交换膜仅允许Na+或Cl-通过。下列说法错误的是
A.A室中充入有机废水,C室中充入含铬废水
B.a、c膜为Cl-离子交换膜,b、d膜为Na+离子交换膜
C.理论上1mol 还原为Cr(III),两装置共可脱除6molNaCl
D.D室电极上发生的反应为CH =CH -2e-+2Cl-=ClCH CH Cl
2 2 2 2
10.(2021·江苏卷)通过下列方法可分别获得H 和O :①通过电解获得NiOOH和H (如图);②在90℃将
2 2 2
NiOOH与H O反应生成Ni(OH) 并获得O 。下列说法正确的是
2 2 2
A.电解后KOH溶液的物质的量浓度减小
B.电解时阳极电极反应式:Ni(OH) +OH--e-=NiOOH+H O
2 2
C.电解的总反应方程式:2H O 2H ↑+O ↑
2 2 2
D.电解过程中转移4mol电子,理论上可获得22.4LO
2