文档内容
德阳三中 2022-2023 学年上期高 2020 级高三第一次综合考
试
理综化学
总分: 100分
单选题(3分*14)
1. 从古至今化学与生产、生活密切相关。下列说法正确的是
A. 喝补铁剂(含Fe2+)时,加服维生素C效果更好,因维生素C具有氧化性
B. 汉代烧制出“明如镜、声如馨”的瓷器,其主要原料为石灰石
C. “司南之杓(勺),投之于地,其柢(勺柄)指南”,司南中的“杓”含FeO
2 3
D. 港珠澳大桥采用超高分子聚乙烯纤维吊绳,其商品名为“力纶”是有机高分子化合物
【答案】D
2. 化学科学需要借助化学专用语言来描述,现有下列化学用语:①Cl-的结构示意图:
;②羟基的电子式: ;③HClO的结构式:H—Cl—O;④NaHCO 在水中的电离
3
方程式:NaHCO =Na++H++CO ;⑤碳酸氢铵与足量的氢氧化钠溶液混合:HCO +OH-
3
=CO +HO;⑥CO 的比例模型: ;⑦原子核内有10个中子的氧原子: O。其中说法
2 2
正确的是( )
A. ④⑤⑥ B. ①②⑦ C. ②③④⑥ D.
②③⑤⑥⑦
【答案】B
3. 设 表示阿伏加德罗常数的值, 下列叙述正确的是
A. 足量铁在 中燃烧时转移电子数为
B. 氯化钾溶液中阴离子所带电荷数为
C. 的 溶液中 和 离子数之和为
D. 标准状况下, 的 和 的 混合后气体体积为
【答案】A
4. X、Y两种短周期元素可形成化合物 , 比 少一个电子层,且 具有与Ne原子
相同的核外电子层结构。下列说法正确的是
A. 是 B. X是第二周期第IIIA族的元素
C. Y是第二周期第IVA族 的元素 D. 与Y的核外电子层数相等
下载最新免费模拟卷,到公众号:一枚试卷君【答案】D
5. 下列物质在给定条件下的转化均能一步实现的是
A.
B.
C. 溶液
D.
【答案】D
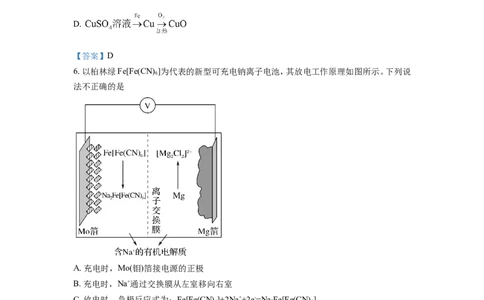
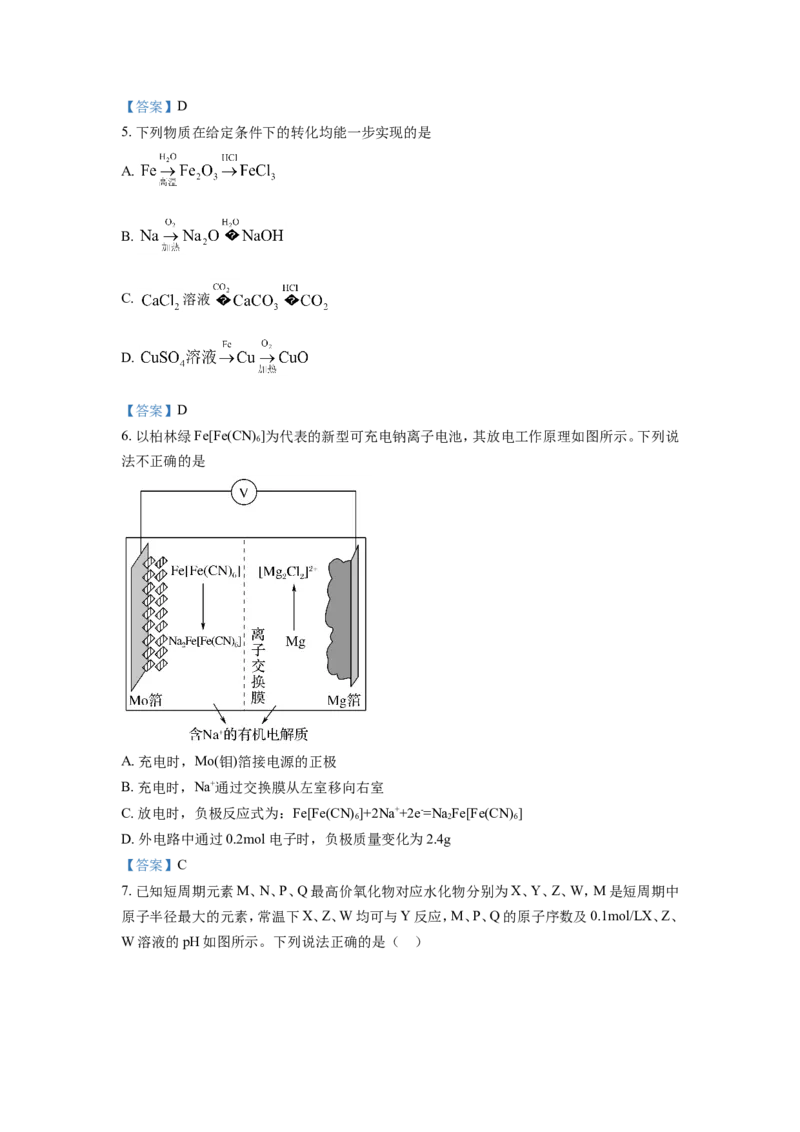
6. 以柏林绿Fe[Fe(CN) ]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说
6
法不正确的是
A. 充电时,Mo(钼)箔接电源的正极
B. 充电时,Na+通过交换膜从左室移向右室
C. 放电时,负极反应式为:Fe[Fe(CN) ]+2Na++2e-=Na Fe[Fe(CN) ]
6 2 6
D. 外电路中通过0.2mol电子时,负极质量变化为2.4g
【答案】C
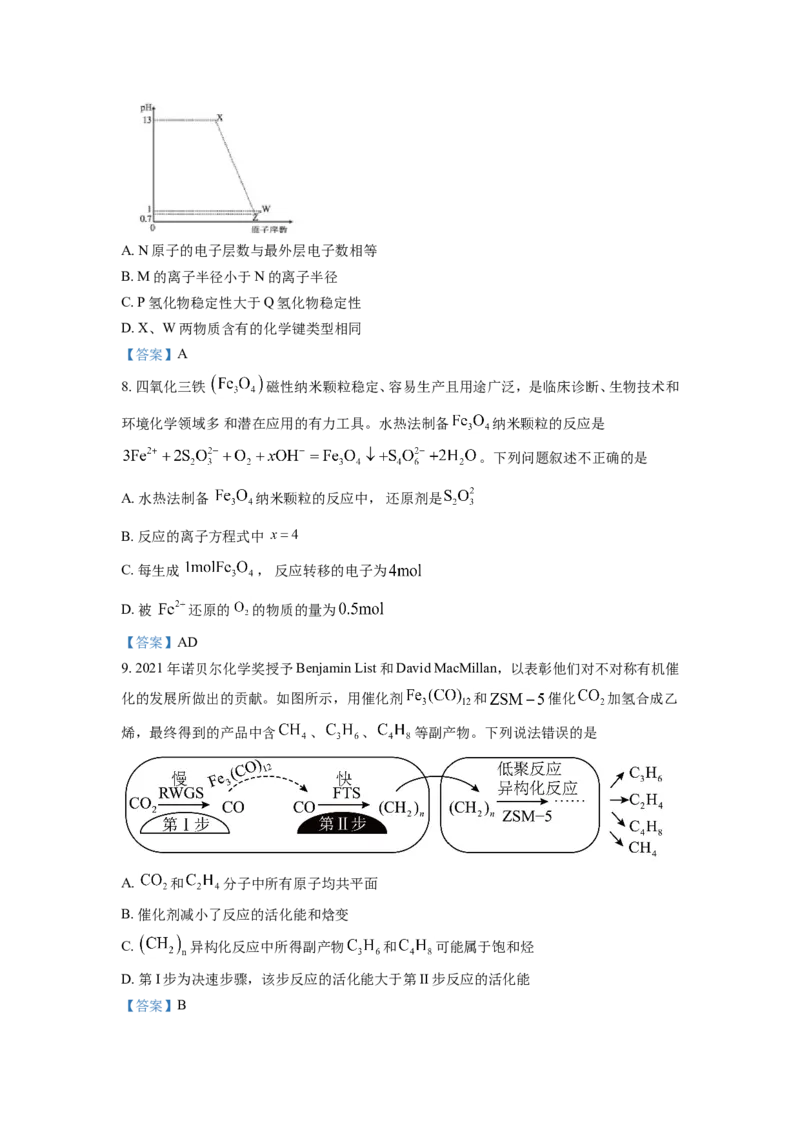
7. 已知短周期元素M、N、P、Q最高价氧化物对应水化物分别为X、Y、Z、W,M是短周期中
原子半径最大的元素,常温下X、Z、W均可与Y反应,M、P、Q的原子序数及0.1mol/LX、Z、
W溶液的pH如图所示。下列说法正确的是( )A. N原子的电子层数与最外层电子数相等
B. M的离子半径小于N的离子半径
C. P氢化物稳定性大于Q氢化物稳定性
D. X、W两物质含有的化学键类型相同
【答案】A
8. 四氧化三铁 磁性纳米颗粒稳定、容易生产且用途广泛, 是临床诊断、生物技术和
环境化学领域多 和潜在应用的有力工具。水热法制备 纳米颗粒的反应是
。下列问题叙述不正确的是
A. 水热法制备 纳米颗粒的反应中, 还原剂是
B. 反应的离子方程式中
C. 每生成 , 反应转移的电子为
D. 被 还原的 的物质的量为
【答案】AD
9. 2021年诺贝尔化学奖授予Benjamin List和David MacMillan,以表彰他们对不对称有机催
化的发展所做出的贡献。如图所示,用催化剂 和 催化 加氢合成乙
烯,最终得到的产品中含 、 、 等副产物。下列说法错误的是
A. 和 分子中所有原子均共平面
B. 催化剂减小了反应的活化能和焓变
C. 异构化反应中所得副产物 和 可能属于饱和烃
D. 第I步为决速步骤,该步反应的活化能大于第II步反应的活化能
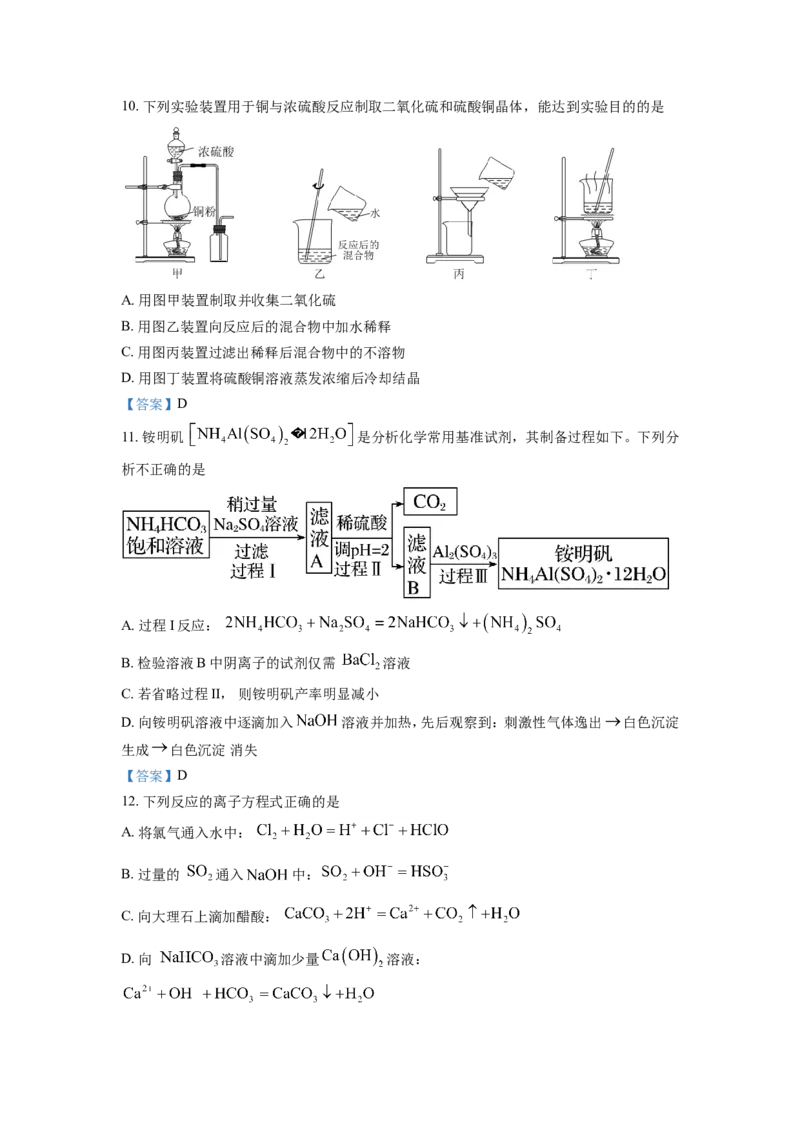
【答案】B10. 下列实验装置用于铜与浓硫酸反应制取二氧化硫和硫酸铜晶体,能达到实验目的的是
A. 用图甲装置制取并收集二氧化硫
B. 用图乙装置向反应后的混合物中加水稀释
C. 用图丙装置过滤出稀释后混合物中的不溶物
D. 用图丁装置将硫酸铜溶液蒸发浓缩后冷却结晶
【答案】D
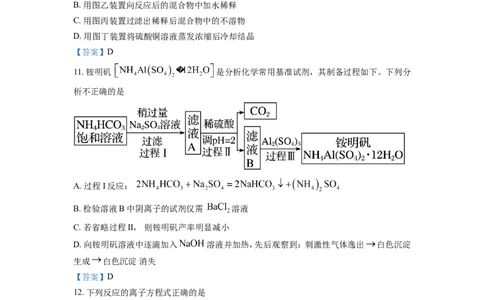
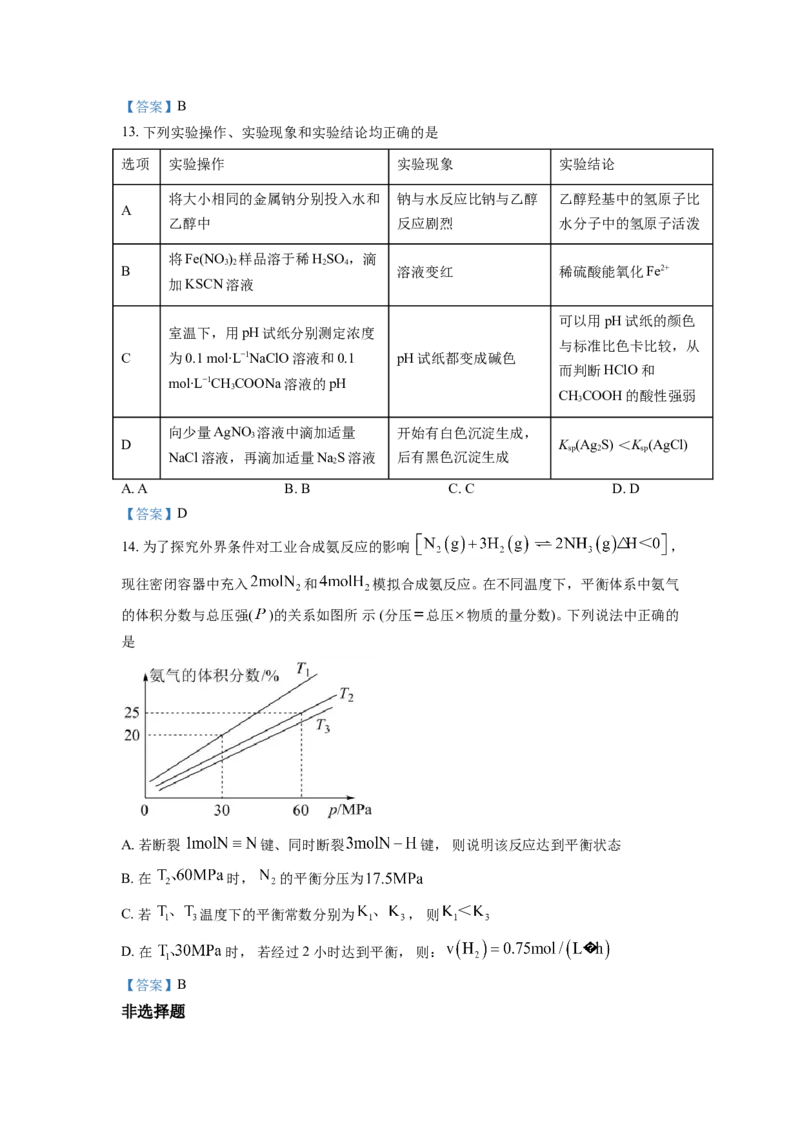
11. 铵明矶 是分析化学常用基准试剂,其制备过程如下。下列分
析不正确的是
A. 过程I反应:
B. 检验溶液B中阴离子的试剂仅需 溶液
C. 若省略过程II, 则铵明矾产率明显减小
D. 向铵明矾溶液中逐滴加入 溶液并加热,先后观察到: 刺激性气体逸出 白色沉淀
生成 白色沉淀 消失
【答案】D
12. 下列反应的离子方程式正确的是
A. 将氯气通入水中:
B. 过量的 通入 中:
C. 向大理石上滴加醋酸:
D. 向 溶液中滴加少量 溶液:【答案】B
13. 下列实验操作、实验现象和实验结论均正确的是
选项 实验操作 实验现象 实验结论
将大小相同的金属钠分别投入水和 钠与水反应比钠与乙醇 乙醇羟基中的氢原子比
A
乙醇中 反应剧烈 水分子中的氢原子活泼
将Fe(NO ) 样品溶于稀HSO ,滴
3 2 2 4
B 溶液变红 稀硫酸能氧化Fe2+
加KSCN溶液
可以用 pH试纸的颜色
室温下,用pH试纸分别测定浓度
与标准比色卡比较,从
C 为0.1 mol∙L−1NaClO溶液和0.1 pH试纸都变成碱色
而判断HClO和
mol∙L−1CHCOONa溶液的pH
3
CHCOOH的酸性强弱
3
向少量AgNO 溶液中滴加适量 开始有白色沉淀生成,
3
D K (Ag S) <K (AgCl)
sp 2 sp
NaCl溶液,再滴加适量NaS溶液 后有黑色沉淀生成
2
A. A B. B C. C D. D
【答案】D
14. 为了探究外界条件对工业合成氨反应的影响 ,
现往密闭容器中充入 和 模拟合成氨反应。在不同温度下, 平衡体系中氨气
的体积分数与总压强( )的关系如图所 示 (分压 总压 物质的量分数)。下列说法中正确的
是
A. 若断裂 键、同时断裂 键, 则说明该反应达到平衡状态
B. 在 时, 的平衡分压为
C. 若 温度下的平衡常数分别为 , 则
D. 在 时, 若经过 2 小时达到平衡, 则:
【答案】B
非选择题15. A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电
子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的
最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防
火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为________。
(2)F在元素周期表中的位置_________。
(3)用电子式表示由元素B和F组成的化合物的形成过程:__________。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方
程式为________、_______。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物EF。该物质可与水反应生成
2 2
一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种
元素化合价发生改变,该反应的化学方程式为_______________。
【答案】(1)Si (2)第3周期第VIIA
(3) (4) ①. 2NaO + 2H O = 4NaOH + O ↑ ②. 2Al+
2 2 2 2
2NaOH + 2H O = 2NaAlO +3H ↑
2 2 2
(5)2SCl + 2H O = 3S↓ + SO ↑+ 4HCl
2 2 2 2
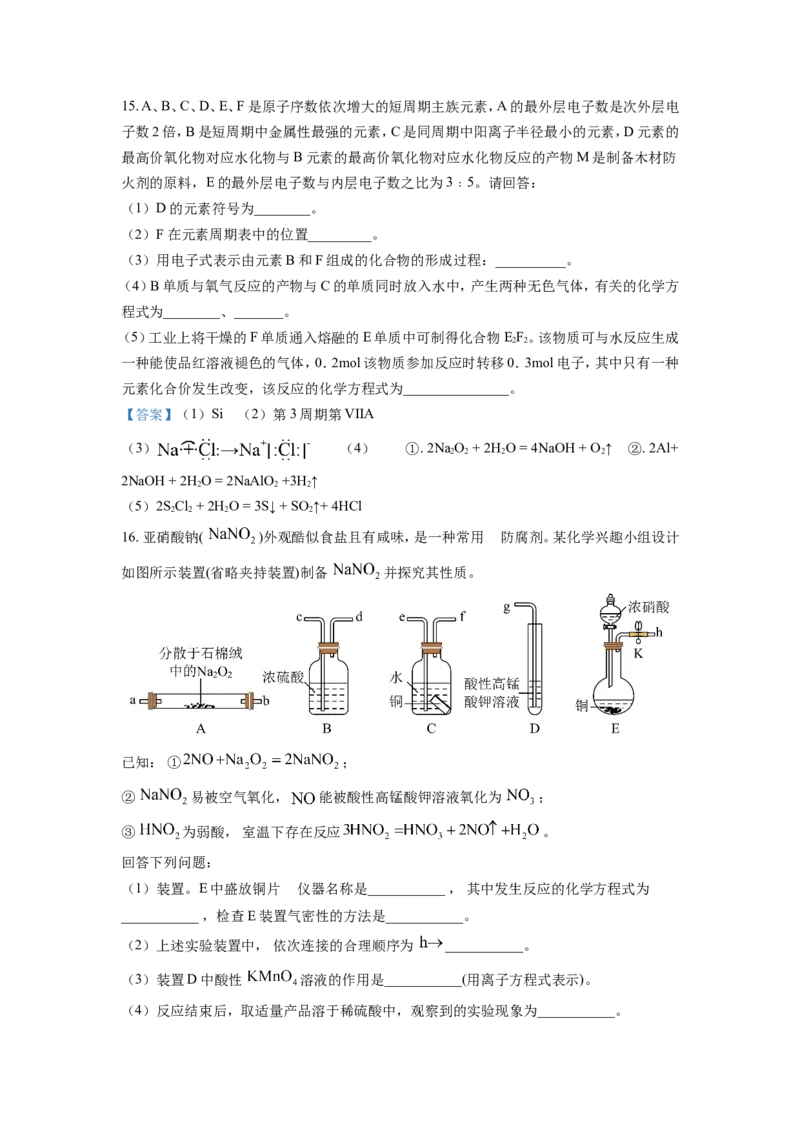
16. 亚硝酸钠( )外观酷似食盐且有咸味,是一种常用 的防腐剂。某化学兴趣小组设计
如图所示装置(省略夹持装置)制备 并探究其性质。
已知: ① ;
② 易被空气氧化, 能被酸性高锰酸钾溶液氧化为 ;
③ 为弱酸, 室温下存在反应 。
回答下列问题:
(1)装置。E中盛放铜片 的仪器名称是___________ , 其中发生反应的化学方程式为
___________ ,检查E装置气密性的方法是___________。
(2)上述实验装置中, 依次连接的合理顺序为 ___________。
(3)装置D中酸性 溶液的作用是___________(用离子方程式表示)。
(4)反应结束后,取适量产品溶于稀硫酸中,观察到的实验现象为___________。(5)测定深水井中亚硝酸钠含量:取 水样于锥形瓶中,立即加入
酸性高锰酸钾溶液,充分反应后用 草酸溶液滴定高锰
酸钾,终点时消耗草酸溶液 。到达滴定终点的现象___________。若所取样品在空
气中放置时间过长,则测定结果___________(填“偏高”“偏低”或“无影响”)。
【答案】(1) ①. 圆底烧瓶 ②. 浓
③. 检查装置 E气密性的方法是先关闭弹簧夹,从滴液漏斗处倒水,若形成一段稳定的水柱,
则证明装置气密性好
(2)efcdabg(或efcdbag)
(3)
(4)固体溶解, 产生无色气体并在液面上方变为红棕色
(5) ①. 当最后一滴标准液加入,溶液红色褪去,30秒不恢复 ②. 偏低
17. 强弱电解质在水中的行为是不同的。
(1)醋酸在水中的电离方程式为_______;醋酸电离平衡常数表达式 _______。
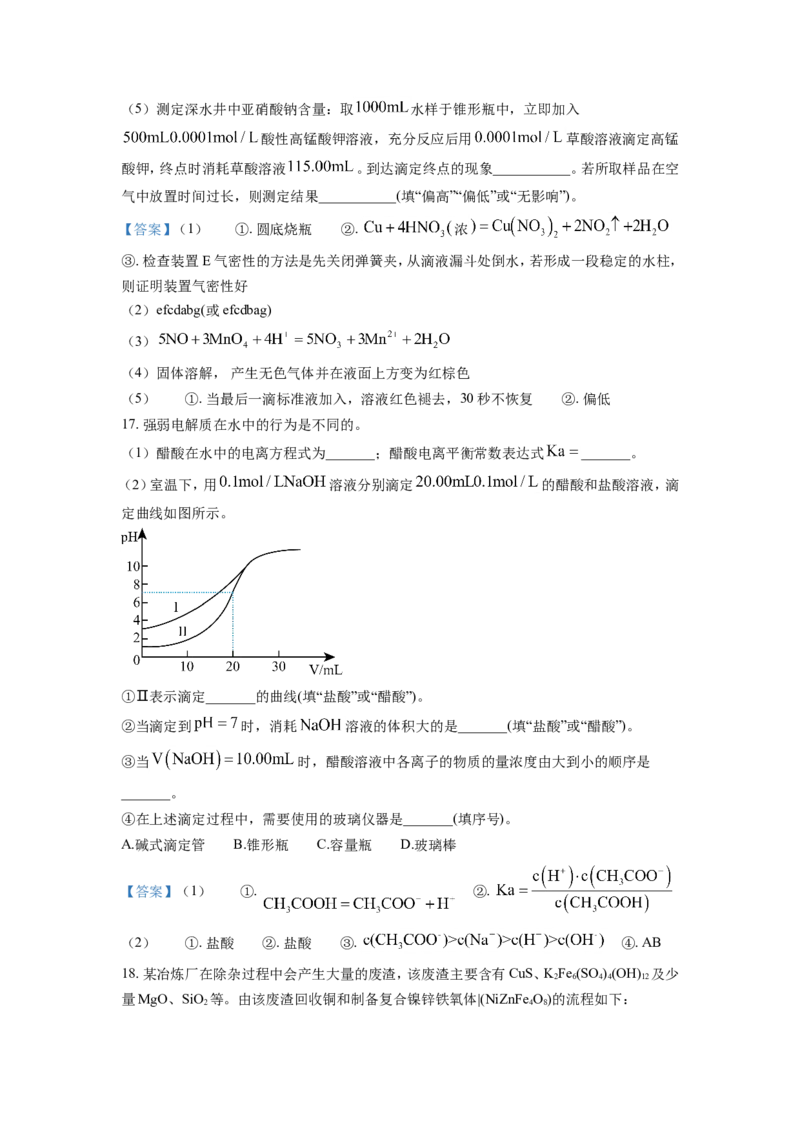
(2)室温下,用 溶液分别滴定 的醋酸和盐酸溶液,滴
定曲线如图所示。
①Ⅱ表示滴定_______的曲线(填“盐酸”或“醋酸”)。
②当滴定到 时,消耗 溶液的体积大的是_______(填“盐酸”或“醋酸”)。
③当 时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是
_______。
④在上述滴定过程中,需要使用的玻璃仪器是_______(填序号)。
A.碱式滴定管 B.锥形瓶 C.容量瓶 D.玻璃棒
【答案】(1) ①. ②.
(2) ①. 盐酸 ②. 盐酸 ③. ④. AB
18. 某冶炼厂在除杂过程中会产生大量的废渣,该废渣主要含有CuS、KFe (SO )(OH) 及少
2 6 4 4 12
量MgO、SiO 等。由该废渣回收铜和制备复合镍锌铁氧体|(NiZnFe O)的流程如下:
2 4 8已知:有关金属离子形成氢氧化物沉淀时的pH如下表:
离子 开始沉淀时pH 完全沉淀时pH
Mg2+ 10.4 12.4
Fe3+ 2.3 4.1
(1)K Fe (SO )(OH) 中Fe的化合价为_______。
2 6 4 4 12
(2)滤渣1的主要成分为_______。
(3)反应Ⅱ中加入氨水的目的是调节溶液的pH,则调节 pH的范围是_______;写出反应Ⅱ生
成沉淀的离子方程式:_______。
(4)滤液中含有的阳离子是_______。
(5)MnO 能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅳ中CuS发生反应的化学方程
2
式:_______,每转移2.408×1024个电子,生成单质硫的质量是_______g。
【答案】 ①. +3 ②. CuS、SiO ③. 4.1≤pH<10.4 ④. Fe3++3NH·H O=Fe(OH) ↓+
2 3 2 3
⑤. 、K+、Mg2+ ⑥. MnO +CuS+2H SO =MnSO +CuSO+S+2H O ⑦. 64g
2 2 4 4 4 2
19. 我国提出 2060 年达“碳中和”目标, 通过反应 将 转化为高附
加值产品 是 实现该目标的一种方式。回答下列问题:
(1)向恒容密闭容器中充入 和 , 发生反应:
。测定不同温度下 的平衡转化率数据如下表所示:
T/K 373 473 573 673
8.4 24.3 37.5
平衡转化率
①该反应的 ___________0(填“ ”或“ ”)。已知: ,
则反应 的 __________用 和 表
示)。
②下列有利于提高 的平衡转化率的措施有___________ (填标号)。A. 增大反应体系的压强
B. 增大
C. 降低反应温度
D. 移出
③ 下, 平衡时压强为P, 用各物质的平衡分压(分压 总压 物质的量分数)表示该反
应的平衡常数 ___________ (用含 和P的代数式表示)。
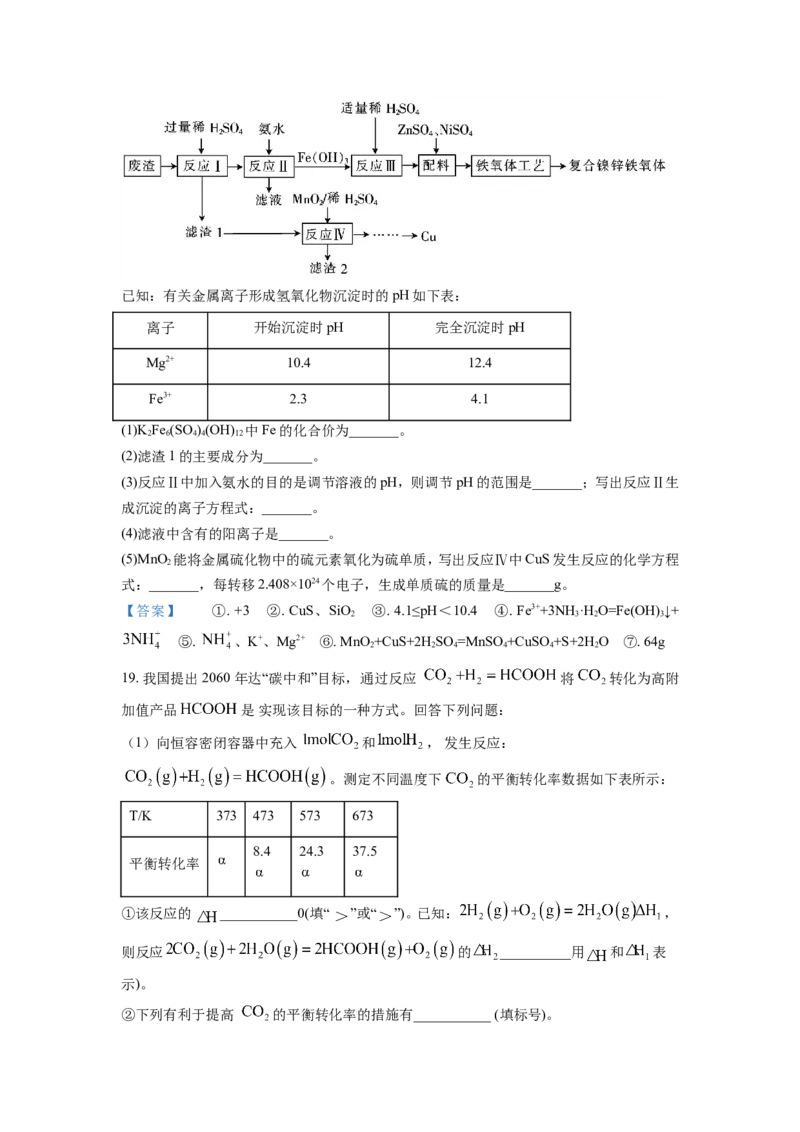
(2)浙江大学某国家实验室用水热法还原 转化为 , 探究了不同条件下
的转化率,数据如下图所示:
依据以上数据,最佳的 摩尔比和反应时间是___________。
【答案】(1) ①. ②. ③. ABD ④.
(2)1:1,