文档内容
选择题突破九 A 组 基础巩固练
题组一 新型化学电源
1.“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应式
为Zn+2MnO +H O ZnO+2MnOOH。下列说法不正确的是( )
2 2
A.该电池中Zn为负极,MnO 为正极
2
B.该电池的正极反应式为MnO +e-+H O MnOOH+OH-
2 2
C.电池工作时水分子和OH-都能通过薄层纸片
D.导电时外电路电子由Zn流向MnO ,内电路电子由MnO 流向Zn
2 2
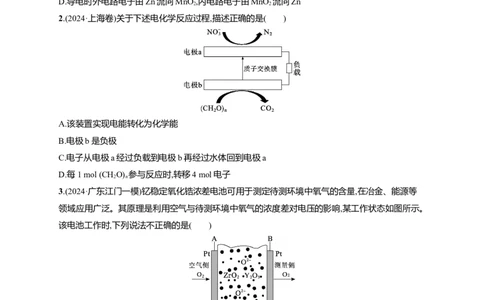
2.(2024·上海卷)关于下述电化学反应过程,描述正确的是( )
A.该装置实现电能转化为化学能
B.电极b是负极
C.电子从电极a经过负载到电极b再经过水体回到电极a
D.每1 mol (CH O) 参与反应时,转移4 mol电子
2 n
3.(2024·广东江门一模)钇稳定氧化锆浓差电池可用于测定待测环境中氧气的含量,在冶金、能源等
领域应用广泛。其原理是利用空气与待测环境中氧气的浓度差对电压的影响,某工作状态如图所示。
该电池工作时,下列说法不正确的是( )
A.电极A为正极
B.O2-由电极A向电极B迁移
C.电极B发生的反应为2O2--4e- O↑
2
D.理论上,电解质中O2-的总物质的量会增加
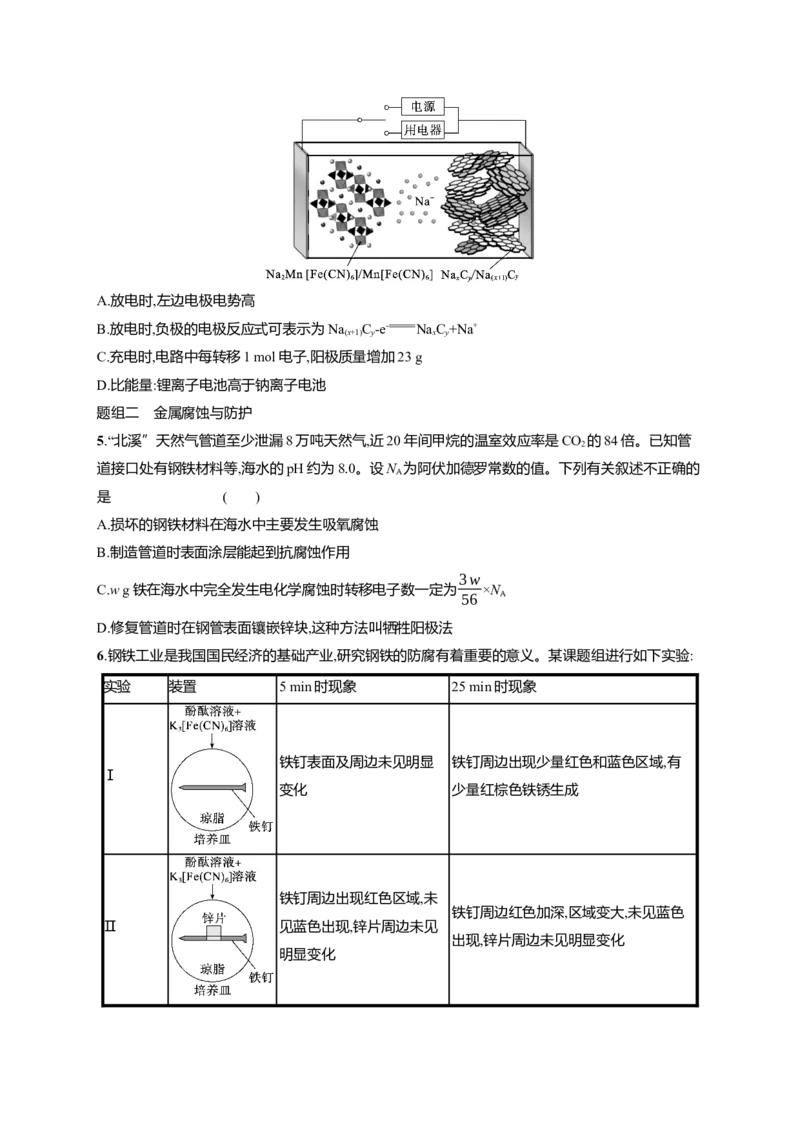
4.(2024·辽宁沈阳一模)2023年星恒电源发布“超钠F1”开启钠电在电动车上产业化元年。该二次电
池的电极材料为NaMn[Fe(CN) ](普鲁士白)和NaC(嵌钠硬碳)。下列说法中错误的是( )
2 6 x yA.放电时,左边电极电势高
B.放电时,负极的电极反应式可表示为Na C-e- NaC+Na+
(x+1) y x y
C.充电时,电路中每转移1 mol电子,阳极质量增加23 g
D.比能量:锂离子电池高于钠离子电池
题组二 金属腐蚀与防护
5.“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷的温室效应率是CO 的84倍。已知管
2
道接口处有钢铁材料等,海水的pH约为8.0。设N 为阿伏加德罗常数的值。下列有关叙述不正确的
A
是 ( )
A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
3w
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为 ×N
56 A
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
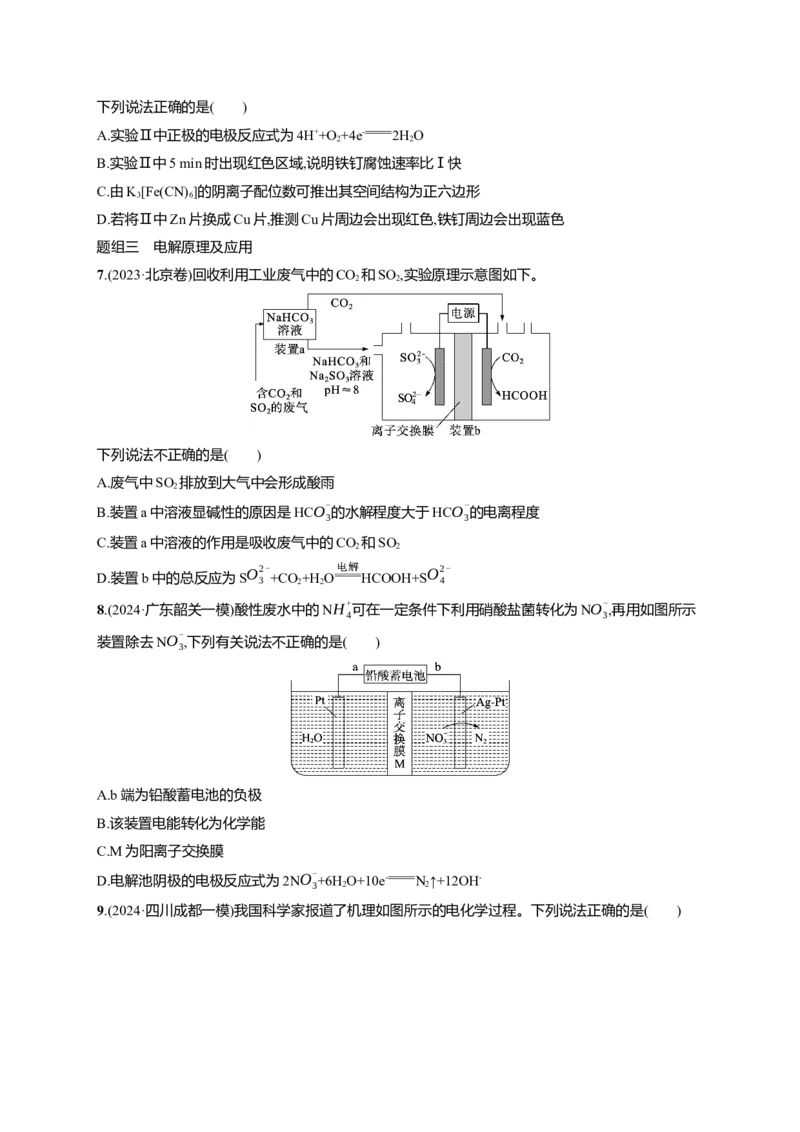
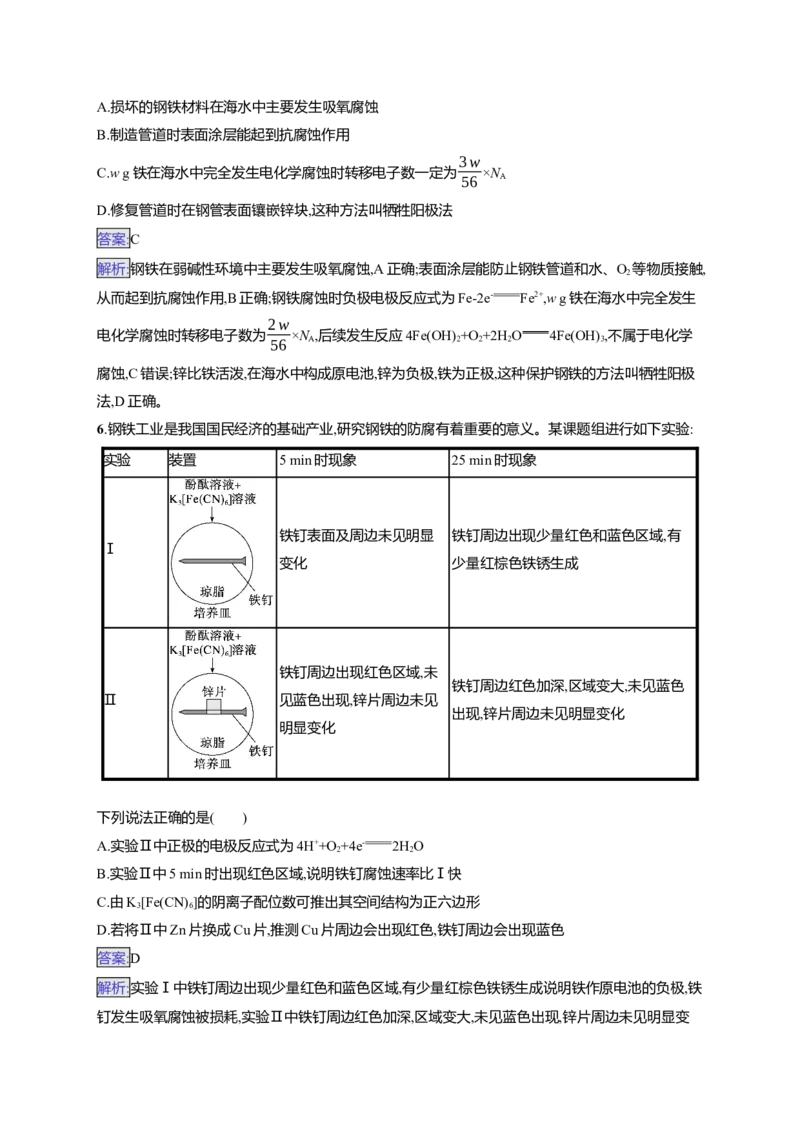
6.钢铁工业是我国国民经济的基础产业,研究钢铁的防腐有着重要的意义。某课题组进行如下实验:
实验 装置 5 min时现象 25 min时现象
铁钉表面及周边未见明显 铁钉周边出现少量红色和蓝色区域,有
Ⅰ
变化 少量红棕色铁锈生成
铁钉周边出现红色区域,未
铁钉周边红色加深,区域变大,未见蓝色
Ⅱ 见蓝色出现,锌片周边未见
出现,锌片周边未见明显变化
明显变化下列说法正确的是( )
A.实验Ⅱ中正极的电极反应式为4H++O +4e- 2HO
2 2
B.实验Ⅱ中5 min时出现红色区域,说明铁钉腐蚀速率比Ⅰ快
C.由K[Fe(CN) ]的阴离子配位数可推出其空间结构为正六边形
3 6
D.若将Ⅱ中Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色
题组三 电解原理及应用
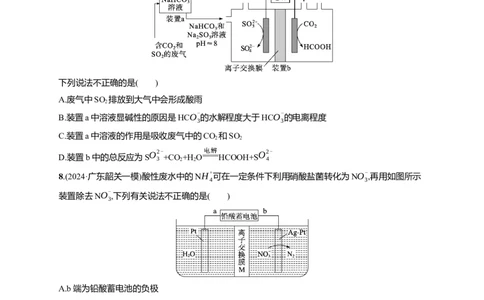
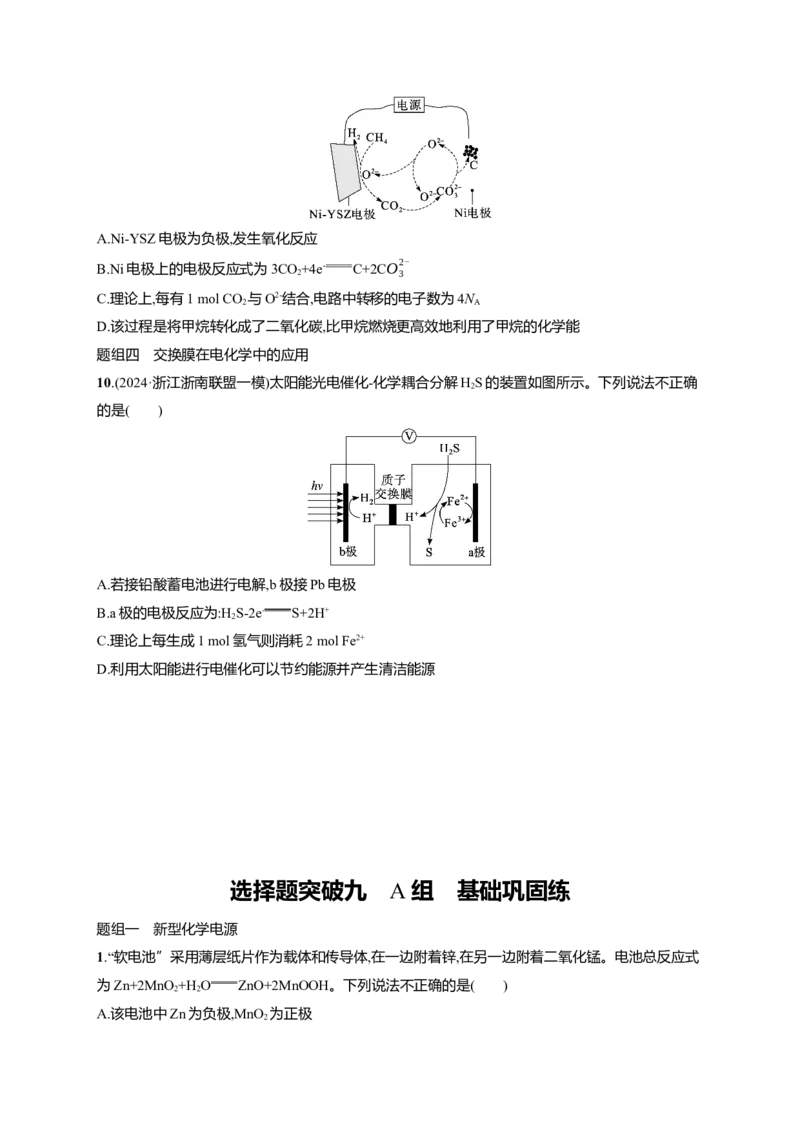
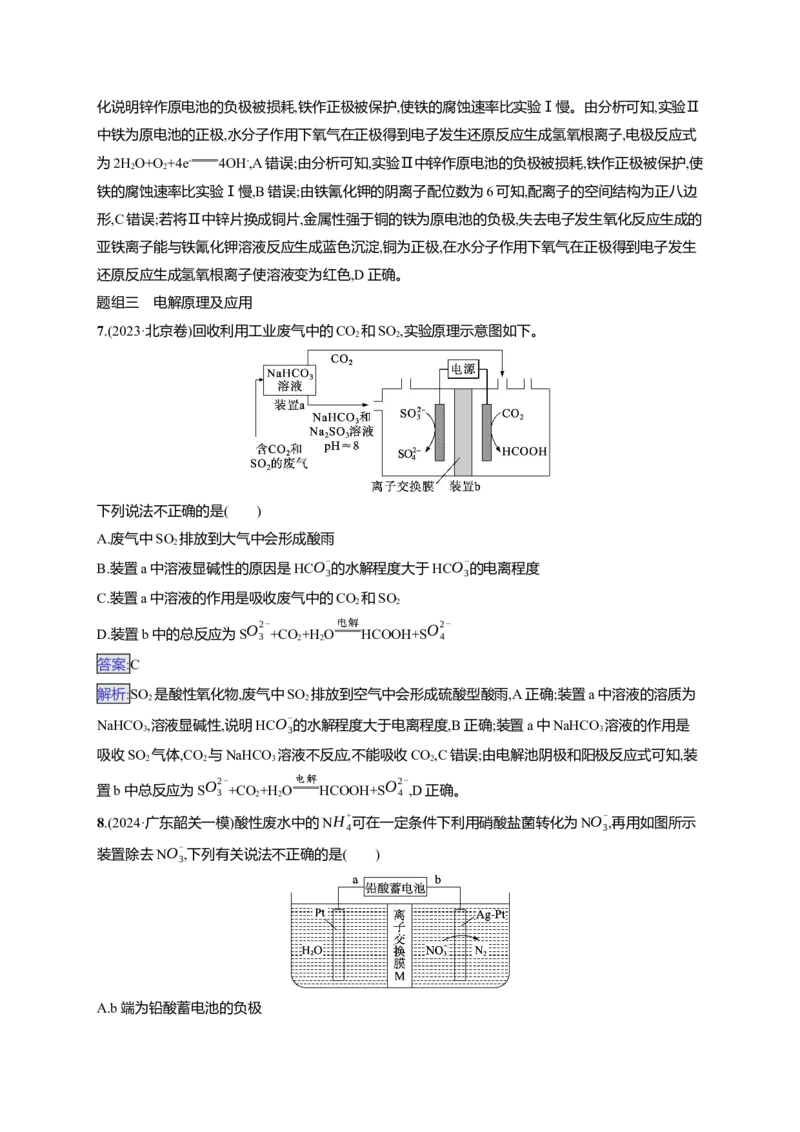
7.(2023·北京卷)回收利用工业废气中的CO 和SO ,实验原理示意图如下。
2 2
下列说法不正确的是( )
A.废气中SO 排放到大气中会形成酸雨
2
B.装置a中溶液显碱性的原因是HCO- 的水解程度大于HCO-
的电离程度
3 3
C.装置a中溶液的作用是吸收废气中的CO 和SO
2 2
O2- O2-
D.装置b中的总反应为S
3
+CO
2
+H
2
O HCOOH+S
4
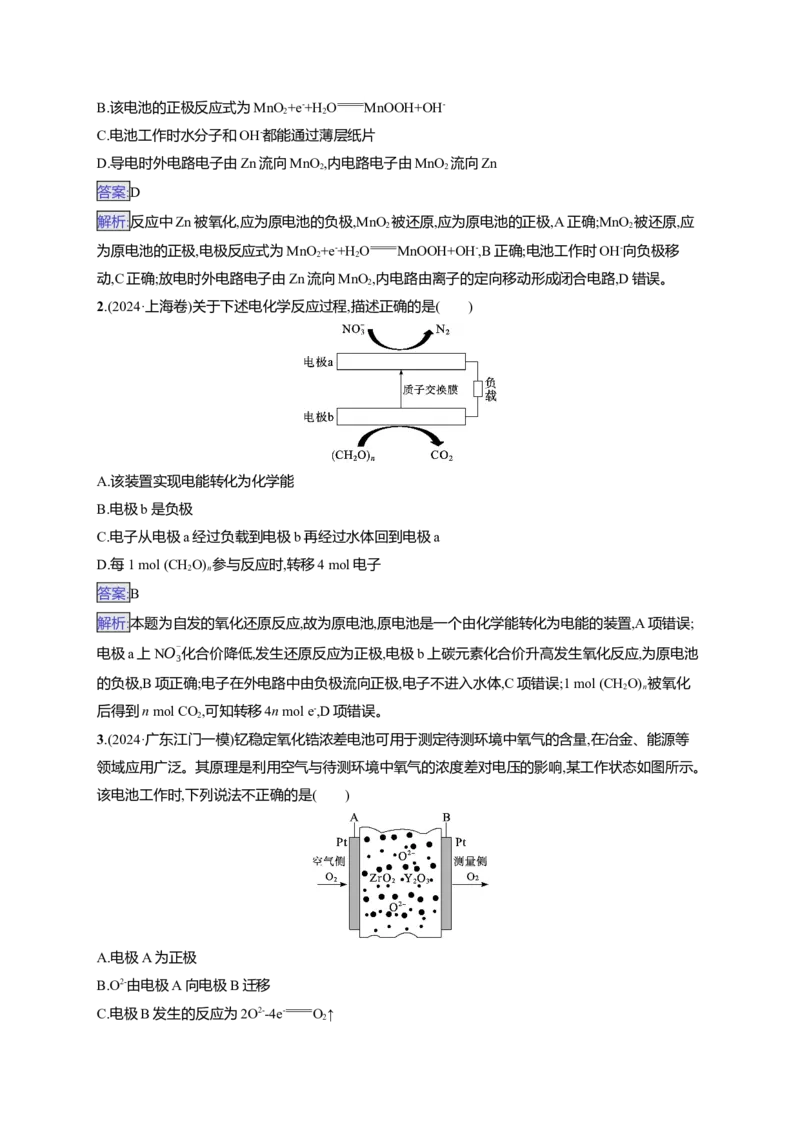
8.(2024·广东韶关一模)酸性废水中的NH+ 可在一定条件下利用硝酸盐菌转化为NO-
,再用如图所示
4 3
装置除去NO-
,下列有关说法不正确的是( )
3
A.b端为铅酸蓄电池的负极
B.该装置电能转化为化学能
C.M为阳离子交换膜
D.电解池阴极的电极反应式为2NO-
+6H O+10e- N↑+12OH-
3 2 2
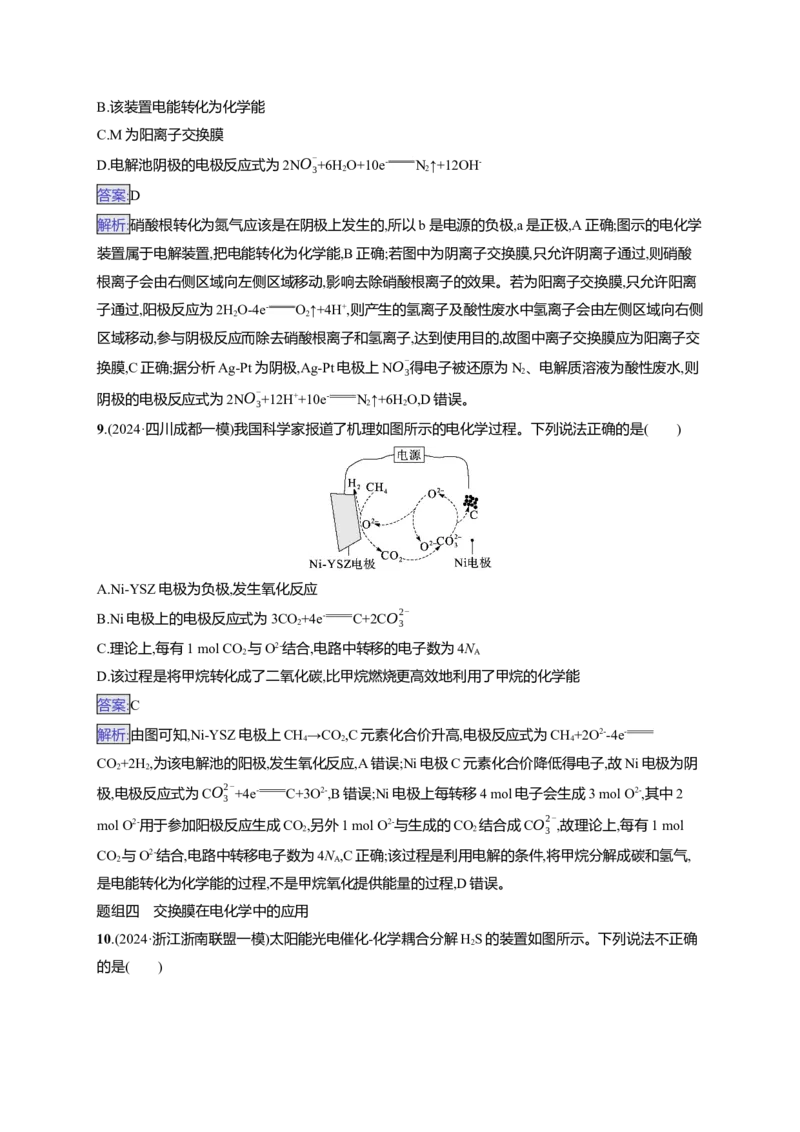
9.(2024·四川成都一模)我国科学家报道了机理如图所示的电化学过程。下列说法正确的是( )A.Ni-YSZ电极为负极,发生氧化反应
B.Ni电极上的电极反应式为3CO+4e-
C+2CO2-
2 3
C.理论上,每有1 mol CO 与O2-结合,电路中转移的电子数为4N
2 A
D.该过程是将甲烷转化成了二氧化碳,比甲烷燃烧更高效地利用了甲烷的化学能
题组四 交换膜在电化学中的应用
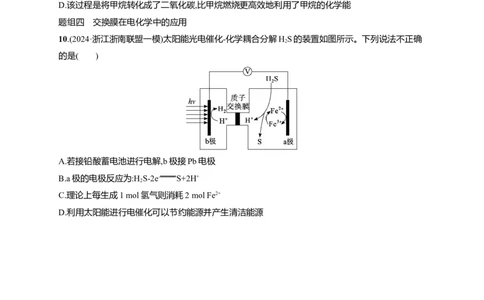
10.(2024·浙江浙南联盟一模)太阳能光电催化-化学耦合分解HS的装置如图所示。下列说法不正确
2
的是( )
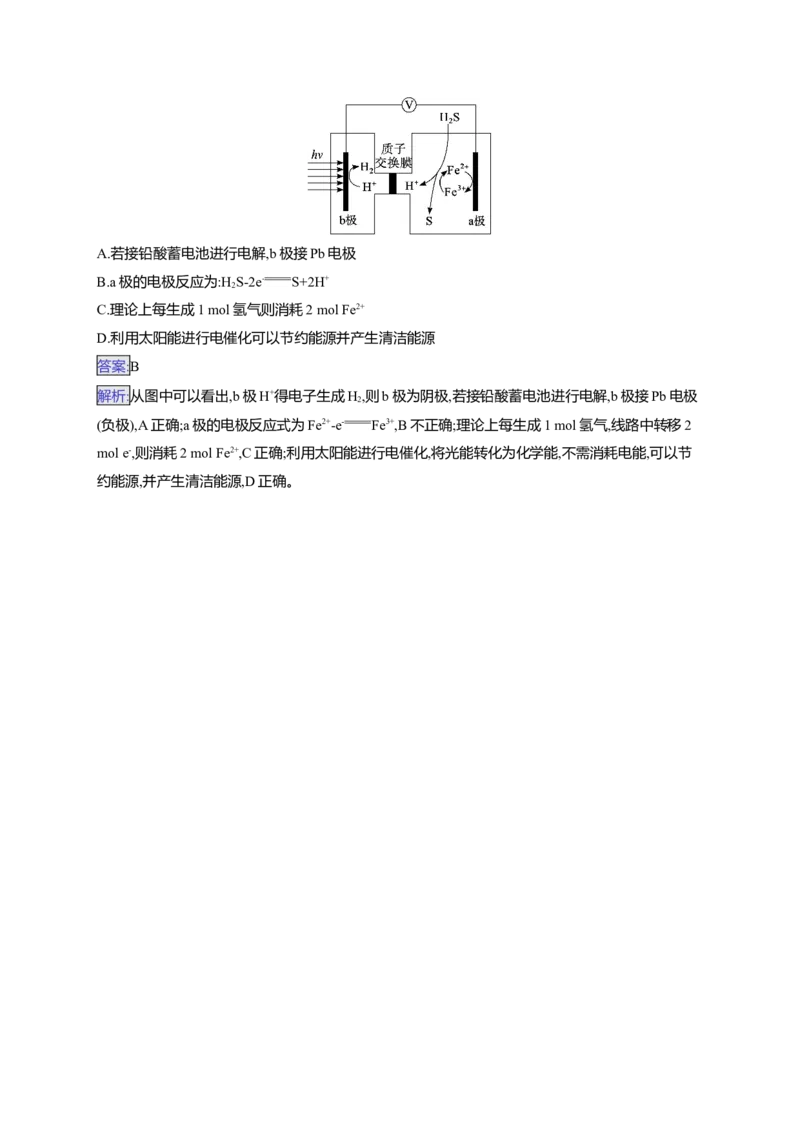
A.若接铅酸蓄电池进行电解,b极接Pb电极
B.a极的电极反应为:H S-2e- S+2H+
2
C.理论上每生成1 mol氢气则消耗2 mol Fe2+
D.利用太阳能进行电催化可以节约能源并产生清洁能源
选择题突破九 A 组 基础巩固练
题组一 新型化学电源
1.“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应式
为Zn+2MnO +H O ZnO+2MnOOH。下列说法不正确的是( )
2 2
A.该电池中Zn为负极,MnO 为正极
2B.该电池的正极反应式为MnO +e-+H O MnOOH+OH-
2 2
C.电池工作时水分子和OH-都能通过薄层纸片
D.导电时外电路电子由Zn流向MnO ,内电路电子由MnO 流向Zn
2 2
答案:D
解析:反应中Zn被氧化,应为原电池的负极,MnO 被还原,应为原电池的正极,A正确;MnO 被还原,应
2 2
为原电池的正极,电极反应式为MnO +e-+H O MnOOH+OH-,B正确;电池工作时OH-向负极移
2 2
动,C正确;放电时外电路电子由Zn流向MnO ,内电路由离子的定向移动形成闭合电路,D错误。
2
2.(2024·上海卷)关于下述电化学反应过程,描述正确的是( )
A.该装置实现电能转化为化学能
B.电极b是负极
C.电子从电极a经过负载到电极b再经过水体回到电极a
D.每1 mol (CH O) 参与反应时,转移4 mol电子
2 n
答案:B
解析:本题为自发的氧化还原反应,故为原电池,原电池是一个由化学能转化为电能的装置,A项错误;
电极a上NO-
化合价降低,发生还原反应为正极,电极b上碳元素化合价升高发生氧化反应,为原电池
3
的负极,B项正确;电子在外电路中由负极流向正极,电子不进入水体,C项错误;1 mol (CH O) 被氧化
2 n
后得到n mol CO ,可知转移4n mol e-,D项错误。
2
3.(2024·广东江门一模)钇稳定氧化锆浓差电池可用于测定待测环境中氧气的含量,在冶金、能源等
领域应用广泛。其原理是利用空气与待测环境中氧气的浓度差对电压的影响,某工作状态如图所示。
该电池工作时,下列说法不正确的是( )
A.电极A为正极
B.O2-由电极A向电极B迁移
C.电极B发生的反应为2O2--4e- O↑
2D.理论上,电解质中O2-的总物质的量会增加
答案:D
解析:由题给信息可知,空气侧的铂电极为浓差电池的正极,氧气在正极得到电子发生还原反应生成氧
负离子,A电极为正极,反应式为O+4e- 2O2-,测量侧的铂电极B为负极,氧负离子在负极失去电子
2
发生氧化反应生成氧气,电极反应式为2O2--4e- O↑,相同压强下,测量侧气体中氧气含量越低,浓差
2
电池的电势差越大。由分析可知,空气侧的铂电极为正极,A正确;阴离子向负极移动,O2-由电极A向
电极B迁移,B正确;测量侧的铂电极B为负极,氧负离子在负极失去电子发生氧化反应生成氧气,电
极反应式为2O2--4e- O↑,C正确;结合得失电子守恒,理论上,电解质中O2-的总物质的量不变,D错
2
误。
4.(2024·辽宁沈阳一模)2023年星恒电源发布“超钠F1”开启钠电在电动车上产业化元年。该二次电
池的电极材料为NaMn[Fe(CN) ](普鲁士白)和NaC(嵌钠硬碳)。下列说法中错误的是( )
2 6 x y
A.放电时,左边电极电势高
B.放电时,负极的电极反应式可表示为Na C-e- NaC+Na+
(x+1) y x y
C.充电时,电路中每转移1 mol电子,阳极质量增加23 g
D.比能量:锂离子电池高于钠离子电池
答案:C
解析:根据图示,放电时,NaC 中的钠失去电子生成Na+,因此NaC 为负极。放电时,左边电极为正极,
x y x y
电极电势高,A正确;放电时,负极的电极反应式可表示为Na C-e- NaC+Na+,B正确;充电时,阳
(x+1) y x y
极反应式为NaMn[Fe(CN) ]-2e- 2Na++Mn[Fe(CN) ],电路中每转移1 mol电子,阳极质量减少23
2 6 6
g,C错误;比能量就是参与电极反应的单位质量的电极材料放出电能的大小,Li、Na原子正常状态下
反应时均失去1个电子,但Li的相对原子质量小于Na的,故锂离子电池的比能量高于钠离子电池
的,D正确。
题组二 金属腐蚀与防护
5.“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷的温室效应率是CO 的84倍。已知管
2
道接口处有钢铁材料等,海水的pH约为8.0。设N 为阿伏加德罗常数的值。下列有关叙述不正确的
A
是 ( )A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
3w
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为 ×N
56 A
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
答案:C
解析:钢铁在弱碱性环境中主要发生吸氧腐蚀,A正确;表面涂层能防止钢铁管道和水、O 等物质接触,
2
从而起到抗腐蚀作用,B正确;钢铁腐蚀时负极电极反应式为Fe-2e- Fe2+,w g铁在海水中完全发生
2w
电化学腐蚀时转移电子数为 ×N ,后续发生反应4Fe(OH) +O +2H O 4Fe(OH) ,不属于电化学
56 A 2 2 2 3
腐蚀,C错误;锌比铁活泼,在海水中构成原电池,锌为负极,铁为正极,这种保护钢铁的方法叫牺牲阳极
法,D正确。
6.钢铁工业是我国国民经济的基础产业,研究钢铁的防腐有着重要的意义。某课题组进行如下实验:
实验 装置 5 min时现象 25 min时现象
铁钉表面及周边未见明显 铁钉周边出现少量红色和蓝色区域,有
Ⅰ
变化 少量红棕色铁锈生成
铁钉周边出现红色区域,未
铁钉周边红色加深,区域变大,未见蓝色
Ⅱ 见蓝色出现,锌片周边未见
出现,锌片周边未见明显变化
明显变化
下列说法正确的是( )
A.实验Ⅱ中正极的电极反应式为4H++O +4e- 2HO
2 2
B.实验Ⅱ中5 min时出现红色区域,说明铁钉腐蚀速率比Ⅰ快
C.由K[Fe(CN) ]的阴离子配位数可推出其空间结构为正六边形
3 6
D.若将Ⅱ中Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色
答案:D
解析:实验Ⅰ中铁钉周边出现少量红色和蓝色区域,有少量红棕色铁锈生成说明铁作原电池的负极,铁
钉发生吸氧腐蚀被损耗,实验Ⅱ中铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化说明锌作原电池的负极被损耗,铁作正极被保护,使铁的腐蚀速率比实验Ⅰ慢。由分析可知,实验Ⅱ
中铁为原电池的正极,水分子作用下氧气在正极得到电子发生还原反应生成氢氧根离子,电极反应式
为2HO+O+4e- 4OH-,A错误;由分析可知,实验Ⅱ中锌作原电池的负极被损耗,铁作正极被保护,使
2 2
铁的腐蚀速率比实验Ⅰ慢,B错误;由铁氰化钾的阴离子配位数为6可知,配离子的空间结构为正八边
形,C错误;若将Ⅱ中锌片换成铜片,金属性强于铜的铁为原电池的负极,失去电子发生氧化反应生成的
亚铁离子能与铁氰化钾溶液反应生成蓝色沉淀,铜为正极,在水分子作用下氧气在正极得到电子发生
还原反应生成氢氧根离子使溶液变为红色,D正确。
题组三 电解原理及应用
7.(2023·北京卷)回收利用工业废气中的CO 和SO ,实验原理示意图如下。
2 2
下列说法不正确的是( )
A.废气中SO 排放到大气中会形成酸雨
2
B.装置a中溶液显碱性的原因是HCO- 的水解程度大于HCO-
的电离程度
3 3
C.装置a中溶液的作用是吸收废气中的CO 和SO
2 2
O2- O2-
D.装置b中的总反应为S
3
+CO
2
+H
2
O HCOOH+S
4
答案:C
解析:SO 是酸性氧化物,废气中SO 排放到空气中会形成硫酸型酸雨,A正确;装置a中溶液的溶质为
2 2
NaHCO
,溶液显碱性,说明HCO-
的水解程度大于电离程度,B正确;装置a中NaHCO 溶液的作用是
3 3 3
吸收SO 气体,CO 与NaHCO 溶液不反应,不能吸收CO,C错误;由电解池阴极和阳极反应式可知,装
2 2 3 2
O2- O2-
置b中总反应为S
3
+CO
2
+H
2
O HCOOH+S
4
,D正确。
8.(2024·广东韶关一模)酸性废水中的NH+ 可在一定条件下利用硝酸盐菌转化为NO-
,再用如图所示
4 3
装置除去NO-
,下列有关说法不正确的是( )
3
A.b端为铅酸蓄电池的负极B.该装置电能转化为化学能
C.M为阳离子交换膜
D.电解池阴极的电极反应式为2NO-
+6H O+10e- N↑+12OH-
3 2 2
答案:D
解析:硝酸根转化为氮气应该是在阴极上发生的,所以b是电源的负极,a是正极,A正确;图示的电化学
装置属于电解装置,把电能转化为化学能,B正确;若图中为阴离子交换膜,只允许阴离子通过,则硝酸
根离子会由右侧区域向左侧区域移动,影响去除硝酸根离子的效果。若为阳离子交换膜,只允许阳离
子通过,阳极反应为2HO-4e- O↑+4H+,则产生的氢离子及酸性废水中氢离子会由左侧区域向右侧
2 2
区域移动,参与阴极反应而除去硝酸根离子和氢离子,达到使用目的,故图中离子交换膜应为阳离子交
换膜,C正确;据分析Ag-Pt为阴极,Ag-Pt电极上NO-
得电子被还原为N、电解质溶液为酸性废水,则
3 2
阴极的电极反应式为2NO-
+12H++10e- N↑+6H O,D错误。
3 2 2
9.(2024·四川成都一模)我国科学家报道了机理如图所示的电化学过程。下列说法正确的是( )
A.Ni-YSZ电极为负极,发生氧化反应
B.Ni电极上的电极反应式为3CO+4e-
C+2CO2-
2 3
C.理论上,每有1 mol CO 与O2-结合,电路中转移的电子数为4N
2 A
D.该过程是将甲烷转化成了二氧化碳,比甲烷燃烧更高效地利用了甲烷的化学能
答案:C
解析:由图可知,Ni-YSZ电极上CH→CO,C元素化合价升高,电极反应式为CH+2O2--4e-
4 2 4
CO+2H ,为该电解池的阳极,发生氧化反应,A错误;Ni电极C元素化合价降低得电子,故Ni电极为阴
2 2
极,电极反应式为CO2-
+4e- C+3O2-,B错误;Ni电极上每转移4 mol电子会生成3 mol O2-,其中2
3
mol O2-用于参加阳极反应生成CO,另外1 mol O2-与生成的CO
结合成CO2-
,故理论上,每有1 mol
2 2 3
CO 与O2-结合,电路中转移电子数为4N ,C正确;该过程是利用电解的条件,将甲烷分解成碳和氢气,
2 A
是电能转化为化学能的过程,不是甲烷氧化提供能量的过程,D错误。
题组四 交换膜在电化学中的应用
10.(2024·浙江浙南联盟一模)太阳能光电催化-化学耦合分解HS的装置如图所示。下列说法不正确
2
的是( )A.若接铅酸蓄电池进行电解,b极接Pb电极
B.a极的电极反应为:H S-2e- S+2H+
2
C.理论上每生成1 mol氢气则消耗2 mol Fe2+
D.利用太阳能进行电催化可以节约能源并产生清洁能源
答案:B
解析:从图中可以看出,b极H+得电子生成H,则b极为阴极,若接铅酸蓄电池进行电解,b极接Pb电极
2
(负极),A正确;a极的电极反应式为Fe2+-e- Fe3+,B不正确;理论上每生成1 mol氢气,线路中转移2
mol e-,则消耗2 mol Fe2+,C正确;利用太阳能进行电催化,将光能转化为化学能,不需消耗电能,可以节
约能源,并产生清洁能源,D正确。