文档内容
热点强化 7 Na CO 、NaHCO 含量测定的思维方法
2 3 3
方法一 热重法
1.某实验小组用热重法测定碳酸钠与碳酸氢钠混合物的组成,实验方法如下。
(1)加热5.00 g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物的质量减小
了 0.31 g , 写 出 发 生 反 应 的 化 学 方 程 式 :
_______________________________________________
_______________________________________________________________________________
,
则原混合物中碳酸钠的质量分数是________________________________________________。
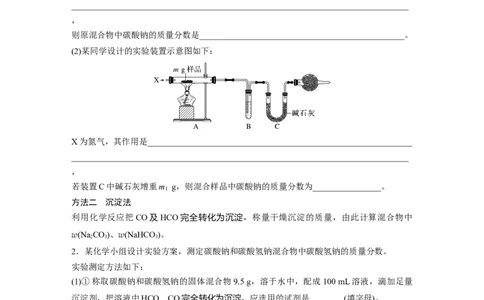
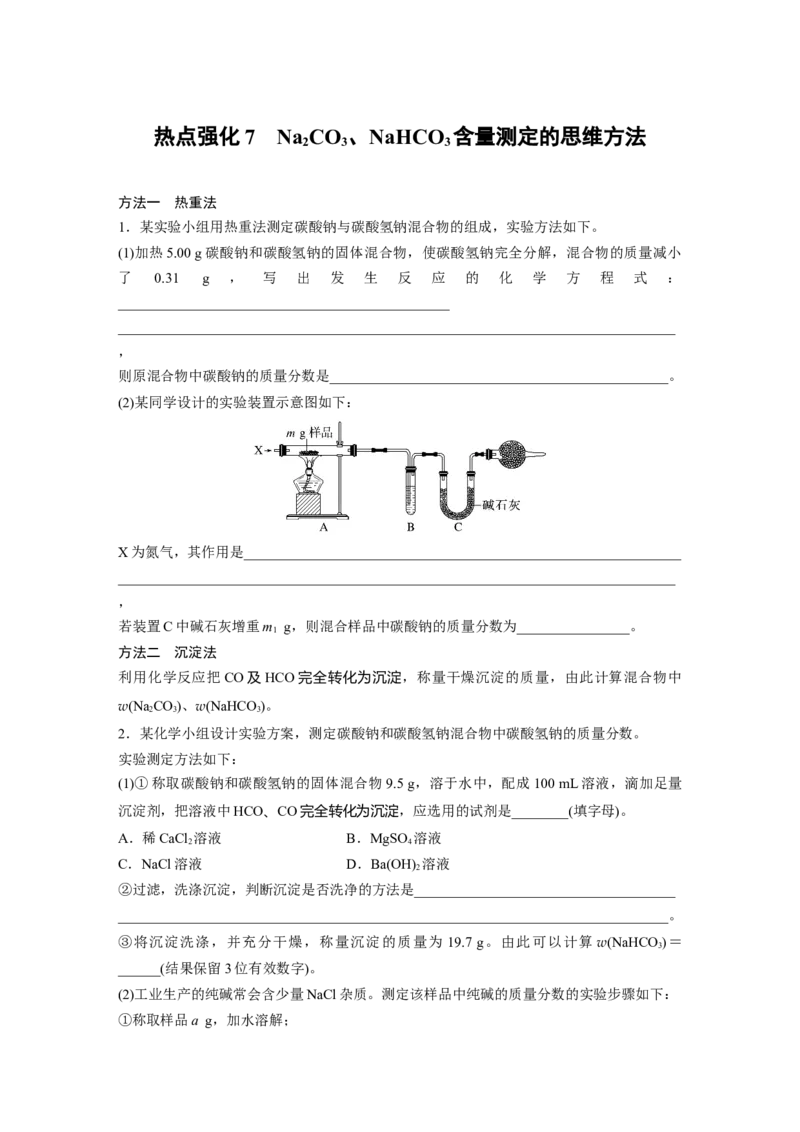
(2)某同学设计的实验装置示意图如下:
X为氮气,其作用是______________________________________________________________
_______________________________________________________________________________
,
若装置C中碱石灰增重m g,则混合样品中碳酸钠的质量分数为________________。
1
方法二 沉淀法
利用化学反应把CO及HCO完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中
w(Na CO)、w(NaHCO )。
2 3 3
2.某化学小组设计实验方案,测定碳酸钠和碳酸氢钠混合物中碳酸氢钠的质量分数。
实验测定方法如下:
(1)①称取碳酸钠和碳酸氢钠的固体混合物9.5 g,溶于水中,配成100 mL溶液,滴加足量
沉淀剂,把溶液中HCO、CO完全转化为沉淀,应选用的试剂是________(填字母)。
A.稀CaCl 溶液 B.MgSO 溶液
2 4
C.NaCl溶液 D.Ba(OH) 溶液
2
②过滤,洗涤沉淀,判断沉淀是否洗净的方法是_____________________________________
______________________________________________________________________________。
③将沉淀洗涤,并充分干燥,称量沉淀的质量为 19.7 g。由此可以计算 w(NaHCO )=
3
______(结果保留3位有效数字)。
(2)工业生产的纯碱常会含少量NaCl杂质。测定该样品中纯碱的质量分数的实验步骤如下:
①称取样品a g,加水溶解;②加入足量的BaCl 溶液;
2
③过滤、________、烘干、冷却、称量、烘干、冷却、________,最终得到固体b g。样品
中纯碱的质量分数为__________________(用含a、b的代数式表示)。
方法三 气体法
一般流程:
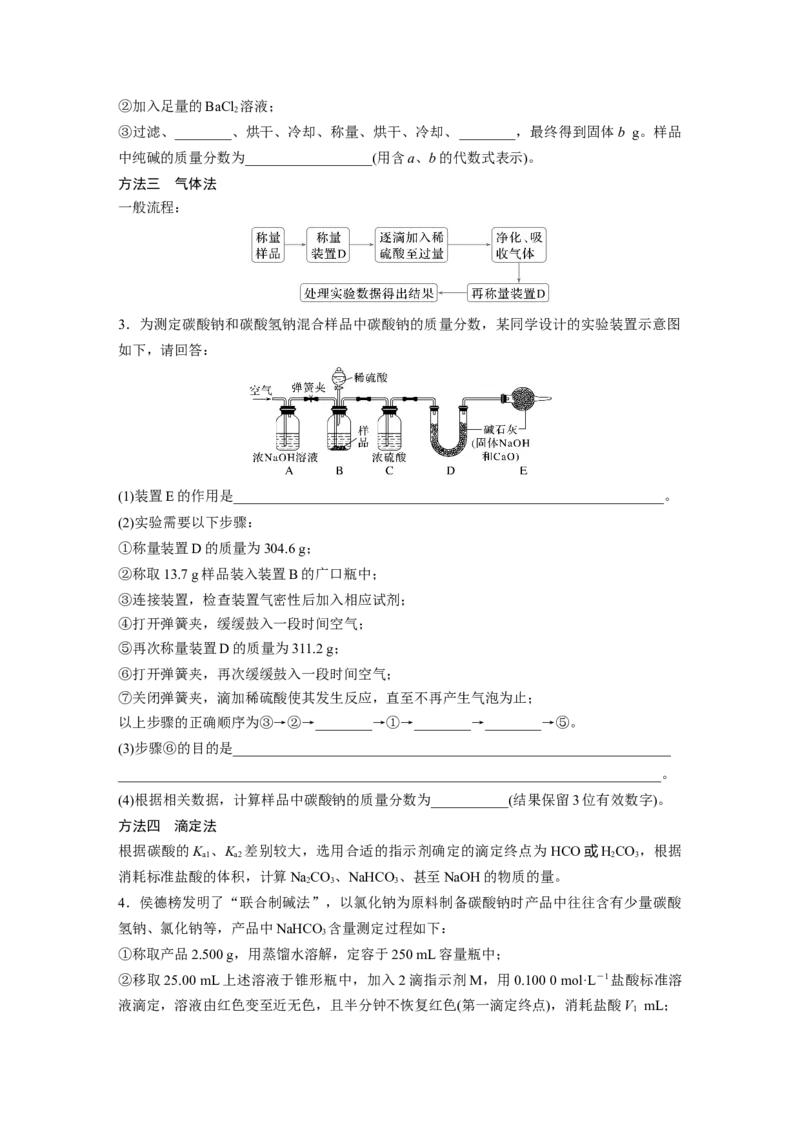
3.为测定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,某同学设计的实验装置示意图
如下,请回答:
(1)装置E的作用是_____________________________________________________________。
(2)实验需要以下步骤:
①称量装置D的质量为304.6 g;
②称取13.7 g样品装入装置B的广口瓶中;
③连接装置,检查装置气密性后加入相应试剂;
④打开弹簧夹,缓缓鼓入一段时间空气;
⑤再次称量装置D的质量为311.2 g;
⑥打开弹簧夹,再次缓缓鼓入一段时间空气;
⑦关闭弹簧夹,滴加稀硫酸使其发生反应,直至不再产生气泡为止;
以上步骤的正确顺序为③→②→________→①→________→________→⑤。
(3)步骤⑥的目的是______________________________________________________________
_____________________________________________________________________________。
(4)根据相关数据,计算样品中碳酸钠的质量分数为___________(结果保留3位有效数字)。
方法四 滴定法
根据碳酸的K 、K 差别较大,选用合适的指示剂确定的滴定终点为HCO或HCO ,根据
a1 a2 2 3
消耗标准盐酸的体积,计算NaCO、NaHCO 、甚至NaOH的物质的量。
2 3 3
4.侯德榜发明了“联合制碱法”,以氯化钠为原料制备碳酸钠时产品中往往含有少量碳酸
氢钠、氯化钠等,产品中NaHCO 含量测定过程如下:
3
①称取产品2.500 g,用蒸馏水溶解,定容于250 mL容量瓶中;
②移取25.00 mL上述溶液于锥形瓶中,加入2滴指示剂M,用0.100 0 mol·L-1盐酸标准溶
液滴定,溶液由红色变至近无色,且半分钟不恢复红色(第一滴定终点),消耗盐酸V mL;
1③在上述锥形瓶中再加入2滴指示剂N,继续用0.100 0 mol·L-1盐酸标准溶液滴定至终点
(第二滴定终点),又消耗盐酸V mL;
2
④平行测定三次,V 平均值为22.45,V 平均值为23.51。
1 2
回答下列问题:
(1)指示剂M为______________;指示剂N为__________,描述第二滴定终点前后颜色变化:
________________________________________________________________________。
(2)上述测量步骤③过程中,某时刻,滴入盐酸使溶液显中性,则此时溶液中的溶质为
__________________________。
(3)产品中NaHCO 的质量分数为__________(结果保留3位有效数字)。
3
(4)第一滴定终点时,某同学俯视读数,其他操作均正确,则 NaHCO 质量分数的计算结果
3
__________(填“偏大”“偏小”或“无影响”)。