文档内容
第 14 讲 铝、镁及其化合物
[复习目标] 1.了解铝、镁及其重要化合物的存在、性质和用途。2.掌握工业提取铝、镁的
一般方法。
考点一 铝及其化合物
1.铝元素的存在
铝是地壳中含量________的金属元素,全部以________的形式存在。
2.铝单质
(1)物理性质
铝单质是________色、有金属光泽的固体,硬度、密度较 ____,具有良好的
________________________________________________________________________。
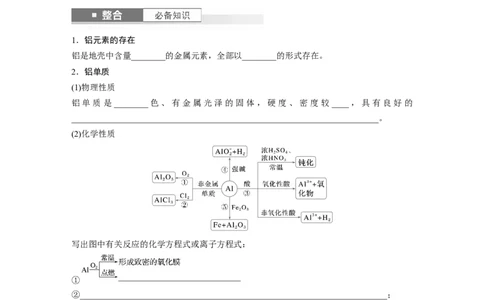
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
①
②________________________________________________________________________;
③
④________________________________________________________________________;
⑤___________________________________________________________________(铝热反应)。
3.氧化铝——两性氧化物4.氢氧化铝
(1)物理性质:白色胶状不溶于水的固体,有较强的吸附性。
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
(3)Al(OH) 的制备
3
写出下列反应的离子方程式:
①Al3+与氨水反应:_____________________________________________________________。
②向含AlO的溶液中通入过量的CO:____________________________________________。
2
③Al3+与AlO发生相互促进的水解反应:_________________________________________。
5.明矾
(1)明矾的化学式为______________________,属于复盐。
(2)明矾净水的原理:明矾溶于水时发生电离,电离方程式为__________________________,
其中Al3+发生水解反应,产生________,其吸附能力很强,可以吸附水中的悬浮杂质并形
成沉淀,使水变澄清。
1.MgO与Al粉的混合物也可称为铝热剂( )
2.实验室可用氧化铝坩埚熔化NaOH、NaCO 固体等( )
2 3
3.铝和酸反应时,氧化剂是酸,铝和碱反应时,氧化剂是碱( )
4.明矾可作净水剂,起到杀菌消毒的作用( )
一、Al、Al O、Al(OH) 分别与酸(碱)反应的特点
2 3 3
1.下列有关铝及其化合物的性质、用途说法正确的有________(填序号)。(1)铝制餐具不能长时间存放酸性、碱性食物
(2)两份相同质量的铝粉,分别与足量的盐酸和氢氧化钠溶液反应,产生的氢气的质量前者
多
(3)用氢氧化钠溶液去除铝条表面的氧化膜:Al O+2OH-===2Al3++HO
2 3 2
(4)向Al (SO ) 溶液中加入过量氨水的离子方程式:Al3++3NH ·H O===Al(OH) ↓+3NH
2 4 3 3 2 3
(5)铝与少量NaOH溶液反应得到铝盐,与足量NaOH溶液反应生成偏铝酸盐
(6)常温下,由于铝与浓硫酸不反应,所以可用铝制槽车运送浓硫酸
(7)与Al反应能放出H 的溶液中可能大量存在:Fe2+、K+、NO、SO
2
2.称取两份铝粉,第一份加入足量氢氧化钠溶液,第二份加入足量盐酸,若要放出等量的
气体,两份铝粉的质量之比为( )
A.1∶3 B.3∶1 C.1∶1 D.4∶3
二、Al3+、NH、H+等与OH-反应的顺序
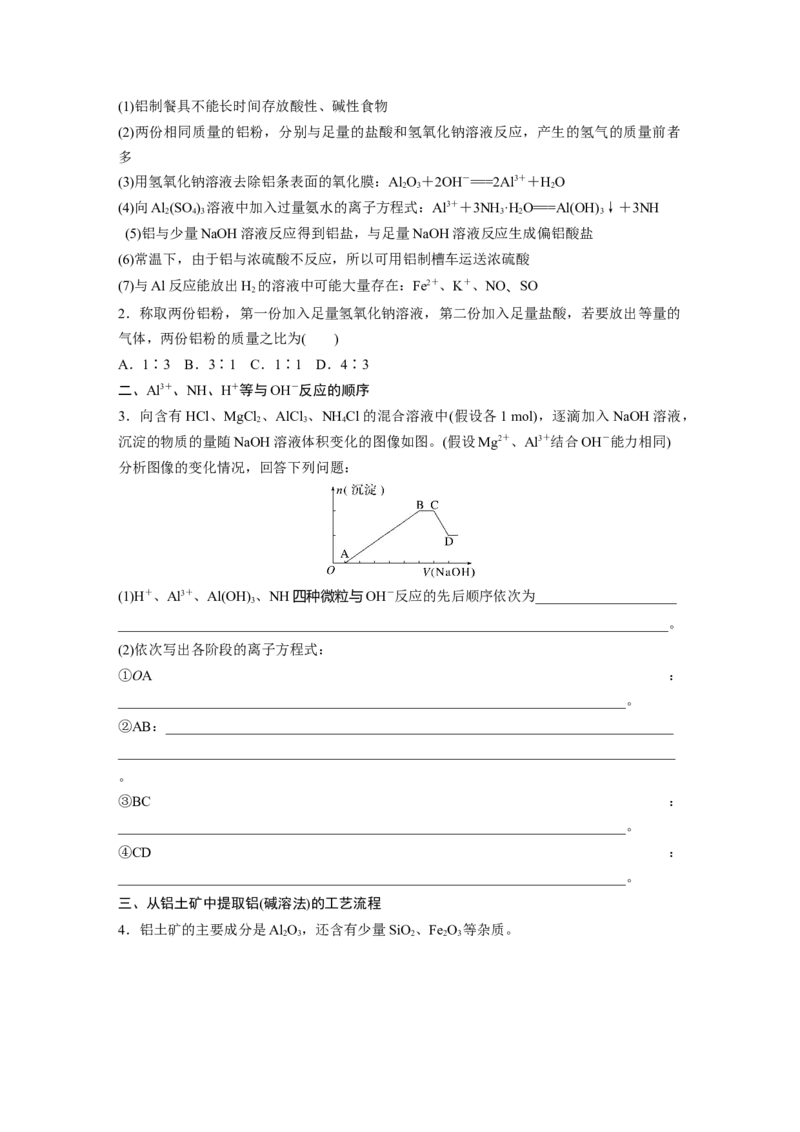
3.向含有HCl、MgCl 、AlCl 、NH Cl的混合溶液中(假设各1 mol),逐滴加入NaOH溶液,
2 3 4
沉淀的物质的量随NaOH溶液体积变化的图像如图。(假设Mg2+、Al3+结合OH-能力相同)
分析图像的变化情况,回答下列问题:
(1)H+、Al3+、Al(OH) 、NH四种微粒与OH-反应的先后顺序依次为____________________
3
______________________________________________________________________________。
(2)依次写出各阶段的离子方程式:
①OA :
________________________________________________________________________。
②AB:________________________________________________________________________
_______________________________________________________________________________
。
③BC :
________________________________________________________________________。
④CD :
________________________________________________________________________。
三、从铝土矿中提取铝(碱溶法)的工艺流程
4.铝土矿的主要成分是Al O,还含有少量SiO、Fe O 等杂质。
2 3 2 2 3(1)氧化铝是________氧化物,资料表明,SiO 在“碱溶”时转化为铝硅酸钠沉淀,除此外,
2
滤渣中还含有________(化学式)。写出“碱溶”时生成 NaAlO 的离子方程式:
2
_______________________________________________________________________________。
(2)采用电解熔融Al O 制备铝而不用氯化铝的原因是_________________________________。
2 3
(3)冰晶石的化学式为_________________________________,电解时加入冰晶石的目的是
________________________________________________________________________。
(4)写出Al(OH) ――→Al O――→Al转化的化学方程式:_______________________________、
3 2 3
_______________________________________________________________________________
。
(5)电解熔融Al O 时作阳极的石墨易消耗,原因是___________________________________,
2 3
应该采取的措施是_______________________________________________________________。
锌、铍的两性化合物
1.铝、铍(Be)及其化合物具有相似的化学性质。已知反应:BeCl +NaBeO +
2 2 2
2HO===2NaCl+2Be(OH) ↓能完全进行,则下列推断正确的是( )
2 2
A.Be(OH) 既能溶于盐酸,又能溶于NaOH溶液
2
B.BeCl 水溶液的导电性强,故BeCl 是离子化合物
2 2
C.NaBeO 溶液的 pH>7,将其蒸干并灼烧后得到的残留物为BeO
2 2
D.BeCl 溶液的 pH>7,将其蒸干并灼烧后得到的残留物可能是BeCl
2 2
2.锌和铝都是活泼金属,其氢氧化物均既能溶于强酸溶液,又能溶于强碱溶液,但是
Al(OH) 不溶于氨水,而Zn(OH) 能溶于氨水,生成[Zn(NH )]2+。
3 2 3 4
回答下列问题:
(1)单质铝溶于NaOH溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和NaOH溶液反应的离子方程式:_________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法可以鉴别的是________(填序号)。
①Al (SO ) 和NaOH ②Al (SO ) 和氨水
2 4 3 2 4 3
③ZnSO 和NaOH ④ZnSO 和氨水
4 4
(4)写出可溶性铝盐和氨水反应的离子方程式:_______________________________________。
试解释实验室不宜用可溶性锌盐与氨水反应制取氢氧化锌的原因:_____________________
________________________________________________________________________。考点二 镁及其化合物
1.镁的化学性质
(1)与氧气反应:________________________________________________________________。
(发出耀眼的强光,生成白色固体物质)
(2)与氮气反应:________________________________________________________________。
(镁在空气中燃烧得到MgO和MgN 的混合物)
3 2
(3)与盐酸(或硫酸)反应:________________________________________________________。
(4)与二氧化碳反应:____________________________________________________________。
(镁着火不能用CO 灭火)
2
(5)与盐溶液反应,如与硫酸铜溶液反应:__________________________________________
______________________________________________________________________________。
(6)与水反应:__________________________________________________________________。
2.镁的重要化合物
(1)氧化镁:白色粉末状固体,____溶于水,属于______________,与盐酸反应的离子方程
式为________________________________________________________________________。
(2)氢氧化镁:白色固体,____溶于水,中强碱,与盐酸反应的离子方程式为
______________________________________________________________________________
______________________________________________________________________________。
特别提醒 氢氧化镁的溶解度小于碳酸镁,能发生反应 MgCO +HO=====Mg(OH) +
3 2 2
CO↑,镁元素在水垢中的存在形式是Mg(OH) 。
2 2
1.从海水中提取镁的流程如图所示:
主要化学反应为
(1)制石灰乳:__________________________________________________________________、
______________________________________________________________________________。
(2) 沉 淀 Mg2 + :
_________________________________________________________________。(3)制备MgCl :________________________________________________________________、
2
______________________________________________________________________________。
(4)电解MgCl :________________________。
2
2.(2023·广西凭祥高三模拟)利用菱镁矿MgCO (含杂质Al O 、FeCO)制取镁的工艺流程如
3 2 3 3
图,下列说法正确的是( )
A.“酸浸”时溶液中有电子转移
B.“氧化”时用稀硝酸代替更好
C.沉淀混合物为Al(OH) 和Fe(OH)
3 3
D.电解MgCl 溶液可得到金属镁
2
1.正误判断,正确的打“√”,错误的打“×”。
(1)氧化铝熔点高,常用于制造耐高温材料(2022·浙江6月选考,8C)( )
(2)工业上通过电解六水合氯化镁制取金属镁(2022·浙江6月选考,9A)( )
(3)铝热反应非常剧烈,操作时要戴上石棉手套和护目镜(2022·浙江6月选考,11B)( )
(4)技术人员开发高端耐腐蚀镀铝钢板,是因为铝能形成致密氧化膜(2022·广东,6D)( )
(5)利用海水制取溴和镁单质,此过程中 Br-可被氧化,Mg2+可被还原(2022·广东,12B)(
)
(6)MgCl 溶液中滴加NaOH溶液至过量,现象为产生白色沉淀后沉淀消失(2022·海南,6A)(
2
)
2.(2020·江苏,3)下列有关物质的性质与用途具有对应关系的是( )
A.铝的金属活泼性强,可用于制作铝金属制品
B.氧化铝熔点高,可用作电解冶炼铝的原料
C.氢氧化铝受热分解,可用于中和过多的胃酸
D.明矾溶于水并水解形成胶体,可用于净水
3.(2022·湖南,7)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
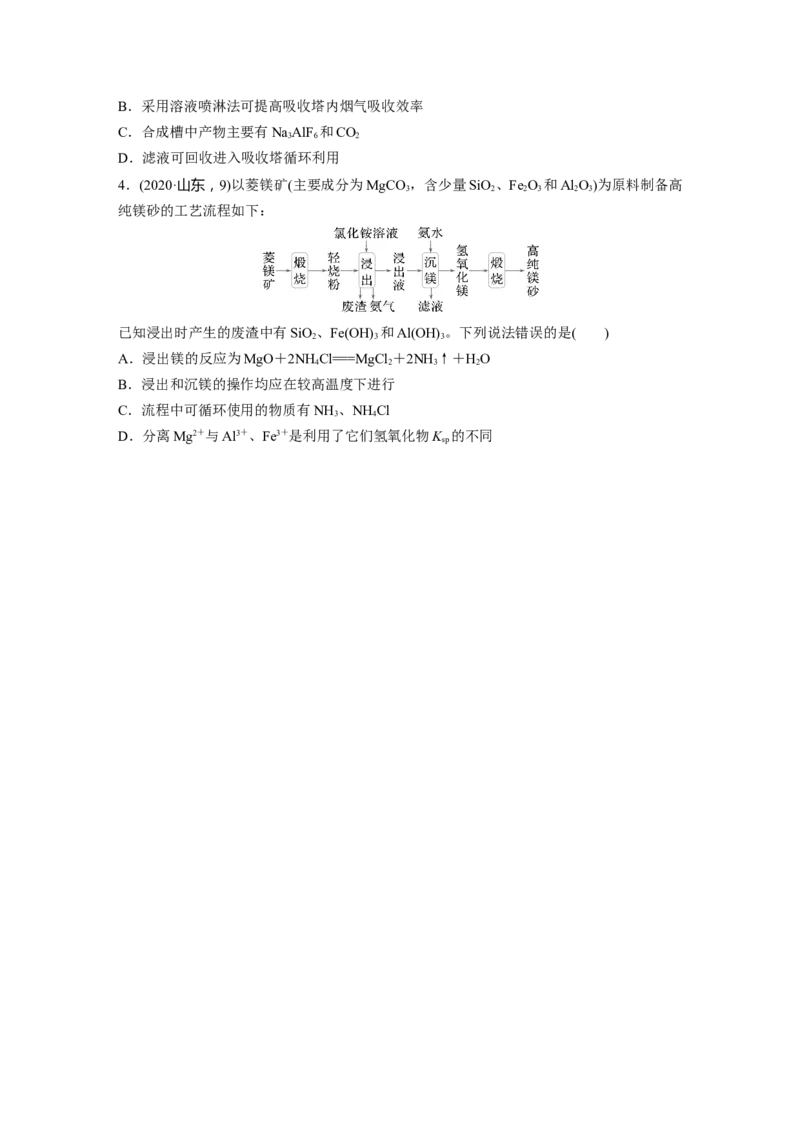
4.(2020·山东,9)以菱镁矿(主要成分为MgCO ,含少量SiO 、Fe O 和Al O)为原料制备高
3 2 2 3 2 3
纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有SiO、Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp