文档内容
微专题 18 金属及其化合物制备流程(Cr)
铬:元素符号Cr,原子序数24,原子量51.996,外围电子排布3d54s1,位于第四周期ⅥB
族。主要化合价+2、+3、+6。
一、物理性质:
银白色有光泽金属,含有杂质的铬硬而脆,高纯铬有延展性。
二、化学性质:
耐腐蚀性强,不溶于水,在空气中即便是在高温下氧化也很缓慢。高温下,铬能与卤素、
硫、氮、碳等化合,也能跟水蒸气反应。能慢慢地溶于稀盐酸、稀硫酸、生成二价铬盐
(蓝色),与空气接触时很快被氧化成三价铬盐(绿色)。铬能与浓硫酸反应,但不溶于浓硝
酸,因表面生成致密氧化膜而呈钝态。能被熔融碱侵蚀。与氢反应生成CrH。
2
三、用途:
主要用于制不锈钢及耐高温耐腐蚀的高强度的合金,制电阻合金,还用于电镀。1797年
法国人沃克兰发现了铬。主要矿物有铬铁矿Fe(CrO )。由电解铬氨钒溶液或铬酸溶液制
2 2
得,也可用铝粉还原氧化铬制得。
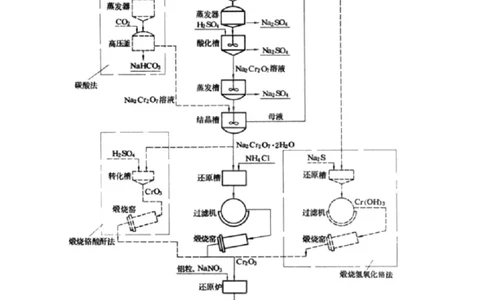
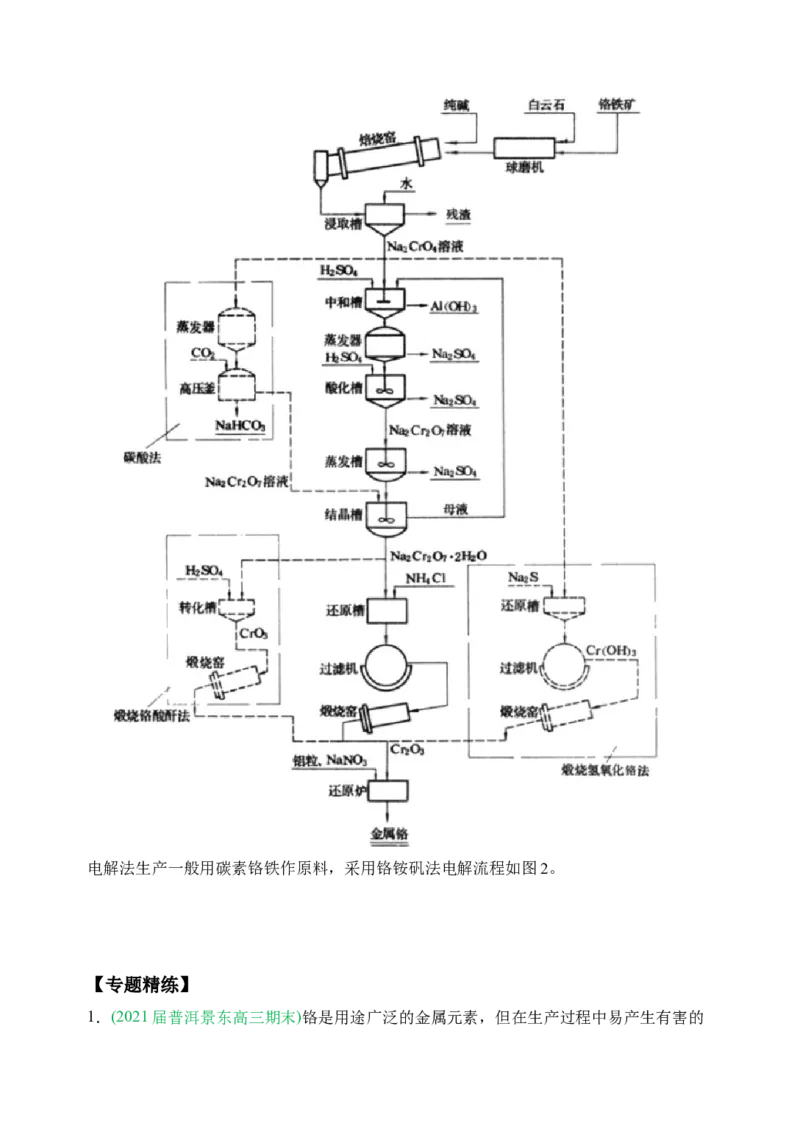
四、铬的冶炼工艺流程
金属 铬 的冶炼方法主要有:金属热还原法(铝热法)、电解法及其他高温冶金法。另外,
钢铁工业中广泛应用的铬铁合金和硅铬合金是用电炉冶炼的。
铝热法包括从铬矿制取氧化铬和铝还原氧化铬制得金属铬两道工序,主要工艺流程如图
1。电解法生产一般用碳素铬铁作原料,采用铬铵矾法电解流程如图2。
【专题精练】
1.(2021届普洱景东高三期末)铬是用途广泛的金属元素,但在生产过程中易产生有害的含铬工业废水。
(1)还原沉淀法是处理含Cr O 和CrO 工业废水的一种常用方法,其工艺流程为:CrO
2
Cr O Cr3+ Cr(OH) ↓
2 3
其中第Ⅰ步存在平衡:2CrO (黄色)+2H+ Cr O (橙色)+H O
2 2
①若平衡体系的pH=0,该溶液显___________色。
②根据2CrO +2H+ Cr O +H O,设计如图装置(均为惰性电极)电解NaCrO 溶液
2 2 2 4
制取NaCr O。 NaCr O 中铬元素的化合价为___________,图中右侧电极连接电源的
2 2 7 2 2 7
___________极,其电极反应式为___________。
③第Ⅱ步反应的离子方程式:___________。
(2)CrO 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火。若该过程中乙醇被
3
氧化成乙酸,CrO 被还原成绿色的Cr (SO ) 。 完成该反应的化学方程式:
3 2 4 3
□CrO +□C HOH+□H SO =□Cr (SO )+□CHCOOH+□_______
3 2 5 2 4 2 4 3 3
【答案】(1) ①橙 ② +6 正 4OH﹣﹣4e﹣=O ↑+2H O ③6Fe2++Cr O +14H+=6Fe3+
2 2 2
+2Cr3++7H O (2) 9H O
2 2
【解析】
(1)①若平衡体系的pH=0,溶液酸性较强,平衡2CrO (黄色)+2H+═Cr O (橙色)+H O正
2 2
向移动,该溶液显橙色,故答案为:橙;②根据2CrO +2H+ Cr O +H O,设计如图装置(均为惰性电极)电解NaCrO 溶液
2 2 2 4
制取NaCr O。由化合价代数和为0可知 NaCr O 中铬元素的化合价为+6,设计图示装
2 2 7 2 2 7
置(均为惰性电极)电解NaCrO 溶液制取NaCr O,需要通过电解生成H+提高溶液的酸性,
2 4 2 2 7
说明在该电极是阳极,连接电源的正极,其电极反应式为4OH﹣﹣4e﹣=O ↑+2H O,故答
2 2
案为:+6;正;4OH﹣﹣4e﹣=O ↑+2H O;
2 2
③亚铁离子与Cr O2-发生氧化还原反应,第Ⅱ步反应的离子方程式:6Fe2++Cr O
2 7 2
+14H+=6Fe3++2Cr3++7H O,故答案为:6Fe2++Cr O +14H+=6Fe3++2Cr3++7H O;
2 2 2
(2)CrO 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火。若该过程中乙醇被
3
氧化成乙酸,碳的平均化合价从-2价升高到0,1个乙醇化合价变化4,CrO 被还原成绿
3
色的硫酸铬[Cr(SO )],铬的化合价从+6价降低到+3价,1个CrO 化合价变化3,两者的
2 4 3 3
最小公倍数是12,再根据原子守恒得
4CrO+3C HOH+6H SO =2Cr (SO )+3CH COOH+9H O,故答案为:9HO。
3 2 5 2 4 2 4 3 3 2 2
2.(2021届荆州高三一检)硒和铬元素都是人体必需的微量元素,请回答下列问题:
(1)硒与氧为同主族元素,硒的原子结构示意图为_______。
(2)由硒在周期表中的位置分析判断下列说法不正确的是_______(填标号)
A.沸点: B.热稳性:
C.还原性: D.原子半径:
(3)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用
及其他富硒物质清除人体内的活性氧,此时 表现出_______性。
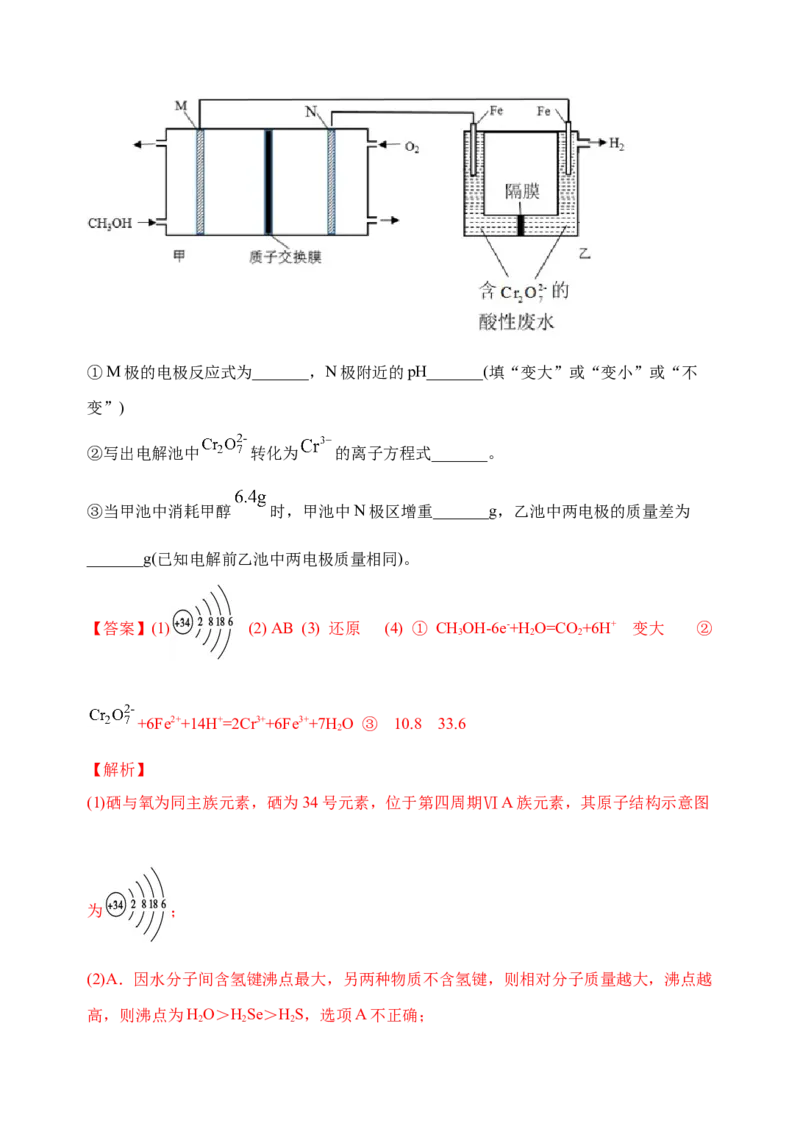
(4)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有
)的原理示意图如下图所示。①M极的电极反应式为_______,N极附近的pH_______(填“变大”或“变小”或“不
变”)
②写出电解池中 转化为 的离子方程式_______。
③当甲池中消耗甲醇 时,甲池中N极区增重_______g,乙池中两电极的质量差为
_______g(已知电解前乙池中两电极质量相同)。
【答案】(1) (2) AB (3) 还原 (4) ① CHOH-6e-+H O=CO+6H+ 变大 ②
3 2 2
+6Fe2++14H+=2Cr3++6Fe3++7H O ③ 10.8 33.6
2
【解析】
(1)硒与氧为同主族元素,硒为34号元素,位于第四周期ⅥA族元素,其原子结构示意图
为 ;
(2)A.因水分子间含氢键沸点最大,另两种物质不含氢键,则相对分子质量越大,沸点越
高,则沸点为HO>HSe>HS,选项A不正确;
2 2 2B.非金属元素的非金属性越强,其氢化物越稳定,非金属性S>P,所以氢化物的稳定
性:PH <HS,选项B不正确;
3 2
C.非金属性 ,因非金属性越强,其对应阴离子的还原性越弱,则还原性:
,选项C正确;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径
, 选项D正确;
答案选AB;
(3) “活性氧”氧化性极强,服用含硒元素(Se)的化合物亚硒酸钠(NaSeO),能消除
2 3
人体內的活性氧,表明NaSeO 能将“活性氧”还原,“活性氧”为氧化剂,NaSeO 为
2 3 2 3
还原剂,表现出还原性;
(4) ①通入甲醇的M极为负极,甲醇失电子产生二氧化碳,则负极的电极反应式为
CHOH-6e-+H O=CO+6H+;N极为正极,酸性条件下正极上氧气得电子产生水,使溶液
3 2 2
中氢离子浓度减小,pH变大;
②连接N极即正极的电极为阳极,则左边铁电极上铁失电子产生 ,将电解池中
还原转化为 ,反应的离子方程式为 +6Fe2++14H+=2Cr3++6Fe3++7H O;
2
③当甲池中消耗甲醇 时,即0.2mol甲醇,根据M极电极反应式CHOH-6e-
3
+H O=CO+6H+可知,M极上消耗0.2mol甲醇时转移1.2mol电子,转移的质子为
2 2
1.2mol,质量为1.2g ,甲池中N极区发生电极反应O+4e-+4H+=2H O,转移1.2mol电子
2 2
消耗0.3mol氧气,即9.6g,故总增重9.6g +1.2g =10.8g,转移电子数为1.2mol,乙池中左
侧电极反应为Fe-2e-=Fe2+,质量减少0.6mol 56g/mol=33.6g,右侧电极上氢离子得电子产
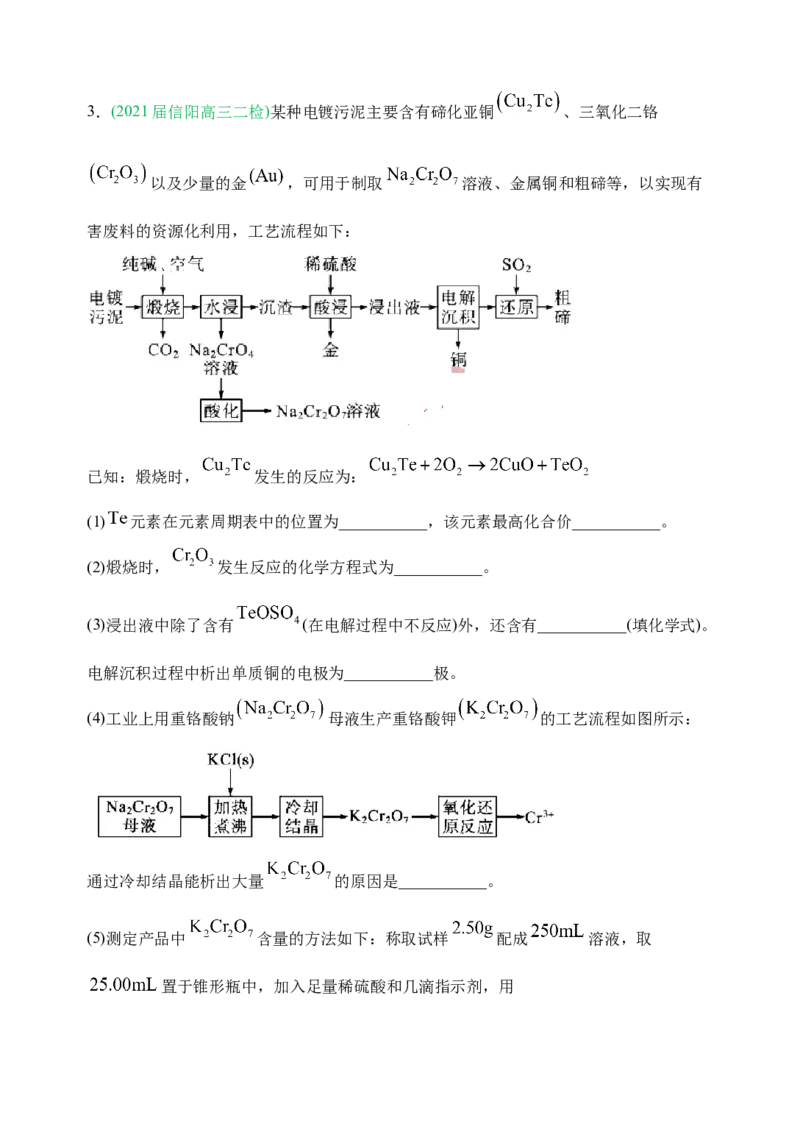
生氢气,电极质量不变,则两电极的质量差为33.6g。3.(2021届信阳高三二检)某种电镀污泥主要含有碲化亚铜 、三氧化二铬
以及少量的金 ,可用于制取 溶液、金属铜和粗碲等,以实现有
害废料的资源化利用,工艺流程如下:
已知:煅烧时, 发生的反应为:
(1) 元素在元素周期表中的位置为___________,该元素最高化合价___________。
(2)煅烧时, 发生反应的化学方程式为___________。
(3)浸出液中除了含有 (在电解过程中不反应)外,还含有___________(填化学式)。
电解沉积过程中析出单质铜的电极为___________极。
(4)工业上用重铬酸钠 母液生产重铬酸钾 的工艺流程如图所示:
通过冷却结晶能析出大量 的原因是___________。
(5)测定产品中 含量的方法如下:称取试样 配成 溶液,取
置于锥形瓶中,加入足量稀硫酸和几滴指示剂,用标准液进行滴定。滴定过程中发生反应的离子方程式
为___________。若三次实验消耗 标准液的体积平均为 ,则
所得产品中 的纯度为___________(保留三位有效数字)。
【答案】(1)第五周期ⅥA族 (2)
(3) 阴 (4) 低温条件下 的溶解度在整个体系中最小,且 的
溶解度随温度的降低而显著减小 (5)
49.0%
【解析】
(1) 碲元素位于第五周期ⅥA族,该元素的最高化合价为+6价,故答案为:第五周期ⅥA
族;+6 ;(2)根据工艺流程可知反应物为 ,纯碱以及空气中的氧气,生成物为二氧
化碳和重铬酸钠,则反应方程式为 ;故答案
为: ;(3)因加入了稀硫酸,则浸出液中一定
含有硫酸铜,铜离子得到电子转换为铜单质,电解池中阴极得到电子,故答案为:
;阴;(4)在低温条件下 的溶解度在整个体系中最小,且 的溶解度随温度的降低而显著减小,故答案为:低温条件下 的溶解度在整个体系中
最小,且 的溶解度随温度的降低而显著减小;(5)重铬酸根与氢离子、二价铁离
子反应经配平后可得离子方程式为 ,根
据方程式可得出重铬酸根与亚铁离子反应为1:6反应,消耗
的体积为25ml,且实验取配置溶液的十分之一进行反
应,则该样品的质量分数:
;故答案为:
;49.0%。
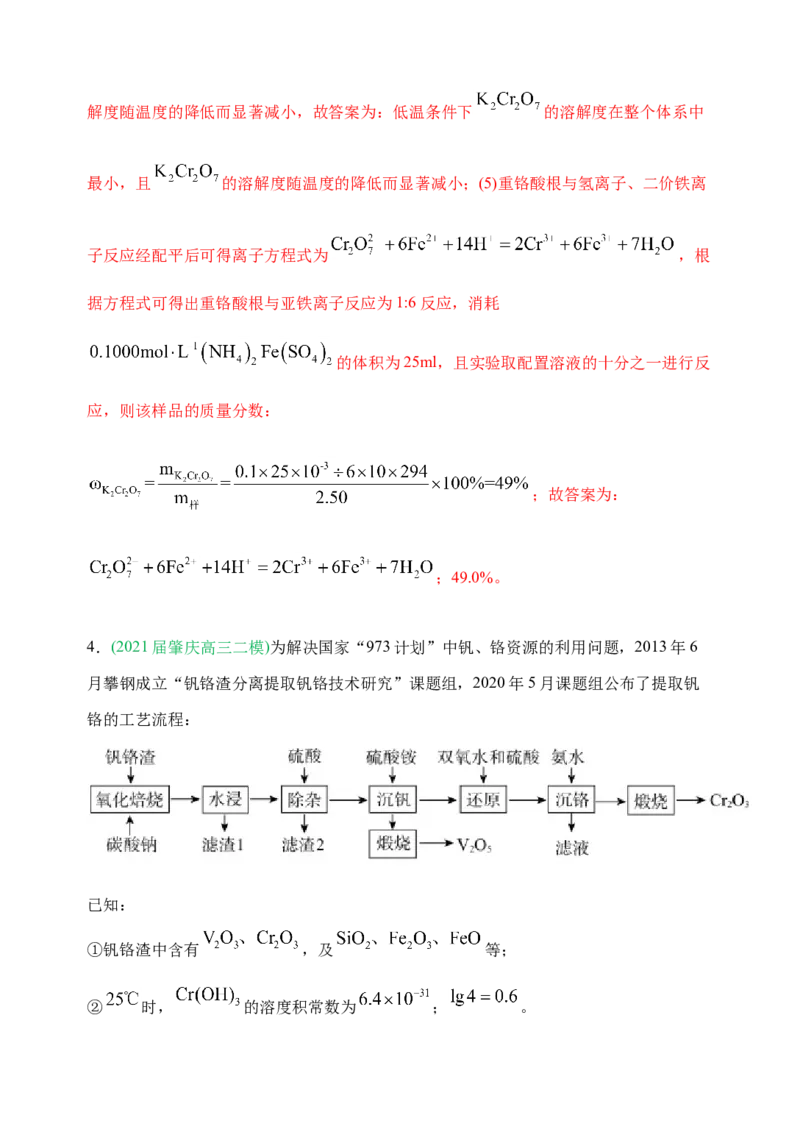
4.(2021届肇庆高三二模)为解决国家“973计划”中钒、铬资源的利用问题,2013年6
月攀钢成立“钒铬渣分离提取钒铬技术研究”课题组,2020年5月课题组公布了提取钒
铬的工艺流程:
已知:
①钒铬渣中含有 ,及 等;
② 时, 的溶度积常数为 ; 。回答下列问题:
(1)“氧化焙烧”时,钒铬渣中化合价发生变化的元素为铬及______(用元素名称表示)。
(2)为加快“水浸”速率,可采取的措施为______(写出一种即可)。
(3)“除杂”产生的滤渣2的成分是______(用化学式表示)。
(4)写出“煅烧”时反应的化学方程式______(已知“沉钒”时析出正五价钒的含氧酸铵盐)。
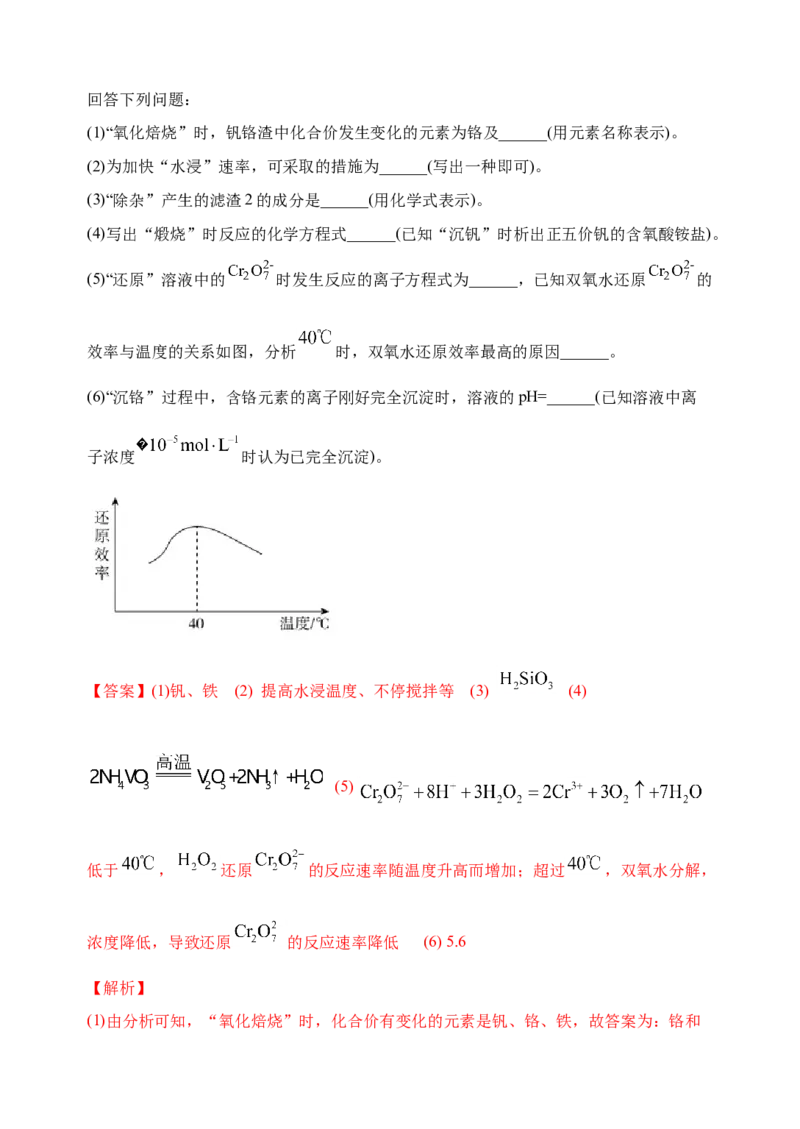
(5)“还原”溶液中的 时发生反应的离子方程式为______,已知双氧水还原 的
效率与温度的关系如图,分析 时,双氧水还原效率最高的原因______。
(6)“沉铬”过程中,含铬元素的离子刚好完全沉淀时,溶液的pH=______(已知溶液中离
子浓度 时认为已完全沉淀)。
【答案】(1)钒、铁 (2) 提高水浸温度、不停搅拌等 (3) (4)
(5)
低于 , 还原 的反应速率随温度升高而增加;超过 ,双氧水分解,
浓度降低,导致还原 的反应速率降低 (6) 5.6
【解析】
(1)由分析可知,“氧化焙烧”时,化合价有变化的元素是钒、铬、铁,故答案为:铬和铁;
(2)“水浸”需要加热,加快可溶于水的物质的溶解速率,故答案为:提高水浸温度、不停
搅拌等;
(3)由分析可知,水浸液中存在 ,与硫酸反应生成的滤渣为 ,故答案为:
;
(4)由分析可知,正五价钒的含氧酸铵盐为 ,“煅烧”时反应的化学方程式为
,故答案为:
;
(5)由分析可知,“还原”溶液中的 时发生反应的离子方程式为
;低于 , 还原 的反
应速率随温度升高而增加;超过 ,双氧水分解,浓度降低,导致还原 的反应
速率降低,故答案为: ;低于 ,
还原 的反应速率随温度升高而增加;超过 ,双氧水分解,浓度降低,
导致还原 的反应速率降低;
(6)由 得,,此时溶液的
,则 ,故答案为:5.6。
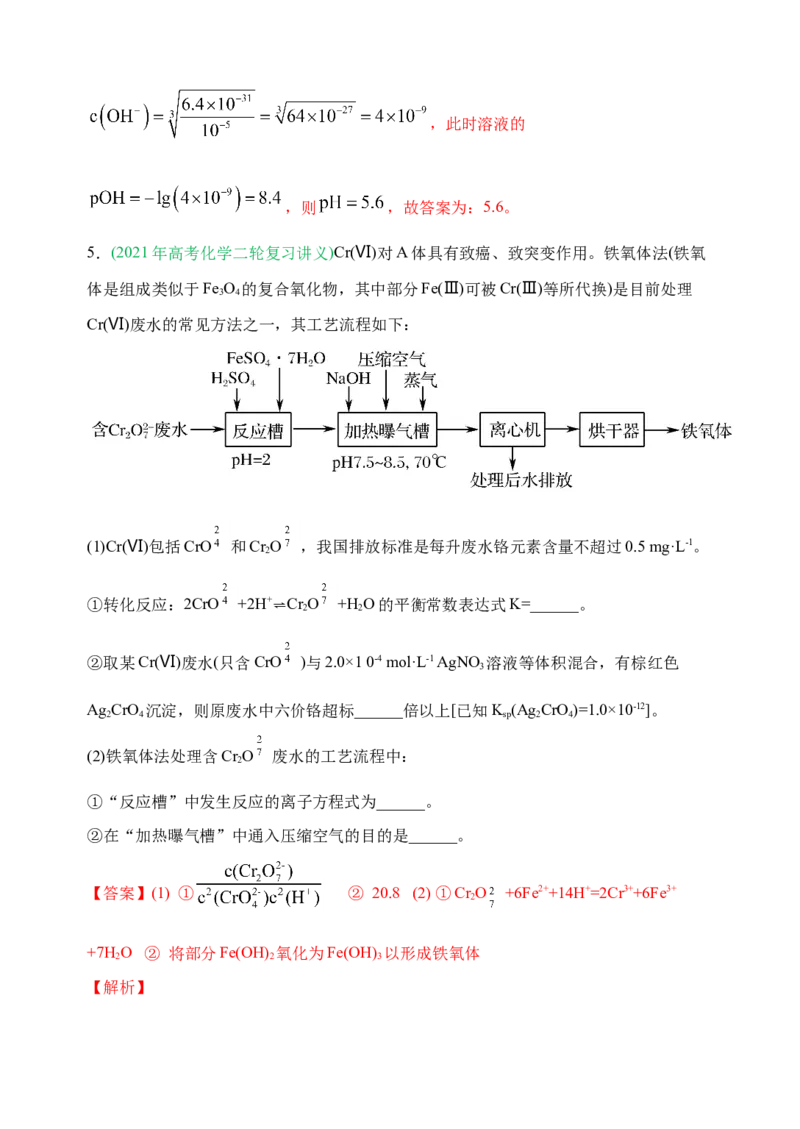
5.(2021年高考化学二轮复习讲义)Cr(Ⅵ)对A体具有致癌、致突变作用。铁氧体法(铁氧
体是组成类似于Fe O 的复合氧化物,其中部分Fe(Ⅲ)可被Cr(Ⅲ)等所代换)是目前处理
3 4
Cr(Ⅵ)废水的常见方法之一,其工艺流程如下:
(1)Cr(Ⅵ)包括CrO 和Cr O ,我国排放标准是每升废水铬元素含量不超过0.5 mg·L-1。
2
①转化反应:2CrO +2H+ ⇌Cr
2
O +H
2
O的平衡常数表达式K=______。
②取某Cr(Ⅵ)废水(只含CrO )与2.0×1 0-4 mol·L-1 AgNO 溶液等体积混合,有棕红色
3
Ag CrO 沉淀,则原废水中六价铬超标______倍以上[已知K (Ag CrO)=1.0×10-12]。
2 4 sp 2 4
(2)铁氧体法处理含Cr O 废水的工艺流程中:
2
①“反应槽”中发生反应的离子方程式为______。
②在“加热曝气槽”中通入压缩空气的目的是______。
【答案】(1) ① ② 20.8 (2) ①Cr O +6Fe2++14H+=2Cr3++6Fe3+
2
+7H O ② 将部分Fe(OH) 氧化为Fe(OH) 以形成铁氧体
2 2 3
【解析】(1)①平衡常数中不写入固体和纯液体,2CrO +2H+ ⇌Cr
2
O +H
2
O的平衡常数表达式K=
。
②设废水中CrO 的浓度为x mol·L-1,与AgNO 溶液等体积混合后,CrO 的浓度变成
3
mol·L-1,c(AgNO )= mol·L-1=1.0×10-4 mol·L-1,K (Ag CrO)=c2(Ag+)·c(CrO
3 sp 2 4
)=(1.0×10-4)2× =1.0×10-12,得x=2.0×10-4 mol·L-1,Cr含量:(2.0×10-4 mol ×52 g·mol-1×1
000 mg/g)/L=10.4 mg·L-1,超标为: =20.8倍。
(2)①反应槽中,Cr O 在酸性条件下氧化Fe2+,生成Fe3+和Cr3+,根据Fe和Cr得失电子
2
守恒,用H+平衡电荷,则离子方程式为Cr O +6Fe2++14H+=2Cr3++6Fe3++7H O。
2 2
②反应槽中Fe2+是过量的,在“加热曝气槽”中,加入NaOH会生成Fe(OH) ,压入空气,
2
可以将Fe(OH) 氧化为Fe(OH) ,最终可以转化铁氧体中的Fe3+。
2 3
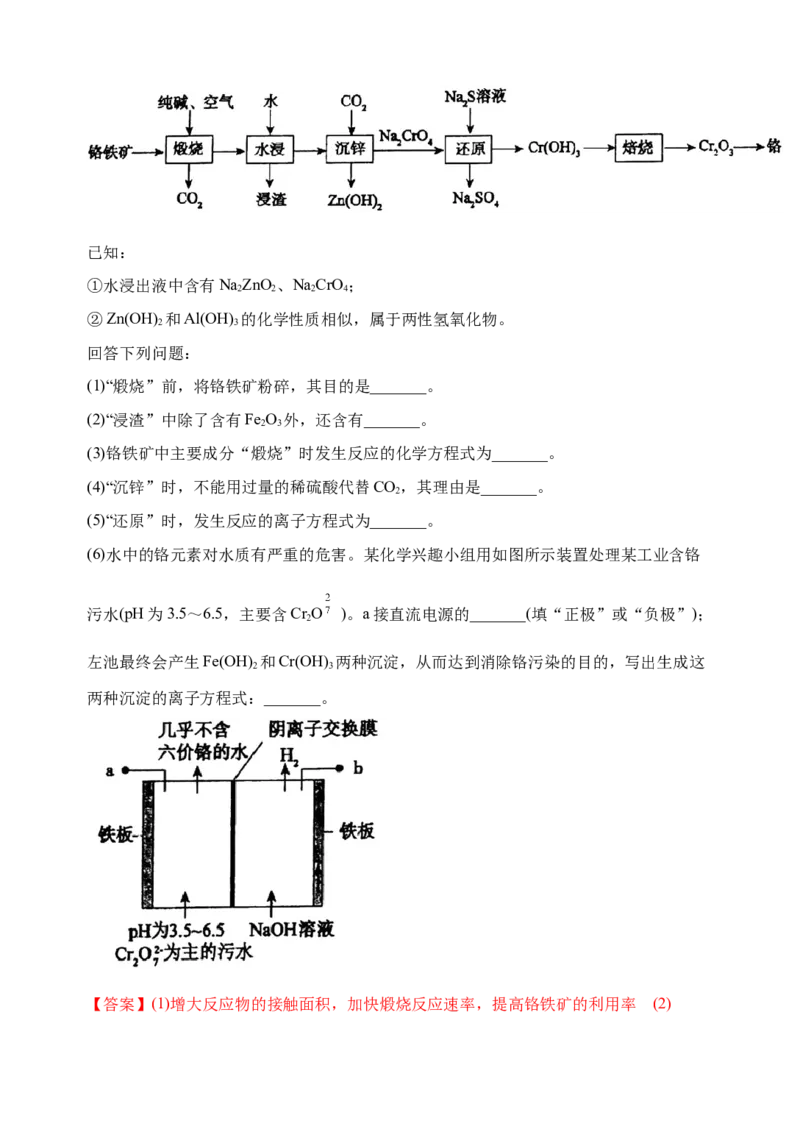
6.(2021届池州高三大联考)铬及其化合物在现代工业上的应用广泛。工业上以铬铁矿(主
要成分为FeO·Cr O,还含有少量的ZnO、CuO等)为原料制备金属铬的工艺流程如下:
2 3已知:
①水浸出液中含有NaZnO、NaCrO;
2 2 2 4
②Zn(OH) 和Al(OH) 的化学性质相似,属于两性氢氧化物。
2 3
回答下列问题:
(1)“煅烧”前,将铬铁矿粉碎,其目的是_______。
(2)“浸渣”中除了含有Fe O 外,还含有_______。
2 3
(3)铬铁矿中主要成分“煅烧”时发生反应的化学方程式为_______。
(4)“沉锌”时,不能用过量的稀硫酸代替CO,其理由是_______。
2
(5)“还原”时,发生反应的离子方程式为_______。
(6)水中的铬元素对水质有严重的危害。某化学兴趣小组用如图所示装置处理某工业含铬
污水(pH为3.5~6.5,主要含Cr O )。a接直流电源的_______(填“正极”或“负极”);
2
左池最终会产生Fe(OH) 和Cr(OH) 两种沉淀,从而达到消除铬污染的目的,写出生成这
2 3
两种沉淀的离子方程式:_______。
【答案】(1)增大反应物的接触面积,加快煅烧反应速率,提高铬铁矿的利用率 (2)CuO(3) (4) 若用稀硫酸,会
将生成的Zn(OH) 沉淀溶解,而无法达到除锌的目的 (5)
2
(6) 正极
【解析】
(1)“煅烧”前,将铬铁矿粉碎,其目的是增大反应物的接触面积,加快煅烧反应速率,提
高铬铁矿的利用率;
(2)在“煅烧”中加入了空气,其中的O 可以把FeO转化为Fe O,水浸出液中含有
2 2 3
NaZnO、NaCrO,所以浸渣中含有Fe O 和CuO;
2 2 2 4 2 3
(3) 在“煅烧”中加入了空气,其中的O 可以把FeO转化为Fe O,水浸出液中含有
2 2 3
NaCrO,此时Cr元素为+6价,是由Cr O 被O 氧化得来,同时释放出了CO,根据得失
2 4 2 3 2 2
电子守恒、元素守恒,化学反应为:
;
(4) Zn(OH) 和Al(OH) 的化学性质相似,属于两性氢氧化物,所以Zn(OH) 能与强酸反应,
2 3 2
故不能用稀硫酸代替CO;
2
(5)根据“还原”是的反应物和产物知离子方程式为:
;
(6)隔膜右边放出H,右边铁板应为电解池的阴极,则左边铁板是电解池的阳极,故a接
2
直流电源的正极;
阳极反应产生的Fe2+,可将 还原为Cr3+,自身被氧化为Fe3+,阴极产生的OH-会将Cr3+、Fe3+转化为沉淀,离子方程式为
【三氧化二铬】亦称氧化铬。化学式Cr2O3,式量151.99。绿色六方晶体或无定形粉末。
密度5.21克/厘米3,熔点2266±25℃,沸点4000℃。不溶于水,不溶于碱溶液,略溶于
酸。具有磁性。用作分析试剂、催化剂、陶瓷釉彩原料、油漆颜料、制备铬合金和铬盐。
实验室由重铬酸铵(NH4)2Cr2O7受热分解制得
【三氧化铬】亦称铬酸酐。化学式CrO3,式量99.99。红色正交晶体,常呈针状或柱状结
晶。密度2.7克/厘米3,熔点196℃。易潮解,易溶于水,水溶液是铬酸。溶于醇、硝酸
或硫酸。有强氧化性。有毒、有腐蚀性。用作分析试剂、强氧化剂,还用于镀铬、制铬
酸盐、玻璃着色。由重铬酸钠与浓硫酸共热制得。
【铬酐】铬酸酐的简称,见三氧化铬条。
【氯化铬】别名三氯化铬。化学式CrCl3,式量158.38。无水氯化铬为强烈发光的紫色六
角晶系的片状结晶。密度2.9克/厘米3,熔点1150℃。几乎不溶于水,与水长时间沸腾可
形成绿色溶液。在空气中灼烧可变为三氧化三铬。六水合氯化铬CrCl3·6H2O有三种变体,
分别呈深绿色、浅绿色和紫色。水合物易潮解,易溶于水。用作媒染剂、催化剂、无机
合成。将三氧化二铬溶解在浓盐酸中,结晶可制得六水合氯化铬。