文档内容
微专题突破15 化学计算考点透视
没有人事先了解自己到底有多大的力量,直到他试过以后才知道。——歌德
目标定位
1.能用水解常数和溶度积进行计算。
2.能运用关系式法和守恒法计算物质的化学式。
教学重点难点
1.物质化学式计算。
2.滴定计算。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.基本要领
①抓住关键字;②注意各量的单位;③弄清题目中隐含的条件,如一定量浓H SO 、浓HNO 参加
2 4 3
清晰 反应的先浓后稀问题,一种氧化剂(或还原剂)和几种还原剂(或氧化剂)反应的先强后弱等问
审题 题;④看清量的变化问题,如某混合液稀释到250 mL,再另取25 mL进行实验;⑤判断反应是否
完全问题,如有机物是完全燃烧还是不完全燃烧等;⑥有关图象中信息的挖掘。
①解题不规范,不带单位运算或单位使用不太合理,没有注意题中有效数字的要求(如保留二位小
数)而造成错解。
②方程式书写不正确或未配平,列比例式时同一物质的关系量(已知、未知)单位不统一而造成错
易错
误。
现象
③反应式所表示的是纯物质的相关量,未将不纯物质或溶液换算为纯物质的量代入计算而导致错
误。
④多步反应,没有注意各步反应中相关物质的化学计量数,建立了错误的关系式进行计算。
关系式法——多步变化用物质的量的关系首尾列式计算。建立关系式的方法主要有:
一个
①利用微粒守恒关系建立关系式;②利用方程式中的化学计量数间的关系建立关系式;③利用
方法
方程式的加合建立关系式。
①质量守恒法——适用于化学反应、溶解度计算、稀释过程 。
②电荷守恒法——适用于电解质溶液中有关离子浓度等式关系的判断,离子的鉴定、物质的量(浓度)、物质的化学式计算
四个
等。
守恒
③电子守恒法——适用于氧化还原反应、电极反应。
④物料守恒法——适用于反应过程中、电解质溶液中某元素的原子或离子守恒。
二 原料利用率=×100% 产物产率=×100%
个 ①反应物中某元素的利用率或损耗率=该反应物的利用率或损耗率
率 ②工业生产中间过程中各步的转化率、产率可累积到原料上,计算结果不受影响
2.平衡常数:
①类型:电离常数、水解常数和溶度积常数及新反应平衡常数的求算;②表达式中必须用物质的量浓度而
不用物质的量,对于水看情况是否写入表达式,水溶液中水不写入表达式,酯化反应中则要写入,不为气体必
须写入;③会用Q 判断反应的方向。
c
3.滴定计算:
①实验需进行三次,如题目只是进行了一次实验,则还要重复有关操作再进行2次。
②若所给的三组实验数据中有一组的数据误差较大,必须要舍去,再取平均值计算。
4.审题方法的关键
(1)“一次性审题”。所谓“一次性审题”就是一次性完成审题,而不是反复多次;审题时要“边读题边
画图”;审题时要用线条、箭头、符号、数据等展示题意。画图就是标注出实验的主要过程和实验数据的测定。微专题突破15 化学计算考点透视 问题的态度:问则少;辩则明
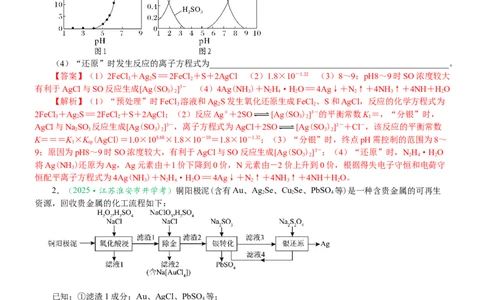
(2)只要根据审题时所画出的图,能用自己的语言准确叙述出题意,审题就是清晰的。
考考位位位
1.(2024·江苏卷)贵金属银应用广泛。Ag与稀HNO 制得AgNO,常用于循环处理高氯废水。
3 3
(1)沉淀Cl-。在高氯水样中加入KCrO 使CrO2-浓度约为5×10-3 mol·L-1,当滴加AgNO 溶液至开
2 4 4 3
始产生Ag CrO 沉淀(忽略滴加过程的体积增加),此时溶液中Cl-浓度约为_______________ mol·L-1。[已知:
2 4
K (AgCl)=1.8×10-10,K (Ag CrO)=2.0×10-12]
sp sp 2 4
【答案】(1)9×10-6
【解析】(1)CrO2-浓度约为5×10-3 mol·L-1,当滴加AgNO 溶液至开始产生Ag CrO 沉淀,此时
4 3 2 4
c(Ag+)== mol·L-1=2×10-5 mol·L-1,c(Cl-)== mol·L-1=9×10-6 mol·L-1。
2.(2024·江苏卷)净化后的NdCl 溶液通过沉钕、焙烧得到Nd O。
3 2 3
的
①向NdCl 溶液中加入(NH )CO 溶液,Nd3+可转化为Nd(OH)CO 沉淀。该反应 离子方程式为
3 4 2 3 3
________________________________________________________________________________。
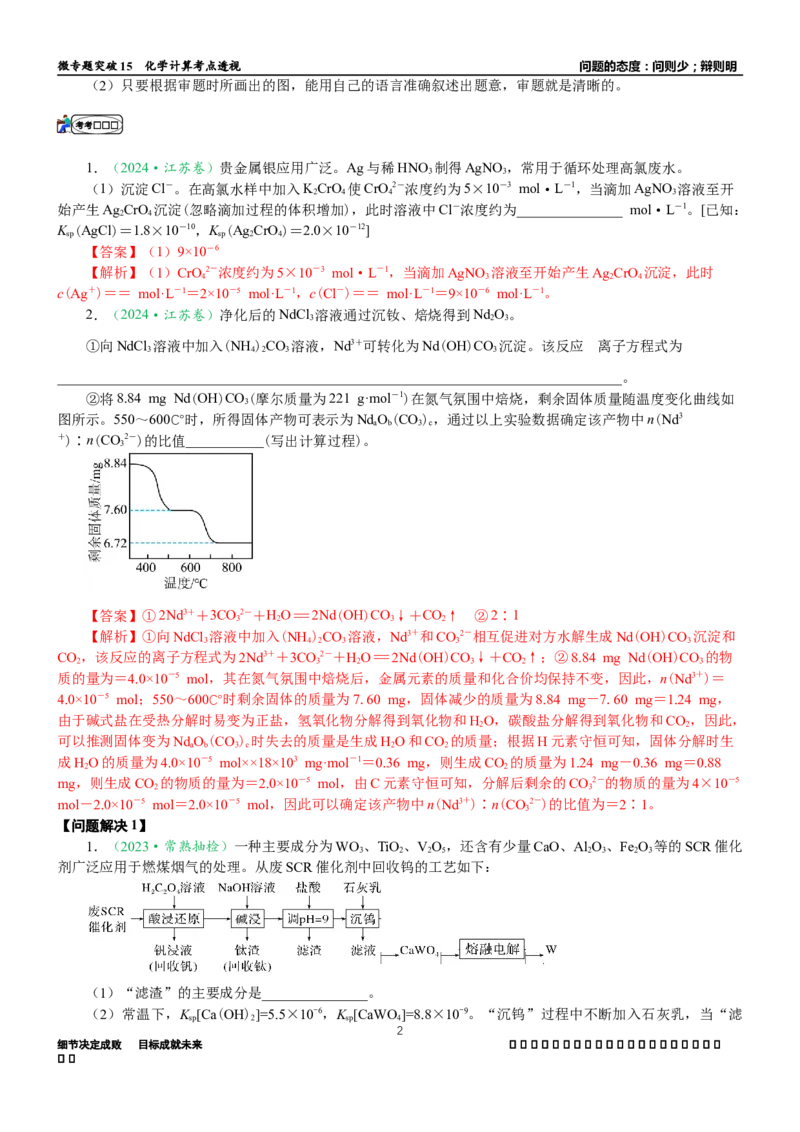
②将8.84 mg Nd(OH)CO(摩尔质量为221 g·mol-1)在氮气氛围中焙烧,剩余固体质量随温度变化曲线如
3
图所示。550~600℃时,所得固体产物可表示为NdO(CO),通过以上实验数据确定该产物中n(Nd3
a b 3 c
+)∶n(CO2-)的比值___________(写出计算过程)。
3
【答案】①2Nd3++3CO2-+HO=2Nd(OH)CO↓+CO↑ ②2∶1
3 2 3 2
【解析】①向NdCl 溶液中加入(NH )CO 溶液,Nd3+和CO2-相互促进对方水解生成Nd(OH)CO 沉淀和
3 4 2 3 3 3
CO,该反应的离子方程式为2Nd3++3CO2-+HO=2Nd(OH)CO↓+CO↑;②8.84 mg Nd(OH)CO 的物
2 3 2 3 2 3
质的量为=4.0×10-5 mol,其在氮气氛围中焙烧后,金属元素的质量和化合价均保持不变,因此,n(Nd3+)=
4.0×10-5 mol;550~600℃时剩余固体的质量为7.60 mg,固体减少的质量为8.84 mg-7.60 mg=1.24 mg,
由于碱式盐在受热分解时易变为正盐,氢氧化物分解得到氧化物和HO,碳酸盐分解得到氧化物和CO,因此,
2 2
可以推测固体变为NdO(CO) 时失去的质量是生成HO和CO 的质量;根据H元素守恒可知,固体分解时生
a b 3 c 2 2
成HO的质量为4.0×10-5 mol××18×103 mg·mol-1=0.36 mg,则生成CO 的质量为1.24 mg-0.36 mg=0.88
2 2
mg,则生成CO 的物质的量为=2.0×10-5 mol,由C元素守恒可知,分解后剩余的CO2-的物质的量为4×10-5
2 3
mol-2.0×10-5 mol=2.0×10-5 mol,因此可以确定该产物中n(Nd3+)∶n(CO2-)的比值为=2∶1。
3
【问题解决1】
1.(2023·常熟抽检)一种主要成分为WO、TiO、VO,还含有少量CaO、Al O、Fe O 等的SCR催化
3 2 2 5 2 3 2 3
剂广泛应用于燃煤烟气的处理。从废SCR催化剂中回收钨的工艺如下:
(1)“滤渣”的主要成分是_______________。
(2)常温下,K [Ca(OH)]=5.5×10-6,K [CaWO ]=8.8×10-9。“沉钨”过程中不断加入石灰乳,当“滤
sp 2 sp 4
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找液”的pH=13时,c(WO2-)=__________mol·L-1。
4
【答案】(1)Al(OH) (2)1.6×10-5
3
【解析】(1)调pH时加入盐酸,NaAlO 转化为Al(OH),“滤渣”的主要成分是Al(OH) ;(2)当“滤
2 3 3
液”的pH=13时,c(Ca2+)== mol·L-1=5.5×10-4 mol·L-1,c(WO2-)== mol·L-1=1.6×10-5 mol·L-1。
4
2.(2023·盐城三模)燃煤烟气脱硫的一种方法如图所示。室温下以150 mL 0.2 mol·L-1 氨水吸收SO,
2
若通入SO 所引起的溶液体积变化和NH 、HO挥发可忽略,溶液中含硫物种的浓度c =c(HSO )+c(HSO)
2 3 2 总 2 3
+c(SO)。HSO 的电离平衡常数分别为:K =1.3×10-2,K =6.3×10-7;NH ·HO的电离平衡常数为K =
2 3 a1 a2 3 2 b
1.8×10-5。下列说法正确的是
A.NH ·HO吸收SO 所得到的溶液中:c(NH)>2c(SO)
3 2 2
B.NH ·HO吸收SO ,c =0.1 mol·L-1 溶液:c(OH-)=c(H+)+c(HSO)+2c(HSO )
3 2 2 总 2 3
C.NH ·HO吸收标况下0.448 L SO,所得溶液中:3c(NH)+3c(NH ·HO)=2c(HSO )+2c(HSO)+
3 2 2 3 2 2 3
2c(SO)
D.题图所示“吸收”“氧化”后的溶液pH增大
【答案】A
【解析】A项,“吸收”过程中,NH ·HO和SO 反应生成(NH )SO ,若NH和SO都不发生水解,则
3 2 2 4 2 3
c(NH)=2c(SO),但NH和SO都发生水解,K (NH)==<K (SO)==,则SO的水解程度大于NH,溶液中:
h h
c(NH)>2c(SO),正确;B项,NH ·HO吸收SO 反应生成(NH )SO ,c =c(HSO )+c(HSO)+c(SO)=
3 2 2 4 2 3 总 2 3
0.1 mol·L-1,则c(NH)+c(NH ·HO)=2c =0.2 mol·L-1,再结合电荷守恒:c(HSO)+2c(SO)+c(OH-)=
3 2 总
c(NH)+c(H+),可得c(OH-)=c(NH)+c(H+)-c(HSO)-2c(SO)=0.2 mol·L-1-c(NH ·HO)+c(H+)-
3 2
c(HSO)-2c(SO)=2c(HSO )+2c(HSO)+2c(SO)-c(NH ·HO)+c(H+)-c(HSO)-2c(SO)=c(H+)+
2 3 3 2
c(HSO)+2c(HSO )-c(NH ·HO),错误;C项,标况下0.448 L SO 的物质的量为=0.02 mol,150 mL 0.2
2 3 3 2 2
mol·L-1 氨水中n(NH ·HO)=0.15 L×0.2 mol·L-1=0.03 mol,得到元素质量守恒:2(NH)+2c(NH ·HO)
3 2 3 2
=3c =3c(HSO )+3c(HSO)+3c(SO),错误;D项,由图可知,“吸收”“氧化”后溶质由NH ·HO转化
总 2 3 3 2
为(NH )SO ,故溶液的pH减小,错误。
4 2 4
平衡常数的计算
1.K表达式书写:固体不写入,注意化学计量数的写入。方程式书写方式不同,其K表达式也不同!
2.K (或K )与K 、K 的关系
a b w h
一元弱酸或弱碱的K 或K 与弱酸根或弱碱离子的K 关系 K=或K =
a b h a b
二元弱酸的K 、K 与相应酸根的水解常数K 、K 的关系 K =,K =
a1 a2 h1 h2 a1 a2
3.K 的计算
sp
①pH控制的范围:杂质离子完全沉淀时pH值~主要离子开始沉淀时pH
计算pH范围 ②一般情况下,当溶液中离子浓度小于1×10-5 mol·L-1时,通常认为沉
淀反应进行完全
如对于反应Cu2+(aq)+ZnS(s) CuS(s)+Zn2+(aq),该反应的平衡常数
计算沉淀转化反应的平衡常数
K===
计算某些反应的平衡常数 如反应CdS(s)+2H+(aq) Cd2+(aq)+HS(aq)的平衡常数为K,则K=
2
考点精练
1.(2023·南通市海门市模拟)从分金渣(主要成分为AgCl、Ag S、PbSO 、BaSO)中获取高纯银的流程如
2 4 4
图所示:微专题突破15 化学计算考点透视 问题的态度:问则少;辩则明
已知:在上述反应的温度下K (AgCl)=1.8×10-10,K (Ag S)=6.38×10-50。
sp sp 2
(1)“预处理”加入FeCl 溶液将Ag S转化为AgCl,反应的化学方程式为
3 2
_______________________________________________________________。
(2)已知:Ag++2SO [Ag(SO )]3-,K=1.0×108.68,“分银”时,AgCl与NaSO 反应生成
3 2 2 3
[Ag(SO )]3-,该反应的平衡常数K=________________。
3 2
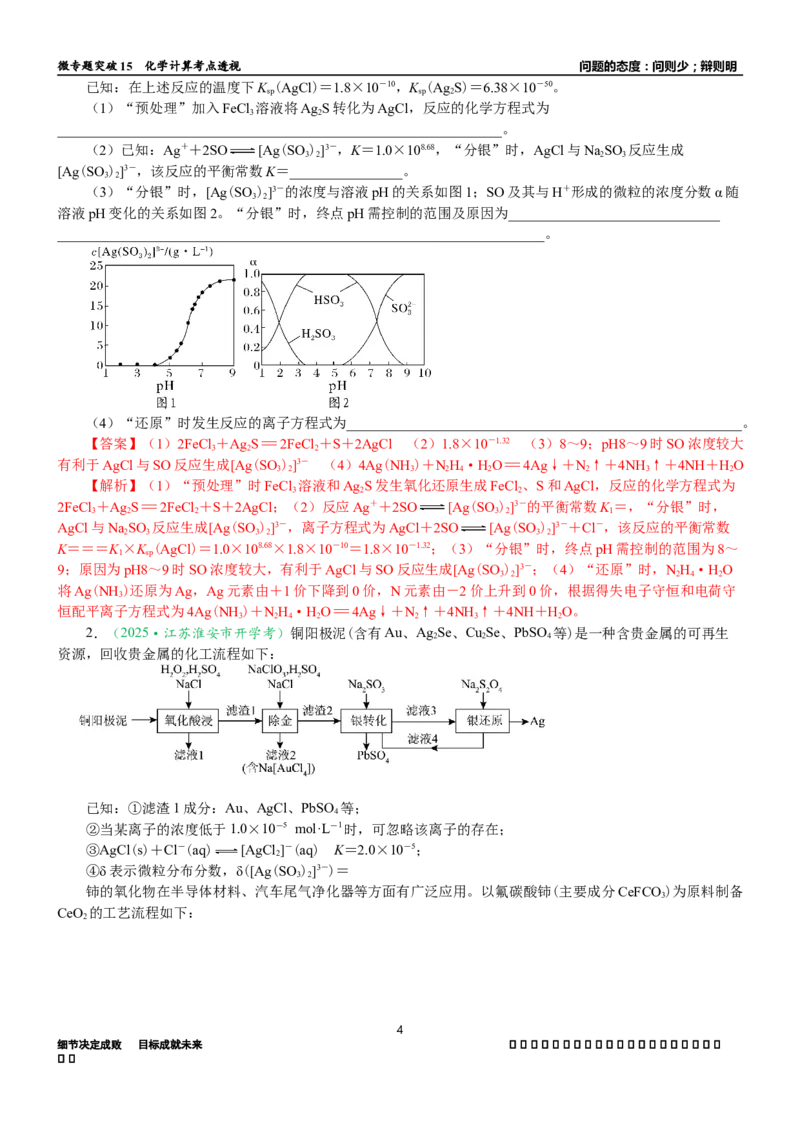
(3)“分银”时,[Ag(SO )]3-的浓度与溶液pH的关系如图1;SO及其与H+形成的微粒的浓度分数α随
3 2
溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为______________________________
_____________________________________________________________________。
(4)“还原”时发生反应的离子方程式为________________________________________________________。
【答案】(1)2FeCl +Ag S=2FeCl +S+2AgCl (2)1.8×10-1.32 (3)8~9;pH8~9时SO浓度较大
3 2 2
有利于AgCl与SO反应生成[Ag(SO )]3- (4)4Ag(NH )+NH·HO=4Ag↓+N↑+4NH ↑+4NH+HO
3 2 3 2 4 2 2 3 2
【解析】(1)“预处理”时FeCl 溶液和Ag S发生氧化还原生成FeCl 、S和AgCl,反应的化学方程式为
3 2 2
2FeCl +Ag S=2FeCl +S+2AgCl;(2)反应Ag++2SO [Ag(SO )]3-的平衡常数K =,“分银”时,
3 2 2 3 2 1
AgCl与NaSO 反应生成[Ag(SO )]3-,离子方程式为AgCl+2SO [Ag(SO )]3-+Cl-,该反应的平衡常数
2 3 3 2 3 2
K===K ×K (AgCl)=1.0×108.68×1.8×10-10=1.8×10-1.32;(3)“分银”时,终点pH需控制的范围为8~
1 sp
9;原因为pH8~9时SO浓度较大,有利于AgCl与SO反应生成[Ag(SO )]3-;(4)“还原”时,NH·HO
3 2 2 4 2
将Ag(NH )还原为Ag,Ag元素由+1价下降到0价,N元素由-2价上升到0价,根据得失电子守恒和电荷守
3
恒配平离子方程式为4Ag(NH )+NH·HO=4Ag↓+N↑+4NH ↑+4NH+HO。
3 2 4 2 2 3 2
2.(2025·江苏淮安市开学考)铜阳极泥(含有Au、Ag Se、Cu Se、PbSO 等)是一种含贵金属的可再生
2 2 4
资源,回收贵金属的化工流程如下:
已知:①滤渣1成分:Au、AgCl、PbSO 等;
4
②当某离子的浓度低于1.0×10-5 mol·L-1时,可忽略该离子的存在;
③AgCl(s)+Cl-(aq) [AgCl ]-(aq) K=2.0×10-5;
2
④δ表示微粒分布分数,δ([Ag(SO )]3-)=
3 2
铈的氧化物在半导体材料、汽车尾气净化器等方面有广泛应用。以氟碳酸铈(主要成分CeFCO)为原料制备
3
CeO 的工艺流程如下:
2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找已知:①CeO 具有较强的氧化性,难溶于一般的酸或碱。
2
②F-能与Ce4+、Al3+结合成稳定的CeF3+、AlF,这有利于酸浸步骤,不利于后续的沉淀步骤。
③溶液中铈的常见离子有Ce4+、Ce3+,其中Ce4+能被萃取剂TBP萃取,而Ce3+不能被萃取。
若“沉铈”后,溶液的pH为6,c(HCO)=0.2 mol·L-1,此时c(Ce3+)=________mol·L-1。已知常温下:
HCO Ce (CO)
2 3 2 3 3
K =4.0×10-7 K =5.0×10-11 K =1.0×10-28
a1 a2 sp
【答案】1×10-6.5
【解析】溶液的pH为6,则c(H+)=10-6 mol·L-1,当c(HCO)=0.2 mol·L-1,根据K (HCO)=,计算
a2 2 3
得到c(CO)===1×10-5 mol·L-1,根据K [Ce (CO)]=c2(Ce3+)·c3(CO)=1.0×10-28,计算得到c(Ce3+)=
sp 2 3 3
1×10-6.5 mol·L-1。
【问题解决2】
(2023·南京模拟节选)(NH )MoS 可通过如下两种方法制取MoS (钼相对原子质量为96):
4 2 4 2
方法一:将(NH )MoS 在一定条件下加热,可分解得到MoS 、NH 、HS和硫单质。其中NH 、HS和硫
4 2 4 2 3 2 3 2
单质的物质的量之比为8∶4∶1。
方法二:将(NH )MoS 在空气中加热可得MoS ,加热时所得剩余固体的质量与原始固体质量的比值与温
4 2 4 2
度的关系如图2所示。
①方法一中,所得硫单质的分子式为________。
②方法二中,500 ℃可得到Mo的一种氧化物,该氧化物的化学式为____________。
【答案】①S ②MoO
4 3
【解析】①将(NH )MoS 在一定条件下加热,可分解得到MoS 、NH 、HS和硫单质。其中NH 、HS和
4 2 4 2 3 2 3 2
硫单质(S)的物质的量之比为8∶4∶1,根据已知信息写出方程式并按照 N原子和Mo原子守恒配平方程式为
x
4(NH )MoS ====4MoS +8NH ↑+4HS↑+S,即4×4=2×4+4×1+x计算得x=4。该硫单质的化学式为
4 2 4 2 3 2 x
S ;②由图可知起始(NH )MoS 的质量可视为260 g即1 mol,根据加热分解过程总Mo元素守恒可知,最终氧
4 4 2 4
化物中Mo的质量为96 g,氧化物中氧元素的质量为144 g-96 g=48 g,Mo原子和O原子的个数比为1∶3,氧
化物的化学式为MoO 。
3
化学式的确定
1.局部确定法
即确定其中各个离子的物质,然后进行组合。微专题突破15 化学计算考点透视 问题的态度:问则少;辩则明
方法:通过反应一一确定离子及其量,最后计算结晶水的量。有些离子,如CO32-、HCO -、NH +常通过
3 4
转化为气体,由题中气体的量求其物质的量;有些离子,如SO 2-、Ba2+、Ca2+则通过生成沉淀,根据沉淀的质
4
量求其物质的量;有的离子如Fe2+、C O2—等则通过氧化还原反应滴定,测定其物质的量。
2 4
2.热重分析法
(1)热重分析法是指在控制温度和一定气氛条件下,测量物质的质量与温度或时间关系的一种热分析方法,
解答热重分析试题的常用方法为:
①设晶体为1 mol。
②失重一般是先失水,再失非金属氧化物。
③计算每步的m(剩余),×100%=固体残留率。
④晶体中金属质量不减少,仍在m(剩余)中。
⑤失重最后一般为金属氧化物,由质量守恒得m(O),由n(金属)∶n(O),即可求出失重后物质的化学式。
(2)三步突破热重分析题
分析失重图像,横坐标一般是分解的温度,纵坐标一般为剩余固体的质量或固
分析图像,明确坐标含义
体残留率
含结晶水的盐加热失重时一般先失去部分或全部结晶水,再失去非金属氧化
依据性质,猜测各段反应 物,失重最后一般为金属氧化物或金属,晶体中金属质量不减少,仍在残留固
体中
根据纵坐标的数据变化或题目给定的数据,根据金属原子守恒,即可求出失重
整合数据,验证猜测结果
后物质的化学式,或者判断出发生的化学反应
考点精练
1.(2025·江苏省镇江市开学考)VO 是接触法制硫酸的催化剂,使用后的废钒催化剂可回收利用。
2 5
一种处理废钒催化剂的流程如下:
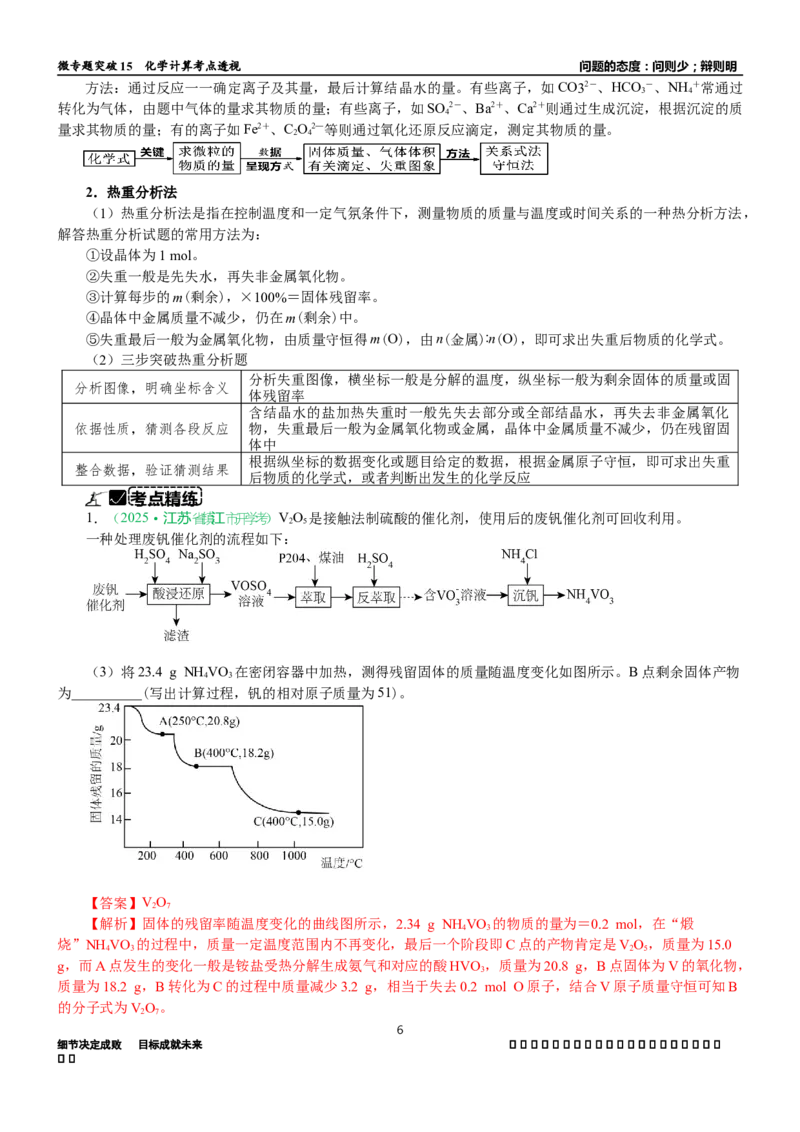
(3)将23.4 g NH VO 在密闭容器中加热,测得残留固体的质量随温度变化如图所示。B点剩余固体产物
4 3
为__________(写出计算过程,钒的相对原子质量为51)。
【答案】VO
2 7
【解析】固体的残留率随温度变化的曲线图所示,2.34 g NH VO 的物质的量为=0.2 mol,在“煅
4 3
烧”NH VO 的过程中,质量一定温度范围内不再变化,最后一个阶段即C点的产物肯定是VO,质量为15.0
4 3 2 5
g,而A点发生的变化一般是铵盐受热分解生成氨气和对应的酸HVO,质量为20.8 g,B点固体为V的氧化物,
3
质量为18.2 g,B转化为C的过程中质量减少3.2 g,相当于失去0.2 mol O原子,结合V原子质量守恒可知B
的分子式为VO。
2 7
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找2.(2022·江苏卷节选)FeS 、FeS在空气中易被氧化,将FeS 在空气中氧化,测得氧化过程中剩余固体
2 2
的质量与起始FeS 的质量的比值随温度变化的曲线如图所示。800℃时,FeS 氧化成含有两种元素的固体产物
2 2
为__________(填化学式)。
【答案】Fe O
2 3
【解析】由图可知,800 ℃时,氧化过程中剩余固体的质量与起始FeS 的质量的比值为66.7%,FeS 的摩
2 2
尔质量 120 g·mol-1,设 FeS 氧化成含有两种元素的固体产物化学式为 FeO ,则 M(FeO)=120 g·mol-
2 x x
1×66.7%≈80 g·mol-1,则56+16x=80,x=,即固体产物为Fe O。
2 3
【问题解决3】
(2023·扬州三模节选)测定软锰矿中MnO 含量的方法如下:
2
步骤一:称取0.150 0 g软锰矿样品于碘量瓶中,加适量硫酸及足量碘化钾溶液充分反应。
步骤二:待反应完全后加入少量淀粉溶液,用0.100 0 mol·L-1 Na SO 溶液滴定至终点,消耗NaSO 溶
2 2 3 2 2 3
液22.00 mL。
已知:MnO +4H++2I-=Mn2++I+2HO I+SO→I-+SO(未配平)
2 2 2 2 2 4
软锰矿中MnO 的质量分数为____________,写出计算过程。
2
【答案】依据方程式MnO +4H++2I-=Mn2++I +2HO与I +2SO=2I-+SO,可得关系式MnO ~I
2 2 2 2 2 4 2 2
~2SO,n(MnO )=0.1×22×10-3× mol=1.1×10-3 mol,软锰矿中MnO 的质量分数为×100%=63.80%。
2 2 2
【解析】已知二氧化锰与KI的反应为MnO +4H++2I-=Mn2++I +2HO,且NaSO 与I 的反应为I +
2 2 2 2 2 3 2 2
2SO=2I-+SO,由关系式可知MnO ~I ~2SO,n(MnO )=0.1×22×10-3× mol=1.1×10-3 mol,故软锰
2 4 2 2 2 2
矿中MnO 的质量分数为×100%=63.80%。
2
滴定法的计算
1.滴定类型与方法
滴定类型 ①酸碱中和滴定;②氧化还原滴定;③配合滴定;④沉淀滴定
直接滴定法 如NaOH滴定盐酸
连续滴定法 如用盐酸滴定NaCO、NaHCO 的混合溶液,先加酚酞滴定后加甲基橙再继续滴定
2 3 3
该法用于滴定剂和被测组分的反应较慢或被测物是固体的滴定分析,如:测定固
返滴定法 体CaCO ,先加入过量的标准盐酸溶液,待反应完全后,用标准 NaOH溶液滴定
3
剩余的HCl,则加入盐酸的总量与剩余量之差就是与碳酸钙反应的量
该法用于滴定剂和被测物之间不呈化学计量关系或伴有副反应的滴定分析,如:
不能用硫代硫酸钠标准溶液直接滴定重铬酸钾等强氧化剂,因为在酸性溶液中,
滴定方法
置换滴定法 这些强氧化剂会将SO2-氧化为SO2-及SO 2-等混合物,它们之间没有一定的
2 3 4 6 4
化学计量关系,但在酸性溶液中让KCr O 与过量的KI反应,定量析出I 来,就
2 2 7 2
可用硫代硫酸钠标准溶液滴定I,而计算重铬酸钾的含量
2
该法用于滴定剂和被测物不能直接反应的滴定分析,如:Ca2+没有可变价态,不
能直接用氧化还原法滴定,但若将Ca2+沉淀为CaC O ,过滤,洗净后溶解于硫
间接滴定法 2 4
酸中,再用KMnO 标准溶液滴定与Ca2+结合的C O2-,从而间接测定Ca2+的含
4 2 4
量
解决这类问题,首先要理解反应的原理,找出物质之间的反应关系,其次还需要细心进行数据的处理,统
一单位进行计算,此外还要注意样品和实验所用质量或体积的差异。
2.碘量法微专题突破15 化学计算考点透视 问题的态度:问则少;辩则明
概念 直接碘量法是用碘滴定液直接滴定还原性物质的方法。在滴定过程中,I 被还原为I-
2
淀粉:淀粉遇碘显蓝色,反应极为灵敏。化学计量点稍后,溶液中有过量的碘,碘与
直接
指示剂 淀粉结合显蓝色而指示终点到达。碘自身的颜色指示终点,化学计量点后,溶液中稍
碘量法
过量的碘显黄色而指示终点
适用对象 I 是较弱的氧化剂,强还原性的S2-、SO、SO、As O、Vc等都可直接滴定
2 2 2 3
剩余碘量法是在供试品(还原性物质)溶液中先加入定量、过量的碘滴定
剩余 液,待I 与测定组分反应完全后,然后用硫代硫酸钠滴定液滴定剩余的
2
碘量法 碘,以求出待测组分含量的方法。滴定反应为I(定量过量)+还原性物
2
质―→2I-+氧化产物,I(剩余)+2SO―→SO+2I-
分类 2 2 4
置换碘量法是先在供试品(氧化性物质)溶液中加入碘化钾,供试品将碘化
间接 置换 钾氧化析出定量的碘,碘再用硫代硫酸钠滴定液滴定,从而可求出待测组
碘量法 碘量法 分含量。滴定反应为氧化性物质+2I-―→I +还原产物,I +
2 2
2SO―→SO+2I-
2 4
淀粉指示剂应在近终点时加入,因为当溶液中有大量碘存在时,碘易吸附在淀粉表
指示剂
面,影响终点的正确判断
I-是中等强度的还原剂。主要用来测氧化态物质:CrO、Cr O、HO 、KMnO 、IO、
适用对象 2 2 2 4
Cu2+、NO、NO等
考点精练
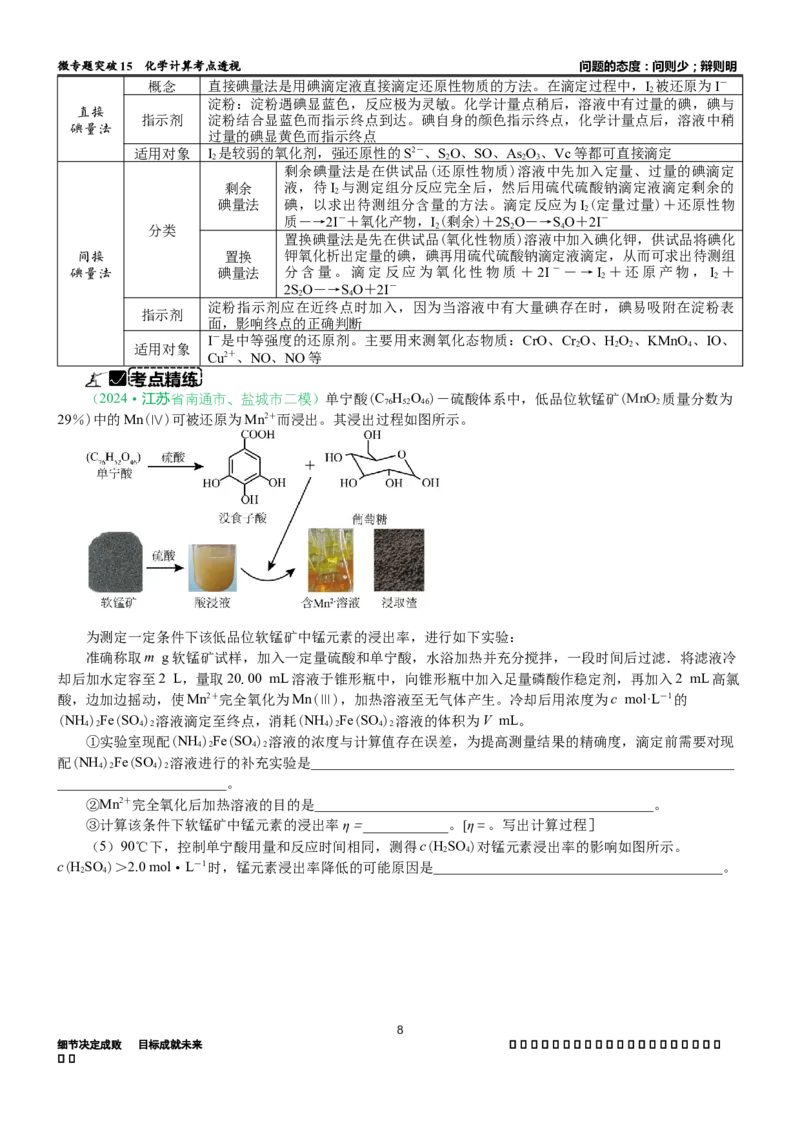
(2024·江苏省南通市、盐城市二模)单宁酸(C H O )-硫酸体系中,低品位软锰矿(MnO 质量分数为
76 52 46 2
29%)中的Mn(Ⅳ)可被还原为Mn2+而浸出。其浸出过程如图所示。
为测定一定条件下该低品位软锰矿中锰元素的浸出率,进行如下实验:
准确称取m g软锰矿试样,加入一定量硫酸和单宁酸,水浴加热并充分搅拌,一段时间后过滤.将滤液冷
却后加水定容至2 L,量取20.00 mL溶液于锥形瓶中,向锥形瓶中加入足量磷酸作稳定剂,再加入2 mL高氯
酸,边加边摇动,使Mn2+完全氧化为Mn(Ⅲ),加热溶液至无气体产生。冷却后用浓度为c mol·L-1的
(NH )Fe(SO ) 溶液滴定至终点,消耗(NH )Fe(SO ) 溶液的体积为V mL。
4 2 4 2 4 2 4 2
①实验室现配(NH )Fe(SO ) 溶液的浓度与计算值存在误差,为提高测量结果的精确度,滴定前需要对现
4 2 4 2
配(NH )Fe(SO ) 溶液进行的补充实验是____________________________________________________________
4 2 4 2
________________________。
②Mn2+完全氧化后加热溶液的目的是________________________________________________。
③计算该条件下软锰矿中锰元素的浸出率η=____________。[η=。写出计算过程]
(5)90℃下,控制单宁酸用量和反应时间相同,测得c(HSO )对锰元素浸出率的影响如图所示。
2 4
c(HSO )>2.0 mol·L-1时,锰元素浸出率降低的可能原因是_________________________________________。
2 4
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】(4)①使用KCr O 基准试剂对(NH )Fe(SO ) 溶液的实际浓度进行标定 ②除去过量高氯酸,
2 2 7 4 2 4 2
防止其氧化硫酸亚铁铵 ③每20.00 mL浸出滤液中:n(Mn2+)=n[(NH )Fe(SO )]=c mol·L-1×V ml×10-3
4 2 4 2
mL·L-1=cV×10-3 mol;m g软锰矿浸出滤液中n(Mn2+)=cV×10-3 mol×=0.1cV mol,浸出的n(MnO )=
2
n(Mn2+)=0.1cV mol,m(MnO )=n(Mn2+)×87 g·mol-1=8.7cV g,m g软锰矿中m(MnO )=m g×29%=
2 2
0.29m g,锰元素浸出率[η=== (5)c(H+)浓度过大,抑制了单宁酸的水解,没食子酸和葡萄糖的浓度降低,
MnO 的还原速率减慢
2
【解析】①为提高测量结果的精确度,滴定前需要使用KCr O 基准试剂对(NH )Fe(SO ) 溶液的实际浓度
2 2 7 4 2 4 2
进行标定;②实验原理是根据Mn(Ⅲ)消耗(NH )Fe(SO ) 的物质的量计算锰元素的物质的量,需要排除其它氧
4 2 4 2
化剂氧化(NH )Fe(SO ),所以Mn2+完全氧化后加热溶液的目的是除去过量高氯酸,防止其氧化硫酸亚铁铵;
4 2 4 2
③每20.00 mL浸出滤液中:n(Mn2+)=n[(NH )Fe(SO )]=c mol·L-1×V ml×10-3 mL·L-1=cV×10-3 mol;m
4 2 4 2
g软锰矿浸出滤液中n(Mn2+)=cV×10-3 mol×=0.1cV mol浸出的n(MnO )=n(Mn2+)=0.1cV mol,m(MnO )
2 2
=n(Mn2+)×87 g·mol-1=8.7cV g,m g软锰矿中m(MnO )=m g×29%=0.29m g,锰元素浸出率[η===;
2
(5)由图可知,c(H+)浓度过大,抑制了单宁酸的水解,没食子酸和葡萄糖的浓度降低,MnO 的还原速率减
2
慢,所以c(HSO )>2.0 mol·L-1时,锰元素浸出率降低。
2 4
成功体验
1.((2024·南京、盐城期末)实验室以菱锰矿(含MnCO 及少量Fe、Si的氧化物等)为原料制备高纯
3
MnCO 和MnO 的流程如下图所示。已知:室温下K (MnS)=2.6×10-13、K [Mn(OH)]=2.0×10-13、HS电离
3 3 4 sp sp 2 2
常数K =1.1×10-7、K =1.3×10-13。
a1 a2
沉铁过程中也会产生少量Mn(OH) 沉淀。Mn(OH) 在工业上可用于去除溶液中HS-,反应为Mn(OH) +
2 2 2
HS-=MnS+OH-+HO,其平衡常数K=_______。
2
【答案】10()
【解析】K======10。
2.镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。NiSO ·6HO晶体是一种绿色易溶于水
4 2
的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu2+、Zn2+、Fe2+等)为原料获得。
操作步骤如图:
(1)加入NaS的目的是______________________________________。
2
[已知:K (FeS)=6.3×10-18,K (CuS)=1.3×10-36,K (ZnS)=1.3×10-24,K (NiS)=1.1×10-21]
sp sp sp sp
(2)可用氯酸钠NaClO 代替HO,写出氯酸钠与滤液Ⅱ反应的离子方程式
3 2 2
__________________________________________________________。微专题突破15 化学计算考点透视 问题的态度:问则少;辩则明
(3)向滤液Ⅱ中加入NaOH调节pH在一范围内生成氢氧化铁沉淀。已知常温下Fe(OH) 的K =1.0×10-
3 sp
39,若要使溶液中c(Fe3+)≤1.0×10-6 mol·L-1,则应该控制溶液pH范围不小于________。
【答案】(1)除去溶液中的Zn2+和Cu2+ (2)6Fe2++ClO+6H+=6Fe3++Cl-+3HO (3)3
2
【解析】废渣(除含镍外,还含有Cu、Zn、Fe等元素的化合物杂质),在硫酸溶解调节pH后过滤,滤液含
有二价铁离子、铜离子、锌离子等杂质,滤液Ⅰ中加入硫化钠形成 CuS、ZnS沉淀,可除去铜离子、锌离子,
过滤,滤液Ⅱ中加HO 是将二价铁氧化成三价铁,再通过调节pH使三价铁形成氢氧化物沉淀而除去,滤液Ⅲ
2 2
含有可溶性硫酸盐,主要是NiSO ,还有NaSO ,再加碳酸钠沉淀二价镍,过滤、洗涤,然后与硫酸反应生成
4 2 4
NiSO 晶体。
4
(1)由上述分析可知,加入NaS的目的是除去溶液中Cu2+、Zn2+;(2)加入氧化剂将滤液Ⅱ中的Fe2+
2
转化成Fe3+,氯酸钠与滤液Ⅱ反应的离子方程式为 6Fe2++ClO+6H+=6Fe3++Cl-+3HO;(3)溶液中
2
c(Fe3+)≤1.0×10-6 mol·L-1,c(OH-)== mol·L-1=1.0×10-11 mol·L-1,常温下,c(H+)==1×10-3
mol·L-1,则应该控制溶液pH不小于3。
3.(2024·南通市海安市)测定氧化锌样品纯度(杂质不参与反应):称取1.000 g样品,酸溶后,配制成
250 mL溶液。用移液管移取25.00 mL溶液于锥形瓶,调节pH至7~8,加入几滴铬黑T(用X-表示)做指示剂,
用0.0800 mol·L-1的EDTA(NaHY)标准液滴定其中的Zn2+(反应方程式为Zn2++X-=ZnX+,Zn2++HY2-
2 2 2
=ZnY2-+2H+),平行滴定三次,平均消耗EDTA标准液15.12 mL。(已知X-呈蓝色、ZnY2-呈无色、ZnX+
呈酒红色)。
①滴定终点时的现象为_____________________________________________________________________。
②计算ZnO样品的纯度___________。(保留四位有效数字,写出计算过程)
【答案】①加入最后半滴标准液,溶液由酒红色变为蓝色,且30s不变色 ②97.98%
【解析】①滴入NaHY标准溶液前,Zn2+与X-形成ZnX+使溶液呈酒红色,达到滴定终点时,Zn2+被完
2 2
全消耗生成无色的ZnY2-,溶液中含有X-而呈蓝色,由此可得出滴定终点时的现象为:加入最后半滴标准液,
溶液由酒红色变为蓝色,且30 s不变色;②根据滴定原理可得关系式ZnO~Zn2+~HY2-,则产品中n(ZnO)=
2
0.0800 mol·L-1×0.01512 L×=0.012096 mol,故ZnO的含量为×100%≈97.98%。
4.(2023·江苏百校联考)实验测定粗产品中NaSO·5HO的含量步骤如下:
2 2 3 2
步骤1:准确称取8.000 0 g样品溶于水,加入5 mL甲醛,配成100 mL溶液。
步骤2:准确称取0.294 0 K Cr O 固体于碘量瓶中,加入20 mL蒸馏水溶解,再加入10 mL 2 mol·L-1
2 2 7
HSO 和20 mL 10% KI溶液使铬元素完全转化为Cr3+,加水稀释至100 mL。
2 4
步骤3:向碘量瓶中加入1 mL 1%淀粉,用待测NaSO 溶液滴定碘量瓶中溶液至滴定终点,消耗NaSO 溶
2 2 3 2 2 3
液20.00 mL。(已知:I+2SO=2I-+SO)
2 2 4
试计算NaSO·5HO的纯度(写出计算过程)。
2 2 3 2
【答案】根据反应Cr O+6I-+14H+=2Cr3++3I+7HO;I+2SO=SO+2I-,可以得到关系式6SO~
2 2 2 2 2 4 2
Cr O,n(KCr O)===0.001 mol,NaSO·5HO 的质量为 0.001 mol×6×248 g·mol-1×=7.44 g,
2 2 2 7 2 2 3 2
NaSO·5HO的纯度为×100%=93%。
2 2 3 2
5.煅烧NH VO 可制得VO,煅烧过程中固体质量随温度变化的曲线如图所示。加热到200 ℃时,得到的
4 3 2 5
固体物质的化学式为_______________,300~350 ℃放出气态物质的化学式为____________。
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】HVO HO
3 2
【解析】煅烧NH VO 时,固体质量随温度变化的曲线如图所示。加热到200 ℃时,质量减少0.17 g,所以
4 3
0.01 mol NH VO 受热分解生成气体为0.01 mol NH ,发生NH VO ===NH ↑+HVO;加热到350 ℃时固体质量
4 3 3 4 3 3 3
又减少0.09 g,失去0.005 mol H O,发生的反应为2HVO===HO+VO,则放出气态物质的化学式为HO。
2 3 2 2 5 2