文档内容
专项训练 有机物的制备、性质实验题
1.(2023·山东·统考高考真题)一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定
有机醇 中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适
量水使剩余乙酸酐完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加
指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。对于上
述实验,下列做法正确的是
A.进行容量瓶检漏时,倒置一次即可
B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
C.滴定读数时,应单手持滴定管上端并保持其自然垂直
D.滴定读数时,应双手一上一下持滴定管
2.(2023·山东·统考高考真题)一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定
有机醇 中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适
量水使剩余乙酸酐完全水解: 。
试卷第1页,共16页
学科网(北京)股份有限公司③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加
指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。 样
品中羟基含量(质量分数)计算正确的是
A. B.
C. D.
3.(2023·山东·统考高考真题)一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定
有机醇 中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适
量水使剩余乙酸酐完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加
指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。根据上
述实验原理,下列说法正确的是
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
4.(2023·全国·统考高考真题)实验室由安息香制备二苯乙二酮的反应式如下:
试卷第2页,共16页 淘宝店铺:向阳百分百相关信息列表如下:
物质 性状 熔点/℃ 沸点/℃ 溶解性
难溶于冷水
安息香 白色固体 133 344
溶于热水、乙醇、乙酸
二苯乙二 不溶于水
淡黄色固体 95 347
酮 溶于乙醇、苯、乙酸
冰乙酸 无色液体 17 118 与水、乙醇互溶
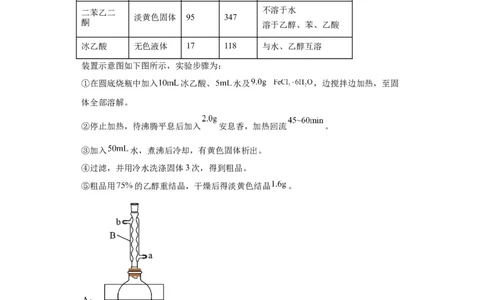
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入 冰乙酸、 水及 ,边搅拌边加热,至固
体全部溶解。
②停止加热,待沸腾平息后加入 安息香,加热回流 。
③加入 水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色结晶 。
回答下列问题:
(1)仪器A中应加入_______(填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______;冷却水应从_______(填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______。
(4)在本实验中, 为氧化剂且过量,其还原产物为_______;某同学尝试改进本实
试卷第3页,共16页
学科网(北京)股份有限公司验:采用催化量的 并通入空气制备二苯乙二酮。该方案是否可行_______?简述
判断理由_______。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______。
(6)若粗品中混有少量未氧化的安息香,可用少量_______洗涤的方法除去(填标号)。若
要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______(填标号)。
a. b. c. d.
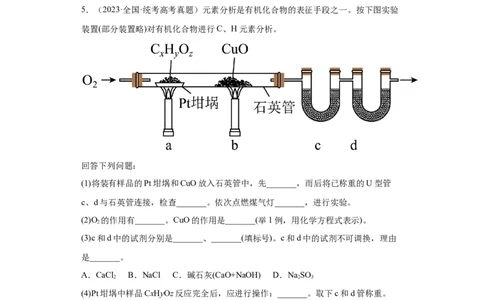
5.(2023·全国·统考高考真题)元素分析是有机化合物的表征手段之一。按下图实验
装置(部分装置略)对有机化合物进行C、H元素分析。
回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先_______,而后将已称重的U型管
c、d与石英管连接,检查_______。依次点燃煤气灯_______,进行实验。
(2)O 的作用有_______。CuO的作用是_______(举1例,用化学方程式表示)。
2
(3)c和d中的试剂分别是_______、_______(填标号)。c和d中的试剂不可调换,理由
是_______。
A.CaCl B.NaCl C.碱石灰(CaO+NaOH) D.NaSO
2 2 3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:_______。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱
测得该有机物的相对分子量为118,其分子式为_______。
6.(2023·辽宁·统考高考真题)2—噻吩乙醇( )是抗血栓药物氯吡格雷的重要
中间体,其制备方法如下:
试卷第4页,共16页 淘宝店铺:向阳百分百Ⅰ.制钠砂。向烧瓶中加入 液体A和 金属钠,加热至钠熔化后,盖紧塞
子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至 ,加入 噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至 ,加入稍过量的环氧乙烷的四氢呋喃溶液,反应
。
Ⅳ.水解。恢复室温,加入 水,搅拌 ;加盐酸调 至4~6,继续反应 ,
分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水 ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋
喃、噻吩和液体A后,得到产品 。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择_______。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是_______。
(3)步骤Ⅱ的化学方程式为_______。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是
_______。
(5)步骤Ⅳ中用盐酸调节 的目的是_______。
(6)下列仪器在步骤Ⅴ中无需使用的是_______(填名称):无水 的作用为_______。
(7)产品的产率为_______(用 计算,精确至0.1%)。
7.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)己二酸是合成尼龙-66的主要原料
试卷第5页,共16页
学科网(北京)股份有限公司之一,实验室以硝酸氧化液态环己醇( )制取己二酸 晶体,
制备实验装置如图(夹持及加热装置省略):
反应方程式: (未配平)
已知:每100g水中己二酸的溶解度如表:
温度/℃ 15 25 50 70 100
溶解度/g 1.44 2.3 8.48 34.1 160
(1)仪器a的名称是_____________.
(2)在三颈烧瓶中加入16mL 50%的硝酸,用水浴预热硝酸溶液到80℃,边搅拌边用仪
器a滴加环己醇,维持温度在85-90℃,滴加环己醇时,需逐滴加入的原因是
____________________。
(3)滴加结束后,继续搅拌并用水浴加热,反应约15分钟,判断反应结束的标志是
_________________。反应结束,冷却,使固体析出,抽滤、洗涤。
(4)用重结晶法提纯己二酸,步骤如下:
把粗产品配成热的浓溶液→加入活性炭脱色→_____________(填操作名称)→冷却至室
温,过滤→用____________(填“冷水”、“热水”或“乙醇”)洗涤晶体→干燥。
(5)己二酸纯度的测定
将1.000g己二酸样品配制成100mL溶液,每次取20.00mL试样溶液于锥形瓶中,滴入
几滴酚酞试液,用 溶液滴定至终点,平均消耗NaOH溶液
20.00mL(己二酸被完全中和)。
①下列说法正确的是_______________。
A.将己二酸样品配制成100mL溶液,定容时仰视,则测定结果偏小
试卷第6页,共16页 淘宝店铺:向阳百分百B.滴定时,未润洗碱式滴定管,测定结果偏大
C.接近滴定终点时,应控制活塞,改为滴加半滴标准溶液,直至溶液变为粉红色,且
半分钟内不变色
D.若滴定前滴定管尖嘴部分气泡未赶走,滴定后气泡消失,则测定结果偏小
②己二酸的纯度为____________%。
(6)本实验装置存在的一处明显不足为_____________________。
8.(2023·湖北武汉·统考模拟预测)2-甲基-2-丁醇是一种重要的有机化合物,可用于
合成香料、农药等。某化学兴趣小组欲利用格氏试剂法制备2-甲基-2-丁醇。实验原理
及具体操作步骤如下:
Ⅰ.乙基溴化镁的制备
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压
滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,
维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚
混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,
分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水
碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产
率。
已知:①RMgBr化学性质活泼,易与 、R′X等发生反应生成RH、R-R′;
②各物质的沸点见下表:
溴乙
物质 无水乙醚 丙酮 2-甲基-2-丁醇
烷
沸点(℃) 34.6 38.4 56.5 102.5
试卷第7页,共16页
学科网(北京)股份有限公司回答下列问题:
(1)仪器a的名称是___________。
(2)干燥管中无水氯化钙的作用是___________。
(3)微热或加入小颗粒碘单质可引发 与镁屑的反应,其中碘的作用可能是
___________;不宜使用长时间放置的镁屑进行实验,其原因是___________。
(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是___________。
(5)蒸去乙醚时采用热水浴的原因是___________。
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量
为2.69g,则2-甲基-2-丁醇的产率为___________(结果保留2位有效数字)。
9.(2023·吉林长春·统考模拟预测)邻硝基苯甲醛是一种重要的精细化学品,实验室
可通过图1装置(夹持仪器已略去),以邻硝基苯甲醇为原料,利用两相反应体系(图2)
实现邻硝基苯甲醛的选择性氧化合成.已知部分物质的性质如下表所示。
物质
溶解 微溶于水,易溶于 难溶于水,易溶于 易溶水,难溶于
性
熔点/
70 43 —
沸点/
270 153 —
性质 (易溶于水)
试卷第8页,共16页 淘宝店铺:向阳百分百实验步骤如下:
I.向三颈瓶中依次加入 邻硝基苯甲醇, 二氯甲烷(沸点 )
和磁子,搅拌使固体全部溶解。再依次加入 水溶液(做催化剂)和
饱和 溶液。在 和剧烈搅拌条件下,滴加 足量 水
溶液后,继续反应 。
II.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用 二氯甲烷萃
取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到
粗品。
III.将粗品溶解在 二氯甲烷中,加入 饱和 溶液,充分作用后,
分离得到水层,水层在冰浴中用 氢氧化钠溶液调节到 ,浅黄色固体析出完
全.抽滤、干燥至恒重,得 产品。
(1)控制反应温度为 的方法是__________;滴加 溶液时,需要先将漏斗上端
玻璃塞打开,目的是_______________。
(2)合成产品的化学方程式为________________。
(3)相比于单相反应体系,利用两相反应体系可以大幅减少副产物的量,原因是
______________;该副产物主要成分是_______________。
(4)步骤II中除去并回收二氯甲烷的实验方法是_________________。
(5)若用一定浓度盐酸代替“步骤III”中的 氢氧化钠溶液调节 ,
_________________(填“能”或“不能”)析出大量产品,原因是___________________。
(6)本实验产率为________________(计算结果保留3位有效数字)。
试卷第9页,共16页
学科网(北京)股份有限公司10.(2023·四川遂宁·统考模拟预测)山梨酸酯是一类广谱、高效、低毒的防腐保鲜剂,
在食品加工、果蔬保鲜等方面有重要的实用价值,其中山梨酸正丁酯抑菌能力最强,
实验室用如图所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
反应方程式如下:
可能用到的有关数据如下表所示:
物质 相对分子质量 密度/( ) 沸点/℃ 水溶性
山梨酸 112 1.204 228 易溶
正丁醇 74 0.8089 117 溶
山梨酸正丁
168 0.926 195 难溶
酯
乙醚 74 0.714 34.6 难溶
环己烷 84 0.779 80.7 难溶
实验步骤:
在三口烧瓶中加入11.2g山梨酸、14.8g正丁醇、少量催化剂和几粒沸石,水浴加热三
口烧瓶,使反应体系保持微沸,回流4小时后停止加热和搅拌,反应液冷却至室温,
滤去催化剂和沸石,将滤液倒入200 水中,加入50 乙醚,倒入分液漏斗中,分
液。有机层先用 的碳酸氢钠溶液洗涤至中性,再用水洗涤分液,收集有机层。
在有机层中加入少量无水 ,静置片刻,过滤。将滤液进行蒸馏,蒸去乙醚,得
到纯净的山梨酸正丁酯12.0g。回答下列问题:
(1)仪器a的名称是___________;仪器b的作用是___________。
(2)洗涤、分液过程中,加入 的碳酸氢钠溶液的目的是___________,之后再
试卷第10页,共16页 淘宝店铺:向阳百分百用水洗的主要目的是___________。
(3)在上述洗涤、分液操作过程中,应先充分振荡,然后静置,待分层后
___________(填选项字母)。
A.直接将有机层从分液漏斗的上口倒出
B.直接将有机层从分液漏斗的下口放出
C.先将水层从分液漏斗的下口放出,再将有机层从下口放出
D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出
(4)实验中加入少量无水 ,的目的是___________。
(5)本实验中,山梨酸正丁酯的产率是___________。(精确至0.1%)。
(6)为提高反应正向进行的程度,实验室常使用如图所示装置(夹持、加热装置已略去)
提高产物的产率。下列说法正确的是___________(填选项字母)。
A.管口A是冷凝水的出水口
B.环己烷可将反应产生的水及时带出
C.工作一段时间后,当环己烷即将流回烧瓶中时,必须将分水器中的水和环己烷放出
D.工作一段时间后,环己烷可在烧瓶与分水器中循环流动
11.(2023·浙江金华·模拟预测)正丁醚是一种常见的有机溶剂,实验室制备原理如下:
主要反应:2CHCHCHCHOH (CHCHCHCH)O+HO
3 2 2 2 3 2 2 2 2 2
有关物质的性质如表所示:
沸点 密度 溶解性
正丁醚 142.4℃ 0.76g•mL-1 微溶于水,难溶于50%H SO
2 4
正丁醇 117.6℃ 0.80g•mL-1 微溶于水,可溶于50%H SO
2 4
实验步骤:先在三颈烧瓶中加入搅拌磁子,如图所示连接好装置。
试卷第11页,共16页
学科网(北京)股份有限公司I.粗产品的制备:
(1)装置a的名称是______,分水器的作用是______。
(2)反应开始阶段,操作的顺序为:打开三颈烧瓶的玻璃塞,
_______→_______→_______→E→_______,_______ 。塞上三颈烧瓶的玻璃塞,保持
130℃左右回流40min,当分水器中下层液体接近分水器支管口,可将下层液体放出,
直至下层液体的体积不再变化,再加热至温度达到150℃后停止加热。
A.加入18.5ml正丁醇
B.加入2.5ml浓硫酸
C.打开加热功能开关
D.打开搅拌功能开关
E.向装置a的进水口通入冷凝水
(3)反应温度保持在130℃左右,原因是_______。
Ⅱ.粗产品的提纯:合并分水器与三颈烧瓶内的液体,进行如图操作。
(4)下列有关说法正确的是______。
A.操作①目的是除去正丁醇等溶于水的杂质
B.操作①、②、③均为分液
C.分液操作必须使用的玻璃仪器有:分液漏斗、玻璃棒、烧杯
D.蒸馏收集140℃~144℃的馏分时,选用空气冷凝管,以防温差过大导致冷凝管破裂
(5)已知:产率= ×100%,当蒸馏至不再有液体馏出,冷却后测得产品体积为
9.6mL,则该实验的产率为______(列出计算式即可)。
12.(2023·重庆·校联考模拟预测)阿司匹林为医药史上三大经典药物之一,又叫乙酰
试卷第12页,共16页 淘宝店铺:向阳百分百水杨酸,其合成原理如图:
(水杨酸)+(CH CO) O(乙酸酐) (乙酰水杨酸)
3 2
+CH COOH。
3
已知:①水杨酸分子间能发生缩合反应,所得聚合物不溶于饱和NaHCO 溶液。
3
②乙酸酐有吸湿性,缓慢地溶于水形成乙酸;
③部分物质数据如表:
溶解度
名称 性质 熔点/℃ 沸点/℃
水 乙醇 乙酸乙酯
水杨酸 白色结晶 157-159 211 溶 易溶 易溶
乙酸酐 无色液体 -73.1 138.6 易溶 溶 易溶
乙酰水杨酸 白色结晶 135 321.4 冰水微溶、热水可溶 易溶 微溶
实验室中合成少量阿司匹林的操作步骤如下:
①在50mL圆底烧瓶中,加入2g干燥的水杨酸和5mL新蒸馏的乙酸酐,再加5滴浓硫
酸,充分摇动使水杨酸全部溶解,加热保持瓶内温度在80~85℃,反应20min。
②稍冷后,将反应混合物在不断搅拌下倒入50mL冷水中,并用冰水浴冷却15min,结
晶完全析出后,抽滤,洗涤,得乙酰水杨酸粗产品。
③将粗产品转移到100mL烧杯中,慢慢加入溶液A,并不断搅拌,直到无气体产生为
止。
④抽滤除去不溶性杂质,滤液倒入盛有盐酸的烧杯中,搅拌后用冰水冷却、结晶,抽
滤并用少量水洗涤,干燥获得产品乙酰水杨酸。
⑤步骤②所得粗产品也可采用重结晶的方式提纯。用如图所示的回流装置,将粗产品
加入乙酸乙酯中进行热溶解,然后趁热过滤,冷却至室温,抽滤,用少许乙酸乙酯洗
涤,干燥,得晶体状乙酰水杨酸。
(1)步骤①中所用仪器和原料需要干燥的原因是____;应采用的加热方法是____。
(2)步骤②和④中“抽滤”操作相对于普通过滤的优点是____;洗涤晶体要用少量冷水,
试卷第13页,共16页
学科网(北京)股份有限公司原因是____。
(3)步骤③中所加溶液A为____。
(4)步骤⑤中粗产品热溶解时需加入两粒沸石,目的是____。
(5)实验时冷凝水应从图中____(填“a”或“b”)口通入,采用回流装置不采用烧杯等敞口
容器的优点是____。
13.(2023·湖北武汉·统考模拟预测)苯胺是一种无色油状液体,主要用于制造染料、
药物和树脂等。利用水蒸气蒸馏法分离提纯粗苯胺(杂质为难以气化的物质)的装置如图
所示。
实验操作:将粗苯胺加入仪器B中,向仪器A中加水,打开F,加热仪器A使水沸腾。
同时对仪器B进行预热,关闭F,让水蒸气导入蒸馏装置,通入冷凝水,开始蒸馏。
回答下列问题:
(1)仪器C的名称是_______;仪器E的作用是_______。
(2)如果加热A一段时间后发现漏加沸石,应该采用的补救操作是______。
(3)水蒸气冷凝放热较多,为了提高冷凝效果可采取的措施是______。
(4)蒸馏至_______时可停止蒸馏。
(5)将D中苯胺分离出来,需要用到的玻璃仪器有_______。
(6)已知混合物的蒸气总压等于外界大气压时,混合物开始沸腾。混合气体的总压等于
各气体的分压之和,各气体的分压之比等于它们的物质的量之比。苯胺与水共沸时,
苯胺的分压为5.6kPa,水蒸气的分压为95.7kPa,理论上每蒸出1g水同时蒸出苯胺的
质量为______g(计算结果保留2位有效数字);苯胺微溶于水,使水的蒸气压降低,则
实际蒸出苯胺的质量______(“偏大”“偏小”或“不变”)。
14.(2023·福建三明·统考模拟预测)甲醛是有毒气体,某实验小组探究能否用氨水吸
收甲醛。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①
试卷第14页,共16页 淘宝店铺:向阳百分百②
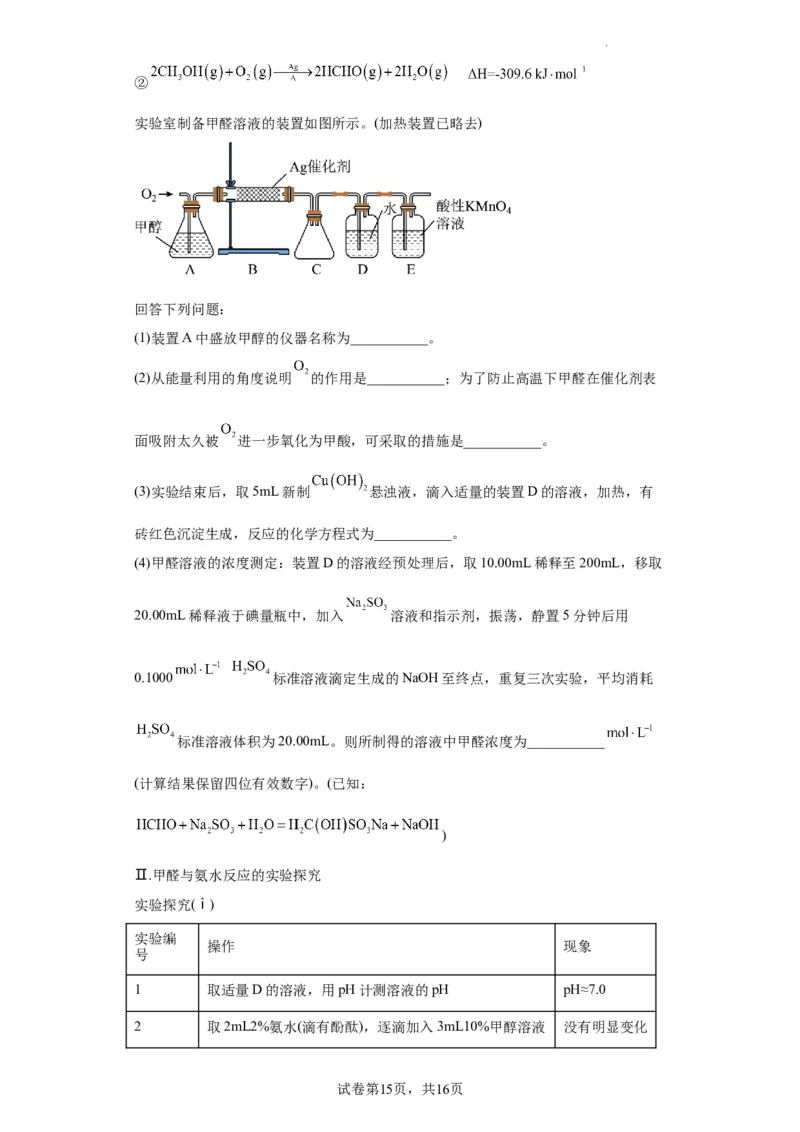
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)
回答下列问题:
(1)装置A中盛放甲醇的仪器名称为___________。
(2)从能量利用的角度说明 的作用是___________;为了防止高温下甲醛在催化剂表
面吸附太久被 进一步氧化为甲酸,可采取的措施是___________。
(3)实验结束后,取5mL新制 悬浊液,滴入适量的装置D的溶液,加热,有
砖红色沉淀生成,反应的化学方程式为___________。
(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取
20.00mL稀释液于碘量瓶中,加入 溶液和指示剂,振荡,静置5分钟后用
0.1000 标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗
标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为___________
(计算结果保留四位有效数字)。(已知:
)
Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
实验编
操作 现象
号
1 取适量D的溶液,用pH计测溶液的pH pH≈7.0
2 取2mL2%氨水(滴有酚酞),逐滴加入3mL10%甲醇溶液 没有明显变化
试卷第15页,共16页
学科网(北京)股份有限公司3 取2mL2%氨水(滴有酚酞),逐滴加入装置D的溶液 红色褪去
(5)实验1的目的是___________。
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
实验编
操作 现象
号
4 取实验3的无色溶液1mL,滴入几滴氨水 溶液变红
5 无明显变化
(6)实验5的操作为___________。由实验4、5说明猜想___________(填标号)正确。
15.(2023·浙江·校联考模拟预测)苯甲酸乙酯是国家允许使用的食品香料,可用下列
流程制备:
已知:环己烷、乙醇和水易形成三元共沸物,沸点为 ;相关数据见如表。
试剂 密度 沸点 熔点 溶解性
乙醇 易溶于水
苯甲酸 微溶于水
环己烷 难溶于水
苯甲酸乙
难溶于水
酯
产品 实验测定 难溶于水
(1)请补全步骤Ⅳ的操作步骤 ______ 。
(2)步骤Ⅵ在如图装置中进行,从下列选项选择合适操作并排序 ______ 。
试卷第16页,共16页 淘宝店铺:向阳百分百按如图组装仪器,检查装置的气密性
用分液法分离出有机层,再加入 乙醚萃取,然后合并至有机层,加入无水
、蒸馏、收集馏分
反应液倒入盛有 水的烧杯中,分批加入碳酸钠至无气体产生
在 的 中依次加入 苯甲酸、 乙醇、 环己烷、 浓硫酸和沸
石,加热回流
在 的 中依次加入 苯甲酸、 浓硫酸、 乙醇、 环己烷和沸
石,加热回流
(3)如图装置中仪器 的名称是 ______ ,虚框内装置的作用是 ______ 。
(4)下列说法正确的是 ______ 。
A.在步骤Ⅰ中,不能选用酸性 溶液氧化
B.步骤Ⅲ是先加 溶液,再进行分液
C.在步骤Ⅳ中采用减压过滤是为了得到纯度更高的苯甲酸
D.在步骤Ⅵ中,加入无水 、蒸馏时应收集 的馏分
E.在步骤Ⅵ中,加热回流至虚框内装置中的下层液面不再升高,停至加热
(5)产品分析:假设环己烷是产品苯甲酸乙酯的唯一杂质,可选用下列方法测定产品纯
度量取 产品于烧杯中,加入 过量的 溶液 ,搅拌充分
反应,转移至容量瓶配成 溶液,取 溶液于锥形瓶中滴加几滴指示剂,用
进行滴定,滴至终点,平均消耗 体积 。选用的指示剂是
______ 填“酚酞”或“甲基橙” ,所得产品的纯度 ______ 保留三位有效数字
。
试卷第17页,共16页
学科网(北京)股份有限公司