文档内容
素养说明:磷、砷及其化合物的探究题,充分体现了考生对陌生物质的分析能力,
以及获取信息和利用信息的能力。
一、磷及其化合物
1.磷的氢化物(PH )
3
磷的氢化物PH (磷化氢)又称为膦,膦分子与氨分子的结构相似,也呈三角锥形。
3
膦是一种较强的还原剂,稳定性较差,在水中的溶解度很小。
2.磷的含氧酸
(1)亚磷酸(H PO )性质和结构:纯净的亚磷酸是一种无色固体,在水中有较大溶解
3 3
度;亚磷酸是一种中强二元酸,它的电离常数是K =1.6×10-2,K =7×10-7。其
1 2
电子式和结构式分别是:
(2)次磷酸(H PO )性质和结构:次磷酸是一种无色的晶体,熔点26.5 ℃,易溶解,
3 2
它是中强酸,又是一元酸,并依下式电离:H PO H++H PO,其电子式和
3 2 2
结构式分别是
二、砷及其化合物1.砷(As)
旧名“砒”。有灰、黄、黑褐三种同素异形体,具有金属性。
2.砷的氢化物(AsH )
3
砷与氢结合生成剧毒的砷化氢(AsH ),砷化氢相当不稳定,加热时分解为单质砷,
3
砷化氢还是一种很强的还原剂。
3.砷的氧化物
砷有两种氧化物,三氧化二砷(As O )和五氧化二砷(As O )。三氧化二砷,俗称砒
2 3 2 5
霜,是最具商业价值的砷化合物及主要的砷化学开始物料。它也是最古老的毒物
之一,无臭无味,外观为白色霜状粉末,故称砒霜。
4.砷化物
砷化物是指一种含有金属砷的化合物。金属与砷生成的化合物。自然界中存在砷
铜矿Cu As、斜方砷铁矿FeAs 、砷钴矿CoAs 等砷化物。
3 2 2
[题型专练]
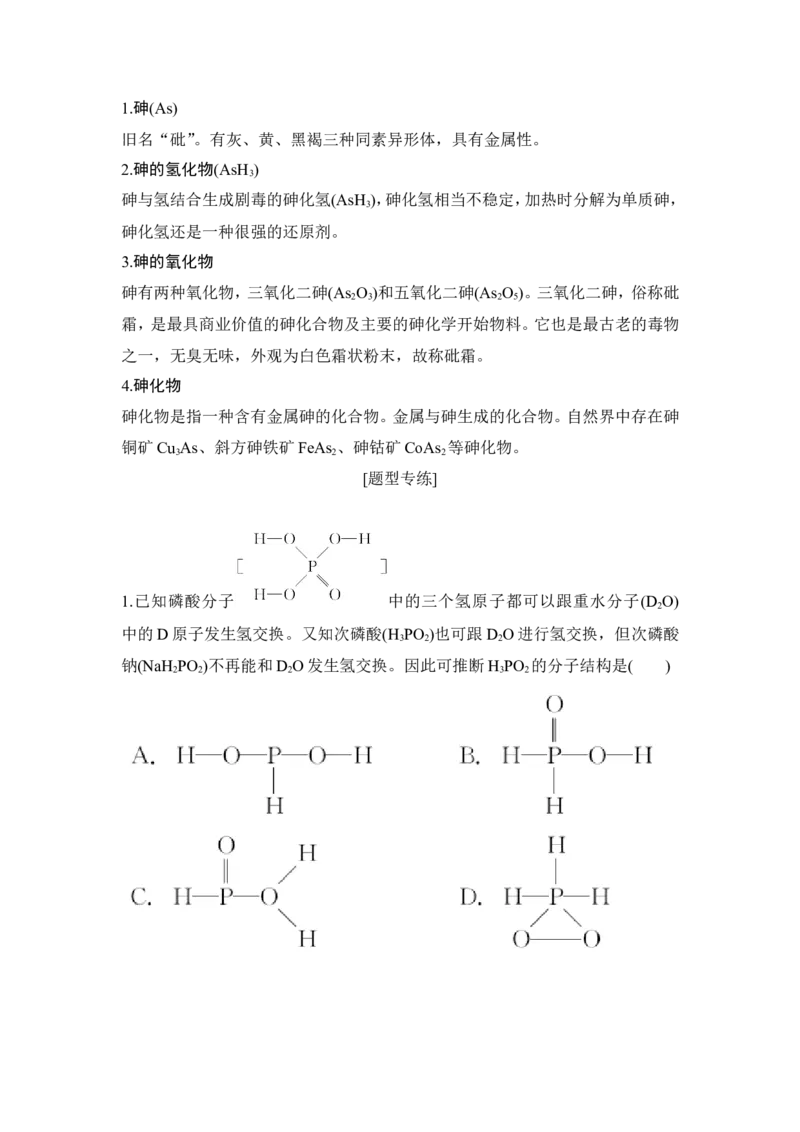
1.已知磷酸分子 中的三个氢原子都可以跟重水分子(D O)
2
中的D原子发生氢交换。又知次磷酸(H PO )也可跟D O进行氢交换,但次磷酸
3 2 2
钠(NaH PO )不再能和D O发生氢交换。因此可推断H PO 的分子结构是( )
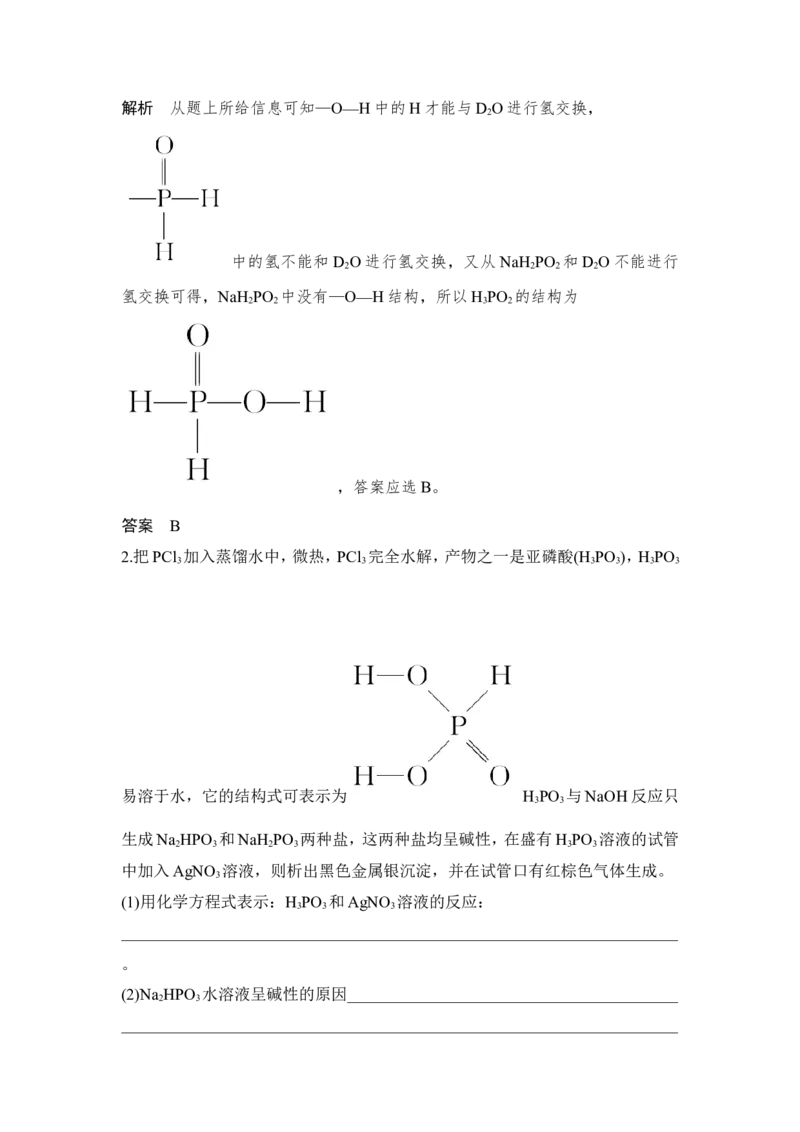
2 2 2 3 2解析 从题上所给信息可知—O—H中的H才能与D O进行氢交换,
2
中的氢不能和D O进行氢交换,又从NaH PO 和D O不能进行
2 2 2 2
氢交换可得,NaH PO 中没有—O—H结构,所以H PO 的结构为
2 2 3 2
,答案应选B。
答案 B
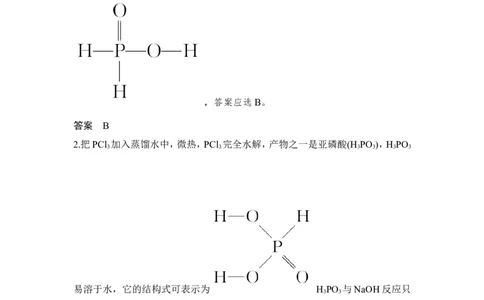
2.把PCl 加入蒸馏水中,微热,PCl 完全水解,产物之一是亚磷酸(H PO ),H PO
3 3 3 3 3 3
易溶于水,它的结构式可表示为 H PO 与NaOH反应只
3 3
生成Na HPO 和NaH PO 两种盐,这两种盐均呈碱性,在盛有H PO 溶液的试管
2 3 2 3 3 3
中加入AgNO 溶液,则析出黑色金属银沉淀,并在试管口有红棕色气体生成。
3
(1)用化学方程式表示:H PO 和AgNO 溶液的反应:
3 3 3
_____________________________________________________________________
。
(2)Na HPO 水溶液呈碱性的原因_________________________________________
2 3
_____________________________________________________________________(用离子方程式表示)。
(3)根据题意,H PO 是________。
3 3
a.弱酸 b.二元酸 c.三元酸 d.具有还原性 e.强酸
答案 (1)2H PO +AgNO ===Ag↓+NO↑+2H PO
3 3 3 3 4
(2)HPO+H O H PO+OH-,H PO+H O H PO +OH- (3)abd
2 2 2 2 3 3
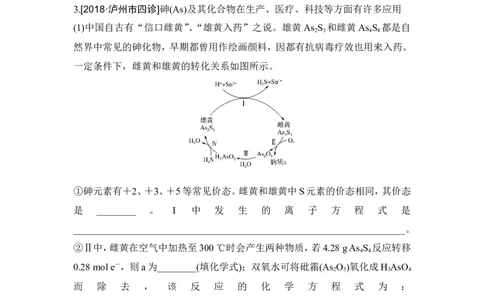
3.[2018·泸州市四诊]砷(As)及其化合物在生产、医疗、科技等方面有许多应用
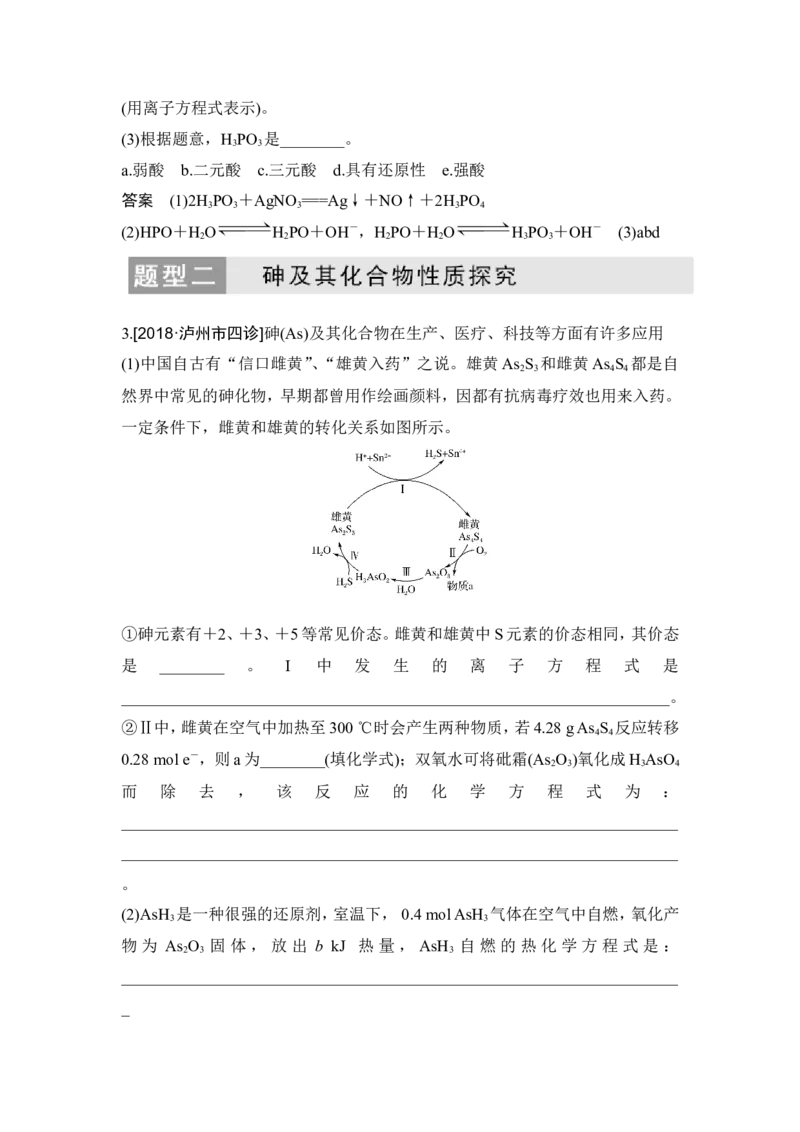
(1)中国自古有“信口雌黄”、“雄黄入药”之说。雄黄As S 和雌黄As S 都是自
2 3 4 4
然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
一定条件下,雌黄和雄黄的转化关系如图所示。
①砷元素有+2、+3、+5等常见价态。雌黄和雄黄中S元素的价态相同,其价态
是 ________ 。 I 中 发 生 的 离 子 方 程 式 是
____________________________________________________________________。
②Ⅱ中,雌黄在空气中加热至300 ℃时会产生两种物质,若4.28 g As S 反应转移
4 4
0.28 mol e-,则a为________(填化学式);双氧水可将砒霜(As O )氧化成H AsO
2 3 3 4
而 除 去 , 该 反 应 的 化 学 方 程 式 为 :
_____________________________________________________________________
_____________________________________________________________________
。
(2)AsH 是一种很强的还原剂,室温下, 0.4 mol AsH 气体在空气中自燃,氧化产
3 3
物 为 As O 固 体 , 放 出 b kJ 热 量 , AsH 自 燃 的 热 化 学 方 程 式 是 :
2 3 3
_____________________________________________________________________
______________________________________________________________________
。
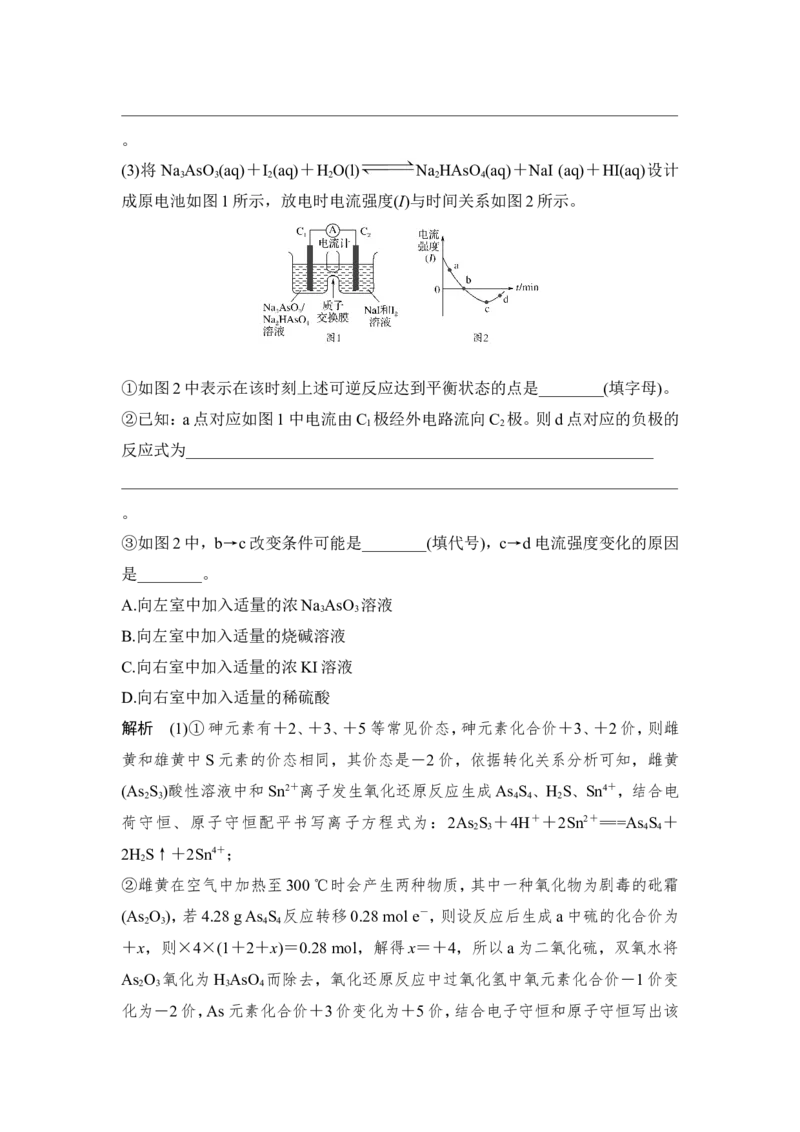
(3)将 Na AsO (aq)+I (aq)+H O(l) Na HAsO (aq)+NaI (aq)+HI(aq)设计
3 3 2 2 2 4
成原电池如图1所示,放电时电流强度(I)与时间关系如图2所示。
①如图2中表示在该时刻上述可逆反应达到平衡状态的点是________(填字母)。
②已知:a点对应如图1中电流由C 极经外电路流向C 极。则d点对应的负极的
1 2
反应式为__________________________________________________________
_____________________________________________________________________
。
③如图2中,b→c改变条件可能是________(填代号),c→d电流强度变化的原因
是________。
A.向左室中加入适量的浓Na AsO 溶液
3 3
B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液
D.向右室中加入适量的稀硫酸
解析 (1)①砷元素有+2、+3、+5等常见价态,砷元素化合价+3、+2价,则雌
黄和雄黄中S元素的价态相同,其价态是-2价,依据转化关系分析可知,雌黄
(As S )酸性溶液中和Sn2+离子发生氧化还原反应生成As S 、H S、Sn4+,结合电
2 3 4 4 2
荷守恒、原子守恒配平书写离子方程式为:2As S +4H++2Sn2+===As S +
2 3 4 4
2H S↑+2Sn4+;
2
②雌黄在空气中加热至300 ℃时会产生两种物质,其中一种氧化物为剧毒的砒霜
(As O ),若4.28 g As S 反应转移0.28 mol e-,则设反应后生成a中硫的化合价为
2 3 4 4
+x,则×4×(1+2+x)=0.28 mol,解得x=+4,所以a为二氧化硫,双氧水将
As O 氧化为H AsO 而除去,氧化还原反应中过氧化氢中氧元素化合价-1价变
2 3 3 4
化为-2价,As元素化合价+3价变化为+5价,结合电子守恒和原子守恒写出该反应的化学方程式为2H O +H O+As O ===2H AsO ;(2)由0.4 mol AsH 气体在
2 2 2 2 3 3 4 3
空气中自燃,氧化产物为As O 固体,放出b kJ热量,则2 mol AsH 气体在空气中
2 3 3
自燃,氧化产物为As O 固体,放出5b kJ热量,则AsH 自燃的热化学方程式为
2 3 3
2AsH (g)+3O (g)===As O (s)+3H O(l) ΔH=-5b kJ/mol;(3)①可逆反应达到
3 2 2 3 2
平衡状态即电流强度为0,则由图像可知表示在该时刻上述可逆反应达到平衡状
态的点是b; ②由a点对应图2中电流由C 极经外电路流向C 极,则d点电流方
1 2
向与a点相反即电流由C 极经外电路流向C 极,则负极C 极失电子发生氧化反
2 1 1
应,反应式为AsO-2e-+H O===HAsO+H+;③由a点对应图2中电流由C 极
2 1
经 外 电 路 流 向 C 极 , 则 电 池 总 反 应 为 HI(aq) + Na HAsO (aq) + NaI
2 2 4
(aq)===Na AsO (aq)+I (aq)+H O(l),图2中,b→c电流方向改变,则电池总反应
3 3 2 2
为Na AsO (aq)+I (aq)+H O(l) Na HAsO (aq)+NaI (aq)+HI(aq),即平衡
3 3 2 2 2 4
向正反应方向移动,A.向左室中加入适量的浓Na AsO 溶液,平衡向正反应方向
3 3
移动,故A正确;B.向左室中加入适量的烧碱溶液,消耗Na HAsO (aq),平衡向正
2 4
反应方向移动,故B正确;C.向右室中加入适量的浓KI溶液,平衡向逆反应方向
移动,故C错误;D.向右室中加入适量的稀硫酸,平衡向逆反应方向移动,故D错
误;c→d电流强度减小,说明随着正反应进行,反应浓度下降,反应速率下降,单
位时间转移的电子(电量)减少。
答案 (1)①-2 4H++2Sn2++2As S ===2H S↑+2Sn4++As S
2 3 2 4 4
②SO As O +2H O +H O===2H AsO
2 2 3 2 2 2 3 4
(2) 2AsH (g)+3O (g)===As O (s)+3H O(l) ΔH=-5b kJ/mol
3 2 2 3 2
(3)①b ②AsO-2e-+H O===HAsO+H+ ③AB 停止改变条件,随着正反
2
应进行,反应浓度下降,反应速率下降,单位时间转移的电子(电量)减少