文档内容
章末常考必备的重要有机转化关系及反应方程式书写强
化练
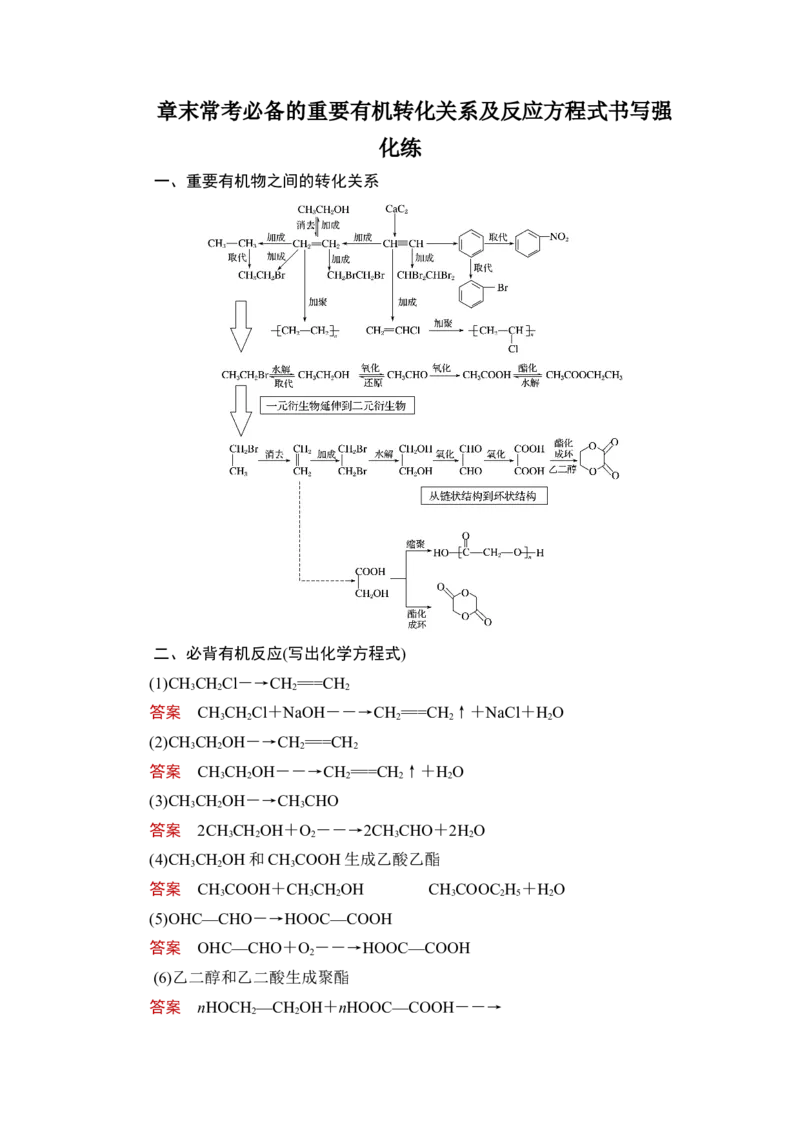
一、重要有机物之间的转化关系
二、必背有机反应(写出化学方程式)
(1)CH CH Cl―→CH ===CH
3 2 2 2
答案 CH CH Cl+NaOH――→CH ===CH ↑+NaCl+H O
3 2 2 2 2
(2)CH CH OH―→CH ===CH
3 2 2 2
答案 CH CH OH――→CH ===CH ↑+H O
3 2 2 2 2
(3)CH CH OH―→CH CHO
3 2 3
答案 2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
(4)CH CH OH和CH COOH生成乙酸乙酯
3 2 3
答案 CH COOH+CH CH OHCH COOC H +H O
3 3 2 3 2 5 2
(5)OHC—CHO―→HOOC—COOH
答案 OHC—CHO+O ――→HOOC—COOH
2
(6)乙二醇和乙二酸生成聚酯
答案 nHOCH —CH OH+nHOOC—COOH――→
2 2+(2n-1)H O
2
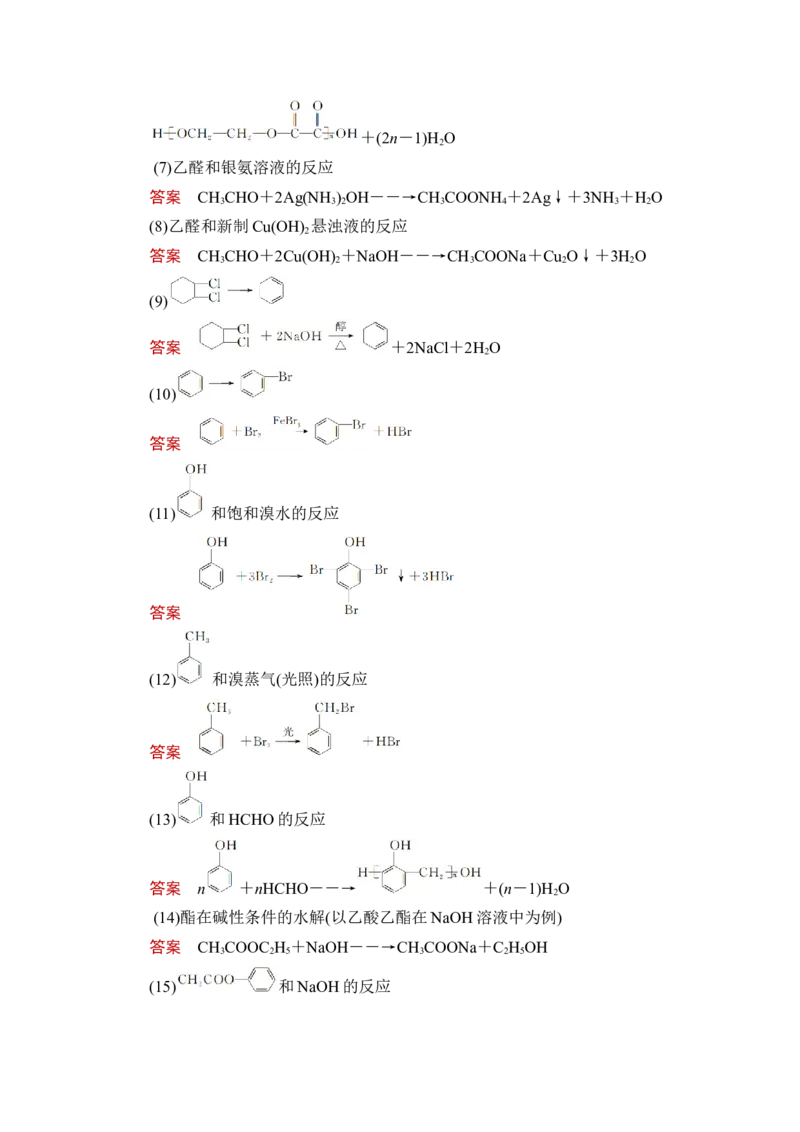
(7)乙醛和银氨溶液的反应
答案 CH CHO+2Ag(NH ) OH――→CH COONH +2Ag↓+3NH +H O
3 3 2 3 4 3 2
(8)乙醛和新制Cu(OH) 悬浊液的反应
2
答案 CH CHO+2Cu(OH) +NaOH――→CH COONa+Cu O↓+3H O
3 2 3 2 2
(9)
答案 +2NaCl+2H O
2
(10)
答案
(11) 和饱和溴水的反应
答案
(12) 和溴蒸气(光照)的反应
答案
(13) 和HCHO的反应
答案 n +nHCHO――→ +(n-1)H O
2
(14)酯在碱性条件的水解(以乙酸乙酯在NaOH溶液中为例)
答案 CH COOC H +NaOH――→CH COONa+C H OH
3 2 5 3 2 5
(15) 和NaOH的反应答案 +2NaOH――→CH COONa+ +H O
3 2
三、常考有机物的检验
1.卤代烃中卤素的检验
取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴
入AgNO 溶液,观察沉淀的颜色,确定是何种卤素。
3
2.烯醛中碳碳双键的检验
(1)若是纯净的液态样品,则可向所取试样中加入溴的四氯 化碳溶液,若褪色
则证明含有碳碳双键。
(2)若样品为水溶液,则先向样品中加入足量的 新制 Cu(OH ) 悬浊液,加热煮
2
沸,充分反应后冷却过滤,向滤液中加入稀硝酸酸化,再加入溴水,若褪色,则证
明含有碳碳双键。
【特别提醒】
若直接向样品水溶液中滴加溴水,则会有反应:—CHO+Br +H O―→—
2 2
COOH+2HBr而使溴水褪色。
3.二糖或多糖水解产物的检验
若二糖或多糖是在稀硫酸作用下水解的,则先向冷却后的水解液中加入足量
的 NaOH 溶液 ,中和稀硫酸,然后再加入银氨溶液或新制的氢氧化铜悬浊液,(水
浴)加热,观察现象,作出判断。
4.如何检验溶解在苯中的苯酚?
取样,向试样中加入NaOH 溶液,振荡后静置、分液,向水溶液中加入盐酸酸
化,再滴入几滴FeCl 溶液(或过量饱和溴水),若溶液呈紫色(或有白色沉淀生成),
3
则说明有苯酚。
【特别提醒】
(1)若向样品中直接滴入FeCl 溶液,则由于苯酚仍溶解在苯中,不能进入水
3
溶液中与Fe3+进行离子反应;若向样品中直接加入饱和溴水,则生成的三溴苯酚
会溶解在苯中而看不到白色沉淀。
(2)若所用溴水浓度太小,则一方面可能由于生成溶解度相对较大的一溴苯
酚或二溴苯酚,另一方面可能生成的三溴苯酚溶解在过量的苯酚之中而看不到沉
淀。
5.检验实验室制得的乙烯气体中含有CH ===CH 、SO 、CO 、H O,可将气体
2 2 2 2 2
依次通过
无水硫酸铜(检验水)→品红溶液(检验SO )→ 饱和 F e (SO ) 溶液(除去SO )→
2 2 4 3 2品红溶液(确认SO 已除尽)→澄清石灰水(检验CO )→溴水或溴的四氯化碳溶液
2 2
或酸性高锰酸钾溶液(检验CH ===CH )
2 2
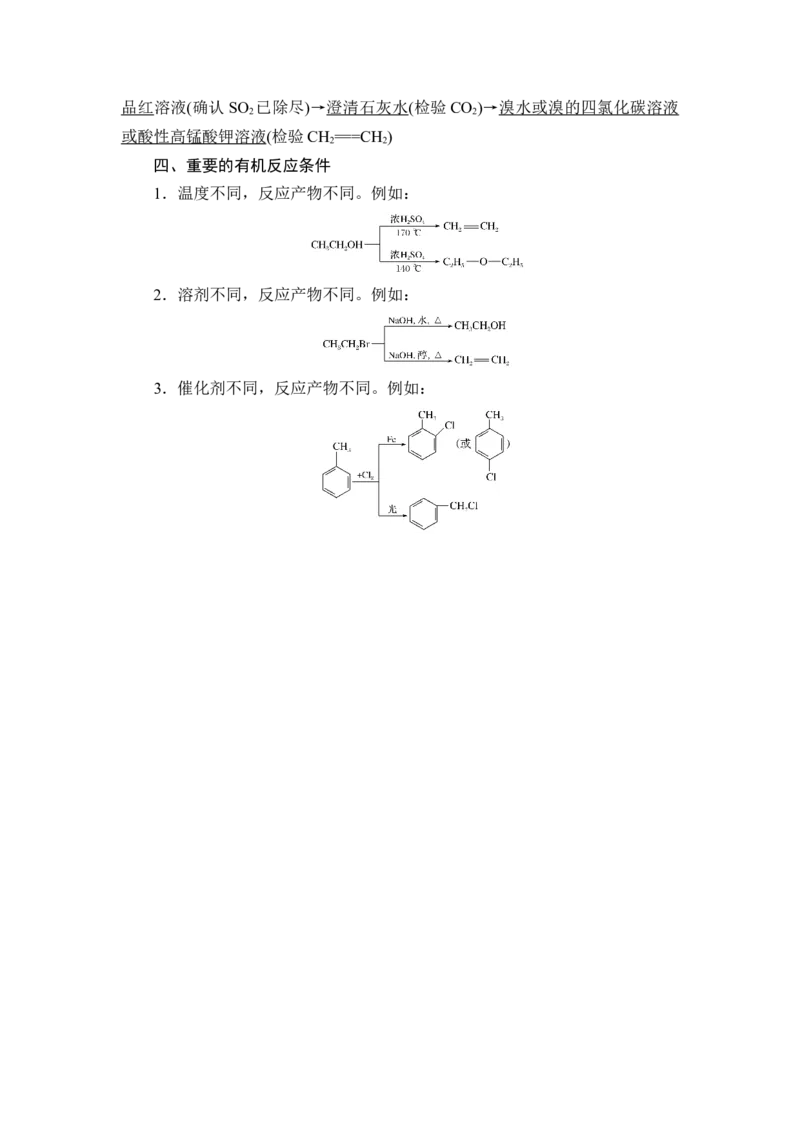
四、重要的有机反应条件
1.温度不同,反应产物不同。例如:
2.溶剂不同,反应产物不同。例如:
3.催化剂不同,反应产物不同。例如: