文档内容
第 1 讲 物质的量 气体摩尔体积
目录
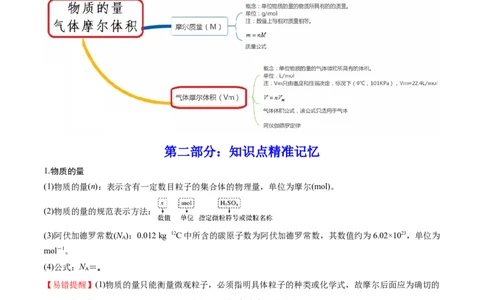
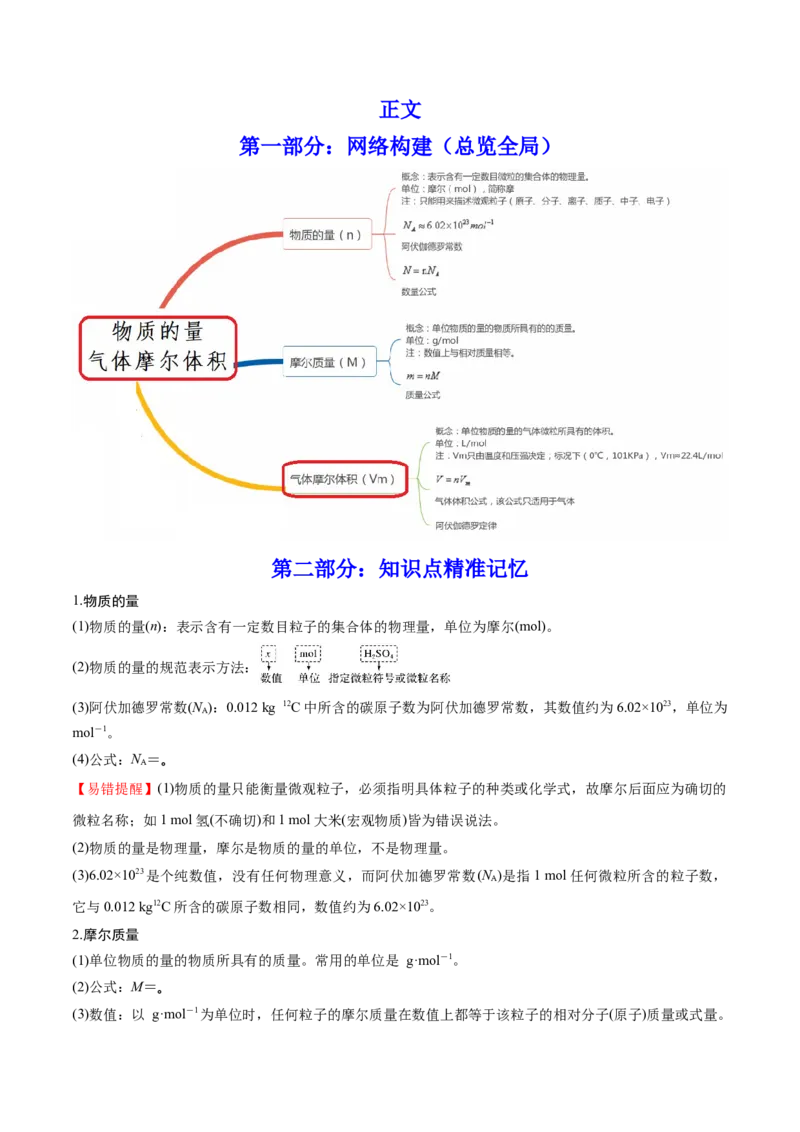
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点一 物质的量 摩尔质量
高频考点二 气体摩尔质量及相对分子质量的计算
高频考点三 有关气体分压的计算
高频考点四 有关气体体积的测定
高频考点五 阿伏加德罗定律及应用
高频考点六 有关阿伏加德罗常数的考查正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
1.物质的量
(1)物质的量(n):表示含有一定数目粒子的集合体的物理量,单位为摩尔(mol)。
(2)物质的量的规范表示方法:
(3)阿伏加德罗常数(N ):0.012 kg 12C中所含的碳原子数为阿伏加德罗常数,其数值约为6.02×1023,单位为
A
mol-1。
(4)公式:N =。
A
【易错提醒】(1)物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式,故摩尔后面应为确切的
微粒名称;如1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。
(2)物质的量是物理量,摩尔是物质的量的单位,不是物理量。
(3)6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子数,
A
它与0.012 kg12C所含的碳原子数相同,数值约为6.02×1023。
2.摩尔质量
(1)单位物质的量的物质所具有的质量。常用的单位是 g·mol-1。
(2)公式:M=。
(3)数值:以 g·mol-1为单位时,任何粒子的摩尔质量在数值上都等于该粒子的相对分子(原子)质量或式量。【易错提醒】(1)物质的量是计量微观粒子“集体”的物理量,只适用于微观粒子(即分子、原子、离子、
质子、中子、电子等),不适用于宏观物质。
(2)摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单位
是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位时,二者在数值上
相等。
(3)对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变化。
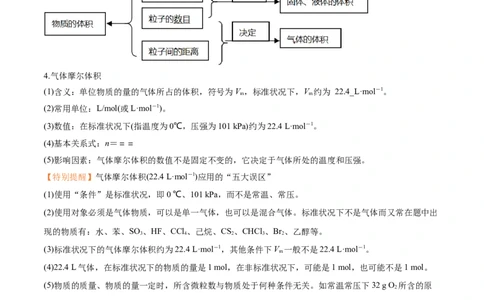
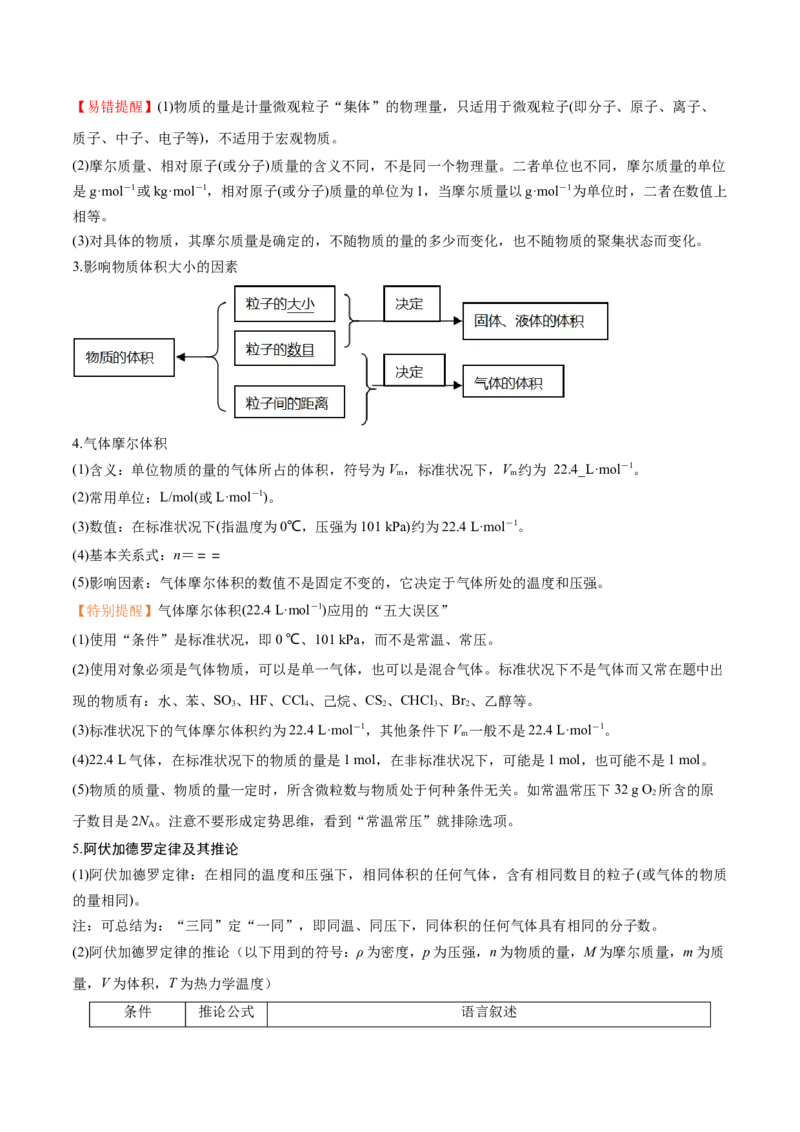
3.影响物质体积大小的因素
4.气体摩尔体积
(1)含义:单位物质的量的气体所占的体积,符号为V ,标准状况下,V 约为 22.4_L·mol-1。
m m
(2)常用单位:L/mol(或L·mol-1)。
(3)数值:在标准状况下(指温度为0℃,压强为101 kPa)约为22.4 L·mol-1。
(4)基本关系式:n===
(5)影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的温度和压强。
【特别提醒】气体摩尔体积(22.4 L·mol-1)应用的“五大误区”
(1)使用“条件”是标准状况,即0 ℃、101 kPa,而不是常温、常压。
(2)使用对象必须是气体物质,可以是单一气体,也可以是混合气体。标准状况下不是气体而又常在题中出
现的物质有:水、苯、SO 、HF、CCl 、己烷、CS、CHCl 、Br 、乙醇等。
3 4 2 3 2
(3)标准状况下的气体摩尔体积约为22.4 L·mol-1,其他条件下V 一般不是22.4 L·mol-1。
m
(4)22.4 L气体,在标准状况下的物质的量是1 mol,在非标准状况下,可能是1 mol,也可能不是1 mol。
(5)物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。如常温常压下32 g O 所含的原
2
子数目是2N 。注意不要形成定势思维,看到“常温常压”就排除选项。
A
5.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有相同数目的粒子(或气体的物质
的量相同)。
注:可总结为:“三同”定“一同”,即同温、同压下,同体积的任何气体具有相同的分子数。
(2)阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质
量,V为体积,T为热力学温度)
条件 推论公式 语言叙述T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比
T、p相同 = 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比
T、p、m相
= 同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
同
T、V、m相
= 同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反比
同
T、p、V相 同温同压下,同体积的任何气体的质量比等于它们的摩尔质量之比,
==
同 也等于它们的密度之比
【方法技巧】
1、记忆方法:三正比、二反比、一连比。
2、应用阿伏加德罗定律推论时可通过pV=nRT及n=、ρ=导出。
第三部分:典型例题剖析
高频考点一 物质的量 摩尔质量
例1、(2022·上海青浦·一模)下列对摩尔(mol)的有关说法中错误的是
A.摩尔是一个单位而非物理量
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1mol任何气体所含气体的分子数目都相等
D.0.5mol氦约含有1.204×1024个电子
【答案】D
【解析】A.摩尔是物质的量的单位,正确;B.摩尔用来计量微粒的量,可以是纯净物的微粒,也可以是混
合物的微粒,正确;C.气体物质的量相等,则气体的分子数目相等,正确;D.氦为单原子分子,0.5mol氦
含有0.5molHe原子,1个He原子含有2个电子,所以0.5mol氦约含有6.02×1023个电子,错误;故选D。
【名师点睛】本题考查的是物质中含有的各种粒子或微观结构的问题,一般来说先计算物质基本微粒中含
有多少个需要计算的粒子或微观结构,再乘以该物质的物质的量,就可以计算出相应结果,稀有气体分子
都是单原子分子。
【变式训练】下列有关叙述正确的是()
A.1 mol任何物质都含有6.02×1023个分子
B.硫酸的摩尔质量为98 g
C.2 mol H O是1 mol H O摩尔质量的2倍
2 2
D.摩尔是物质的量的单位
【解析】A.物质的构成粒子有分子、原子或离子,如水由 分子构成,1mol HO含有6.02×1023个分子,而
2NaCl由离 子构成,不存在分子,1mol NaCl含有1mol Na+和1mol Cl-,故A不正确;B.摩尔质量的单位
为g/mol,故B不正确;C.对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物
质的聚集状态而变化,故C不正确;D.摩尔是物质的量的单位,故D正确,本题选D。
【归纳总结】以物质的量为中心计算的思维模型:
高频考点二 气体摩尔质量及相对分子质量的计算
例2、按要求解答问题
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______,可能是_______气
体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(3)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是_______g·L-1。
②混合气体的平均摩尔质量是_______ g·mol-1。
【解析】(1)M=ρ×22.4 L·mol-1≈64 g·mol-1;根据相对分子质量,推测可能是二氧化硫气体。
(2) 。
(3)CO燃烧发生反应:2CO+O 2CO,CO的体积与生成CO 的体积相等,燃烧后CO 的总体积为
2 2 2 2
11.2 L,故18 g CO和CO 的混合气体的总体积为11.2 L,在标准状况下,18 g CO和CO 的混合气体的物
2 2
质的量为0.5 mol,设CO的物质的量为x mol,CO 的物质的量为y mol,
2
则 ,解得x=0.25,y=0.25。
①原混合气体的密度= = ≈1.61 g·L-1。
② =ρ·V=ρ·22.4 L·mol-1=1.61 g·L-1×22.4 L·mol-1≈36 g·mol-1。
【答案】(1)64 (2) SO 64 (3)①1.61 ②36
2【方法总结】求气体摩尔质量M及相对分子质量的常用方法:
(1)根据物质的质量(m)和物质的量(n):M=m/n。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M=N ·m/N。
A A
(3)根据标准状况下气体的密度ρ:
M=ρ×22.4 L·mol-1。
(4)根据气体的相对密度(D=ρ/ρ):M/M=D。
1 2 1 2
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=M×a%+M×b%+
1 2
M×c%……,a%、b%、c%……指混合物中各成分的物质的量分数(或体积分数)。
3
【变式训练】(2022·上海·模拟预测)打火机里装有液态的丙烷和丁烷。下列说法错误的是
A.打开打火机开关,分子间距变大
B.摩擦打火石,达到气体着火点
C. 丙烷完全燃烧需要空气约为
D.若n(丙烷):n(丁烷) ,该混合物的摩尔质量为
【答案】C
【解析】A.打开打火机开关,压强减小,燃料气化,分子间距变大,A正确;B.摩擦打火石,使温度达
到气体着火点,引燃燃料,B正确;C.没有说明具体的温度、压强,不能判断 丙烷完全燃烧需要空
气的体积,C错误;D.若n(丙烷):n(丁烷) ,该混合物的摩尔质量为
,D正确。故选C。
高频考点三 有关气体分压的计算
例3、F.Daniels等曾利用测压法在刚性反应器中研究了 时 分解反应:
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如表所示(t= 时,
2 2 4
完全分解):
t/min 0 40 80 160 260 1300 1700p/kPa
研究表明, 分解的反应速率v= 。 时,测得体系中
,则此时的 ___________________ ,v= ___________________ 。
【解析】根据物质反应时,压强比等于相应物质的化学计量数的比分析计算。在反应开始时,p =35.8
N2O5
kPa, 时,体系中 ,则根据方程式:2NO(g)=2NO(g)+O(g)中物质转化关系可
2 5 2 4 2
知NO(g)压强为p =2×2.9kPa=5.8 kPa,则此时p = 35.8 kPa-5.8 kPa=30.0 kPa,带入速率公式,可
2 4 N2O4(g) N2O5(g)
得v=2.0×10-3×30.0 kPa·min-1=6.0×10-2 kPa·min-1。
【答案】30.0 6.0×10-2
p n
【练后归纳】恒温恒容体系中(1)
1
=
1
;(2)p 分压=p ×n %;(3)用p 分压可代替n 列式计算。
p n A T A A A
2 2
【变式训练】已知N(g)+3H(g) 2NH (g) H<0,平衡时NH 的体积分数φ(NH )与氢氮比x(H 与N 的
2 2 3 3 3 2 2
物质的量比)的关系如图: △
a点总压为50MPa,T 时K=_______(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
2 p
【解析】根据题意得到氨气、氮气、氢气体积分数,再得到它们的压强,再根据压强平衡常数进行计算。
由题意可知,a点总压为50MPa,平衡时氢气与氮气之比为3:1,氨气的体积分数为0.2,则氮气的体积分
数为0.2,氢气的体积分数为0.6,氨气的体积分数为0.2,平衡时氮气分压为10MPa,氢气分压为
30MPa,氨气分压为10MPa,T 时 ,故答案为 。
2
【答案】
高频考点四 有关气体体积的测定
例4、(2020·安徽高三月考)现有一瓶NaO 因保管不善,部分变质转化为NaOH、NaCO 某小组设计实
2 2 2 3.
验,测定样品中NaO 的纯度。
2 2实验I:
连接好图1装置,检查气密性。在倒置量筒中充满水,准确称取10.0 g样品,加入锥形瓶中,并加入少量
MnO 粉末,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取量筒内气
2
体的数据。
(1)实验中加MnO 的目的是___________。
2
(2)若冷却至室温后水槽的图示如图2,则应进行的操作是___________。
小红提出实验I的误差较大,设计完成了实验II。
实验II:
连接好图3装置,检查气密性。在碱式滴定管中加入适量水,准确称取10.0 g样品,加入锥形瓶中,并加
入少量MnO 粉末。准确读取碱式滴定管读数V mL,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,
2 1
待整个装置冷却到室温,读取碱式滴定管读数V mL。
2
(3)导管a的作用:___________、___________。
(4)已知该实验条件下,气体摩尔体积为V L/mol,则样品中NaO 的纯度为___________。
m 2 2
(5)下列操作导致测量样品纯度偏大的是___________。
a.实验前读数时,俯视刻度线读数
b.实验结束读数时,未冷却至室温
c.实验结束读数时,仰视刻度线读数
d.实验结束读数时,量气装置中右侧液面高于左侧液面
【解析】实验I:
(1)过氧化钠与水反应生成的中间产物为过氧化氢,实验中加MnO 的目的是:二氧化锰具有催化作用,使
2
过氧化氢完全分解,以减小实验误差;
(2)由图2可知,若冷却到室温后,应进行的操作是上下移动量筒,至量筒内外液面高度相同,以减小读数
产生的误差;实验II:
(3)导管a的作用:平衡分液漏斗内上下气压,便于水的加入,同时消除加入水的体积对气体体积的影响,
使气体体积测量的更加准确;
(4)准确称取10.0 g样品,加入锥形瓶中,并加入少量MnO 粉末;准确读取碱式滴定管读数V mL,从分
2 1
液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取碱式滴定管读数V mL,产
2
生氧气的体积为(V - V )mL;气体的总量为: mol;根据反应:2NaO+2H O=4NaOH+O
1 2 2 2 2 2
可知,则样品中NaO 的纯度为: ×100%= ;
2 2
(5) a.实验前读数时,俯视刻度线读数,V 偏小,(V - V )偏小,测定结果偏低;b.实验结束读数时,未
1 1 2
冷却至室温,V 偏小,(V - V )偏大,测定结果偏高;c.实验结束读数时,仰视刻度线读数,V 偏大,
2 1 2 2
(V - V )偏小,测定结果偏低;d.实验结束读数时,量气装置中右侧液面高于左侧液面,气体压强偏大,
1 2
体积偏小,测定结果偏低;故选b。
【答案】(1)二氧化锰具有催化作用,使过氧化氢完全分解,以减小实验误差
(2)上下移动量筒,至量筒内外液面高度相同
(3)平衡分液漏斗上下气压,便于水的加入 消除加入水的体积影响,使气体体积测量的更加准确
(4)
(5)b
【方法技巧】气体体积的测量
气体体积的测定既可通过测量气体排出的液体体积来确定(二者体积值相等)。也可直接测量收集的气体体
积。测量气体体积的常用方法:
(1)直接测量法。如图A、B、C、D、E是5种直接测量气体体积的常见装置。A装置:测量前可先通过调整左右两管的高度使左管(有刻度)充满液体,且两管液面相平。
B装置:排液体法收集气体后直接测量其体积。
C装置:直接将一种反应物置于倒置的量筒中,另一反应物置于水槽中,二者反应产生的气体可以直接测
量。
D装置:用于测量混合气体中被吸收(或不被吸收)的气体的体积。读数时,球形容器和量气管液面相平,
量气管内增加的液体的体积等于被反应管吸收后剩余气体的体积。
(2)间接测量法。如图F装置是通过测量气体排出的液体体积来确定气体体积。
(3)消除外因(温度、压强)对气体体积的影响。
(4)读数时,请勿使用“视线与凹液面相切”之类的描述,“相切”表达语意不准确,仰视、俯视的情况下,
视线都能与凹液面相切。
【变式训练】铝镁合金是飞机制造、建筑等行业的重要材料。研究性学习小组的同学,为测定某铝镁合金
(不含其他元素)中铝的质量分数,设计了下列两种不同实验方案进行探究。填写下列空白:
(方案一)将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
(1)实验中发生反应的离子方程式是_____。
(2)称取10.8 g铝镁合金粉末样品,溶于体积为V、物质的量浓度为4.0 mol·L-1NaOH溶液中,为了保证铝
镁合金粉末能充分反应,则NaOH溶液的体积V≥_____mL。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得铝的质量分数将____(填“偏高”、“偏
低”或“无影响”)。
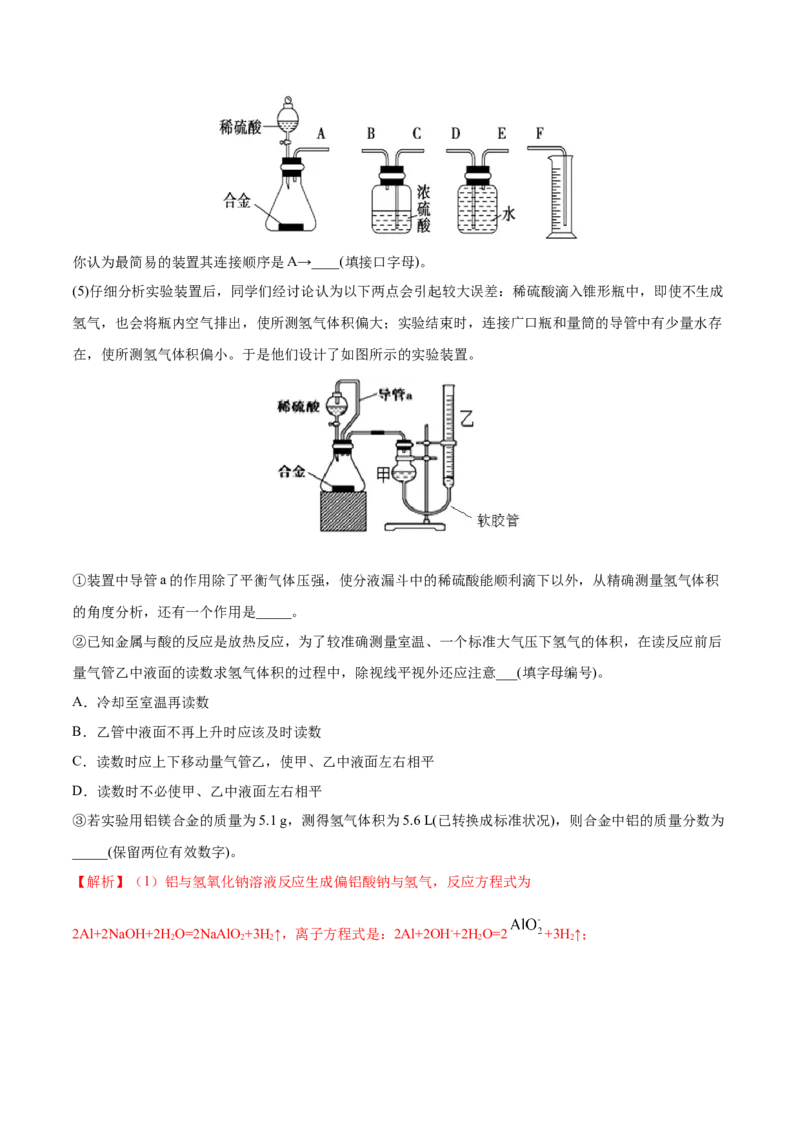
(方案二)将一定量铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
(4)同学们拟选用下列实验装置完成实验:你认为最简易的装置其连接顺序是A→____(填接口字母)。
(5)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成
氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存
在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。
①装置中导管a的作用除了平衡气体压强,使分液漏斗中的稀硫酸能顺利滴下以外,从精确测量氢气体积
的角度分析,还有一个作用是_____。
②已知金属与酸的反应是放热反应,为了较准确测量室温、一个标准大气压下氢气的体积,在读反应前后
量气管乙中液面的读数求氢气体积的过程中,除视线平视外还应注意___(填字母编号)。
A.冷却至室温再读数
B.乙管中液面不再上升时应该及时读数
C.读数时应上下移动量气管乙,使甲、乙中液面左右相平
D.读数时不必使甲、乙中液面左右相平
③若实验用铝镁合金的质量为5.1 g,测得氢气体积为5.6 L(已转换成标准状况),则合金中铝的质量分数为
_____(保留两位有效数字)。
【解析】(1)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为
2Al+2NaOH+2H O=2NaAlO +3H ↑,离子方程式是:2Al+2OH-+2H O=2 +3H ↑;
2 2 2 2 2(2)假设10.8g合金全是Al的质量,由关系式 ,解得V=100mL,为了
保证铝镁合金粉末能充分反应,则NaOH溶液的体积V≥100mL;
(3)镁上会附着偏铝酸钠等物质,未洗涤导致测得铝的质量分数将偏低;
(4)装置的组装顺序:合金与水反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短
进长出,利用增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,
故连接顺序为:(A)接(E)(D)接(F);
(5)①装置中导管a的作用是:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时
稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引
起的氢气体积误差;
②反应放热导致氢气的温度偏高,故应冷却后再进行读取氢气的体积,读取实验中生成氢气的体积时上下
移动量筒,使其中液面与广口瓶中液面相平,视线与凹液面的最低点水平读取氢气的体积;故选AC;
③设5.1 g镁铝合金中铝的质量为x,则产生的气体由Mg、Al与稀硫酸反应产生的,则由关系式:
,解得 , ,解得 ,
V+V =5.6L,解得x=2.7g,则合金中铝的质量分数为 。
1 2
【答案】(1)2Al+2OH-+2H O=2 +3H ↑(2)100(3)偏低(4)EDF
2 2
(5)①消除加入稀硫酸排开空气的体积对测量氢气体积所带来的误差②AC③53%
高频考点五 阿伏加德罗定律及应用
例5、(2021·山东·模拟预测)NH N(叠氮化铵)易发生分解反应生成N 和H,且两种气体的物质的量相等。
4 3 2 2
若得到NH N 的分解产物(简称a)28g,则下列关于a的说法错误的是
4 3
A.a中两种气体的体积(同温同压)比为1∶1
B.a中两种气体的质量比为14∶1
C.a的密度为1.25gL-1
D.a的平均摩尔质量为15gmol-1【答案】C
【解析】A.同温同压下,气体体积与物质的量成正比,两种气体的体积(同温同压)比为1∶1,A正确;
B. ,两种气体的质量比为14∶1,B正确;C.a气体的质量确定,但
一定物质的量的气体体积与温度、压强有关,所以密度比确定,C错误;D.分解产物质量为28g,两种气
体的物质的量相等则n =2× = mol, =15 gmol-1,D正确;答案选C。
总
【拓展提升】解答该题时要注意两个问题:
①温度问题:气体的压强与温度有关,物质的量不相等时,若温度也不相等,气体的压强有可能相等。
②O 和O 的组成问题:尽管O 和O 的物质的量不相等,但质量相等,而质量实际上是氧原子的质量,所
2 3 2 3
以二者所含原子数也相等。
【变式训练】(2021·山西吕梁·一模)三容器内分别装有相同压强下的NO、NO 、O,设三容器容积依次
2 2
为V、V、V,若将三气体混合于一个容积为V+V+V 的容器中后,倒立于水槽中,最终容器内充满
1 2 3 1 2 3
水。则V、V、V 之比可能是
1 2 3
A.2:4:5 B.9:5:8 C.7:2:6 D.4:5:6
【答案】B
【解析】若将三气体混合于一个容积为V+V+V 的容器中后,倒立于水槽中,最终容器内充满水,即三
1 2 3
种气体恰好完全反应生成HNO,根据同温同压下,气体的体积之比等于其物质的量之比,结合氧化还原
3
反应中得失电子总数相等,固有:3V+V =4V ,故3×2+4≠4×5,3×9+5=4×8,3×7+2≠4×6,3×4+5≠4×6,只
1 2 3
有B项符合题意,故答案为:B。
高频考点六 有关阿伏加德罗常数的考查
例6、(2021·福建·高考真题)设 为阿伏加德罗常数的值.下列说法正确的是
A. 所含极性共价键的数目为
B. 晶体中阴、阳离子总数为
C. 与足量 反应生成 的分子数为
D.电解熔融 制 ,电路中通过的电子数为【答案】B
【解析】A.没有标明气体的存在状态, 的物质的量不一定为0.5mol,故A错误;B.硫酸氢钠
晶体中存在钠离子和硫酸氢根离子,硫酸氢钠的摩尔质量为120g/mol,所以12g硫酸氢钠晶体的物质的量
为0.1mol,阴、阳离子总数为 ,故B正确;C.甲烷与足量氯气反应生成一氯甲烷、二氯甲烷、三
氯甲烷、四氯化碳和氯化氢,因此 与足量 反应生成 的分子数小于 ,故C错误;
D.电解熔融的氯化镁生成金属镁,镁由+2价降低到0价,因此1mol氯化镁完全电解生成金属镁,转移
2mol电子,电解熔融 制 (物质的量为0.1mol),电路中通过的电子数为 ,故D错误;
故选B。
【练后归纳】 阿伏加德罗常数判断的陷阱
陷阱一、抓“两看”,突破气体与状况陷阱
一看“气体”是否处在“标准状况”。
二看“标准状况”下,物质是否为“气体”[如CCl 、CHCl 、CHCl(注:CHCl为气体)、HO、溴、
4 3 2 2 3 2
SO 、己烷、苯、HF等在标准状况下均不为气体]。
3
陷阱二、排“干扰”,突破质量(或物质的量)与状况无关陷阱
给出非标准状况下气体的物质的量或质量,干扰正确判断,误以为无法求解物质所含的粒子数,实际上,
此时物质所含的粒子数与温度、压强等外界条件无关。
陷阱三、记“组成和结构”,突破陷阱
1.记特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、—OH、OH-等。
2 2
2.记最简式相同的物质,如NO 和NO、乙烯(C H)和丙烯(C H)等。
2 2 4 2 4 3 6
3.记摩尔质量相同的物质,如N、CO、C H 等。
2 2 4
4.记物质中所含化学键的数目,如1分子HO 、C H 中化学键的数目分别为3、3n+1。1 mol SiO 中
2 2 n 2n+2 2
含4 N 个Si—O键,1 mol Si中含Si—Si键数目为2N ,1 mol P (白磷)中含P—P键数目为6N 。
A A 4 A
陷阱四、理解反应原理,突破“隐含”陷阱
1.可逆反应不能进行到底,反应物不能全部转化为产物。常见的可逆反应:①2NO NO ;②Cl +
2 2 4 2
HO HCl+HClO;③NH +HO NH ·H O NH+OH-;④2SO +O 2SO ;⑤N +
2 3 2 3 2 2 2 3 23H 2NH 。
2 3
2.常温下,不能共存的气体间的反应
(1)HCl+NH ===NHCl;
3 4
(2)2NO+O===2NO;
2 2
(3)2H S+SO ===3S↓+2HO。
2 2 2
3.“隐含”浓度变化
(1)在MnO 与浓盐酸的反应中,随着反应的进行,浓盐酸逐渐变为稀盐酸,MnO 与稀盐酸不反应。
2 2
(2)在Cu与浓硫酸的反应中,随着反应的进行,浓硫酸逐渐变为稀硫酸,Cu与稀硫酸不反应。
(3)常温下,Fe在浓硝酸、浓硫酸中钝化,反应不具有持续性。
4.常在难电离、易水解的粒子数目上设题
判断电解质溶液中粒子数目时注意“三看”:一看是否有弱电解质的电离;二看是否有弱离子的水解;三
看是否指明了溶液的体积。弱电解质在水溶液中部分电离,可水解盐溶液中离子发生微弱水解,都会导致
相关粒子数目减少。
陷阱五、突破氧化还原反应中电子转移的陷阱
1.同一种物质在不同反应中做氧化剂、还原剂的判断,如(1)Cl 和Fe、Cu等反应,Cl 只做氧化剂,而Cl
2 2 2
和NaOH反应,Cl 既做氧化剂又做还原剂;(2)Na O 与CO 或HO反应,NaO 既做氧化剂又做还原剂,
2 2 2 2 2 2 2
而NaO 与SO 反应,NaO 只做氧化剂;(3)NO 和HO反应,NO 既做氧化剂又做还原剂。
2 2 2 2 2 2 2 2
2.反应物量不同,生成物所表现的化合价不同,如Fe和HNO 反应,Fe不足时生成Fe3+,Fe过量时生成
3
Fe2+。
3.氧化剂或还原剂不同,生成物所表现的化合价不同,如Cu和Cl 反应生成CuCl ,而Cu和S反应生成
2 2
Cu S。
2
4.注意氧化还原反应的顺序,如向FeI 溶液中通入Cl,Cl 先氧化I-,再氧化Fe2+。
2 2 2
陷阱六、突破电解质溶液中微粒数目上的陷阱
1.是否存在弱电解质的电离或盐类水解。
2.已知浓度,是否指明体积,是否能用公式“n=cV ”计算。
3.在判断溶液中微粒总数时,是否忽视溶剂水。
4.胶粒是大量难溶分子、离子的聚集体。
【变式训练】(2022·河北·石家庄二中模拟预测)用 表示阿伏加德罗常数的值,,下列有关叙述错误的
是A.含有3molC-C键的石墨中含有的碳原子数为2 N
A
B.标准状况下,22.4L 与22.4L 充分反应,生成的气体分子数大于N
A
C.分别向含0.1mol氯化铁的溶液中加入足量镁粉和铜粉,转移的电子数目均为0.1 N
A
D.用铅蓄电池电解氯化钠溶液,当消耗4mol硫酸时,产生 分子数目为2N
A
【答案】C
【解析】A.石墨结构中,一个碳原子与相邻的3个碳原子形成共价键,相当于一个共价键占 个碳原子,
则3molC-C键的石墨中含有的碳原子物质的量为3 =2mol,则含有的碳原子数为 ,故A正确;B.
标准状况下,22.4L 与22.4L 物质的量都是1mol,甲烷和氯气发生取代反应,生成的产物一氯甲烷
和HCl都是气体,根据取代反应的特点,生成的HCl分子是1 mol,在加上一氯甲烷分子,生成的气体分
子数大于N ,故B正确;C.0.1mol氯化铁的溶液中加入足量镁粉,发生的反应是Mg+ Fe3+=Mg2++ Fe,
A
Fe3+→Fe转移的电子数是0.3N ,而加入足量铜粉发生的反应是Cu+ 2Fe3+=Cu2++ 2Fe2+,Fe3+→Fe2+,则转移
A
的电子数是0.1N ,两者并不相等,故C错误;D.铅蓄电池的电池反应式是
A
Pb+PbO+2H SO =2PbSO+2H O, Pb元素的化合价由0价升到+2价,失去了2个电子,则当消耗4mol硫
2 2 4 4 2
酸时,转移的电子是4mol,同理,电解食盐水2NaCl + 2H O 2NaOH + Cl ↑ + H ↑,生成1mol氢气转
2 2 2
移了2mol电子,则用铅蓄电池电解氯化钠溶液,当消耗4mol硫酸时,转移的4mol电子电解食盐水时可生
成2mol氢气,产生 分子数目为2N ,故D正确;答案C。
A