文档内容
专题 03 铁 金属材料
第 07 练 铁及其化合物
1.铁元素是维持生命活动不可缺少的微量元素之一。铁的元素符号是( )
A.Mg B.Ca C.Fe D.Zn
2.下列反应不能通过化合反应直接制得的是( )
A.FeCl B.FeCl C.Fe(OH) D.Fe(OH)
2 3 3 2
3.既有氧化性,又有还原性的微粒是( )
A.Fe B.Fe2+ C.Fe3+ D.Cu2+
4.将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A.硫酸 B.氯水 C.硫酸锌 D.氯化铜
5.下列关于铁及其化合物的说法中,不正确的是( )
A.金属铁可被磁铁吸引 B.铁元素有可变化合价
C.铁丝在氯气中燃烧生成FeCl D.常温下铁片遇浓硫酸会发生钝化
2
6.某些补铁剂的成分中含有硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是(
)
A.稀盐酸 B.石蕊溶液 C.KSCN溶液 D.氯水
7.证明溶液中是否含Fe2+,操作的正确顺序是( )
①加入少量KMnO 溶液 ②滴入少量KSCN溶液 ③加入少量氯水
4
A.先①后② B.先②后① C.先②后③ D.先③后②
8.明代宋应星所著《天工开物》中有记载:“黄矾,乃即炼皂矾(FeSO ·7H O)炉侧土墙……刮取下来,
4 2
名日黄矾,染家用之。金色浅者涂炙,立成紫赤色也。”下列有关黄矾说法错误的是( )
A.黄矾的主要成分中含有Fe3+ B.黄矾在医药上可以作补铁剂
C.黄矾可以应用于印染工业 D.黄矾经火烤,立刻生成Fe O
2 3
9.下列关于铁及其化合物说法错误的是( )
A.Fe在潮湿的空气中容易生锈 B.丹霞地貌的岩层因含Fe O 而呈红色
2 3
C.FeO中铁元素的化合价呈+2价 D.含Fe2+盐溶液遇KSCN溶液显红色
10.印刷电路板的制作原理是用足量的FeCl 溶液腐蚀覆铜板上不需要的铜箔。下列说法正确的是(
3
)A.用KSCN溶液可检验腐蚀后溶液中的Fe2+
B.Fe3+能溶解Cu,说明金属性Cu>Fe
C.当有1mol电子转移时,溶液中Cu2+增加1mol
D.腐蚀后溶液中的金属阳离子有Fe3+、Fe2+、Cu2+
11.贫血是一种常见的疾病,其中缺铁性贫血是贫血中最常见的类型,通常补铁剂会与维生素C同服。
下列有关叙述中错误的是( )
A.补铁剂中的铁以Fe3+形式存在 B.铁是人体必需的微量元素
C.补铁剂搭配的维生素C具有还原性 D.Fe2+具有还原性,能被氧化成Fe3+
12.下列有关铁和铁的化合物的说法正确的是( )
A.氧化亚铁与水反应可以生成氢氧化亚铁 B.铁在纯氧中燃烧生成三氧化二铁
C.Fe(OH) 在空气中加强热生成Fe O D.Fe O 是FeO和Fe O 的混合物
3 2 3 3 4 2 3
13.关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的下列说法中不正确的是( )
A.铁元素化合价不完全相同 B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体 D.铁在氧气中燃烧的产物为黑色固体
1.铁是人类应用较早,当前应用量最大的金属元素。下列有关铁及其化合物的有关说法中正确的是
( )
A.赤铁矿的主要成分是Fe O
3 4
B.铁与水蒸气在高温下的反应产物为Fe O 和H
2 3 2
C.除去FeCl 溶液中的FeCl 杂质可以向溶液中加入铁粉,然后过滤
2 3
D.Fe3+与KSCN产生血红色沉淀
2.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉
淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
A.Fe(OH) Fe O B.Fe(OH) Fe O C.Fe(OH) Fe(OH) D.Fe(OH) Fe O
3 2 3 2 2 3 2 3 2 3 4
3.铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发生钝化时,可生成一种化学式为
3
Fe O 的化合物,它可以看作由FeO和Fe O 组成的复杂氧化物。该化合物可以表示为( )
8 11 2 3
A.FeO·3Fe O B.2FeO·3Fe O C.FeO·2Fe O D.2FeO·Fe O
2 3 2 3 2 3 2 3
4.下列反应的离子方程式正确的是( )
A.将铜屑加入Fe3+溶液中:2Fe3++Cu===2Fe2++Cu2+
B.将磁性氧化铁溶于盐酸:Fe O+8H+===3Fe3++4HO
3 4 2
C.FeCl 酸性溶液放在空气中变质:2Fe2++4H++O===2Fe3++2HO
2 2 2
D.将铁粉加入稀硫酸中:2Fe+6H+===2Fe3++3H↑
2
5.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一,对下列实验事实的解释正确的是( )
操作、现象 解释
A. 向KI淀粉溶液中加入FeCl 溶液,溶液变蓝 Fe3+能与淀粉发生显色反应
3
B. 常温下,可以用铁质容器存放浓硫酸 常温下,铁与浓硫酸不反应
说明Fe置换出硝酸中的氢,
C. 向稀硝酸中加入少量铁粉,有气泡产生
生成了氢气
新制Fe(OH) 露置于空气中一段时间,物质 说明Fe(OH) 易被O 氧化成
D. 2 2 2
变成了红褐色 Fe(OH)
3
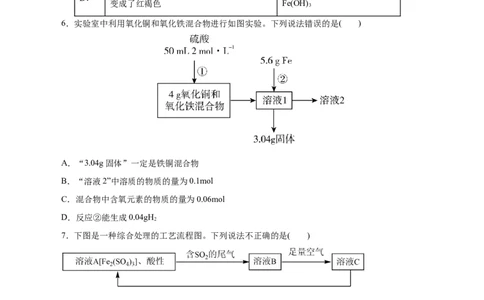
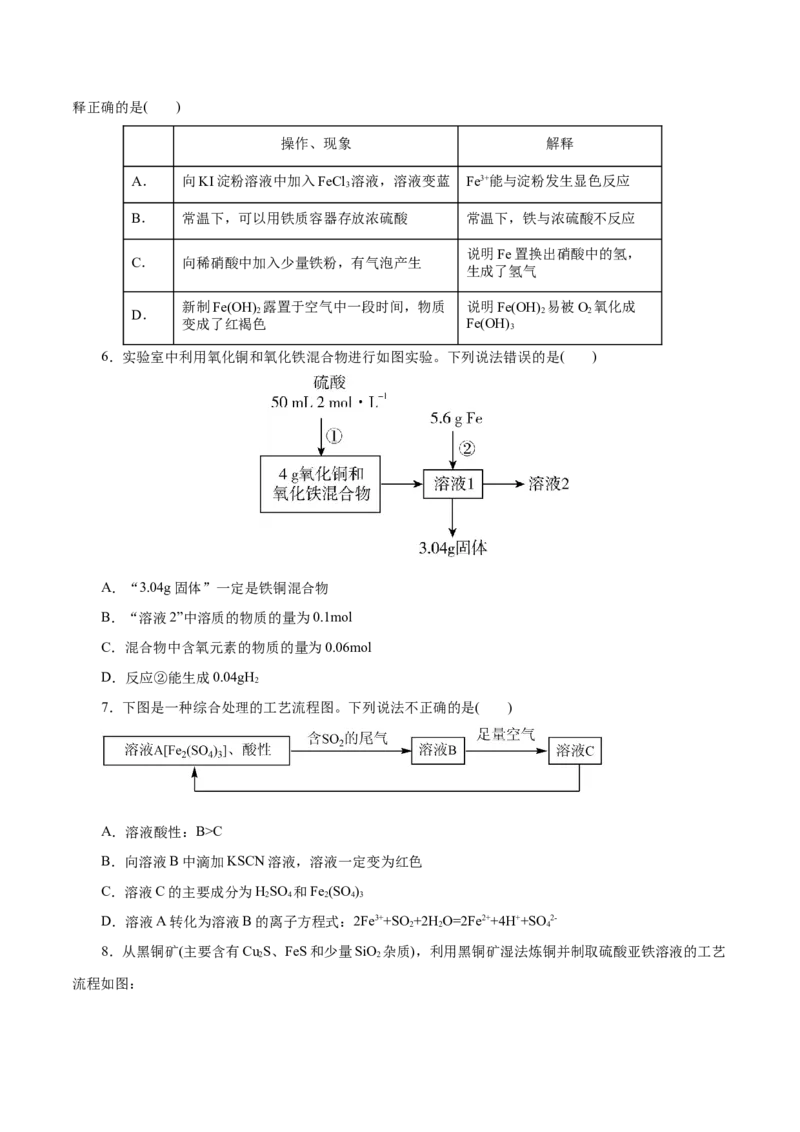
6.实验室中利用氧化铜和氧化铁混合物进行如图实验。下列说法错误的是( )
A.“3.04g固体”一定是铁铜混合物
B.“溶液2”中溶质的物质的量为0.1mol
C.混合物中含氧元素的物质的量为0.06mol
D.反应②能生成0.04gH
2
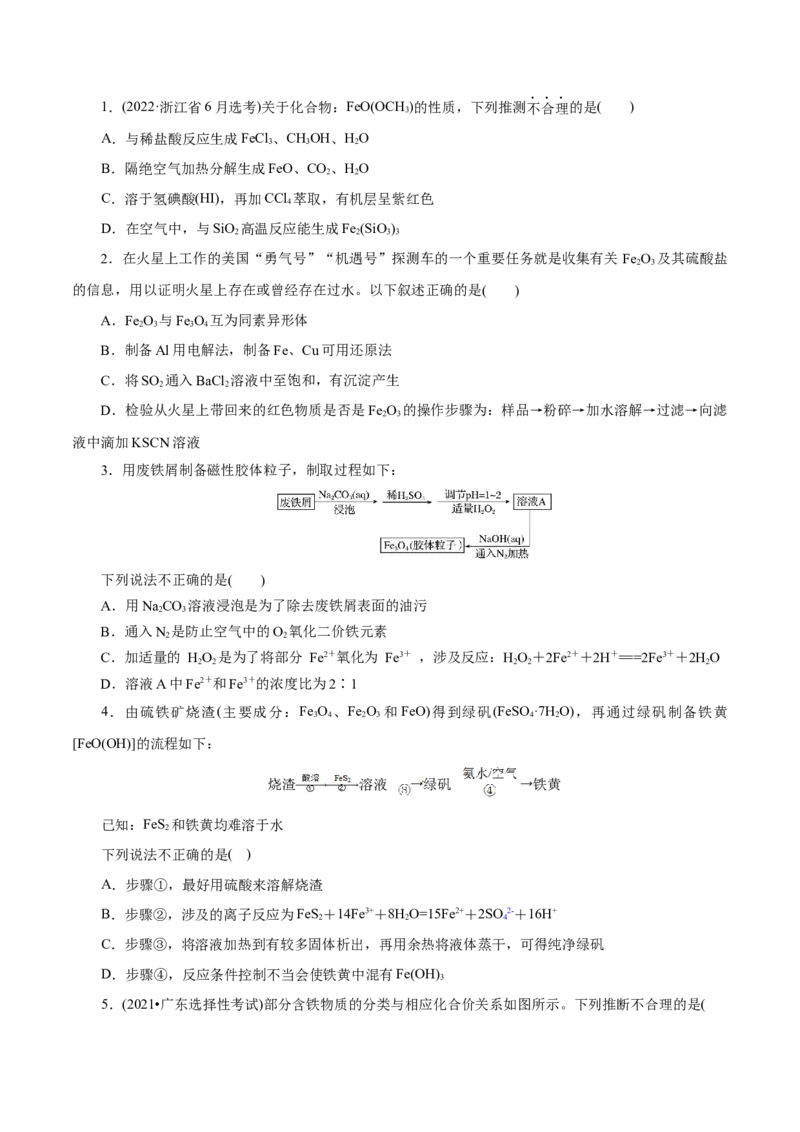
7.下图是一种综合处理的工艺流程图。下列说法不正确的是( )
A.溶液酸性:B>C
B.向溶液B中滴加KSCN溶液,溶液一定变为红色
C.溶液C的主要成分为HSO 和Fe (SO )
2 4 2 4 3
D.溶液A转化为溶液B的离子方程式:2Fe3++SO+2H O=2Fe2++4H++SO2-
2 2 4
8.从黑铜矿(主要含有Cu S、FeS和少量SiO 杂质),利用黑铜矿湿法炼铜并制取硫酸亚铁溶液的工艺
2 2
流程如图:下列说法错误的是( )
A.黑铜矿在“高温煅烧”前需要经过粉碎处理
B.“高温煅烧”时,每生成1molSO ,转移6mol电子
2
C.酸浸时,应加入稍过量的稀硫酸,提高浸出率
D.固体X可以为铁粉,试剂Y可以为CuSO 溶液
4
9.FeSO 在工业上用途广泛,通过下列实验探究FeSO 溶液性质
4 4
实验l:向FeSO 溶液中滴入少许NaCO 溶液,出现白色沉淀。
4 2 3
实验2:向FeSO 溶液中加入NaOH溶液,出现白色絮状沉淀,渐变成灰绿色,最后成红褐色沉淀。
4
实验3:向FeSO 溶液中滴入KSCN溶液,出现红色。
4
实验4:向FeSO 溶液中滴入酸性KMnO 溶液,KMnO 溶液褪色。
4 4 4
下列说法不正确的是( )
A.实验1中发生的离子反应为:Fe2++CO 2-=FeCO ↓
3 3
B.实验2现象说明Fe(OH) 具有还原性
2
C.实验3现象说明FeSO 氧化变质
4
D.实验4现象说明FeSO 具有漂白性
4
10.现有16.8gFe粉,加入VL1mol·L-1HNO 溶液使其恰好完全溶解后,向所得溶液中继续滴加稀硫酸,
3
至不再产生气泡。下列说法正确的是( )
A.反应过程中产生气体的总体积为6.72L
B.V=0.8
C.该实验可以证明Fe2+与NO -不能大量共存
3
D.滴加稀硫酸时,产生的气体为SO
2
11.1.12g铁粉加入25mL2mol/L的三氯化铁溶液中,充分反应后,其结果不可能的是( )
A.铁有剩余
B.往溶液中滴入无色KSCN溶液,溶液显红色
C.氧化产物和还原产物的物质的量之比为2∶1
D.Fe2+和Fe3+的物质的量之比为6∶1
12.FeCO 与砂糖混用可以作补血剂,实验室里制备FeCO 的流程如图所示,下列说法不正确的是(
3 3)
A.产品FeCO 在空气中高温分解不能得到纯净的FeO
3
B.沉淀过程中没有CO 气体放出
2
C.过滤操作常用的玻璃仪器有烧杯、漏斗和玻璃棒
D.可利用KSCN溶液检验FeSO 溶液是否变质
4
13.为了比较铁和铜金属活动性强弱,某研究小组的同学设计了如下一些方案,并将实验结果记录如
下:
方案 现象或产物
①将铁片置于CuSO 溶液中 铁片上有亮红色物质析出
4
②将铁丝和铜丝分别在氯气中燃烧 产物分别为FeCl 和CuCl
3 2
③将铁片和铜片分别放入热浓硫酸中 产物分别为Fe (SO ) 和CuSO
2 4 3 4
④将铁片和铜片分别置于稀硫酸溶液中 铁片上有气泡,铜片上不产生气泡
⑤将铁片和铜片同时插入盛有稀硫酸
铁片溶解,铜片上有气泡产生
的烧杯中,并用导线连接
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案一共有( )
A.2种 B.3种 C.4种 D.5种
14.对印刷电路板制作过程中产生废液X进行回收处理,流程如图所示。下列说法错误的是( )
A.若废液X中含 ,则X中存在
B.操作①的名称为过滤,需要用到的玻璃仪器有烧杯、漏斗和玻璃棒
C.可以用酸性KMnO 溶液检验溶液A中是否含Fe2+
4
D.若向溶液B中加入少量铁粉,发生的反应为2Fe+6H+=2Fe3++3H ↑
21.(2022·浙江省6月选考)关于化合物:FeO(OCH)的性质,下列推测不合理的是( )
3
A.与稀盐酸反应生成FeCl 、CHOH、HO
3 3 2
B.隔绝空气加热分解生成FeO、CO、HO
2 2
C.溶于氢碘酸(HI),再加CCl 萃取,有机层呈紫红色
4
D.在空气中,与SiO 高温反应能生成Fe (SiO)
2 2 3 3
2.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关 Fe O 及其硫酸盐
2 3
的信息,用以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.Fe O 与Fe O 互为同素异形体
2 3 3 4
B.制备Al用电解法,制备Fe、Cu可用还原法
C.将SO 通入BaCl 溶液中至饱和,有沉淀产生
2 2
D.检验从火星上带回来的红色物质是否是Fe O 的操作步骤为:样品→粉碎→加水溶解→过滤→向滤
2 3
液中滴加KSCN溶液
3.用废铁屑制备磁性胶体粒子,制取过程如下:
下列说法不正确的是( )
A.用NaCO 溶液浸泡是为了除去废铁屑表面的油污
2 3
B.通入N 是防止空气中的O 氧化二价铁元素
2 2
C.加适量的 HO 是为了将部分 Fe2+氧化为 Fe3+ ,涉及反应:HO+2Fe2++2H+===2Fe3++2HO
2 2 2 2 2
D.溶液A中Fe2+和Fe3+的浓度比为2∶1
4.由硫铁矿烧渣(主要成分:Fe O 、Fe O 和FeO)得到绿矾(FeSO ·7H O),再通过绿矾制备铁黄
3 4 2 3 4 2
[FeO(OH)]的流程如下:
烧渣 溶液 绿矾 铁黄
已知:FeS 和铁黄均难溶于水
2
下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS+14Fe3++8HO=15Fe2++2SO 2-+16H+
2 2 4
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)
3
5.(2021•广东选择性考试)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是()
A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在b→c→d→e→b的循环转化关系
6.(2022•湖南选择性考试)为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为
3 3 2 3
)。
实验 操作与现象
① 在 水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;
3 2 3
②
再滴加K[Fe(CN) ]溶液,产生蓝色沉淀。
3 6
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;
2 3 3
将上述混合液分成两份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生
③ 3 6
成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO 2-对Fe3+的水解反应无影响,但对还原反应有影响
3
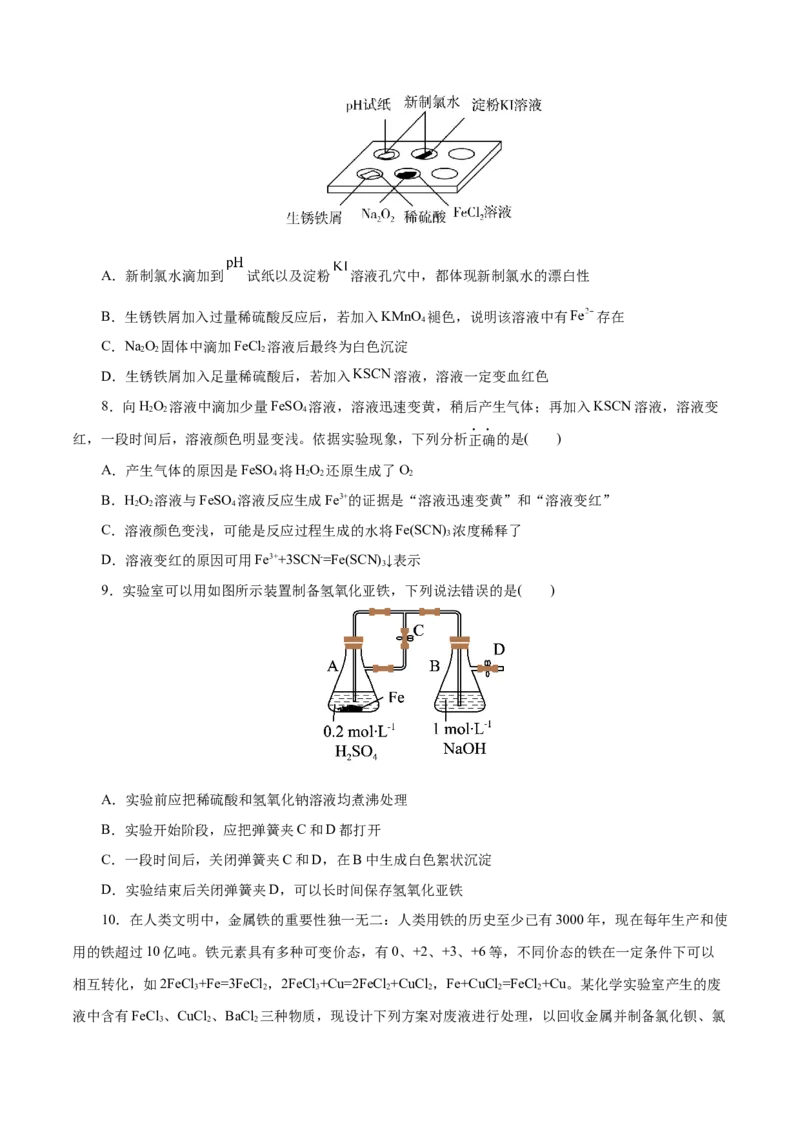
7.实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象。图中
所示的实验点滴板上描述的实验现象或推论正确的是( )A.新制氯水滴加到 试纸以及淀粉 溶液孔穴中,都体现新制氯水的漂白性
B.生锈铁屑加入过量稀硫酸反应后,若加入KMnO 褪色,说明该溶液中有 存在
4
C.NaO 固体中滴加FeCl 溶液后最终为白色沉淀
2 2 2
D.生锈铁屑加入足量稀硫酸后,若加入 溶液,溶液一定变血红色
8.向HO 溶液中滴加少量FeSO 溶液,溶液迅速变黄,稍后产生气体;再加入KSCN溶液,溶液变
2 2 4
红,一段时间后,溶液颜色明显变浅。依据实验现象,下列分析正确的是( )
A.产生气体的原因是FeSO 将HO 还原生成了O
4 2 2 2
B.HO 溶液与FeSO 溶液反应生成Fe3+的证据是“溶液迅速变黄”和“溶液变红”
2 2 4
C.溶液颜色变浅,可能是反应过程生成的水将Fe(SCN) 浓度稀释了
3
D.溶液变红的原因可用Fe3++3SCN-=Fe(SCN) ↓表示
3
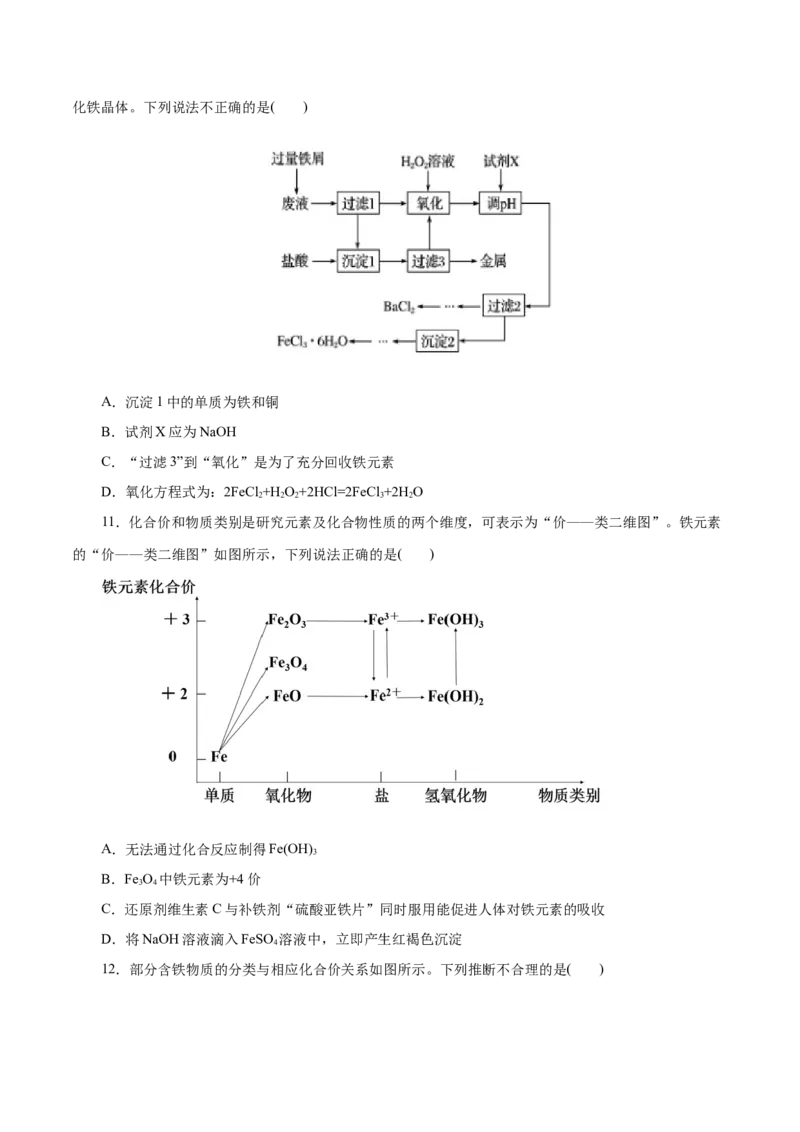
9.实验室可以用如图所示装置制备氢氧化亚铁,下列说法错误的是( )
A.实验前应把稀硫酸和氢氧化钠溶液均煮沸处理
B.实验开始阶段,应把弹簧夹C和D都打开
C.一段时间后,关闭弹簧夹C和D,在B中生成白色絮状沉淀
D.实验结束后关闭弹簧夹D,可以长时间保存氢氧化亚铁
10.在人类文明中,金属铁的重要性独一无二:人类用铁的历史至少已有3000年,现在每年生产和使
用的铁超过10亿吨。铁元素具有多种可变价态,有0、+2、+3、+6等,不同价态的铁在一定条件下可以
相互转化,如2FeCl +Fe=3FeCl ,2FeCl +Cu=2FeCl +CuCl ,Fe+CuCl =FeCl +Cu。某化学实验室产生的废
3 2 3 2 2 2 2
液中含有FeCl 、CuCl 、BaCl 三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯
3 2 2化铁晶体。下列说法不正确的是( )
A.沉淀1中的单质为铁和铜
B.试剂X应为NaOH
C.“过滤3”到“氧化”是为了充分回收铁元素
D.氧化方程式为:2FeCl +H O+2HCl=2FeCl +2H O
2 2 2 3 2
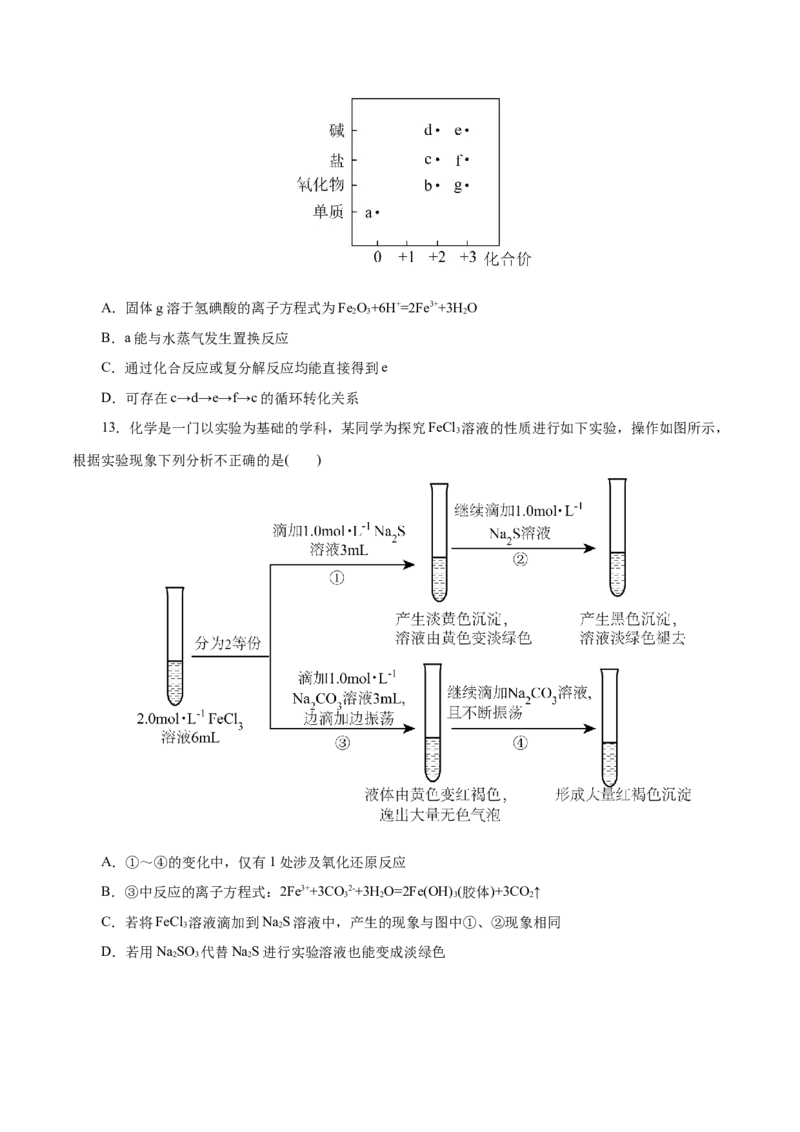
11.化合价和物质类别是研究元素及化合物性质的两个维度,可表示为“价——类二维图”。铁元素
的“价——类二维图”如图所示,下列说法正确的是( )
A.无法通过化合反应制得Fe(OH)
3
B.Fe O 中铁元素为+4价
3 4
C.还原剂维生素C与补铁剂“硫酸亚铁片”同时服用能促进人体对铁元素的吸收
D.将NaOH溶液滴入FeSO 溶液中,立即产生红褐色沉淀
4
12.部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )A.固体g溶于氢碘酸的离子方程式为Fe O+6H+=2Fe3++3H O
2 3 2
B.a能与水蒸气发生置换反应
C.通过化合反应或复分解反应均能直接得到e
D.可存在c→d→e→f→c的循环转化关系
13.化学是一门以实验为基础的学科,某同学为探究FeCl 溶液的性质进行如下实验,操作如图所示,
3
根据实验现象下列分析不正确的是( )
A.①~④的变化中,仅有1处涉及氧化还原反应
B.③中反应的离子方程式:2Fe3++3CO 2-+3H O=2Fe(OH) (胶体)+3CO ↑
3 2 3 2
C.若将FeCl 溶液滴加到NaS溶液中,产生的现象与图中①、②现象相同
3 2
D.若用NaSO 代替NaS进行实验溶液也能变成淡绿色
2 3 2