文档内容
第 13 讲 原子结构 化学键
1.核泄漏地区可检测到的放射性元素有137Cs、134Cs、131I等。下列叙述正确的是( )
A.Cs和Cs形成的单质物理性质相同
B.Cs比I多3个中子
C.Cs和Cs形成的单质化学性质相同
D.Cs与Cs都是铯的同素异形体2.Tc是医用放射性同位素。下列关于Tc的叙述正确的是( )
A.中子数是56 B.质量数是43
C.质子数是56 D.原子序数是99
3.下列说法中肯定错误的是( )
A.某原子K层上只有一个电子
B.某原子M层上电子数为L层电子数的4倍
C.某离子M层上和L层上的电子数均为K层的4倍
D.阳离子的最外层电子数可能为2,也可能为8
4.下列关于C 、H、O、N等微粒的叙述错误的是( )
60 3
A.碳、氢、氧、氮元素中各含有不同核素
B.H 与H 化学性质相同,互为同位素
3 2
C.C 与N中都含有共价键
60
D.KO 属于含有共价键的离子化合物
2
5.关于氢键,下列说法正确的是( )
A.氢键比范德华力强,所以它属于化学键
B.分子间形成的氢键使物质的熔点和沸点升高
C.由于冰中水分子间存在氢键,所以其密度大于液态水
D.HO是一种稳定的化合物,这是由于HO之间形成氢键所致
2 2
6.三硫化磷(P S)可用于制造火柴,分子结构如图所示。下列说法不正确的是( )
4 3
A.PS 中磷元素为+3价
4 3
B.PS 属于共价化合物
4 3
C.PS 含有非极性键
4 3
D.1 mol P S 分子含有9 mol共价键
4 37.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的核外电子结
构与氦相同,b和c的次外层有8个电子,c-和d+的核外电子结构相同。下列叙述正确的是( )
A.a元素的三种核素的氧化物互为同素异形体
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a与b、c、d均能形成18电子微粒
8.用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答下
列问题:
(1)A元素是________、B元素是________、C元素是________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是________。
(4)F是由两种元素组成的三原子分子,其分子式是________。
(5)G分子中含有4个原子,其分子式是________。
(6)H分子中含有8个原子,其分子式是________。
1.在当前空气污染日益严重,人们的健康受到来自空气威胁的情况下,“空气罐头”应运而生。16O
和 18O是氧元素的两种核素,下列说法正确的是( )
A.16O 与 18O 互为同素异形体
2 2
B.16O与 18O核外电子排布方式不同
C.通过化学变化可以实现16O与 18O间的相互转化
D.16O与 18O互为同位素
2.某元素的一个原子形成的离子可表示为 Xn-,下列说法正确的是( )
A.Xn-含有的中子数为a+b
B.Xn-含有的电子数为a-n
C.X原子的质量数为a+b+n
D.1个X原子的质量约为 g
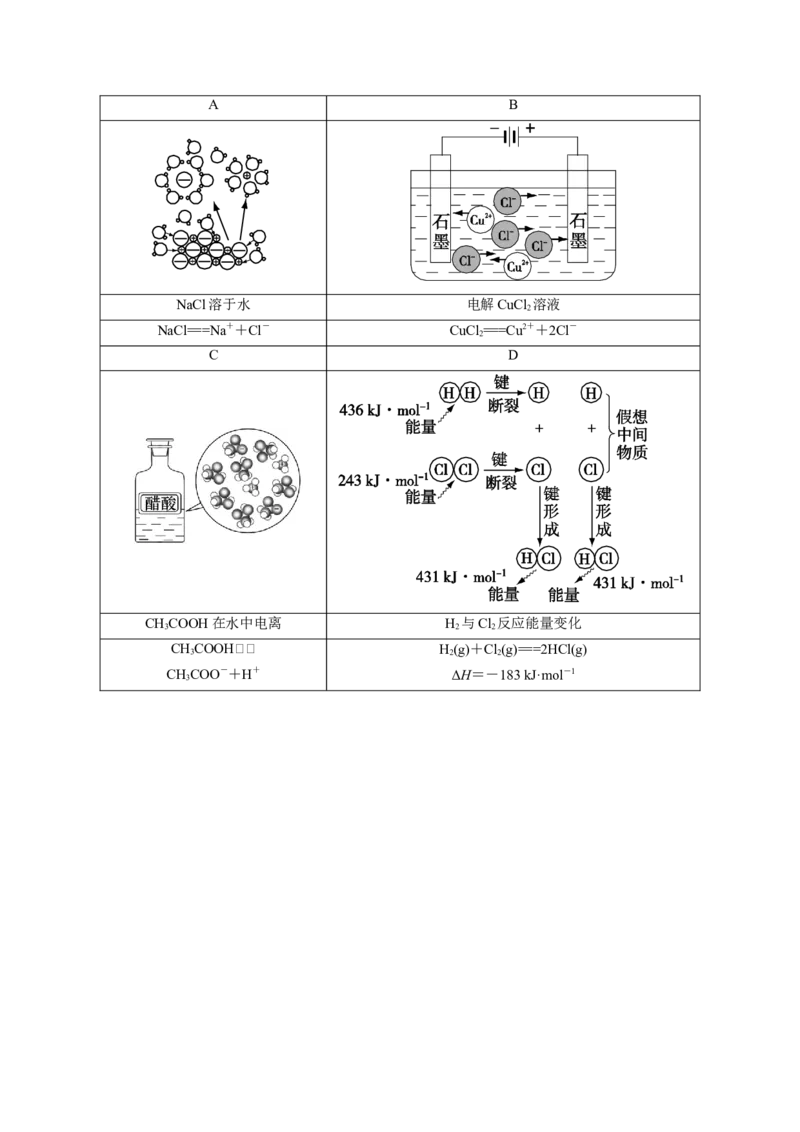
3.下列物质中,既属于离子化合物又属于电解质且含有极性键的是( )
A.NaO B.HSO
2 2 2 4
C.CS D.BaSO
2 44.利用固体表面催化工艺进行NO分解的过程如图所示。下列说法不正确的是( )
A.NO属于共价化合物
B.O 含有非极性共价键
2
C.过程②吸收能量,过程③释放能量
D.标准状况下,NO分解生成11.2 L N 转移电子数为N
2 A
5.NaN是离子化合物,它和水作用可产生NH 。下列叙述正确的是( )
3 3
A.Na+和N3-的电子结构都与氖原子相同
B.Na+的半径大于N3-的半径
C.NaN与足量的盐酸反应后生成一种盐
3
D.在NaN与水的反应中,NaN作还原剂
3 3
6.全氮类物质具有高密度、超高能量及爆轰产物无污染等优点。中国科学家成功合成全氮阴离子 N,
N是制备全氮类物质,NN的重要中间体。下列说法中不正确的是( )
A.全氮类物质属于绿色能源
B.每个N中含有35个质子
C.,NN属于离子化合物
D.,NN结构中含共价键和离子键
7.下表中相关物质的信息都正确的一项是( )
与性质相对应
选项 化学式 电子式或含有的化学键类型 物质的性质
的用途
A NaClO 离子键、共价键 强氧化性 消毒剂
不稳定,易
B HO 医用消毒剂
2 2 分解
水溶液呈弱
C NH 共价键 工业制硝酸
3 碱性
D NaHCO 离子键 受热易分解 泡沫灭火器
3
【答案】ANaClO中钠离子和次氯酸根离子之间存在离子键,O、Cl原子之间存在共价键,次氯酸钠具有强氧化性,所以可作消毒剂,A正确;HO 是共价化合物,电子式为 ,HO 具有强
2 2 2 2
氧化性,可用于消毒,B错误;NH 在工业上用于制取硝酸是利用其还原性,与其水溶液呈碱性无关,C
3
错误;碳酸氢钠中既存在离子键又存在共价键,碳酸氢钠可与铝离子发生双水解反应生成二氧化碳,故可
用于灭火,与其稳定性强弱无关,D错误。
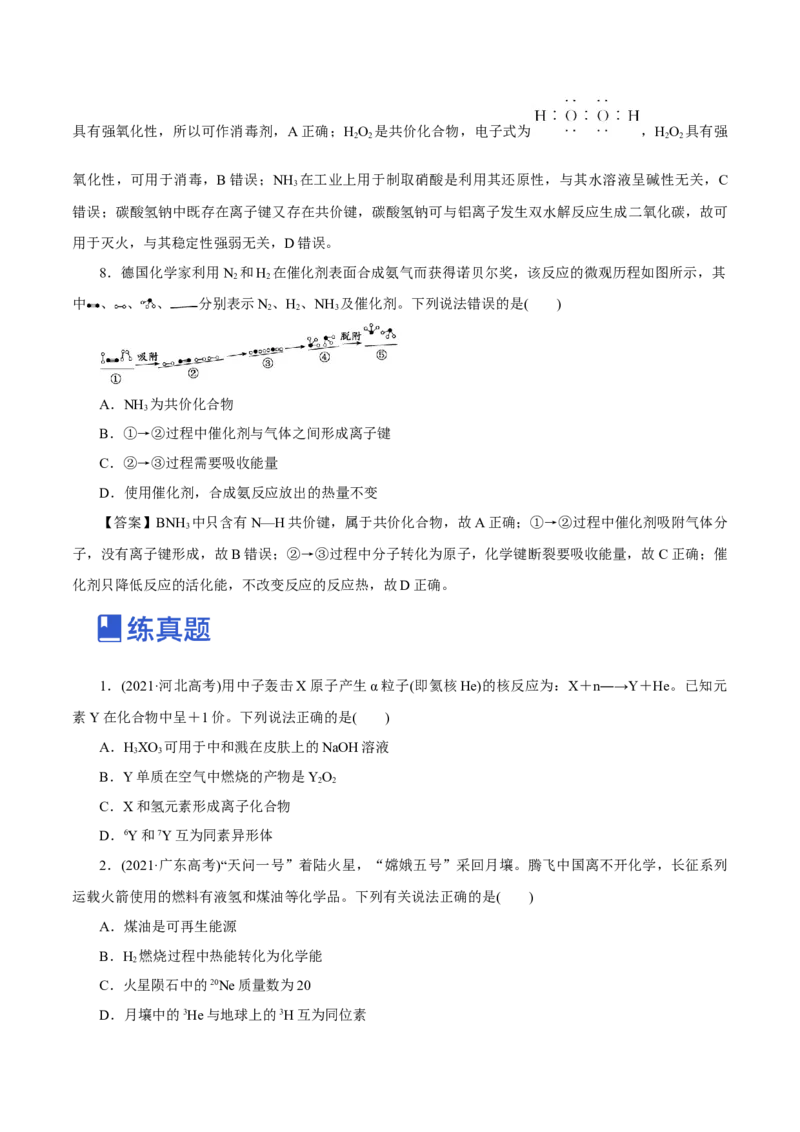
8.德国化学家利用N 和H 在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程如图所示,其
2 2
中 、 、 、 分别表示N、H、NH 及催化剂。下列说法错误的是( )
2 2 3
A.NH 为共价化合物
3
B.①→②过程中催化剂与气体之间形成离子键
C.②→③过程需要吸收能量
D.使用催化剂,合成氨反应放出的热量不变
【答案】BNH 中只含有N—H共价键,属于共价化合物,故A正确;①→②过程中催化剂吸附气体分
3
子,没有离子键形成,故B错误;②→③过程中分子转化为原子,化学键断裂要吸收能量,故C正确;催
化剂只降低反应的活化能,不改变反应的反应热,故D正确。
1.(2021·河北高考)用中子轰击X原子产生α粒子(即氦核He)的核反应为:X+n―→Y+He。已知元
素Y在化合物中呈+1价。下列说法正确的是( )
A.HXO 可用于中和溅在皮肤上的NaOH溶液
3 3
B.Y单质在空气中燃烧的产物是YO
2 2
C.X和氢元素形成离子化合物
D.6Y和7Y互为同素异形体
2.(2021·广东高考)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列
运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是( )
A.煤油是可再生能源
B.H 燃烧过程中热能转化为化学能
2
C.火星陨石中的20Ne质量数为20
D.月壤中的3He与地球上的3H互为同位素3.(2020·全国Ⅰ卷)1934年约里奥—居里夫妇在核反应中用α粒子(即氦核He)轰击金属原子X,得到
核素Y,开创了人造放射性核素的先河:
其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26 B.X、Y均可形成三氯化物
C.X的原子半径小于Y的 D.Y仅有一种含氧酸
4.(2020·全国卷Ⅰ)1934年约里奥-居里夫妇在核反应中用α粒子(即氦核He)轰击金属原子W X,得
Z
到核素Y,开创了人造放射性核素的先河:
W X+He―→Y+n
Z
其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.W X的相对原子质量为26
Z
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
5.(2020·浙江7月选考)下列说法正确的是( )
A.35Cl和37Cl是两种不同的元素
B.单晶硅和石英互为同素异形体
C.HCOOH和HOCH CHO互为同系物
2
D.H与Na在元素周期表中处于同一主族
6.(2019上海高考)元素Og中文名为 ,是一种人工合成的稀有气体元素,下列说法正确的是( )
A.核外电子数是118 B.中子数是295
C.质量数是177 D.第六周期0族元素
7.(2019北京理综)2019年是元素周期表发表150周年。期间科学家为完善周期表做出了不懈努力。中
国科学院院士张青莲教授曾主持测定了铟( In)等9种元素相对原子质量的新值,被采用为国际新标准。铟
49
与铷( Rb)同周期。下列说法不正确的是( )
37
A.In是第五周期第ⅢA族元素
B.In的中子数与电子数的差值为17
C.原子半径:In>Al
D.碱性:In(OH) >RbOH
3
8.(2019浙江高考)下列说法正确的是( )
A.18O 和16O 互为同位素
2 2
B.正己烷和2,2二甲基丙烷互为同系物C.C 和C 是具有相同质子数的不同核素
60 70
D.HNCH COOCH 和CHCHNO 是同分异构体
2 2 3 3 2 2
9.(2019全国卷Ⅲ)今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、
Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
A.原子半径:W