文档内容
第 2 讲 离子反应 离子方程式
[复习目标] 1.了解电解质及其分类,掌握强弱电解质的本质区别。2.理解电解质在水溶液
中的电离以及电解质溶液的导电性。3.了解离子反应的概念、离子反应发生的条件,并能正
确书写离子方程式。
考点一 电解质及电离
1.电解质及分类
(1)概念
在____________或____________能够导电的化合物,称为电解质,二者情况下均不导电的化
合物称为非电解质。
(2)分类
电解质
应用举例
现有12种物质:①Al ②稀硝酸 ③HNO
3
④NH ·H O ⑤CO ⑥空气 ⑦NaCl
3 2 2
⑧CaCO ⑨NaHCO ⑩乙醇 ⑪Al O
3 3 2 3
⑫Cu(OH)
2
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 电解质,熔融状态下能导电
(2) 非电解质
(3) 强电解质,但熔融状态下并不导电
(4) 强电解质,但难溶于水
(5) 弱电解质
(6) 既不是电解质,也不是非电解质,但本身能导电
2.电解质的电离
(1)电离:电解质溶于水或受热熔化时,形成______________________的过程。
(2)电离方程式的书写
强电解质在水溶液中完全电离,用“===”连接。
弱电解质在水溶液中部分电离,用“”连接,多元弱酸分步电离,一般以第一步电离为主;多元弱碱,分步电离,一步完成。
应用举例
按要求书写下列电解质的电离方程式:
①Ba(OH) :__________________________________________________________________;
2
②KAl(SO ):_________________________________________________________________;
4 2
③CHCOOH :
3
_________________________________________________________________;
④HCO:____________________________________________________________________;
2 3
⑤Cu(OH) :__________________________________________________________________;
2
⑥NaHSO 溶于水:____________________________________________________________;
4
⑦NaHSO 熔融:______________________________________________________________;
4
⑧NaHCO :__________________________________________________________________。
3
离子反应过程中溶液导电性变化的判断
1.下列几种导电性变化图像,把符合要求的图像字母填在相应的题目后面的括号中。
(1)向HSO 溶液中加入等体积、等物质的量浓度的Ba(OH) 溶液( )
2 4 2
(2)向HS溶液中通入Cl 直至过量( )
2 2
(3)向AgNO 溶液中通入少量HCl( )
3
(4)向氨水中通入HCl直至过量( )
(5)向NaOH溶液中通入少量Cl( )
2
(6)向饱和石灰水中不断通入CO( )
2
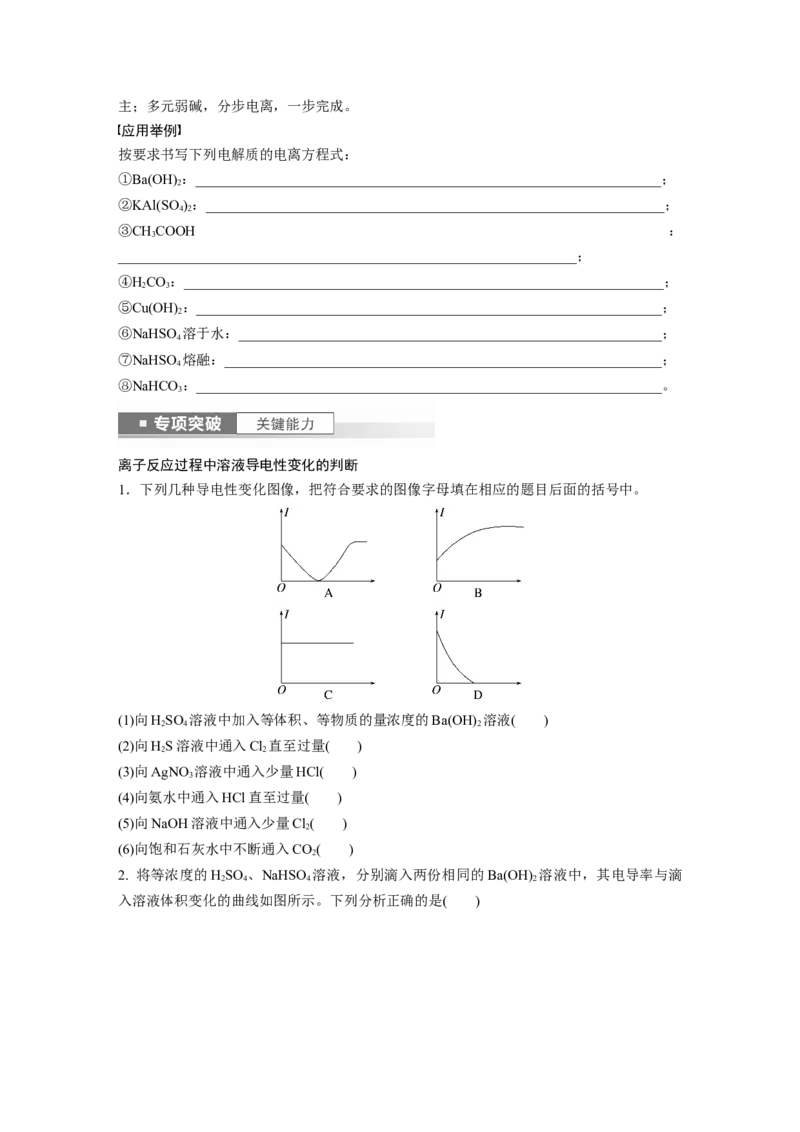
2. 将等浓度的HSO 、NaHSO 溶液,分别滴入两份相同的Ba(OH) 溶液中,其电导率与滴
2 4 4 2
入溶液体积变化的曲线如图所示。下列分析正确的是( )A.b→d反应的离子方程式为H++OH-===HO
2
B.d点溶液中,Na+与SO的物质的量之比为1∶1
C.c点导电能力相同,所以两溶液中含有相同量的OH-
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
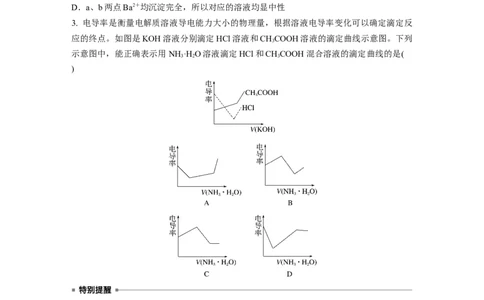
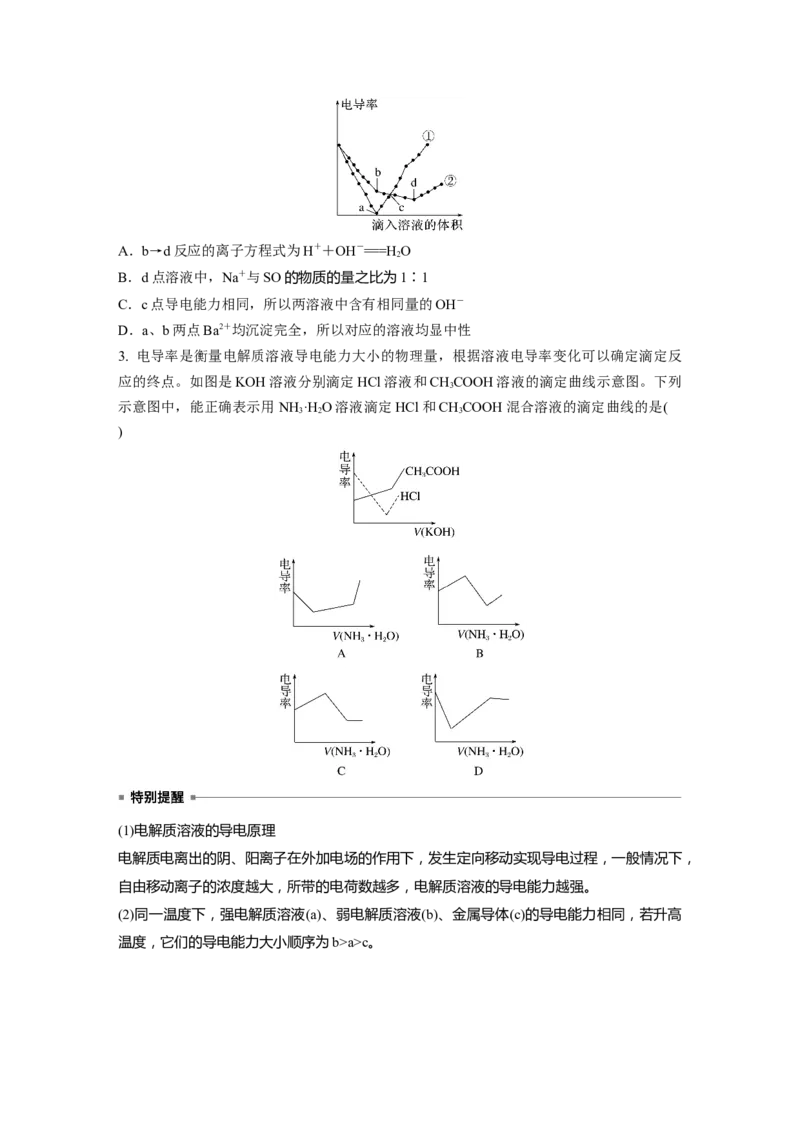
3. 电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反
应的终点。如图是KOH溶液分别滴定HCl溶液和CHCOOH溶液的滴定曲线示意图。下列
3
示意图中,能正确表示用NH ·H O溶液滴定HCl和CHCOOH混合溶液的滴定曲线的是(
3 2 3
)
(1)电解质溶液的导电原理
电解质电离出的阴、阳离子在外加电场的作用下,发生定向移动实现导电过程,一般情况下,
自由移动离子的浓度越大,所带的电荷数越多,电解质溶液的导电能力越强。
(2)同一温度下,强电解质溶液(a)、弱电解质溶液(b)、金属导体(c)的导电能力相同,若升高
温度,它们的导电能力大小顺序为b>a>c。考点二 离子反应 离子方程式书写的基本方法
1.离子反应
(1)概念:有离子参加或有离子生成的反应统称为离子反应。
(2)本质:离子反应的本质是溶液中某些离子的物质的量的________。
(3)离子反应发生的条件
①发生复分解反应:生成难溶的物质,生成难电离的物质,生成易挥发的物质。
②发生氧化还原反应。
③发生络合反应。
2.离子方程式
(1)离子方程式:用________________________来表示反应的式子。
(2)离子方程式的意义
离子方程式不仅可以表示________________,还可以表示____________________。
3.离子方程式中物质的“拆分”
(1)一般规律
①能拆分写成离子形式的物质是易溶的强电解质,包括________、________、大多数
____________。
②不能拆分的物质包括单质、氧化物、弱电解质、难溶电解质、气体。
(2)微溶物的处理
①微溶物作为产物视为沉淀,不拆分;
②作反应物时,澄清溶液拆分为离子,浑浊液不拆分,如Ca(OH) 。
2
(3)产物NH ·H O的处理
3 2
①不加热或稀溶液中,写成NH ·H O。
3 2
②加热或浓溶液中,写成NH 和HO。
3 2
一、书写离子方程式,注意微粒的书写形式
1.(1)完成下列反应的离子方程式,注意难溶微粒、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸
________________________________________________________________________。
②向AlCl 溶液中滴加过量的氨水
3
________________________________________________________________________。
③向NaHSO 溶液中加入过量NaHSO 溶液
3 4
________________________________________________________________________。(2)完成下列反应的离子方程式,注意微溶物质、NH与碱反应的条件。
①向澄清石灰水中加入稀盐酸
________________________________________________________________________。
②NaSO 溶液与AgNO 溶液混合
2 4 3
________________________________________________________________________。
③铵盐溶液与强碱溶液混合加热检测NH
________________________________________________________________________。
(3)完成下列反应的离子方程式,注意单质、氧化物、浓酸的书写形式。
①过氧化钠溶于水
________________________________________________________________________。
②用MnO 与浓盐酸共热制Cl
2 2
________________________________________________________________________。
③Cl 溶于水
2
________________________________________________________________________。
④铜溶于浓硝酸
________________________________________________________________________。
二、多重反应离子方程式的书写
2.完成下列反应的离子方程式。
(1)Ba(OH) 溶液与HSO 溶液混合
2 2 4
________________________________________________________________________。
(2)Ba(OH) 溶液与(NH )SO 溶液混合
2 4 2 4
________________________________________________________________________。
(3)CuSO 溶液与Ba(OH) 溶液混合
4 2
________________________________________________________________________。
多重反应离子方程式书写时的注意点
两种电解质溶液混合,至少电离出两种阴离子和两种阳离子,这四种(或更多种)离子之间都
能两两结合成难电离(或难溶)的物质或后续离子之间的氧化还原反应,这样的离子反应称为
多重反应。在写这类反应的离子方程式时易丢失其中的一组反应。
三、信息给予型离子方程式的书写
3.写出符合下列情况的离子方程式。
(1)向MgSO 溶液中加入(NH )CO 溶液生成Mg(OH) ·MgCO :_________________
4 4 2 3 2 3
________________________________________________________________________。
(2)BaS溶液与硫酸锌溶液混合生成立德粉(ZnS·BaSO ):________________________。
4
(3)向MnCl 溶液中加入NH HCO 生成MnCO :______________________________
2 4 3 3________________________________________________________________________。
(4)已知 PbSO 不溶于水,但可溶于醋酸铵溶液,反应方程式如下: PbSO +
4 4
2CHCOONH===(CHCOO) Pb+(NH )SO
3 4 3 2 4 2 4
将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:
_______________________________________________________________________。
考点三 与量有关的离子方程式的书写
类型一 连续型
1.反应生成的离子因又能跟剩余(过量)的反应物继续反应而跟用量有关。
(1)盐酸滴入NaCO 溶液中:
2 3
①盐酸少量:___________________________________________________________________;
②盐酸过量:___________________________________________________________________。
(2)CO 通入NaOH溶液中:
2
①CO 少量:___________________________________________________________________;
2
②CO 过量:____________________________________________________________________。
2
(3)CO 通入NaAlO 溶液中:
2 2
①CO 少量:____________________________________________________________________;
2
②CO 过量:____________________________________________________________________。
2
(4)NaOH滴入AlCl 溶液中:
3
①NaOH少量:__________________________________________________________________;
②NaOH过量:__________________________________________________________________。
(5)盐酸滴入NaAlO 溶液中:
2
①盐酸少量:___________________________________________________________________;
②盐酸过量:___________________________________________________________________。
(6)Fe与稀HNO 反应:
3
①Fe过量:____________________________________________________________________;
②稀HNO 过量:_______________________________________________________________。
3
类型二 先后型
2.一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因
反应次序不同而跟用量有关,又可称为竞争型。
(1)NH HSO 溶液与NaOH溶液的反应:
4 4
NaOH不足:___________________________________________________________________;
NaOH过量:___________________________________________________________________。
(2)向含有H+、Al3+、NH的溶液中,逐滴加入NaOH溶液至过量,反应依次为
________________________________________________________________________;________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________。
(3)向含有OH-、CO、AlO的溶液中,逐滴加入稀盐酸至过量,反应依次为
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________。
(4)向FeBr 溶液中通Cl:
2 2
通 入 少 量 Cl :
2
___________________________________________________________________;
通 入 过 量 Cl :
2
___________________________________________________________________。
类型三 配比型
3.当一种反应物中有两种或两种以上组成离子参与反应时,因其组成比例不协调(一般为复
盐或酸式盐),当一种组成离子恰好完全反应时,另一种组成离子不能恰好完全反应(有剩余
或不足),因而跟用量有关。
(1)Ca(HCO ) 溶液与NaOH溶液反应:
3 2
①NaOH不足:__________________________________________________________
________________________________________________________________________;
②NaOH过量:___________________________________________________________
________________________________________________________________________。
(2)NaHCO 溶液与Ca(OH) 溶液反应:
3 2
①NaHCO 不足:_________________________________________________________
3
________________________________________________________________________;
②NaHCO 过量:_________________________________________________________
3
________________________________________________________________________。
(3)Ba(OH) 溶液与NaHSO 溶液反应:
2 4
①n[Ba(OH) ]∶n(NaHSO)=1∶1
2 4
________________________________________________________________________,
此时溶液呈____性;
②n[Ba(OH) ]∶n(NaHSO)=1∶2
2 4
________________________________________________________________________,
此时溶液呈______性,若向该溶液中再加入Ba(OH) 溶液,反应为________________。
2
(4)NH Al(SO ) 与Ba(OH) 溶液反应:
4 4 2 2
①n[NH Al(SO )]∶n[Ba(OH) ]=1∶1
4 4 2 2________________________________________________________________________;
②n[NH Al(SO )]∶n[Ba(OH) ]=1∶2
4 4 2 2
________________________________________________________________________。
“少定多变”法书写与量有关的离子方程式
先根据题给条件判断“少量物质”,以“少量物质”的离子计量数(充分反应)确定所需“过
量物质”的离子数目。如向Ca(HCO ) 溶液中加入过量NaOH溶液的离子方程式的书写方法
3 2
为
1.(2022·浙江6月选考,2)下列物质属于强电解质的是( )
A.HCOOH B.Fe C.NaCO D.C H
2 3 2 2
2.(2022·全国甲卷,9)能正确表示下列反应的离子方程式为( )
A.硫化钠溶液和硝酸混合:S2-+2H+===HS↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2HO===AlO+4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO+CO+HO===HSiO+HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H+
2 4 4
+SO===BaSO↓+2HO
4 2
3.(2022·广东,14)下列关于Na的化合物之间转化反应的离子方程式书写正确的是( )
A.碱转化为酸式盐:OH-+2H++CO===HCO+2HO
2
B.碱转化为两种盐:2OH-+Cl===ClO-+Cl-+HO
2 2
C.过氧化物转化为碱:2O+2HO===4OH-+O↑
2 2
D.盐转化为另一种盐:NaSiO+2H+===HSiO↓+2Na+
2 3 2 3
4.(2022·浙江6月选考,13)下列反应的离子方程式不正确的是( )
A.盐酸中滴加NaSiO 溶液:SiO+2H+===HSiO↓
2 3 2 3
B.NaCO 溶液中通入过量SO :CO+2SO +HO===2HSO+CO
2 3 2 2 2 2
C.乙醇与KCr O 酸性溶液反应:3CHCHOH+2Cr O+16H+―→3CHCOOH+4Cr3++
2 2 7 3 2 2 3
11HO
2
D.溴与冷的NaOH溶液反应:Br +OH-===Br-+BrO-+H+
2
5.(2022·湖南,11改编)下列离子方程式正确的是( )
A.Cl 通入冷的NaOH溶液:Cl+OH-===Cl-+HClO
2 2
B.用醋酸和淀粉KI溶液检验加碘盐中的IO:IO+5I-+6H+===3I+3HO
2 2C.FeSO 溶液中加入HO 产生沉淀:2Fe2++HO+4HO===2Fe(OH) ↓+4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO+Ba2++OH-===BaCO ↓+HO
3 2 3 2