文档内容
大题突破 3 无机化工流程题题型研究
1.(2022·河北五校联盟高三下学期3月模拟)随着新能源汽车的不断推广,近几年动力电池
迎来退役潮爆发。大量淘汰的LiFePO 电池(LFP)若得不到正确的处理,必然会带来严重的
4
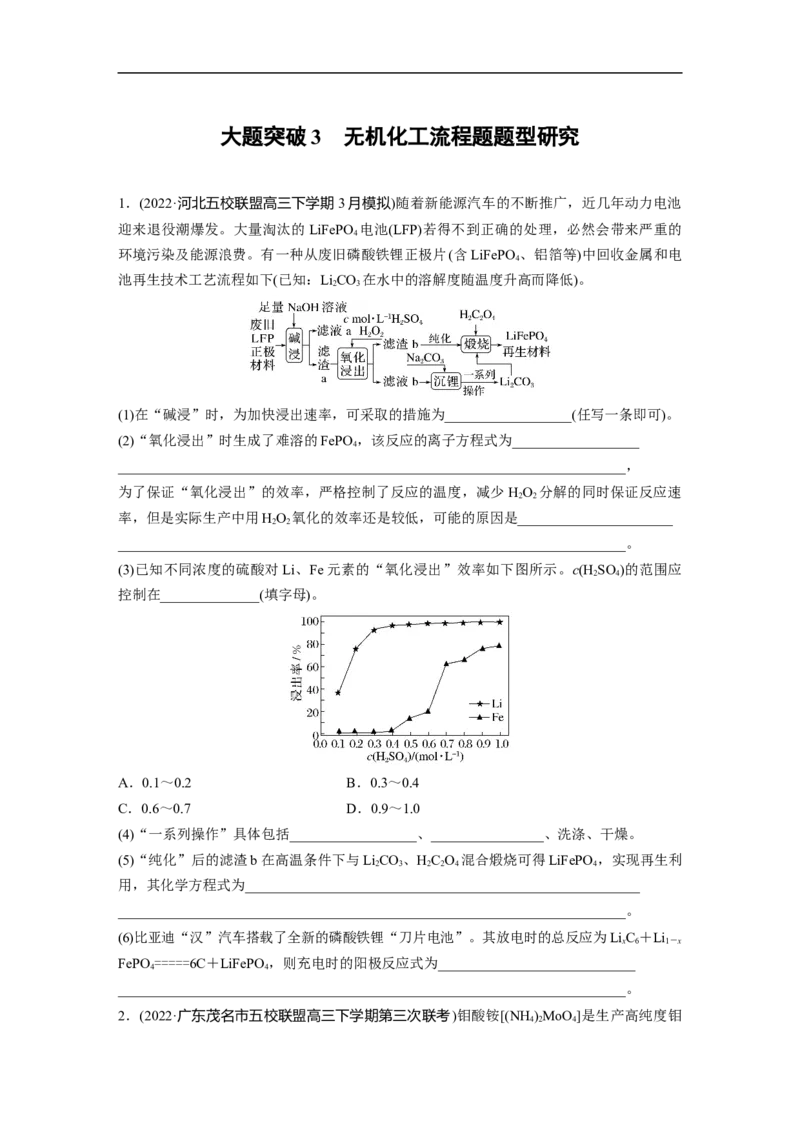
环境污染及能源浪费。有一种从废旧磷酸铁锂正极片(含LiFePO 、铝箔等)中回收金属和电
4
池再生技术工艺流程如下(已知:LiCO 在水中的溶解度随温度升高而降低)。
2 3
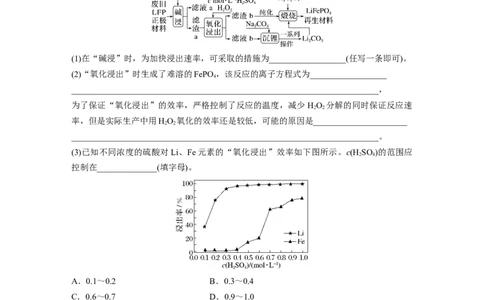
(1)在“碱浸”时,为加快浸出速率,可采取的措施为__________________(任写一条即可)。
(2)“氧化浸出”时生成了难溶的FePO ,该反应的离子方程式为__________________
4
________________________________________________________________________,
为了保证“氧化浸出”的效率,严格控制了反应的温度,减少 HO 分解的同时保证反应速
2 2
率,但是实际生产中用HO 氧化的效率还是较低,可能的原因是______________________
2 2
________________________________________________________________________。
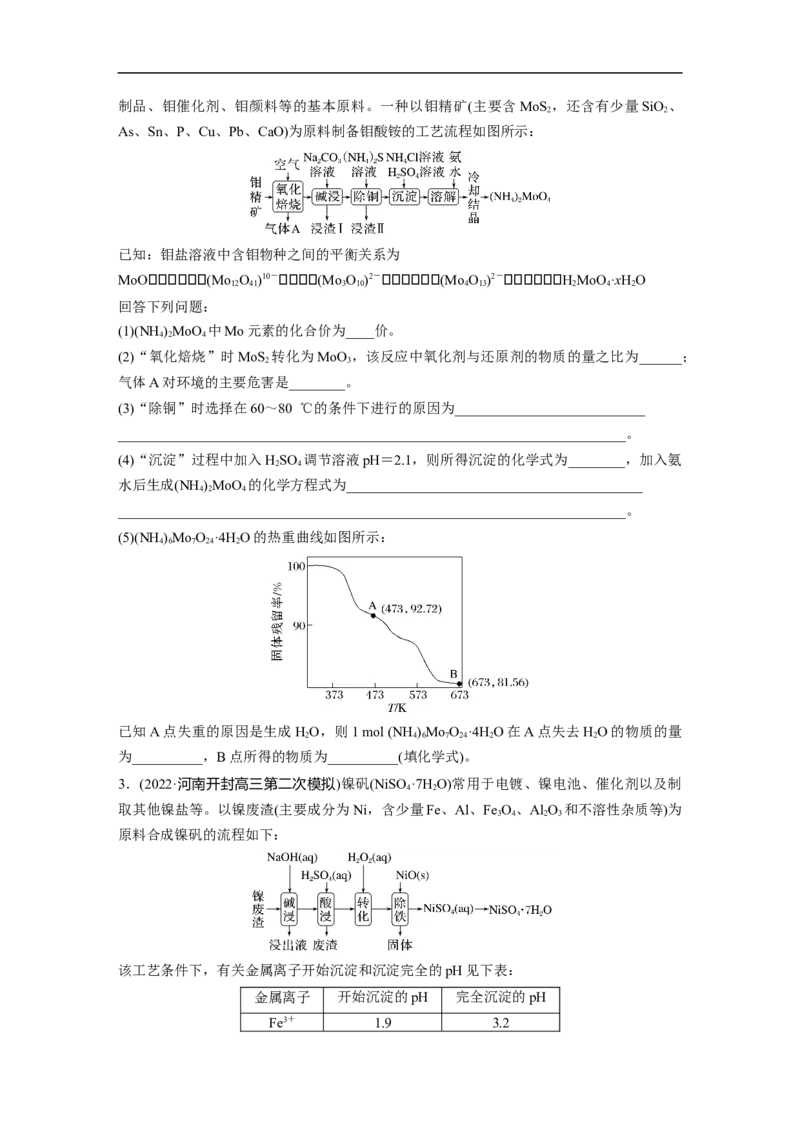
(3)已知不同浓度的硫酸对Li、Fe元素的“氧化浸出”效率如下图所示。c(H SO )的范围应
2 4
控制在______________(填字母)。
A.0.1~0.2 B.0.3~0.4
C.0.6~0.7 D.0.9~1.0
(4)“一系列操作”具体包括__________________、________________、洗涤、干燥。
(5)“纯化”后的滤渣b在高温条件下与LiCO 、HC O 混合煅烧可得LiFePO ,实现再生利
2 3 2 2 4 4
用,其化学方程式为________________________________________________________
________________________________________________________________________。
(6)比亚迪“汉”汽车搭载了全新的磷酸铁锂“刀片电池”。其放电时的总反应为LiC +Li
x 6 1-x
FePO =====6C+LiFePO ,则充电时的阳极反应式为____________________________
4 4
________________________________________________________________________。
2.(2022·广东茂名市五校联盟高三下学期第三次联考)钼酸铵[(NH )MoO ]是生产高纯度钼
4 2 4制品、钼催化剂、钼颜料等的基本原料。一种以钼精矿(主要含MoS ,还含有少量SiO 、
2 2
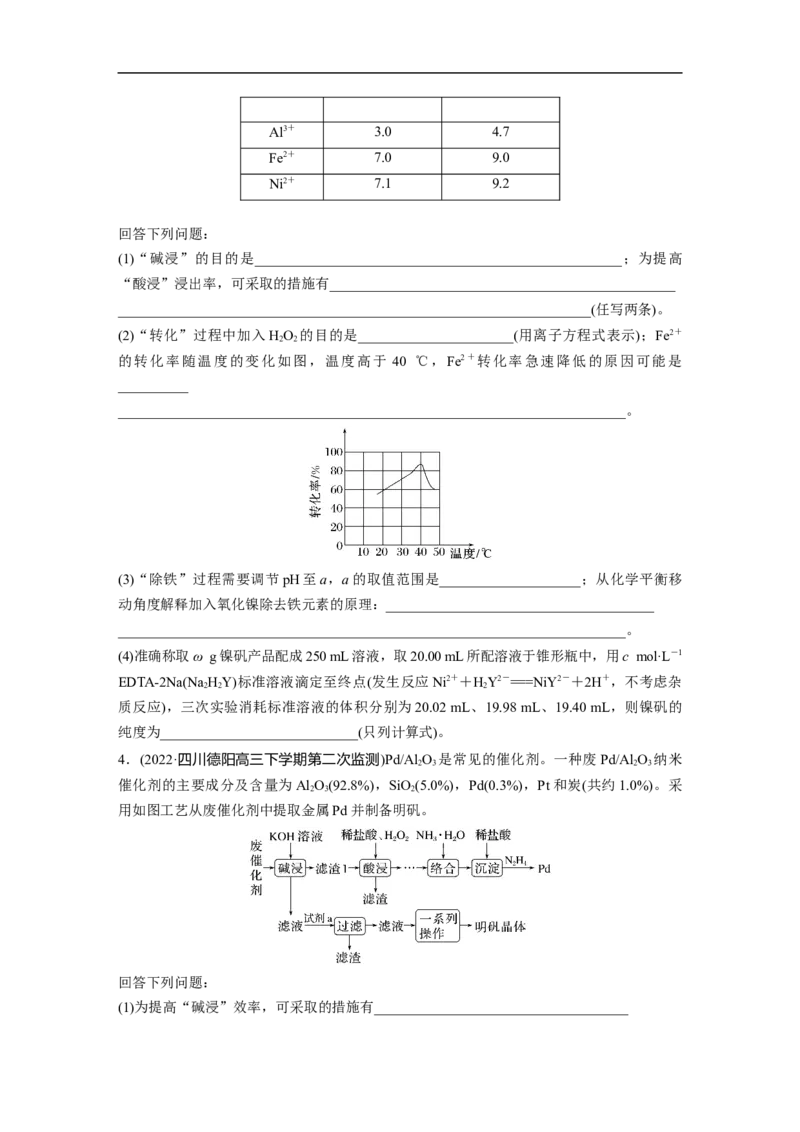
As、Sn、P、Cu、Pb、CaO)为原料制备钼酸铵的工艺流程如图所示:
已知:钼盐溶液中含钼物种之间的平衡关系为
MoO(Mo O )10-(Mo O )2-(Mo O )2-HMoO ·xHO
12 41 3 10 4 13 2 4 2
回答下列问题:
(1)(NH )MoO 中Mo元素的化合价为____价。
4 2 4
(2)“氧化焙烧”时MoS 转化为MoO ,该反应中氧化剂与还原剂的物质的量之比为______;
2 3
气体A对环境的主要危害是________。
(3)“除铜”时选择在60~80 ℃的条件下进行的原因为___________________________
________________________________________________________________________。
(4)“沉淀”过程中加入HSO 调节溶液pH=2.1,则所得沉淀的化学式为________,加入氨
2 4
水后生成(NH )MoO 的化学方程式为__________________________________________
4 2 4
________________________________________________________________________。
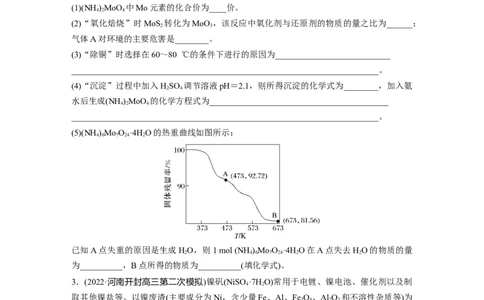
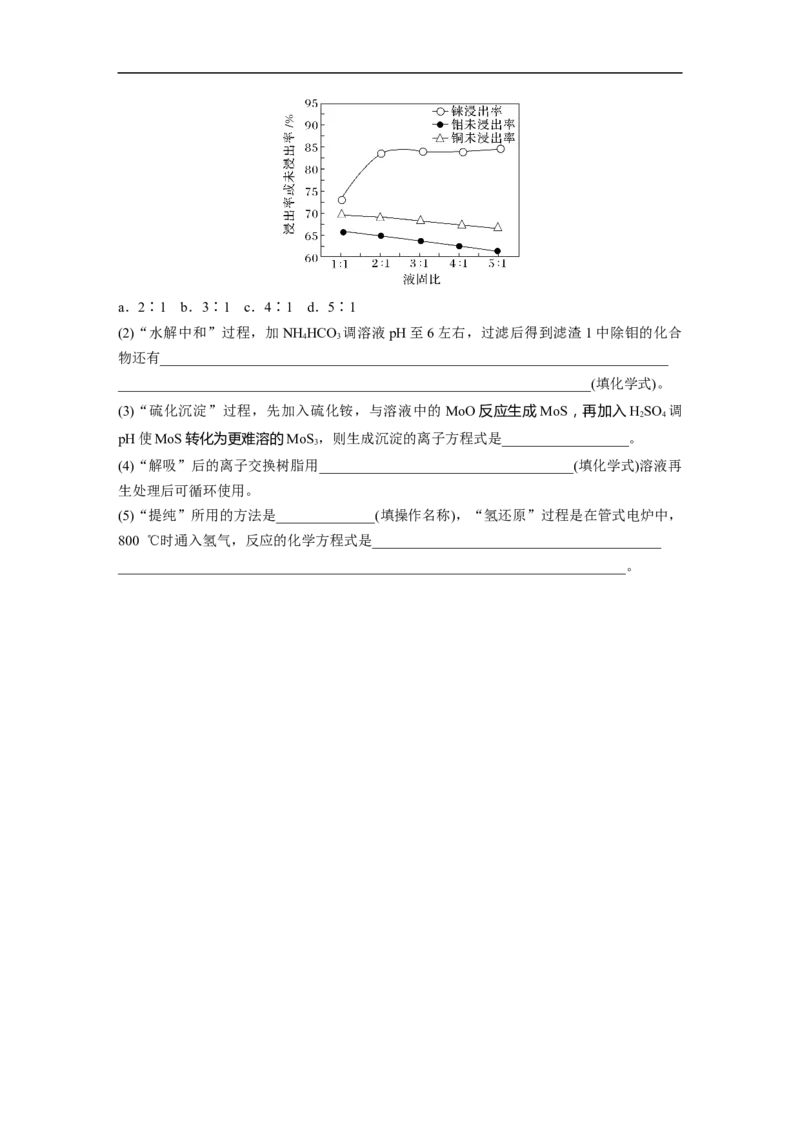
(5)(NH )MoO ·4H O的热重曲线如图所示:
4 6 7 24 2
已知A点失重的原因是生成HO,则1 mol (NH )MoO ·4H O在A点失去HO的物质的量
2 4 6 7 24 2 2
为__________,B点所得的物质为__________(填化学式)。
3.(2022·河南开封高三第二次模拟)镍矾(NiSO ·7H O)常用于电镀、镍电池、催化剂以及制
4 2
取其他镍盐等。以镍废渣(主要成分为Ni,含少量Fe、Al、Fe O 、Al O 和不溶性杂质等)为
3 4 2 3
原料合成镍矾的流程如下:
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 开始沉淀的pH 完全沉淀的pH
Fe3+ 1.9 3.2Al3+ 3.0 4.7
Fe2+ 7.0 9.0
Ni2+ 7.1 9.2
回答下列问题:
(1)“碱浸”的目的是____________________________________________________;为提高
“酸浸”浸出率,可采取的措施有_________________________________________________
___________________________________________________________________(任写两条)。
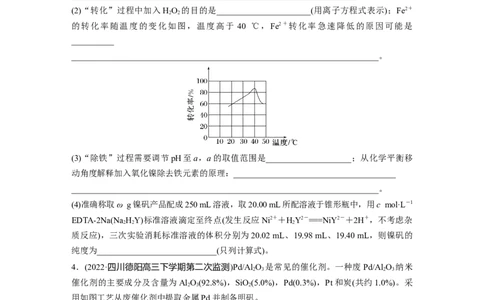
(2)“转化”过程中加入HO 的目的是______________________(用离子方程式表示);Fe2+
2 2
的转化率随温度的变化如图,温度高于 40 ℃,Fe2+转化率急速降低的原因可能是
__________
________________________________________________________________________。
(3)“除铁”过程需要调节pH至a,a的取值范围是____________________;从化学平衡移
动角度解释加入氧化镍除去铁元素的原理:______________________________________
________________________________________________________________________。
(4)准确称取ω g镍矾产品配成250 mL溶液,取20.00 mL所配溶液于锥形瓶中,用c mol·L-1
EDTA-2Na(Na HY)标准溶液滴定至终点(发生反应Ni2++HY2-===NiY2-+2H+,不考虑杂
2 2 2
质反应),三次实验消耗标准溶液的体积分别为20.02 mL、19.98 mL、19.40 mL,则镍矾的
纯度为____________________________(只列计算式)。
4.(2022·四川德阳高三下学期第二次监测)Pd/Al O 是常见的催化剂。一种废Pd/Al O 纳米
2 3 2 3
催化剂的主要成分及含量为Al O(92.8%),SiO(5.0%),Pd(0.3%),Pt和炭(共约1.0%)。采
2 3 2
用如图工艺从废催化剂中提取金属Pd并制备明矾。
回答下列问题:
(1)为提高“碱浸”效率,可采取的措施有_________________________________________________________________________________________________(任写两条)。
(2)试剂a的化学式为_____________________________________________________。
(3)“一系列操作”是指________、过滤、洗涤。
(4)“酸浸”时,Pt和Pd分别转化为PtCl和PdCl,写出Pd转化为PdCl的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(5)“酸浸”时,若用 O 替代 HO ,则氧化效率(单位质量的物质得到的电子数)将
3 2 2
__________(填“提高”“降低”或“不变”)。
(6)“络合”过程后得到 Pd(NH )和 Pt(NH ),“沉淀”时,搅拌滴加盐酸调节 pH 将
3 3
[Pd(NH)]Cl 转化为[Pd(NH)]Cl 沉淀,结合平衡移动原理解释实现转化的原因是
3 4 2 3 2 2
________________________________________________________________________
________________________________________________________________________。
(7)采用工艺:“ ”也能得到金属Pd,试从绿色化学角度分析
该工艺的不足:________________。
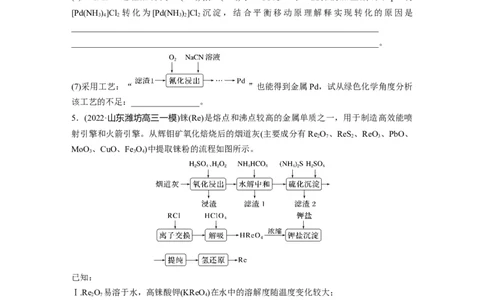
5.(2022·山东潍坊高三一模)铼(Re)是熔点和沸点较高的金属单质之一,用于制造高效能喷
射引擎和火箭引擎。从辉钼矿氧化焙烧后的烟道灰(主要成分有Re O 、ReS 、ReO 、PbO、
2 7 2 3
MoO 、CuO、Fe O)中提取铼粉的流程如图所示。
3 3 4
已知:
Ⅰ.Re O 易溶于水,高铼酸钾(KReO )在水中的溶解度随温度变化较大;
2 7 4
Ⅱ.RCl为阴离子交换树脂,对铼具有良好的选择性,在酸性体系中能够有效的吸附铼。
回答下列问题:
(1)“氧化浸出”过程,ReS 、ReO 被氧化为 ReO,ReO 被氧化的离子方程式是
2 3 3
________________________________________________________________________
________________________________________________________________________。
浸出过程中,在浸出时间相同的条件下改变液固比,实验结果如图所示,则实际生产中应选
择的液固比是________________(填字母)。a.2∶1 b.3∶1 c.4∶1 d.5∶1
(2)“水解中和”过程,加NH HCO 调溶液pH至6左右,过滤后得到滤渣1中除钼的化合
4 3
物还有________________________________________________________________________
___________________________________________________________________(填化学式)。
(3)“硫化沉淀”过程,先加入硫化铵,与溶液中的 MoO反应生成MoS,再加入HSO 调
2 4
pH使MoS转化为更难溶的MoS ,则生成沉淀的离子方程式是__________________。
3
(4)“解吸”后的离子交换树脂用____________________________________(填化学式)溶液再
生处理后可循环使用。
(5)“提纯”所用的方法是______________(填操作名称),“氢还原”过程是在管式电炉中,
800 ℃时通入氢气,反应的化学方程式是_________________________________________
________________________________________________________________________。