文档内容
第 21 讲 化学反应的热效应
目录
考情分析 知识点3 能源及利用
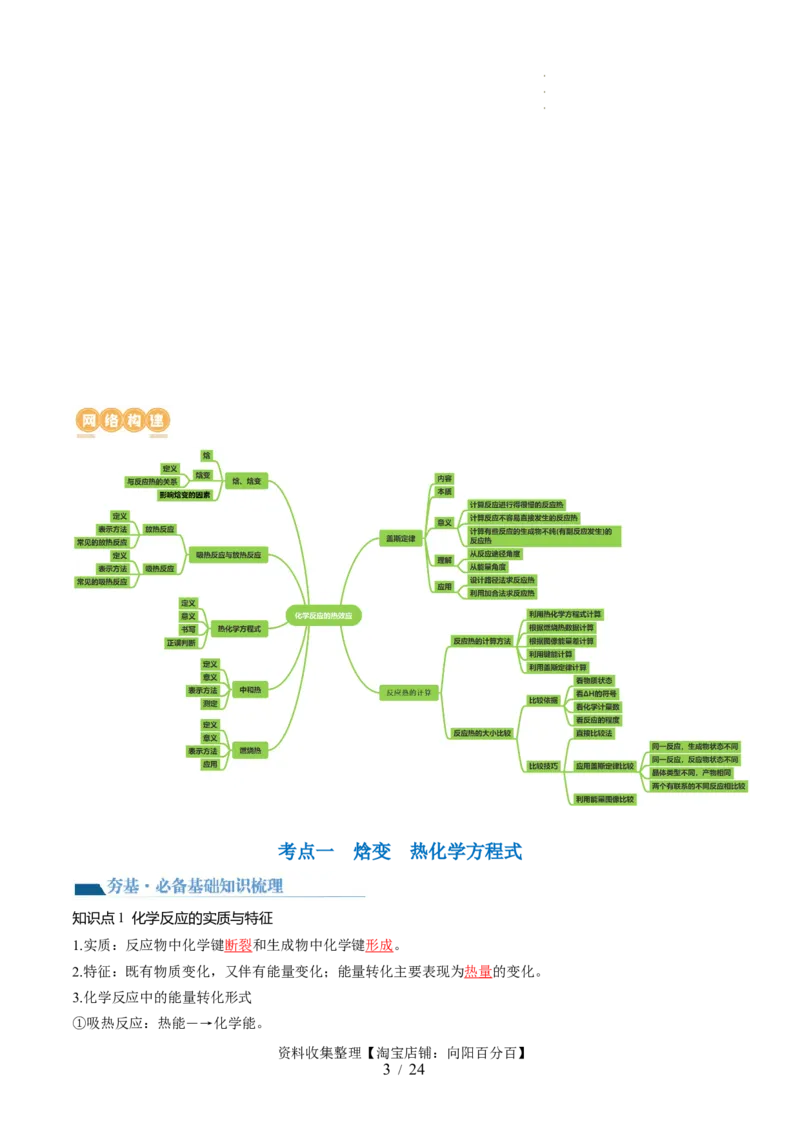
网络构建 【提升·必考题型归纳】
考向1 考查燃烧热和中和反应反应热的概念
考点一 焓变 热化学方程式
考向2 考查中和反应反应热的测定
【夯基·必备基础知识梳理】
考向3 考查能源的开发与利用
知识点1 化学反应的实质与特征
知识点2 焓变 反应热
考点三 盖斯定律 反应热计算
知识点3 放热反应和吸热反应
【夯基·必备基础知识梳理】
知识点4 热化学方程式
知识点1 盖斯定律
【提升·必考题型归纳】
知识点2 反应热的计算
考向1 考查化学反应中能量变化图形探析
知识点3 反应热大小的比较
考向2 考查热化学方程式的书写与判断
【提升·必考题型归纳】
考向1 考查盖斯定律的应用
考点二 燃烧热 中和反应反应热和能源
考向2 考查反应热的相关计算
【夯基·必备基础知识梳理】
考向3 考查反应热大小的比较
知识点1 燃烧热和中和反应反应热的比较
知识点2 中和反应反应热的测定
真题感悟
考点要求 考题统计 考情分析
分析近三年的高考试题,高考命题在本讲有以下规律:
2023浙江1月卷14题,2
1.从考查题型和内容上看,高考命题以选择题和非选择题的
资料收集整理【淘宝店铺:向阳百分百】
1 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司反应热 分 形式呈现,考查内容主要有以下三个方面:
焓变 热 2022浙江1月卷18题,2 (1)反应热的概念及计算;
化学方程 分 (2)热化学方程式的书写与正误判断;
式 2021广东卷3题,3分 (3)盖斯定律及其应用。
燃烧热 2.从命题思路上看,侧重结合能量变化图像、化学反应历程
中和反应 2023湖北卷1题,3分 和燃烧热等,考查反应中的能量变化、反应热的比较及盖斯
反应热 2021重庆卷10题,3分 定律的计算。
能源 (1)以化学反应与能量的基本概念命题,考查化学反应中能量
转化的形式和反应热的有关计算;
(2)以盖斯定律的应用命题,以非选择题中某一问的形式考查
热化学方程式的书写和反应热的计算,分值一般为2~3分。
3.根据高考命题的特点和规律,复习时要注意以下几个方面:
盖斯定律 2023浙江月卷14题,2分
(1)对化学反应中的能量变化,复习备考应从两个角度进行,
反应热的 2022重庆卷13题,3分
一是从总能量变化的角度,二是从化学键键能的角度。
计算 2021广东卷19题,2分
(2)对热化学方程式的复习,一要抓住热化学方程式的书写规
则,二要注意题目条件的设置。
(3)对盖斯定律有关问题的复习,要理解盖斯定律的本质,熟
悉历年高考考查类型(图像型、字母型、数值型等)。
资料收集整理【淘宝店铺:向阳百分百】
2 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司考点一 焓变 热化学方程式
知识点1 化学反应的实质与特征
1.实质:反应物中化学键断裂和生成物中化学键形成。
2.特征:既有物质变化,又伴有能量变化;能量转化主要表现为热量的变化。
3.化学反应中的能量转化形式
①吸热反应:热能―→化学能。
资料收集整理【淘宝店铺:向阳百分百】
3 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司②放热反应:化学能―→热能。
③光合作用:光能―→化学能。
④燃烧反应:化学能―→热能,化学能―→光能。
⑤原电池反应:化学能―→电能。
⑥电解池反应:电能―→化学能。
知识点2 焓变 反应热
1.焓与焓变
①焓(H):焓是与内能有关的物理量。
②焓变(ΔH):生成物的焓与反应物的焓之差。
【名师点拨】关于焓的理解
①焓是与内能有关的相对比较抽象的一个物理量,焓变的值只与始末状态有关而与过程无关。
②物质的焓越小,具有的能量越低,稳定性越强。
2.反应热:化学反应过程中吸收或放出的能量。
3.焓变与反应热的关系:对于恒压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能,
则有关系:ΔH=Qp。
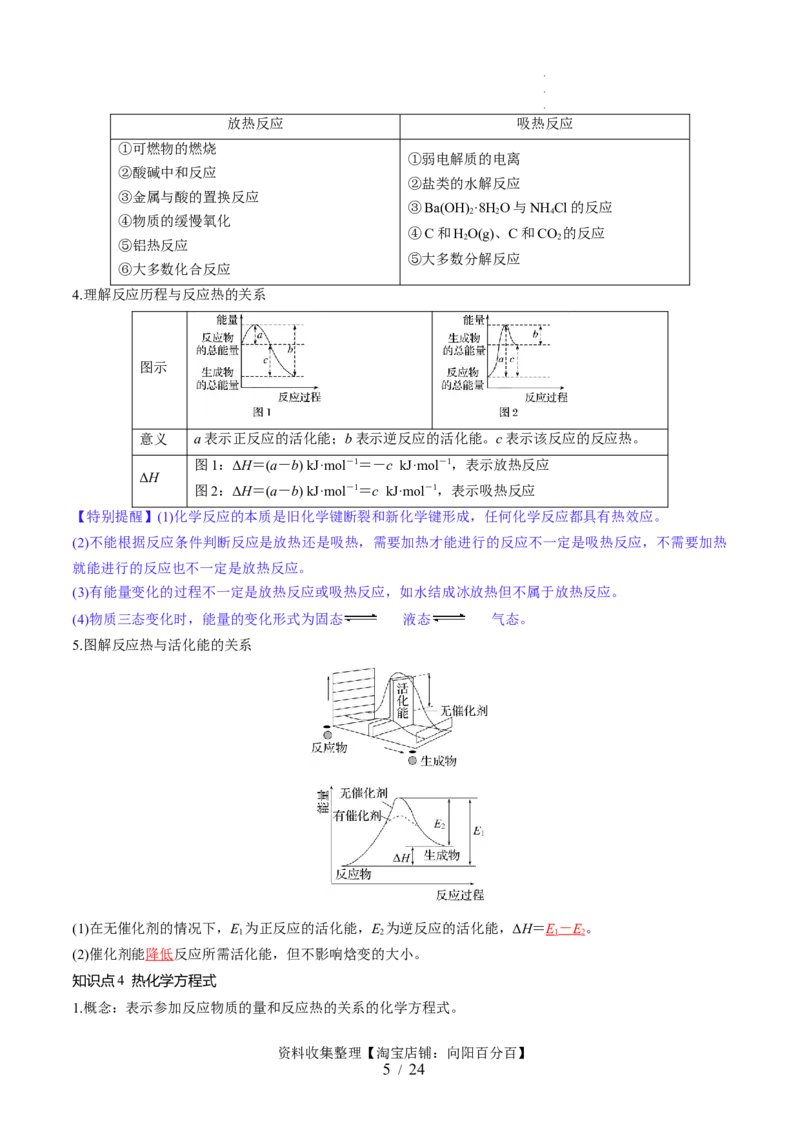
知识点3 放热反应和吸热反应
1.概念
(1)放热反应:释放热量的化学反应。反应物的总能量大于生成物的总能量。反应体系的能量降低,故ΔH
<0,即ΔH为 负 值 。
(2)吸热反应:吸收热量的化学反应。反应物的总能量小于生成物的总能量。反应体系的能量升高,故ΔH
>0,即ΔH为 正 值 。
2.放热反应和吸热反应的判断
(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析
3.记忆常见的放热反应和吸热反应
资料收集整理【淘宝店铺:向阳百分百】
4 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司放热反应 吸热反应
①可燃物的燃烧
①弱电解质的电离
②酸碱中和反应
②盐类的水解反应
③金属与酸的置换反应
③Ba(OH) ·8H O与NH Cl的反应
2 2 4
④物质的缓慢氧化
④C和HO(g)、C和CO 的反应
2 2
⑤铝热反应
⑤大多数分解反应
⑥大多数化合反应
4.理解反应历程与反应热的关系
图示
意义 a表示正反应的活化能;b表示逆反应的活化能。c表示该反应的反应热。
图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反应
【特别提醒】(1)化学反应的本质是旧化学键断裂和新化学键形成,任何化学反应都具有热效应。
(2)不能根据反应条件判断反应是放热还是吸热,需要加热才能进行的反应不一定是吸热反应,不需要加热
就能进行的反应也不一定是放热反应。
(3)有能量变化的过程不一定是放热反应或吸热反应,如水结成冰放热但不属于放热反应。
(4)物质三态变化时,能量的变化形式为固态 液态 气态。
5.图解反应热与活化能的关系
(1)在无催化剂的情况下,E 为正反应的活化能,E 为逆反应的活化能,ΔH=E - E 。
1 2 1 2
(2)催化剂能降低反应所需活化能,但不影响焓变的大小。
知识点4 热化学方程式
1.概念:表示参加反应物质的量和反应热的关系的化学方程式。
资料收集整理【淘宝店铺:向阳百分百】
5 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司2.意义:表明了化学反应中的物质变化和能量变化。
如:2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1,表示:2 mol氢气和1 mol氧气反应生成2 mol液态
2 2 2
水时放出571.6 kJ的热量。
3.书写热化学方程式的步骤及要求
一写化学方程式——写出配平的化学方程式。
二标状态——用s、1、g、aq标明物质的聚集状态,不标“↑”或“↓”。
三标条件——标明反应的温度和压强(101kPa、25℃时可不标注)。
四标△H——在方程式后写出△H,并根据信息注明△H的“+”或“-”。
五标数值——根据化学计量数计算写出△H的值,并注明单位kJ·mol。
【方法技巧】①焓变与反应发生的条件、反应进行是否彻底无关。
②催化剂能降低反应所需活化能,但不影响焓变的大小。
③在化学反应中,反应物各原子之间的化学键不一定完全断裂。
4.热化学方程式与化学(离子)方程式的3个不同点
①热化学方程式不注明反应条件;
②热化学方程式不标“↑”“↓”,但必须用s、l、g、aq等标出物质的聚集状态。
③热化学方程式的化学计量数只表示物质的量,其ΔH必须与化学方程式及物质的聚集状态相对应。
5.判断热化学方程式正误的“五看”
一看状态―→看各物质的聚集状态是否正确;
二看符号―→看ΔH的“+”“-”是否正确;
三看单位―→看反应热的单位是否为kJ/mol;
四看数值―→看反应热数值与化学计量数是否相对应;
五看概念―→看燃烧热、中和反应反应热的热化学方程式。
考向1 考查化学反应中能量变化图形探析
例1.(2023·上海崇明·统考一模)反应A(g)+B(g)→C(g)-Q (Q >0)分两步进行:①A(g)+B(g)→X(g)
1 1
+Q (Q >0);②X(g)→C(g)-Q (Q >0)。下列图中,能正确表示总反应过程中能量变化的是
2 2 3 3
A. B. C. D.
【解析】A(g)+B(g)→C(g)-Q (Q >0)说明A和B的总能量小于C的总能量,A(g)+B(g)→X(g)+Q (Q >0)说
1 1 2 2
明A和B的总能量大于X的能量,X(g)→C(g)-Q (Q >0)说明X的能量小于C的能量,因此能量的关系为
3 3
C>A+B>X,故选A。
【答案】A
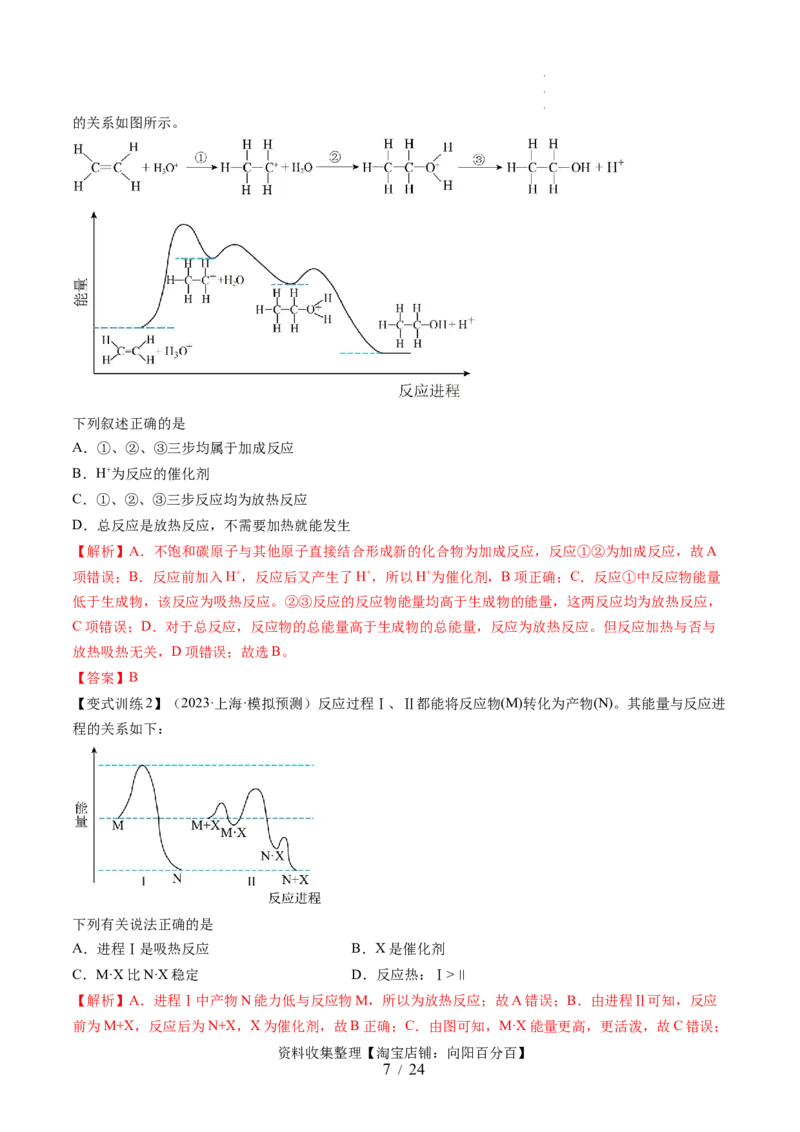
【变式训练1】(2023·上海·模拟预测)乙烯与水通过加成反应可得乙醇。反应机理、能量变化与反应进程
资料收集整理【淘宝店铺:向阳百分百】
6 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司的关系如图所示。
下列叙述正确的是
A.①、②、③三步均属于加成反应
B.H+为反应的催化剂
C.①、②、③三步反应均为放热反应
D.总反应是放热反应,不需要加热就能发生
【解析】A.不饱和碳原子与其他原子直接结合形成新的化合物为加成反应,反应①②为加成反应,故A
项错误;B.反应前加入H+,反应后又产生了H+,所以H+为催化剂,B项正确;C.反应①中反应物能量
低于生成物,该反应为吸热反应。②③反应的反应物能量均高于生成物的能量,这两反应均为放热反应,
C项错误;D.对于总反应,反应物的总能量高于生成物的总能量,反应为放热反应。但反应加热与否与
放热吸热无关,D项错误;故选B。
【答案】B
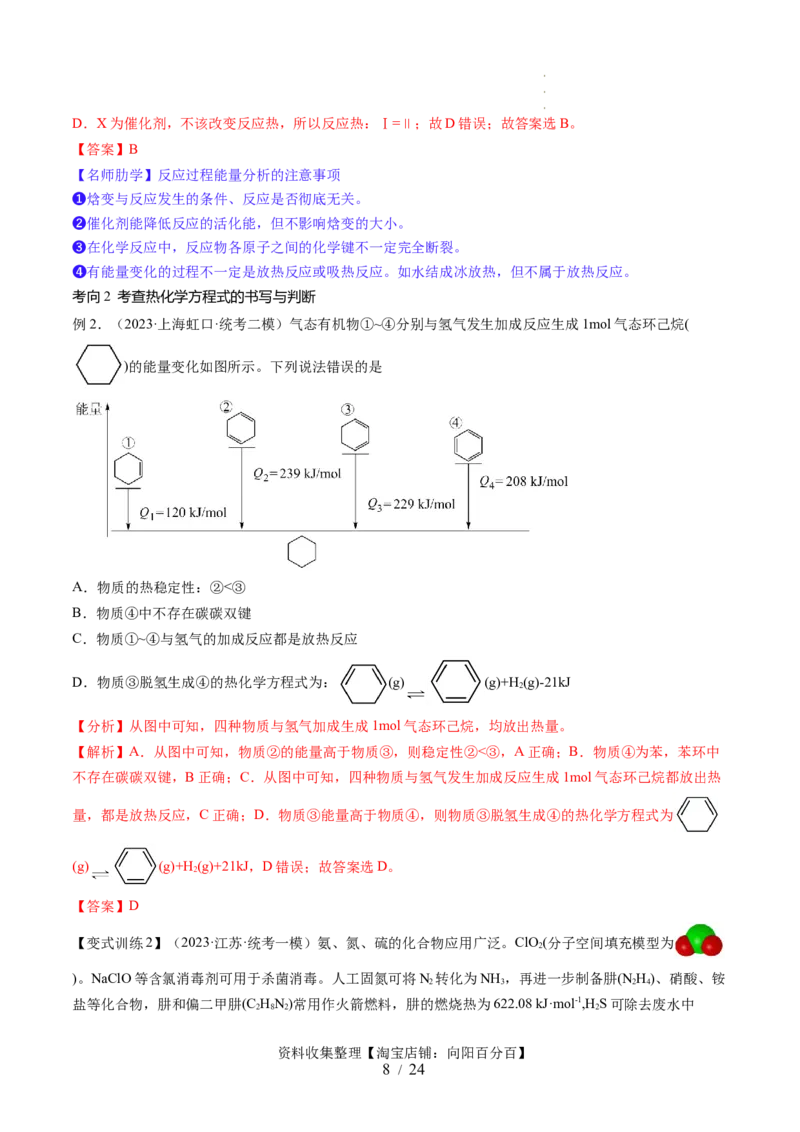
【变式训练2】(2023·上海·模拟预测)反应过程Ⅰ、Ⅱ都能将反应物(M)转化为产物(N)。其能量与反应进
程的关系如下:
下列有关说法正确的是
A.进程Ⅰ是吸热反应 B.X是催化剂
C.M·X比N·X稳定 D.反应热:Ⅰ>Ⅱ
【解析】A.进程Ⅰ中产物N能力低与反应物M,所以为放热反应;故A错误;B.由进程Ⅱ可知,反应
前为M+X,反应后为N+X,X为催化剂,故B正确;C.由图可知,M·X能量更高,更活泼,故C错误;
资料收集整理【淘宝店铺:向阳百分百】
7 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司D.X为催化剂,不该改变反应热,所以反应热:Ⅰ=Ⅱ;故D错误;故答案选B。
【答案】B
【名师肋学】反应过程能量分析的注意事项
❶焓变与反应发生的条件、反应是否彻底无关。
❷催化剂能降低反应的活化能,但不影响焓变的大小。
❸在化学反应中,反应物各原子之间的化学键不一定完全断裂。
❹有能量变化的过程不一定是放热反应或吸热反应。如水结成冰放热,但不属于放热反应。
考向2 考查热化学方程式的书写与判断
例2.(2023·上海虹口·统考二模)气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷(
)的能量变化如图所示。下列说法错误的是
A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应
D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
【分析】从图中可知,四种物质与氢气加成生成1mol气态环己烷,均放出热量。
【解析】A.从图中可知,物质②的能量高于物质③,则稳定性②<③,A正确;B.物质④为苯,苯环中
不存在碳碳双键,B正确;C.从图中可知,四种物质与氢气发生加成反应生成1mol气态环己烷都放出热
量,都是放热反应,C正确;D.物质③能量高于物质④,则物质③脱氢生成④的热化学方程式为
(g) (g)+H(g)+21kJ,D错误;故答案选D。
2
【答案】D
【变式训练2】(2023·江苏·统考一模)氨、氮、硫的化合物应用广泛。ClO (分子空间填充模型为
2
)。NaClO等含氯消毒剂可用于杀菌消毒。人工固氮可将N 转化为NH ,再进一步制备肼(N H)、硝酸、铵
2 3 2 4
盐等化合物,肼和偏二甲肼(C HN)常用作火箭燃料,肼的燃烧热为622.08 kJ·mol-1,H S可除去废水中
2 8 2 2
资料收集整理【淘宝店铺:向阳百分百】
8 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司Hg2+等重金属离子,HS 水溶液在空气中会缓慢氧化生成S而变诨浊。下列化学反应的方程式表示不正确
2
的是
A.NaClO溶液与CO 反应生成NaHCO : ClO-+ CO+ H O = HClO+ HCO
2 3 2 2
B.HS水溶液在空气中变浑浊的化学方程式: 2HS+ O = 2S↓ + 2H O
2 2 2 2
C.用石墨作电极电解NaCl溶液的离子方程式: 2Cl-+2H O Cl↑+H ↑+2OH-
2 2 2
D.肼燃烧的热化学方程式: NH(l)+O (g)=N(g) +2H O(g) H=-622.08 kJ·mol-1
2 4 2 2 2
【解析】A.HClO的酸性比碳酸弱,比碳酸氢根的酸性强,故NaClO溶液与CO 反应生成NaHCO :ClO-
△ 2 3
+ CO+ H O = HClO+ ,A正确;B.HS水溶液在空气中,和氧气反应后生成单质硫和水,变浑浊
2 2 2
的化学方程式: 2HS+ O = 2S↓ + 2H O,B正确;C.用石墨作电极电解NaCl溶液,产生氯气、氢气和氢
2 2 2
氧化钠,离子方程式: 2Cl-+2H O Cl↑+H ↑+2OH-,C正确;D.标准燃烧热,水为液态,肼燃烧的热
2 2 2
化学方程式: NH(l)+O (g)=N(g) +2H O(l) H=-622.08 kJ·mol-1,D错误;故答案为:D。
2 4 2 2 2
【答案】D
△
【思维建模】判断热化学方程式正误的“五看”
一看状态―→看各物质的聚集状态是否正确;
二看符号―→看ΔH的“+”“-”是否正确;
三看单位―→看反应热的单位是否为kJ/mol;
四看数值―→看反应热数值与化学计量数是否相对应;
五看概念―→看燃烧热、中和反应反应热的热化学方程式。
考点二 燃烧热 中和反应反应热和能源
知识点1 燃烧热和中和反应反应热的比较
燃烧热 中和反应反应热
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1 mol 不一定为1 mol
生成物的量 不确定 生成水的量为1 mol
101 kPa时,1 mol纯物质完
在稀溶液里,酸与碱发生中和
全燃烧生成稳定的氧化物时所
不同点 反应热的含义 反应生成1 mol水时所放出的
放出的热量,即C―→CO(g)、
2
热量
H―→HO(l)、S―→SO (g)。
2 2
强酸与强碱反应的中和反应反
表示方法 燃烧热ΔH=-a kJ·mol-1(a>0)
应热ΔH=-57.3 kJ·mol-1
特点 物质燃烧一定放热,ΔH一定为 弱酸、弱碱电离吸热,中和反
资料收集整理【淘宝店铺:向阳百分百】
9 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司负值 应反应热数值比57.3小
【名师点拨】(1)有关燃烧热的判断,一看是否以1 mol可燃物为标准,二看是否生成指定产物。
(2)在书写燃烧热的热化学方程式时,应以燃烧1 mol物质为标准来配平其余物质的化学计量数。如C H (l)
8 18
+O(g)===8CO (g)+9HO(l) ΔH=-5 518 kJ·mol-1。
2 2 2
知识点2 中和反应反应热的测定
1.实验装置
2.测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;
n为生成HO的物质的量。
2
3.实验步骤
①绝热装置组装
②量取一定体积酸、碱稀溶液:量取50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1氢氧化钠溶液
③测反应前酸碱液温度:测量混合前50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1氢氧化钠溶液的温度,
取两温度平均值,记录为起始温度t。
1
④混合酸碱液测反应时最高温度:将酸碱溶液迅速混合,用玻璃搅拌器轻轻搅动溶液,并准确读取混合溶
液的最高温度,记录为终止温度t。
2
⑤重复2~3次实验:记录每次的实验数据,取其平均值作为计算依据。
⑥求平均温度差(t -t )
终 始
⑦计算中和热ΔH。
【特别说明】❶为了保证盐酸完全被中和,采用稍过量的NaOH溶液;❷测量完盐酸的温度后,温度计应
冲洗干净并擦干;❸酸碱溶液一次迅速混合。
4.实验数据处理
反应前体系 反应后体系
反应物的温度/℃ 温度差
实验次数 温度 温度
盐酸 NaOH溶液 t/℃ t ℃ (t-t)/℃
1 2/ 1 2
1 25.0 25.2 25.1 28.5 3.4
2 24.9 25.1 25.0 28.3 3.3
3 25.6 25.4 25.5 29.0 3.5
设溶液的密度均为1 g·cm-3,中和后溶液的比热容c=4.18 J·g-1·℃-1,则反应放出的热量Q=cmΔt=
c·[m(盐酸)+m(NaOH溶液)]·(t-t)=4.18 J·g-1·℃-1×(50 g+50 g)×℃≈1 421 J≈1.42 kJ。
2 1
资料收集整理【淘宝店铺:向阳百分百】
10 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司那么生成1 mol H O放出的热量为==56.8 kJ。
2
5.误差分析
若实验时有热量损失,所测中和热偏小,ΔH偏大。求算出的中和热是否接近 kJ·mol-1,取决于溶液
的浓度、溶液的体积及温度的变化。引起中和热测定有较大误差的因素主要有:①溶液浓度不准确;②溶
液量取不准确;③隔热较差;④室温太低;⑤温度未读取到最高点等。
6.中和反应反应热测定实验的注意事项
①隔热关。如量热计保温层内隔热填充材料要填满,故泡沫塑料板和碎泡沫塑料(或纸条)的作用是保温;
盖板上的两孔只需要正好使温度计和环形玻璃棒通过即可;倒入NaOH溶液要迅速,尽可能减少实验过程
中的热量损失。中和热测定实验时用环形玻璃搅拌棒搅拌溶液的方法是上下搅动,不能用金属丝搅拌棒代
替环形玻璃搅拌棒的理由是金属传热快,热量损失大。
②准确关。如配制溶液的浓度要准确;NaOH溶液要新制;量取溶液体积时读数要准确;对温度计的读数
要读到最高点。为保证酸完全中和,采取的措施是若采用的酸、碱浓度相等,可采用碱体积稍过量。
③中和热是强酸强碱的稀溶液生成1 mol H O放出的热量,为57.3 kJ,弱酸弱碱电离时吸热,生成1 mol
2
HO时放出的热量小于57.3 kJ。若用浓硫酸发生中和反应生成1 mol H O时放出的热量大于57.3 kJ。
2 2
④计算时应注意单位的统一,且要注意数据的取舍,无效数据要舍去。
【特别提醒】(1)中和反应反应热是强酸强碱的稀溶液生成1 mol H O放出的热量为57.3 kJ,弱酸弱碱电离
2
时吸热,生成1 mol H O时放出的热量小于57.3 kJ。浓硫酸稀释时放热,生成1 mol H O时放出的热量大
2 2
于57.3 kJ。
(2)对于中和反应反应热、燃烧热,由于它们反应放热是确定的,所以描述中不带“一”,但其焓变为负值。
(3)当用热化学方程式表示中和反应反应热时,生成HO的物质的量必须是1 mol,当用热化学方程式表示
2
燃烧热时,可燃物的物质的量必须为1 mol。
知识点3 能源及利用
1.能源分类
2.解决能源问题的措施
①提高能源的利用效率:a.改善开采、运输、加工等各个环节;b.科学控制燃烧反应,使燃料充分燃烧。
②开发新能源:开发资源丰富、可以再生、没有污染或污染很小的新能源。
考向1 考查燃烧热和中和反应反应热的概念
资料收集整理【淘宝店铺:向阳百分百】
11 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司例1.(2022·河北衡水·河北衡水中学校考模拟预测)化学反应中的能量变化,通常主要表现为热量的变化。
下列相关表述正确的是
A.一定条件下,将 和 置于密闭容器中充分反应生成 放热 ,其热化学方程式为:
B.在 时, 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程式表示为:
C.
D. 和 反应的中和热 ,则 和足量 反应的
【解析】A. 一定条件下,将 和 置于密闭容器中充分反应生成 放热 ,则I 和
2
H 反应生成1molHI(g)时放热大于akJ,放热焓变为负,则其热化学方程式I(g )+H (g) 2HI(g) H
2 2 2
<-2akJ•mol-1,故A错误;B.燃烧热是指在一定压强下,1 mol的可燃物完全燃烧生成稳定的氧化物的时
⇌ △
候所放出的热量;在 时, 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学
方程式表示为: ,B正确;C.硫蒸气的能量比等质量的固态硫
能量高、则等量的硫蒸汽燃烧生成二氧化硫气体比固态硫燃烧放出的热量多,焓变为负值时,放出热量越
多,焓变越小,则 ,故C错误;D.
和 反应的中和热 ,硫酸和足量 反应生成硫酸钡沉淀和水,由于生成沉淀,
也要放热,则 和足量 反应放出的热量大于盐酸和氢氧化钠反应1mol液态HO时放出
2
的热量、即大于57.3kJ,则 和足量 反应的 ,故D错误;答案选B。
【答案】B
【变式训练】有关热化学方程式书写与对应表述均正确的是( )
A.稀硫酸与0.1 mol·L-1NaOH溶液反应:H+(aq)+OH-(aq)= HO(l) H = -57.3 kJ·mol-1
2
B.在101KPa下氢气的燃烧热△H =-285.5 kJ·mol-1, 则水分解的热化学方程式:2HO(l)=2H(g)+O(g)
△ 2 2 2
H = +285.5 kJ·mol-1
C.已知2C(s)+O(g)=2CO(g) H=-221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol-1
△ 2
D.1mol氢气完全燃烧生成液态水放热为285.8kJ,则氢气燃烧的热化学方程式为2H(g)+O(g)=2HO(g)
△ 2 2 2
H=-285.8 kJ· mol-1
【解析】A.在稀溶液中,强酸跟强碱发生中和反应生成1mol液态水时的反应热叫做中和热,则稀硫酸与
△
0.1 mol·L-1NaOH溶液反应:H+(aq)+OH-(aq)= HO(l) H = -57.3 kJ·mol-1,A正确;B.燃烧热是指在
2
25℃、101 kPa时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,则水分解的热化学方程式:
△
2HO(l)=2H(g)+O(g) H = +571.0 kJ·mol-1,B错误;C.根据燃烧热的概念:1mol可燃物完全燃烧生成稳
2 2 2
定的氧化物时放出的热量判断,已知2C(s)+O(g)=2CO(g) H=-221 kJ·mol-1,C燃烧生成的稳定氧化物是
△ 2
CO 而不是CO,CO能和氧气继续反应生成CO,释放能量,则C的燃烧热大于110.5 kJ·mol-1,C错误;
2 2 △
资料收集整理【淘宝店铺:向阳百分百】
12 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司D.1mol氢气完全燃烧生成液态水放热为285.8kJ,而液态水变为气态水需要吸收热量,则氢气燃烧的热化
学方程式应为 H(g)+ O(g)=HO(l) H=-285.8 kJ· mol-1,D错误;故选A。
2 2 2
△
【答案】A
【名师指导】反应热答题规范指导
(1)描述反应热时,无论是用“反应热”“焓变”表示还是用 ΔH表示,其后所跟数值都需要带“+”
“-”符号。如:某反应的反应热(或焓变)为ΔH=-Q kJ·mol-1或ΔH=+Q kJ·mol-1。
(2)由于中和反应和燃烧均是放热反应,表示中和反应反应热和燃烧热时可不带“-”号。如:某物质的燃
烧热为ΔH=-Q kJ·mol-1或Q kJ·mol-1。
考向2 考查中和反应反应热的测定
例2.(双选)下列关于中和反应的反应热测定实验的说法正确的是( )
A.小烧杯内残留水,会使测得的反应热数值偏小
B.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅
C.烧杯间填满碎纸条的作用是固定小烧杯
D.不可用相同浓度和体积的氨水代替稀氢氧化钠溶液进行实验
【解析】小烧杯内残留水,会导致混合液的体积变大,混合液温度降低,温度差减小,测得的反应热数值
偏小,A项正确;在中和热的测定过程中,酸、碱混合时要迅速,防止热量的散失,B项错误;烧杯间填
满碎纸条的作用是保温,减少热量的散失,C项错误;中和热是稀的强酸和强碱溶液反应生成1 mol水时
所放出的热量,若用相同浓度和体积的氨水代替稀氢氧化钠溶液进行实验,测得的中和热数值偏小,D项
正确。
【答案】AD
【变式训练】(1)中和反应反应热测定的实验中,用到的玻璃仪器有烧杯、温度计、____________、
________。
(2)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是________(填选项字母)。
A.50 mL 0.50 mol·L-1NaOH溶液
B.50 mL 0.55 mol·L-1NaOH溶液
C.1.0 g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得中和反应反应热的数值________(填“偏大”“偏小”或“无影
响”)。
【解析】(1)中和反应的反应热测定的实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒。
(2)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入等体积但浓度略大的NaOH溶液,使酸被完全
中和,并且根据酸的浓度和体积计算生成水的物质的量。(3)实验时大烧杯上若不盖硬纸板,则中和放出的
热量散失较多,温度计测得的温度偏小,中和反应放出的热量偏小。
【答案】(1)环形玻璃搅拌棒 量筒 (2)B (3)偏小
【思维建模】中和反应反应热的测定实验中的注意事项
(1)实验所用的酸和碱溶液应当用稀溶液,否则会造成较大误差。
资料收集整理【淘宝店铺:向阳百分百】
13 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(2)量取酸和碱时,应当分别使用不同的量筒量取。
(3)使用同一温度计分别先后测量酸、碱及混合液的最高温度时,测完一种溶液后必须用水冲洗干净并用滤
纸擦干再测另一种溶液的温度。
(4)取多次实验起始温度(t)、终止温度(t)的平均值代入公式计算,计算时应注意单位的统一。
1 2
考向3 考查能源的开发与利用
例3.中国向全世界宣布,努力争取2060年前实现碳中和。下列措施不利于大气中CO 减少的是( )
2
A.用氨水捕集废气中的CO,将其转化为氮肥
2
B.大力推广使用风能、水能、氢能等清洁能源
C.大力推广使用干冰实现人工增雨,缓解旱情
D.通过植树造林,利用光合作用吸收大气中的CO
2
【解析】氨水能与酸性氧化物二氧化碳反应生成碳酸铵或碳酸氢铵,则用氨水捕集废气中的二氧化碳,将
其转化为氮肥有利于大气中二氧化碳的减少,故A不符合题意;大力推广使用风能、水能、氢能等清洁能
源可以减少化石能源的使用,从而减少二氧化碳气体的排放,有利于大气中二氧化碳的减少,故B不符合
题意;大力推广使用干冰实现人工增雨,会增加大气中二氧化碳的量,不利于大气中二氧化碳的减少,故
C符合题意;通过植树造林,利用光合作用吸收大气中的二氧化碳有利于大气中二氧化碳的减少,故D不
符合题意。
【答案】C
【名师归纳】新能源是指以新技术为基础,系统开发利用的能源,包括太阳能、生物质能、风能、海洋能、
地热能等。
考点三 盖斯定律 反应热计算
知识点1 盖斯定律
1.内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的反应
热只与反应体系的始态和终态有关,而与反应的途径无关。
2.意义:应用盖斯定律可以间接计算以下情况(不能直接测定)的反应热
(1)有些反应进行得很慢。
(2)有些反应不容易直接发生。
(3)有些反应的生成物不纯(有副反应发生)。
3.应用
热化学方程式 焓变之间的关系
aA===B ΔH
1
ΔH=ΔH 或ΔH=aΔH
2 1 1 2
A===B ΔH
2
aA===B ΔH
1
ΔH=-ΔH
1 2
B===aA ΔH
2
资料收集整理【淘宝店铺:向阳百分百】
14 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司ΔH=ΔH+ΔH
1 2
运算规则:根据目标方程式,确定要保留的物质和要消去的物质,运用加、减、乘、除四则运算得
到所求目标方程式(调整位置和系数)。
目标物质 方程式数学运算 反应热 小技巧
调位置 加减 同时相加减 将一个热化学方程式颠倒时,ΔH的
调系数 乘除某数 同时相乘除某数 “+”“-”随之改变,但数值不变。
知识点2 反应热的计算
1.利用热化学方程式进行有关计算
根据已知的热化学方程式和已知的反应物或生成物的物质的量或反应吸收或放出的热量,可以把反应热当
作“产物”,计算反应放出或吸收的热量。
2.根据燃烧热数据,计算反应放出的热量
计算公式:Q=燃烧热×n(可燃物的物质的量)
3.根据旧键断裂和新键形成过程中的能量差计算焓变
若反应物旧化学键断裂吸收能量E,生成物新化学键形成放出能量E,则反应的ΔH=E-E。
1 2 1 2
4.利用键能计算反应热的方法
A.熟记反应热ΔH的计算公式:ΔH=E(反应物的总键能之和)-E(生成物的总键能之和)
B.注意特殊物质中键数的判断
物质(1 mol) P C(金刚石) 石墨 Si SiO CO CH
4 2 2 4
化学键 P—P C—C C—C Si—Si Si—O C==O C—H
键数(mol) 6 2 1.5 2 4 2 4
5.利用盖斯定律计算
A.运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已知的热化学
方程式。
二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
B.运用盖斯定律的三个注意事项
①热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
资料收集整理【淘宝店铺:向阳百分百】
15 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司②热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
③将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
知识点3 反应热大小的比较
1、比较方法:
1)看物质状态。物质的气、液、固三态转化时的能量变化如下:
2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热反应的ΔH越小,吸热反应的
ΔH越大。
4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应的程度越大,热量变化越大。
2.名师技巧
(1)直接比较法
①物质燃烧时,可燃物物质的量越大,燃烧放出的热量越多。
②等量的可燃物完全燃烧所放出的热量肯定比不完全燃烧所放出的热量多。
③生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱或弱碱和强酸或弱酸和弱碱的稀溶液反应放出
的热量多。
④对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的热量要小于相应热化学方程式中的
反应热数值。例如:2SO (g)+O(g ) 2SO (g) ΔH=-197 kJ·mol-1,表示2 mol SO (g)和1 mol
2 2 3 2
O(g)完全反应生成2 mol SO (g)时,放出的热量为197 kJ,实际上向密闭容器中通入2 mol SO (g)和1 mol
2 3 2
O(g),反应达到平衡后,放出的热量要小于197 kJ。
2
(2)盖斯定律比较法
①同一反应,生成物状态不同时
如A(g)+B(g)===C(g) ΔH<0
1
A(g)+B(g)===C(l) ΔH<0
2
C(g)===C(l) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
1 3 2 1 2 3
所以ΔH<ΔH。
2 1
②同一反应,反应物状态不同时
如S(g)+O(g)===SO (g) ΔH<0
2 2 1
资料收集整理【淘宝店铺:向阳百分百】
16 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司S(s)+O(g)===SO (g) ΔH<0
2 2 2
S(g)===S(s) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
2 3 1 1 2 3
所以ΔH<ΔH。
1 2
③晶体类型不同,产物相同时
C(石墨,s)+O(g)===CO(g) ΔH=-a kJ·mol-1
2 2 1
C(金刚石,s)+O(g)===CO(g) ΔH=-b kJ·mol-1
2 2 2
因为石墨能量低,则C(石墨,s)===C(金刚石,s) ΔH=ΔH-ΔH>0,所以ΔH>ΔH。
3 1 2 1 2
④两个有联系的不同反应相比较时
C(s)+O(g)===CO(g) ΔH<0
2 2 1
C(s)+(1/2)O(g)===CO(g) ΔH<0
2 2
C(s)――→CO(g)
2
C(s)――→CO(g)――→CO(g)
2
因为ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,所以ΔH<ΔH。
2 3 1 1 2 3 1 2
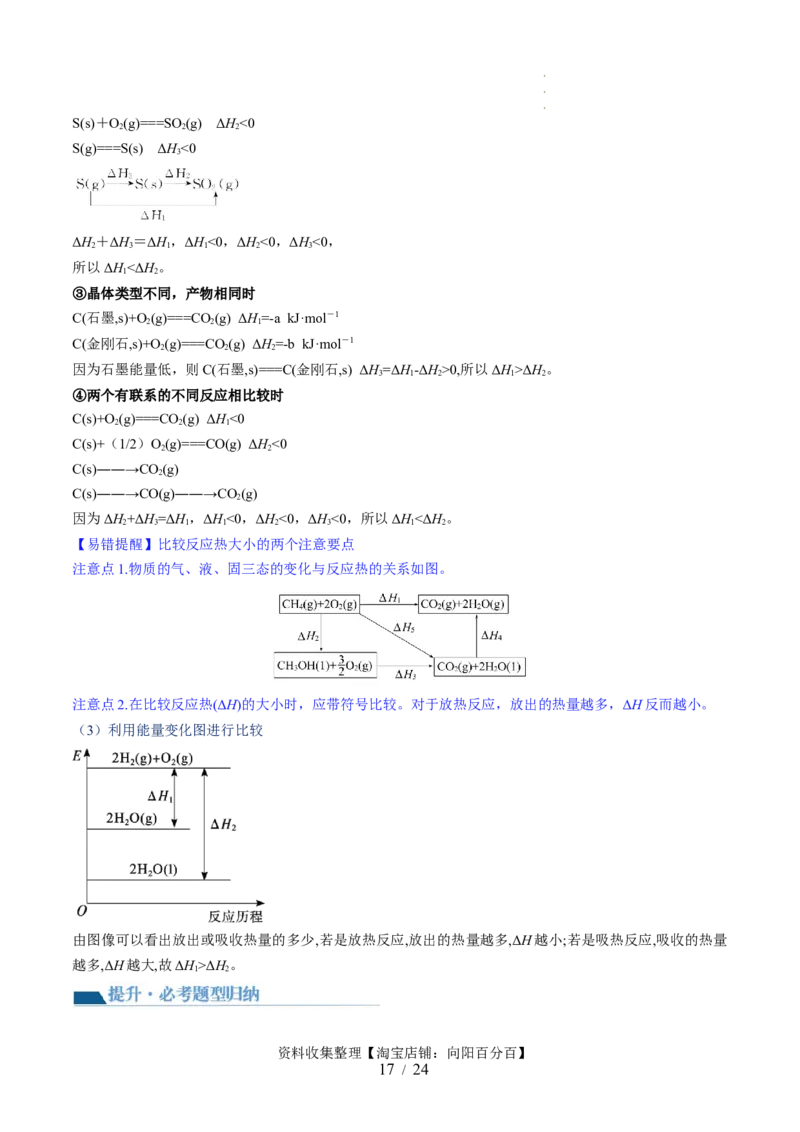
【易错提醒】比较反应热大小的两个注意要点
注意点1.物质的气、液、固三态的变化与反应热的关系如图。
注意点2.在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。
(3)利用能量变化图进行比较
由图像可以看出放出或吸收热量的多少,若是放热反应,放出的热量越多,ΔH越小;若是吸热反应,吸收的热量
越多,ΔH越大,故ΔH>ΔH。
1 2
资料收集整理【淘宝店铺:向阳百分百】
17 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司考向1 考查盖斯定律的应用
例1.(2023·浙江金华·校联考模拟预测)某小组为测定NaCl晶体中离子键断裂时所需要的能量( H),设
4
计了如图所示的转化关系,则△H 可表示为
4 △
A.△H+ H- H- H+ H B.△H+ H+ H- H+ H
1 2 3 5 6 1 2 3 5 6
C.△H+ H+ H- H- H D.△H+ H- H- H- H
1 △ 2 △ 3△ 5 △ 6 3 △ 5 △ 1 △ 2 △ 6
【解析】由图可知,氯化钠和溴化钠固体通过过程1、2、6得到的微粒和通过过程3、4、5得到的微粒都
△ △ △ △ △ △ △ △
是Na+(g)、Br-(aq)、Na+(aq)、Cl-(aq),故两部分的反应热相同,△H+ H + H= H+ H+ H,即
3 4 5 1 2 6
△H= H+ H- H- H+ H;故选A。
4 1 2 3 5 6 △ △ △ △ △
【答案】A
△ △ △ △ △
【变式训练】(2022·浙江·模拟预测)已知离子键的强弱与离子电荷高低和离子半径大小等有关;当离子
电荷相同时,离子半径越小,离子键相对越强。 ( ,Na)体系的能量循环如图,下列判断正确的
是
A. ,
B.
C.
D.
【解析】A.非金属得电子生成阴离子(更加稳定)是放热的, ; (断键吸热),A错误;B.
一般金属失电子生成金属阳离子是吸热的(需消耗能量), ,由于 的离子半径大于 的离子半
径, 的离子键强度弱于 , ,B错误;C. ,生成 放出热量
多, ,C错误;D.根据盖斯定律, ,
, (晶体吸热变气体)、 (断键吸热),D正确;故选:D。
【答案】D
【思维建模】利用盖斯定律求反应热的三步流程
资料收集整理【淘宝店铺:向阳百分百】
18 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司根据待求解的热化学方程式中的反应物和生成物找出可用的已知热化学方
找出
程式
①根据待求解的热化学方程式调整可用热化学方程式的方向,同时调整
ΔH的符号。
调整
②根据待求解的热化学方程式将调整好的热化学方程式进行缩小或扩大相
应的倍数,同时调整ΔH的值
加和
将调整好的热化学方程式和ΔH分别进行加和。确定目标反应的焓变ΔH
求ΔH
考向2 考查反应热的相关计算
例2.(2023·重庆·重庆南开中学校考三模)将2 mol 和3 mol 置于密闭容器中,在250℃下只发生
如下两个反应:
kJ/mol
kJ/mol
一段时间后, 和 恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
化学键 (ClF中) ( 中)
键能/(kJ/mol) 157 243 248 X
则X的值为
A.172 B.202 C.238 D.258
【分析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),可求出a,以及用x把b表示出
来,然后根据化学方程式的计算可解。
【解析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),由题意Cl
2
+F
2
═2ClF ΔH
1
=
akJ/mol;Cl
2
+3F
2
═2ClF
3
ΔH
2
=bkJ/mol可知;ΔH
1
=(243+157−2×248)kJ/mol=−96kJ/mol,ΔH
2
=(243
+3×157−2×3x)kJ/mol=(714−6x)kJ/mol,即a=−96,b=714−6x,设参与Cl
2
+F
2
═2ClF ΔH1=akJ/mol
的氯气物质的量为m,则消耗的氟气也为m,剩下的氯气和氟气正好按Cl+3F═2ClF ΔH=bkJ/mol的系
2 2 3 2
数比反应,即 ,解之得,m=1.5mol,则有1.5mol×(−96kJ/mol)+0.5mol×(714−6x)kJ/mol=
303kJ,解之得x=172,故答案选A。
【答案】A
【变式训练】(2023·重庆九龙坡·统考二模)火箭发射时可以用液态肼作燃料, 作氧化剂。相关物质
的能量转化关系如下。已知 ,则
的反应热 为
资料收集整理【淘宝店铺:向阳百分百】
19 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司A. B. C. D.
【解析】根据图示信息,可得已知反应:
可得目标方程式: ,所以
,故选A。
【答案】A
【思维建模】计算ΔH的三种基本公式
(1)利用键能计算反应热的方法
①熟记反应热ΔH的计算公式:ΔH=E(反应物的总键能之和)-E(生成物的总键能之和)
②注意特殊物质中键数的判断
物质(1 mol) P C(金刚石) 石墨 Si SiO
4 2
键数(mol) 6 2 1.5 2 4
(2)ΔH=生成物总能量-反应物总能量=H(生成物)-H(反应物)。
(3)ΔH=正反应活化能-逆反应活化能。
考向3 考查反应热大小的比较
例3.(2023·江西抚州·江西省乐安县第二中学校考一模)已知:S(s)+O (g)=SO (g) H=-297.23kJ/mol,
2 2
下列说法正确的
△
A.S(g)+O(g)=SO (g) H=-QkJ/mol;Q的值等于297.23
2 2
B.S(g)+O(g)=SO (g) H=-QkJ/mol;Q的值小于297.23
2 2 △
C.1molSO (g)的能量总和大于1molS(s)和1molO (g)的能量总和
2 △ 2
D.1molSO (g)的能量总和小于1molS(s)和1molO (g)的能量总和
2 2
【分析】物质由固态转变成气态要吸收热量,放热反应中反应物的总能量大于生成物的总能量。
【解析】A. 因物质由固态转变成气态也要吸收热量,所以S(g)+O(g)=SO (g) H=-QkJ/mol中Q的值大于
2 2
297.23,故A错误;B. 因物质由固态转变成气态也要吸收热量,所以S(g)+O(g)=SO (g) H=-QkJ/mol中
2△ 2
Q的值大于297.23,故B错误;C. 放热反应中反应物的总能量大于生成物的总能量,所以1molSO (g)的能
△ 2
量总和小于1molS(s)和1molO (g)的能量总和,故C错误;D. 放热反应中反应物的总能量大于生成物的总
2
能量,所以1molSO (g)的能量总和小于1molS(s)和1molO (g)的能量总和,故D正确;答案选D。
2 2
【答案】D
资料收集整理【淘宝店铺:向阳百分百】
20 / 24
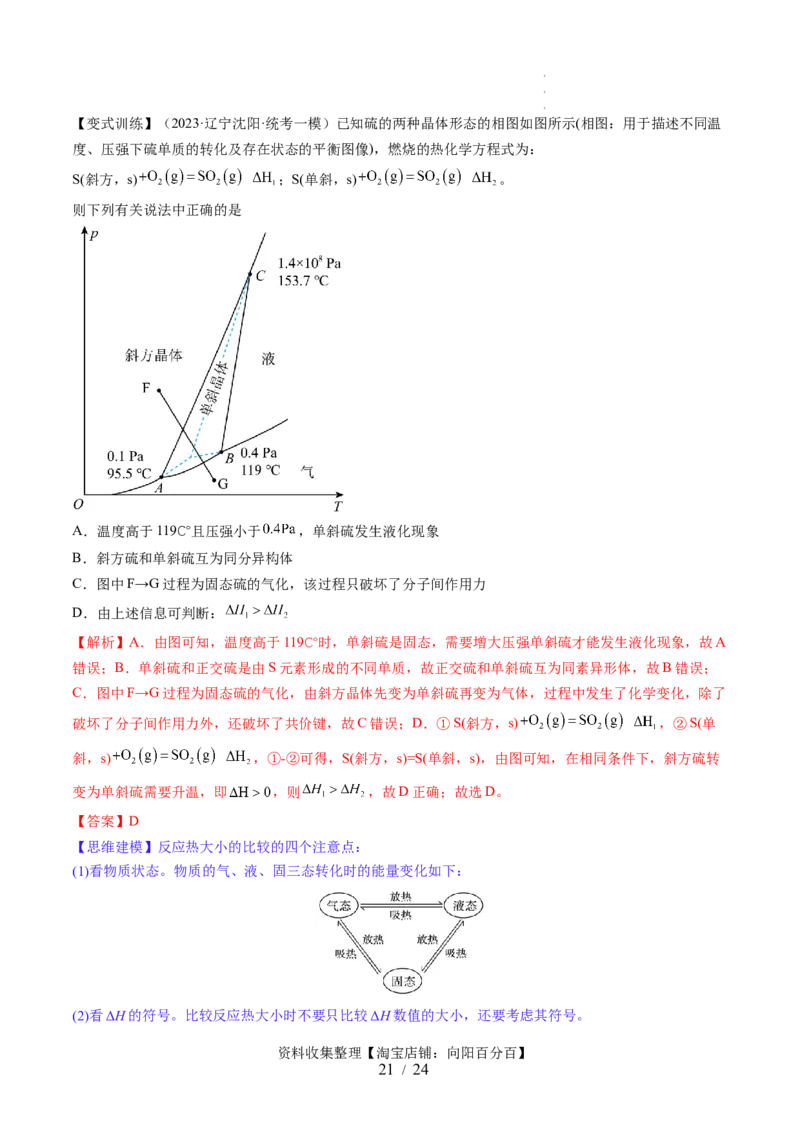
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【变式训练】(2023·辽宁沈阳·统考一模)已知硫的两种晶体形态的相图如图所示(相图:用于描述不同温
度、压强下硫单质的转化及存在状态的平衡图像),燃烧的热化学方程式为:
S(斜方,s) ;S(单斜,s) 。
则下列有关说法中正确的是
A.温度高于119℃且压强小于 ,单斜硫发生液化现象
B.斜方硫和单斜硫互为同分异构体
C.图中F→G过程为固态硫的气化,该过程只破坏了分子间作用力
D.由上述信息可判断:
【解析】A.由图可知,温度高于119℃时,单斜硫是固态,需要增大压强单斜硫才能发生液化现象,故A
错误;B.单斜硫和正交硫是由S元素形成的不同单质,故正交硫和单斜硫互为同素异形体,故B错误;
C.图中F→G过程为固态硫的气化,由斜方晶体先变为单斜硫再变为气体,过程中发生了化学变化,除了
破坏了分子间作用力外,还破坏了共价键,故C错误;D.①S(斜方,s) ,②S(单
斜,s) ,①-②可得,S(斜方,s)=S(单斜,s),由图可知,在相同条件下,斜方硫转
变为单斜硫需要升温,即 ,则 ,故D正确;故选D。
【答案】D
【思维建模】反应热大小的比较的四个注意点:
(1)看物质状态。物质的气、液、固三态转化时的能量变化如下:
(2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
资料收集整理【淘宝店铺:向阳百分百】
21 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热反应的ΔH越小,吸热反应的
ΔH越大。
(4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应的程度越大,热量变化越大。
1.(2022·重庆·统考高考真题)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH )SO 的
4 2 4
离子键强弱,设计如图所示的循环过程,可得△H/(kJ•mol-1)为
4
A.+533 B.+686 C.+838 D.+1143
【答案】C
【解析】① ;② ;③
;④ ;⑤
;⑥ ;则⑤+①-⑥-
②+③得④,得到 +838 kJ•mol-1 所以A B D错误, C正确,故选C。
,
2.(2023·北京·统考高考真题)一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表
或 中的一种。下列说法正确的是
A.a、c分别是
B. 既可以是 ,也可以是
C.已知 为副产物,则通入水蒸气可减少 的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
资料收集整理【淘宝店铺:向阳百分百】
22 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【答案】C
【分析】 分解的产物是 和 ,分解得到的 与 反应生成 , 又可
以分解得到 和 ,则a为 ,b为 ,c为 ,d为 。
【解析】A.由分析可知,a为 ,c为 ,A项错误;B.d为 ,B错误;C.可以水解生成
,通入水蒸气可以减少 的生成,C正确;D.反应①和反应②相加即为氯化铵直接分解
的反应,由盖斯定律可知,等压条件下,反应①、反应②的反应热之和等于氯化铵直接分解的反应热,D
错误;故选C。
3.(2021·浙江·统考高考真题)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,
2 2 3
N (g) 、H(g)和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物
2 2 3
[N (g) +3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是
2 2 3
A. B.
C. D.
【答案】B
【解析】该反应为放热反应,反应物的总能量大于生成物的总能量,根据题目中给出的反应物与生成物的
比热容可知,升高温度反应物能量升高较快,反应结束后反应放出的热量也会增大,比较4个图象B符合
资料收集整理【淘宝店铺:向阳百分百】
23 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司题意,故答案选B。
4.(2023·浙江·高考真题)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
和 的相对能量为0],下列说法不正确的是
A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【分析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。
【解析】A.催化剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;B.已知
的相对能量为0,对比两个历程可知, 的相对能量为 ,则 键能为
,B正确;C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转化率:
历程Ⅱ=历程Ⅰ,C错误;D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最
低,所以速率最快的一步反应的热化学方程式为: ,D
正确;故答案为:C。
资料收集整理【淘宝店铺:向阳百分百】
24 / 24
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司