文档内容
第 21 讲 化学平衡状态 化学平衡的移动
第一部分:高考真题感悟
1.(2022·海南·高考真题)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,
2 2 2 3 2
下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
2.(2022·北京·高考真题)某 的多孔材料刚好可将 “固定”,实现了 与 分离并制备
,如图所示:
己知:
下列说法不正确的是
A.气体温度升高后,不利于 的固定
B. 被固定后,平衡正移,有利于 的去除
C.制备 的原理为:
D.每制备 ,转移电子数约为
3.(2022·辽宁·高考真题)某温度下,在 恒容密闭容器中 发生反应 ,有关数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
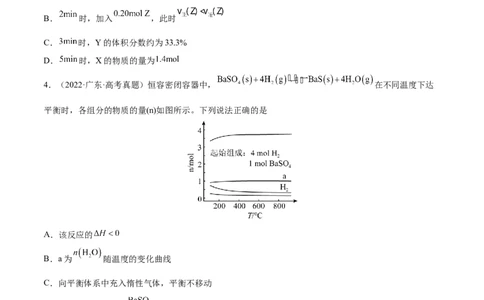
4.(2022·广东·高考真题)恒容密闭容器中, 在不同温度下达
平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
5.(2022·浙江·高考真题)关于反应 ,达到平衡后,
下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上
述反应存在限度
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海交大附中模拟预测) 可生产 并进而制得硫酸等,其反应原理为:
。下列说法正确的是
A.该反应在工业上需要在高温高压下进行
B.反应速率平衡后再通入 、 的体积分数一定增加
C.反应在高温、催化剂条件下进行可提高 的平衡转化率
D. 和 充分反应放出的热量小于196.6kJ
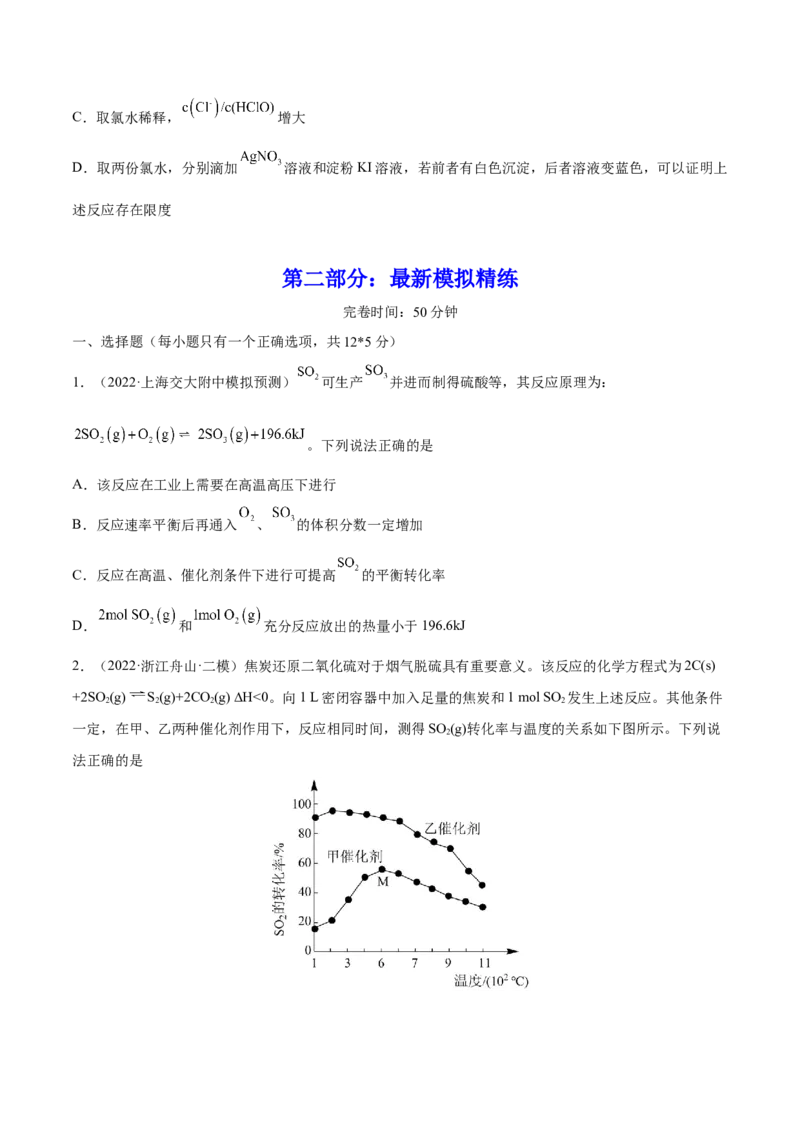
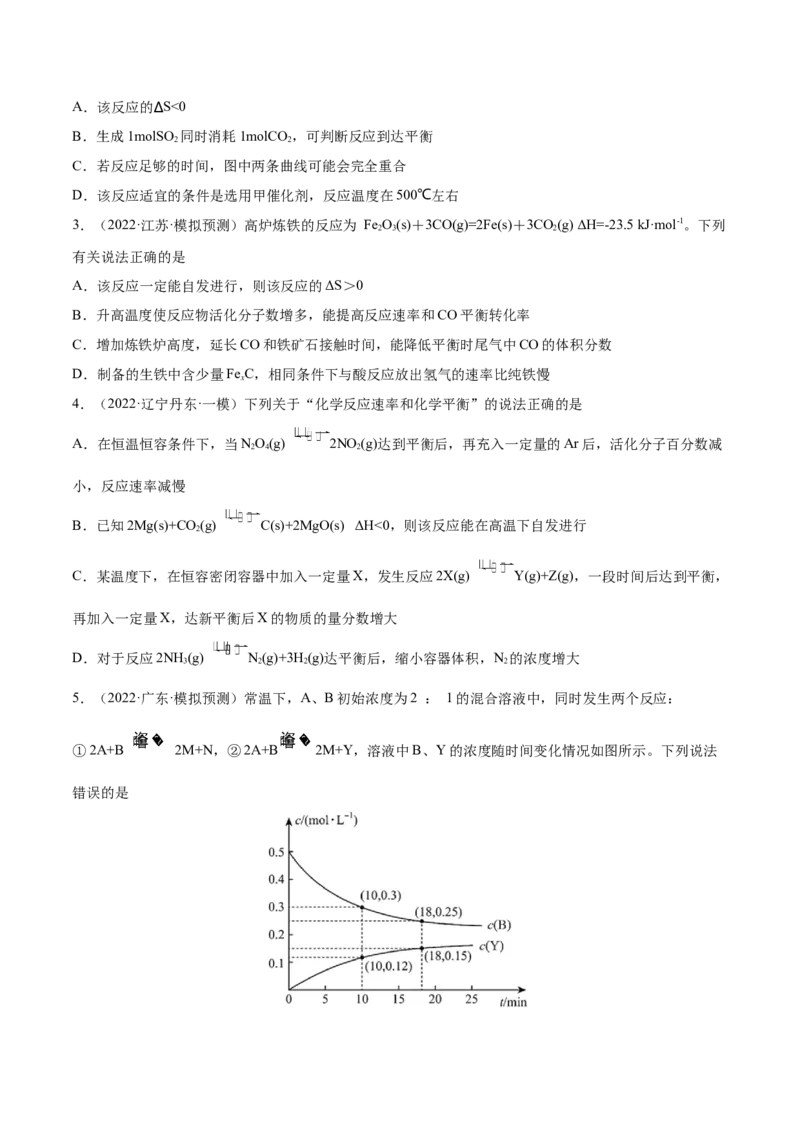
2.(2022·浙江舟山·二模)焦炭还原二氧化硫对于烟气脱硫具有重要意义。该反应的化学方程式为2C(s)
+2SO(g) S(g)+2CO (g) ∆H<0。向1 L密闭容器中加入足量的焦炭和1 mol SO 发生上述反应。其他条件
2 2 2 2
一定,在甲、乙两种催化剂作用下,反应相同时间,测得SO (g)转化率与温度的关系如下图所示。下列说
2
法正确的是A.该反应的∆S<0
B.生成1molSO 同时消耗1molCO ,可判断反应到达平衡
2 2
C.若反应足够的时间,图中两条曲线可能会完全重合
D.该反应适宜的条件是选用甲催化剂,反应温度在500℃左右
3.(2022·江苏·模拟预测)高炉炼铁的反应为 Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=-23.5 kJ·mol-1。下列
2 3 2
有关说法正确的是
A.该反应一定能自发进行,则该反应的ΔS>0
B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率
C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数
D.制备的生铁中含少量FeC,相同条件下与酸反应放出氢气的速率比纯铁慢
x
4.(2022·辽宁丹东·一模)下列关于“化学反应速率和化学平衡”的说法正确的是
A.在恒温恒容条件下,当NO(g) 2NO (g)达到平衡后,再充入一定量的Ar后,活化分子百分数减
2 4 2
小,反应速率减慢
B.已知2Mg(s)+CO (g) C(s)+2MgO(s) ΔH<0,则该反应能在高温下自发进行
2
C.某温度下,在恒容密闭容器中加入一定量X,发生反应2X(g) Y(g)+Z(g),一段时间后达到平衡,
再加入一定量X,达新平衡后X的物质的量分数增大
D.对于反应2NH (g) N(g)+3H(g)达平衡后,缩小容器体积,N 的浓度增大
3 2 2 2
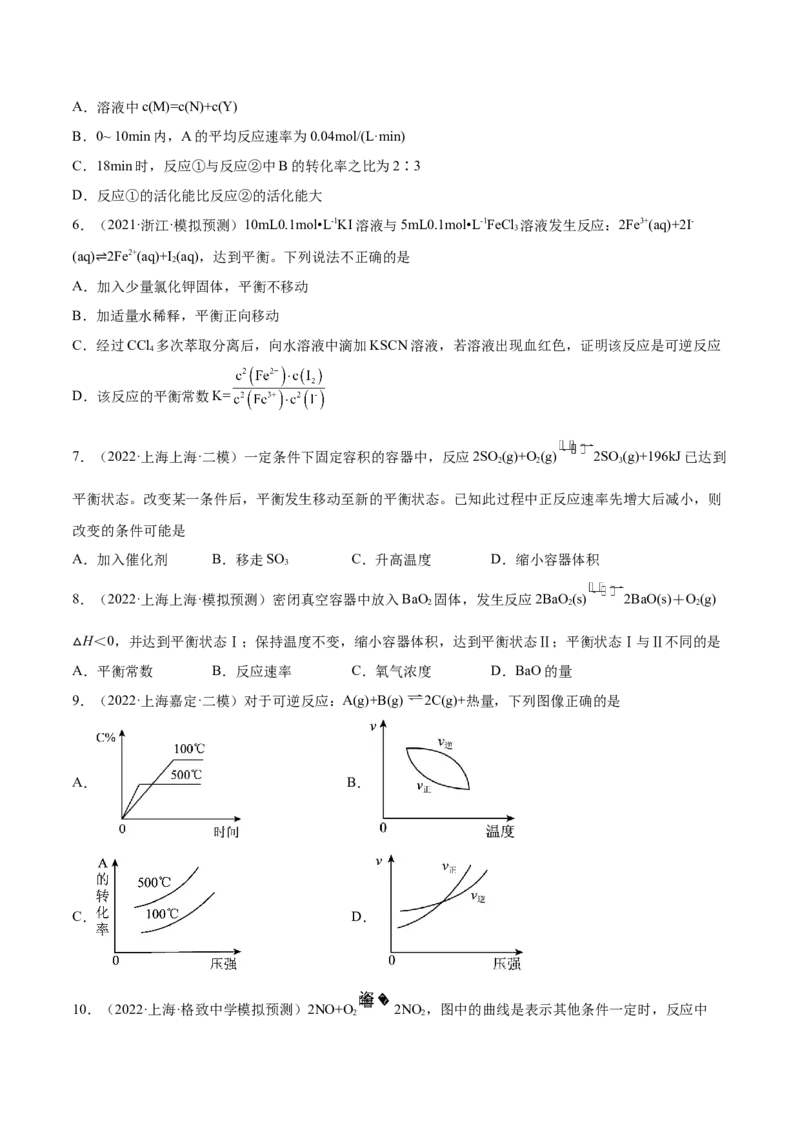
5.(2022·广东·模拟预测)常温下,A、B初始浓度为2 : 1的混合溶液中,同时发生两个反应:
①2A+B 2M+N,②2A+B 2M+Y,溶液中B、Y的浓度随时间变化情况如图所示。下列说法
错误的是A.溶液中c(M)=c(N)+c(Y)
B.0~ 10min内,A的平均反应速率为0.04mol/(L·min)
C.18min时,反应①与反应②中B的转化率之比为2∶3
D.反应①的活化能比反应②的活化能大
6.(2021·浙江·模拟预测)10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl 溶液发生反应:2Fe3+(aq)+2I-
3
(aq) 2Fe2+(aq)+I (aq),达到平衡。下列说法不正确的是
2
A.⇌加入少量氯化钾固体,平衡不移动
B.加适量水稀释,平衡正向移动
C.经过CCl 多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该反应是可逆反应
4
D.该反应的平衡常数K=
7.(2022·上海上海·二模)一定条件下固定容积的容器中,反应2SO (g)+O(g) 2SO (g)+196kJ已达到
2 2 3
平衡状态。改变某一条件后,平衡发生移动至新的平衡状态。已知此过程中正反应速率先增大后减小,则
改变的条件可能是
A.加入催化剂 B.移走SO C.升高温度 D.缩小容器体积
3
8.(2022·上海上海·模拟预测)密闭真空容器中放入BaO 固体,发生反应2BaO(s) 2BaO(s)+O(g)
2 2 2
H<0,并达到平衡状态Ⅰ;保持温度不变,缩小容器体积,达到平衡状态Ⅱ;平衡状态Ⅰ与Ⅱ不同的是
△A.平衡常数 B.反应速率 C.氧气浓度 D.BaO的量
9.(2022·上海嘉定·二模)对于可逆反应:A(g)+B(g) 2C(g)+热量,下列图像正确的是
A. B.
C. D.
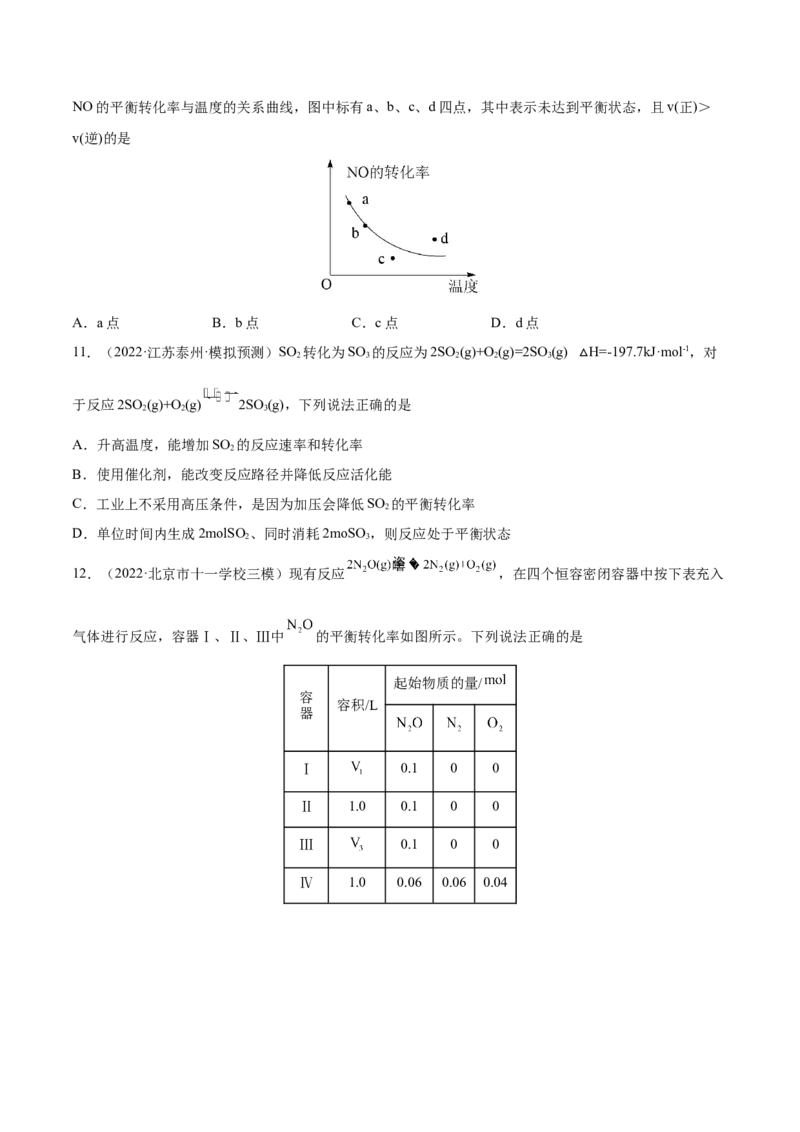
10.(2022·上海·格致中学模拟预测)2NO+O 2NO ,图中的曲线是表示其他条件一定时,反应中
2 2NO的平衡转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>
v(逆)的是
A.a点 B.b点 C.c点 D.d点
11.(2022·江苏泰州·模拟预测)SO 转化为SO 的反应为2SO (g)+O(g)=2SO(g) H=-197.7kJ·mol-1,对
2 3 2 2 3
△
于反应2SO (g)+O(g) 2SO (g),下列说法正确的是
2 2 3
A.升高温度,能增加SO 的反应速率和转化率
2
B.使用催化剂,能改变反应路径并降低反应活化能
C.工业上不采用高压条件,是因为加压会降低SO 的平衡转化率
2
D.单位时间内生成2molSO 、同时消耗2moSO,则反应处于平衡状态
2 3
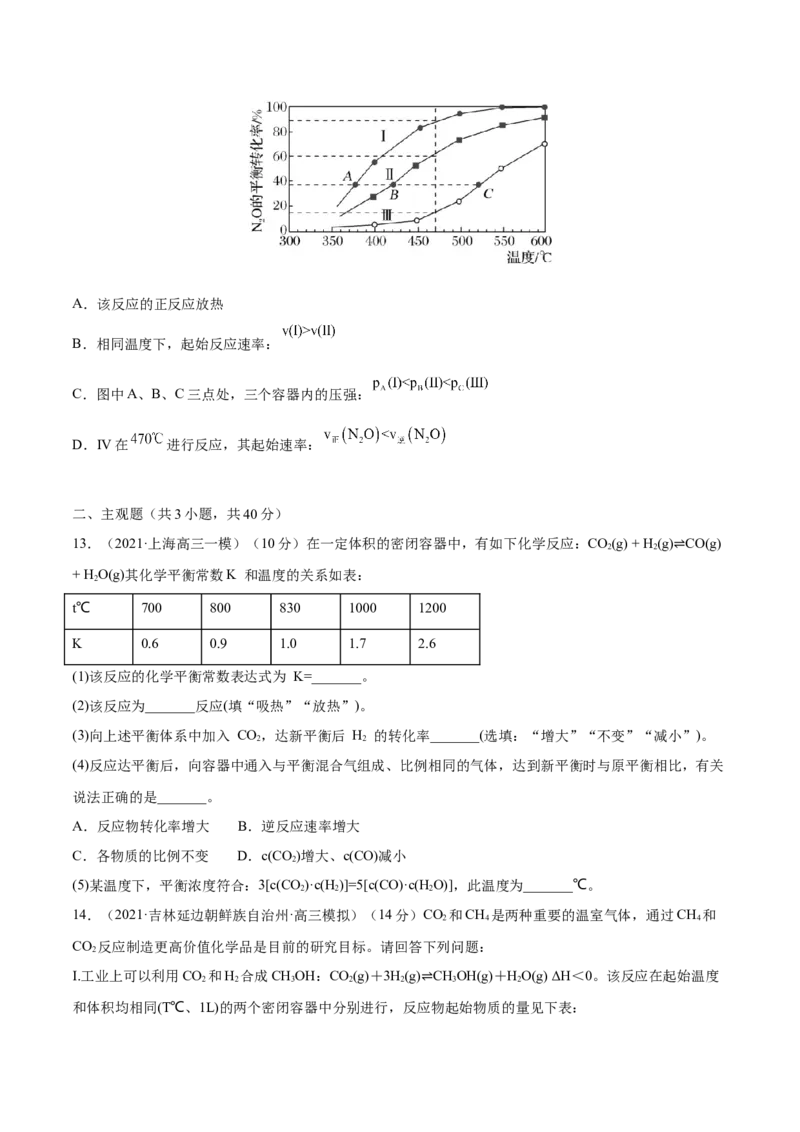
12.(2022·北京市十一学校三模)现有反应 ,在四个恒容密闭容器中按下表充入
气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中 的平衡转化率如图所示。下列说法正确的是
起始物质的量/
容
容积/L
器
Ⅰ 0.1 0 0
Ⅱ 1.0 0.1 0 0
Ⅲ 0.1 0 0
Ⅳ 1.0 0.06 0.06 0.04A.该反应的正反应放热
B.相同温度下,起始反应速率:
C.图中A、B、C三点处,三个容器内的压强:
D.IV在 进行反应,其起始速率:
二、主观题(共3小题,共40分)
13.(2021·上海高三一模)(10分)在一定体积的密闭容器中,有如下化学反应:CO(g) + H(g) CO(g)
2 2
+ H O(g)其化学平衡常数K 和温度的关系如表: ⇌
2
t℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
(1)该反应的化学平衡常数表达式为 K=_______。
(2)该反应为_______反应(填“吸热”“放热”)。
(3)向上述平衡体系中加入 CO,达新平衡后 H 的转化率_______(选填:“增大”“不变”“减小”)。
2 2
(4)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关
说法正确的是_______。
A.反应物转化率增大 B.逆反应速率增大
C.各物质的比例不变 D.c(CO)增大、c(CO)减小
2
(5)某温度下,平衡浓度符合:3[c(CO)·c(H)]=5[c(CO)·c(H O)],此温度为_______℃。
2 2 2
14.(2021·吉林延边朝鲜族自治州·高三模拟)(14分)CO 和CH 是两种重要的温室气体,通过CH 和
2 4 4
CO 反应制造更高价值化学品是目前的研究目标。请回答下列问题:
2
I.工业上可以利用CO 和H 合成CHOH:CO(g)+3H(g) CHOH(g)+HO(g) ΔH<0。该反应在起始温度
2 2 3 2 2 3 2
和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应⇌物起始物质的量见下表:CO(mol) H(mol) CHOH(mol) HO(mol)
2 2 3 2
反应a(恒温恒容) 1 3 0 0
反应b(绝热恒容) 0 0 1 1
(1)达到平衡时,反应a,b对比:CO 的体积分数φ(a)_______φ(b)(填“>”、“<”或“=”))。
2
(2)下列能说明反应a达到平衡状态的是_______(填字母)。
A.v (CO)=3v (H )
正 2 逆 2
B.混合气体的平均摩尔质量不再改变
C.c(CHOH)=c(H O)
3 2
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO(g)+4H(g) CH(g)+2HO(g) ΔH<0
2 2 4 2
反应2:CO
2
(g)+H
2
(g) CO(g)+⇌H
2
O(g) ΔH>0
在密闭容器中通入3m⇌ol的的H
2
和1mol的CO
2
,分别在1MPa和10MPa下进行反应。实验中对平衡体系组
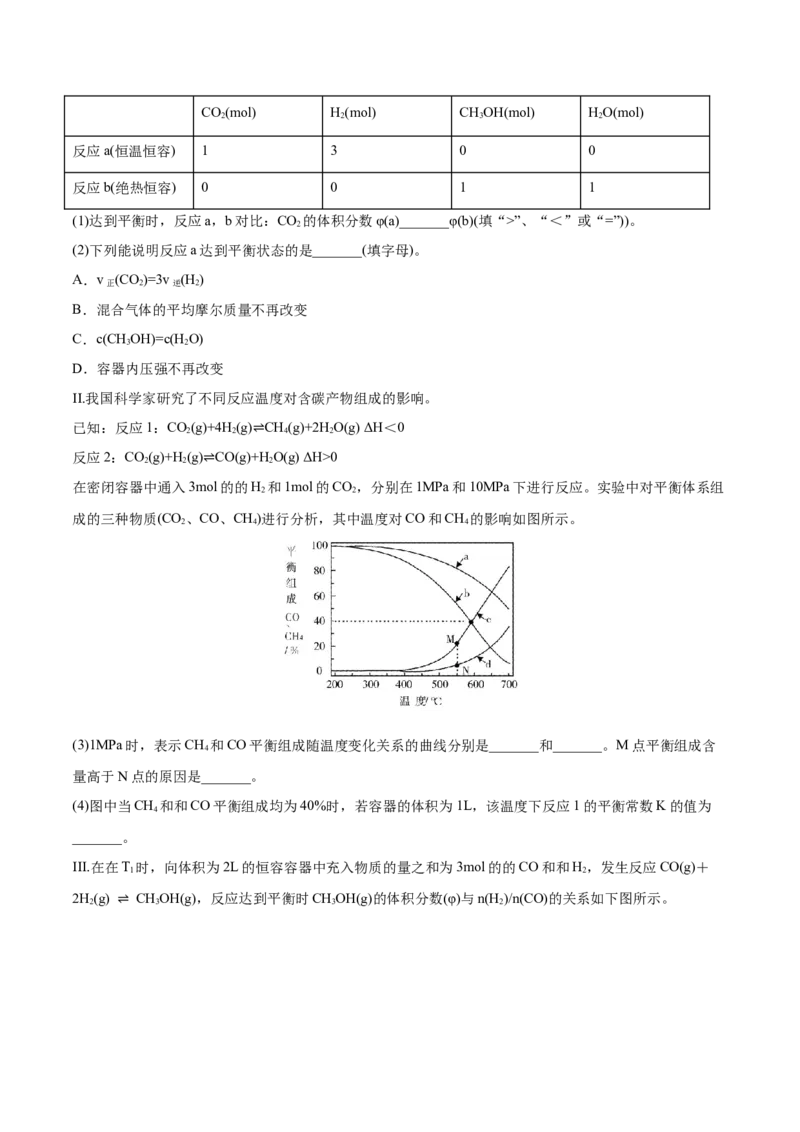
成的三种物质(CO、CO、CH)进行分析,其中温度对CO和CH 的影响如图所示。
2 4 4
(3)1MPa时,表示CH 和CO平衡组成随温度变化关系的曲线分别是_______和_______。M点平衡组成含
4
量高于N点的原因是_______。
(4)图中当CH 和和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为
4
_______。
III.在在T 时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和和H,发生反应CO(g)+
1 2
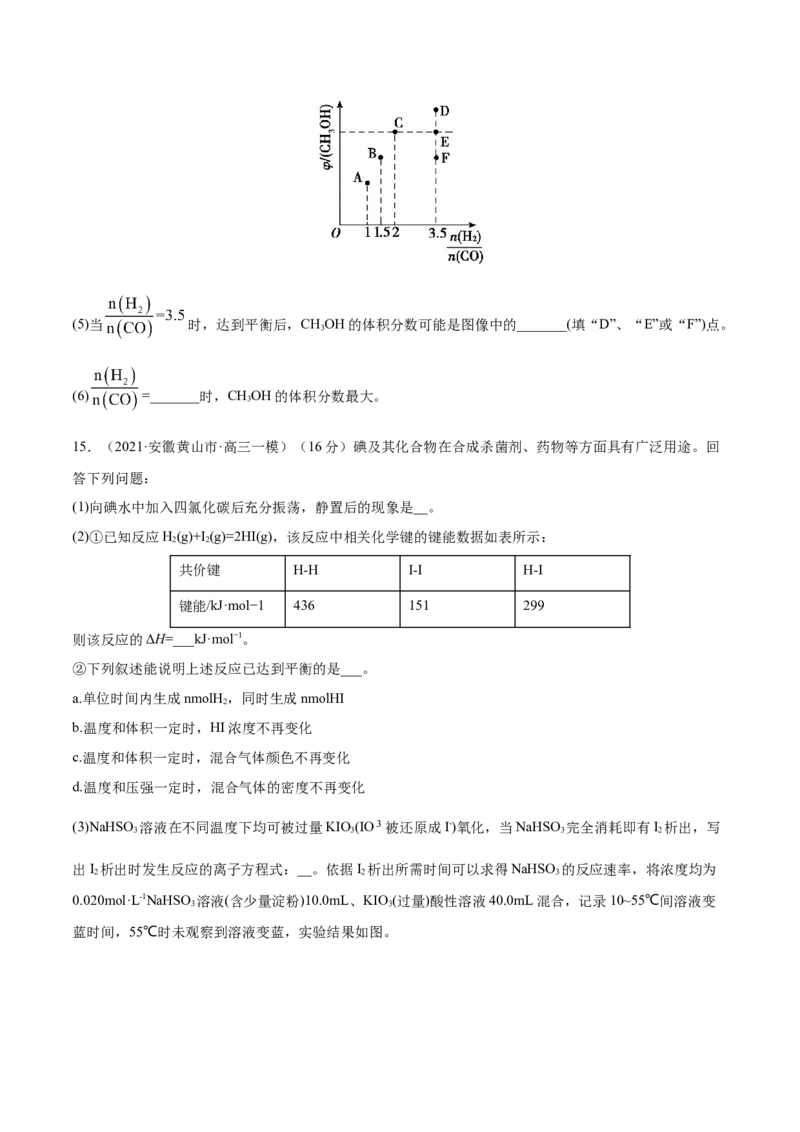
2H(g) CHOH(g),反应达到平衡时CHOH(g)的体积分数(φ)与n(H )/n(CO)的关系如下图所示。
2 3 3 2
⇌(5)当 时,达到平衡后,CHOH的体积分数可能是图像中的_______(填“D”、“E”或“F”)点。
3
(6) =_______时,CHOH的体积分数最大。
3
15.(2021·安徽黄山市·高三一模)(16分)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回
答下列问题:
(1)向碘水中加入四氯化碳后充分振荡,静置后的现象是__。
(2)①已知反应H(g)+I (g)=2HI(g),该反应中相关化学键的键能数据如表所示:
2 2
共价键 H-H I-I H-I
键能/kJ·mol−1 436 151 299
则该反应的ΔH=___kJ·mol−1。
②下列叙述能说明上述反应已达到平衡的是___。
a.单位时间内生成nmolH ,同时生成nmolHI
2
b.温度和体积一定时,HI浓度不再变化
c.温度和体积一定时,混合气体颜色不再变化
d.温度和压强一定时,混合气体的密度不再变化
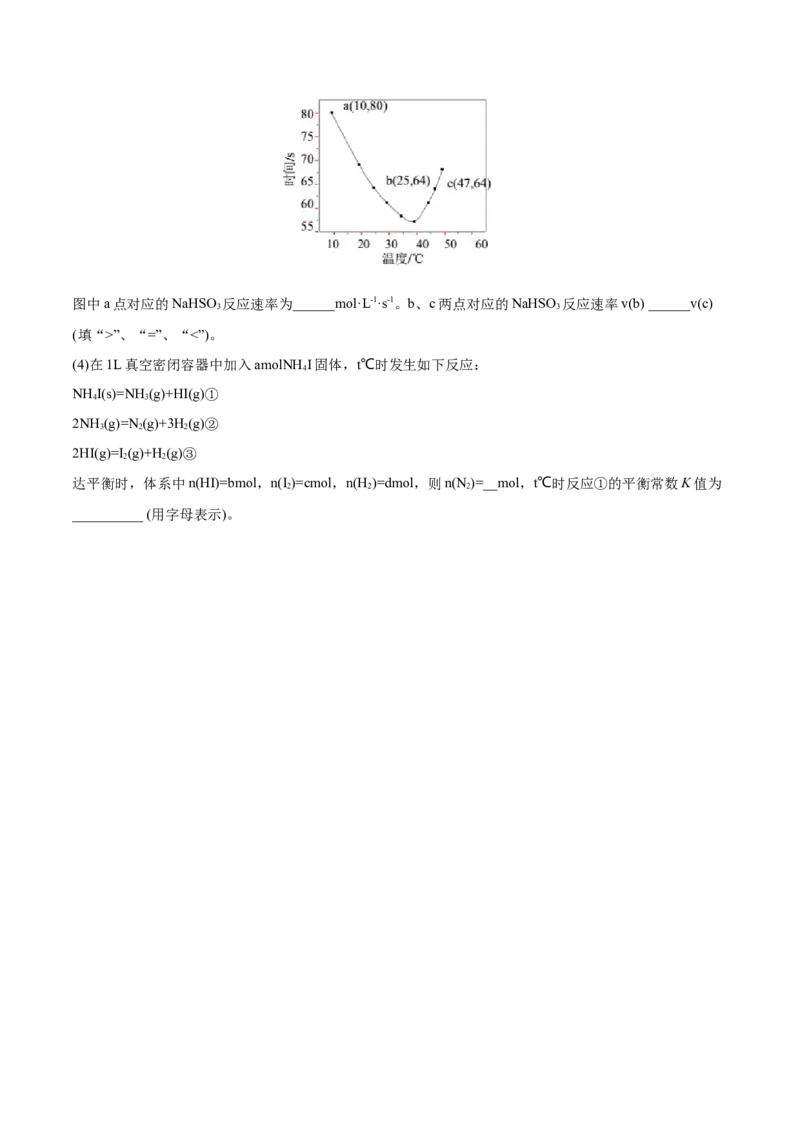
(3)NaHSO 溶液在不同温度下均可被过量KIO (IO 被还原成I-)氧化,当NaHSO 完全消耗即有I 析出,写
3 3 3 2
出I 析出时发生反应的离子方程式:__。依据I 析出所需时间可以求得NaHSO 的反应速率,将浓度均为
2 2 3
0.020mol·L-1NaHSO 溶液(含少量淀粉)10.0mL、KIO (过量)酸性溶液40.0mL混合,记录10~55℃间溶液变
3 3
蓝时间,55℃时未观察到溶液变蓝,实验结果如图。图中a点对应的NaHSO 反应速率为______mol·L-1·s-1。b、c两点对应的NaHSO 反应速率v(b) ______v(c)
3 3
(填“>”、“=”、“<”)。
(4)在1L真空密闭容器中加入amolNH I固体,t℃时发生如下反应:
4
NH I(s)=NH (g)+HI(g)①
4 3
2NH (g)=N(g)+3H(g)②
3 2 2
2HI(g)=I (g)+H(g)③
2 2
达平衡时,体系中n(HI)=bmol,n(I)=cmol,n(H )=dmol,则n(N )=__mol,t℃时反应①的平衡常数K值为
2 2 2
__________ (用字母表示)。