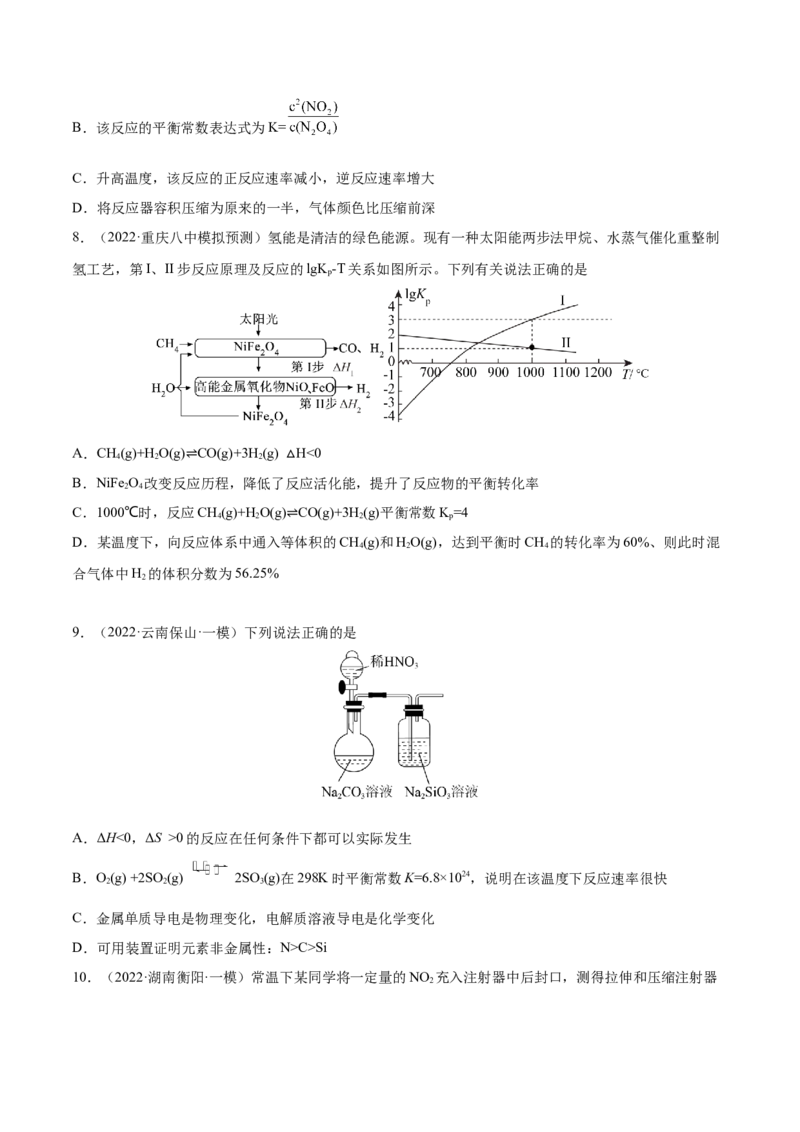文档内容
第 22 讲 化学平衡常数及转化率的计算
第一部分:高考真题感悟
1.(2021·海南·高考真题)制备水煤气的反应 ,下列说法正确的是
A.该反应
B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变
2
D.恒温恒压下,加入催化剂,平衡常数增大
2.(2017·天津·高考真题)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO) (g)。230 ℃时,
4
该反应的平衡常数K=2×10-5,已知:Ni(CO) 的沸点为42.2 ℃,固体杂质不参与反应。第一阶段:将粗镍
4
与CO反应转化成气态Ni(CO) ;第二阶段:将第一阶段反应后的气体分离出来,加热至230 ℃制得高纯镍。
4
下列判断正确的是
A.第一阶段,增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,若在30 ℃和50 ℃两者之间选择反应温度,应选50 ℃
C.第二阶段的Ni(CO) 分解率较低
4
D.第一阶段反应达到平衡时,v [Ni(CO) ]=4v (CO)
生成 4 生成
3.(2020·海南·高考真题)NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
CO(g)+ NO(g)=CO (g)+ N(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确
2 2
的是
A.K很大,NO与CO在排入大气之前就已反应完全
B.增大压强,平衡将向右移动,K> 2.5×1060
C.升高温度,既增大反应速率又增大K
D.选用适宜催化剂可达到尾气排放标准
4.(2020·江苏·高考真题)反应 可用于纯硅的制备。下列有关该反应的
说法正确的是
A.该反应 、
B.该反应的平衡常数C.高温下反应每生成1 mol Si需消耗
D.用E表示键能,该反应
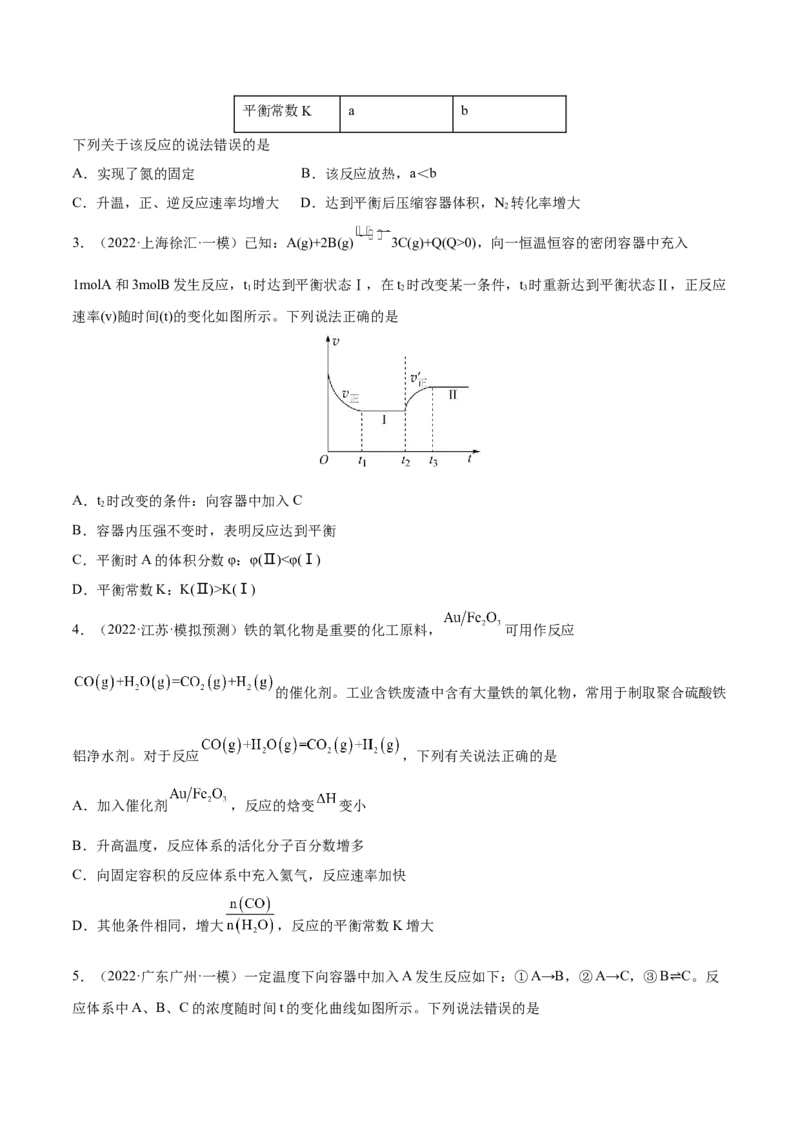
5.(2021·湖南·高考真题)已知: ,向一恒温恒容的密闭容器中充入
和 发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态Ⅱ,正反应
速率随时间的变化如图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件:向容器中加入C
C.平衡时A的体积分数 :
D.平衡常数K:
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(共12*5分)
1.(2021·江苏南通·模拟预测)下列关于2SO (g)+O(g) 2SO (g) ∆H=-197kJ∙mol-1的说法正确的是
2 2 3
A.该反应的∆S>0 ⇌
B.该反应中,反应物的总能量小于生成物的总能量
C.生产过程中将SO 分离出去,逆反应速率减慢
3
D.其他条件不变,增大压强,平衡右移,平衡常数增大
2.(2022·上海金山·一模)合成氨工业N(g)+3H(g) 2NH (g)在不同温度下的平衡常数如表:
2 2 3
温度/℃ 25 400平衡常数K a b
下列关于该反应的说法错误的是
A.实现了氮的固定 B.该反应放热,a<b
C.升温,正、逆反应速率均增大 D.达到平衡后压缩容器体积,N 转化率增大
2
3.(2022·上海徐汇·一模)已知:A(g)+2B(g) 3C(g)+Q(Q>0),向一恒温恒容的密闭容器中充入
1molA和3molB发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条件,t 时重新达到平衡状态Ⅱ,正反应
1 2 3
速率(v)随时间(t)的变化如图所示。下列说法正确的是
A.t 时改变的条件:向容器中加入C
2
B.容器内压强不变时,表明反应达到平衡
C.平衡时A的体积分数φ:φ(Ⅱ)<φ(Ⅰ)
D.平衡常数K:K(Ⅱ)>K(Ⅰ)
4.(2022·江苏·模拟预测)铁的氧化物是重要的化工原料, 可用作反应
的催化剂。工业含铁废渣中含有大量铁的氧化物,常用于制取聚合硫酸铁
铝净水剂。对于反应 ,下列有关说法正确的是
A.加入催化剂 ,反应的焓变 变小
B.升高温度,反应体系的活化分子百分数增多
C.向固定容积的反应体系中充入氦气,反应速率加快
D.其他条件相同,增大 ,反应的平衡常数K增大
5.(2022·广东广州·一模)一定温度下向容器中加入A发生反应如下:①A→B,②A→C,③B C。反
应体系中A、B、C的浓度随时间t的变化曲线如图所示。下列说法错误的是 ⇌A.反应①的活化能大于反应② B.该温度下,反应③的平衡常数大于1
C.t 时,B的消耗速率大于生成速率 D.t 时,c(C)=c -c(B)
1 2 0
6.(2022·江苏·徐州市第七中学模拟预测)氯元素具有多种化合价,可形成 、 、 、 和
等离子,在一定条件下能发生相互转化。在新型催化剂 作用下, 氧化HCl可获得 :
。对于反应
,下列说法正确的是
A.该反应
B.4mol HCl与1mol 反应转移电子数约为
C. 的使用能降低该反应的焓变
D.反应的平衡常数为
7.(2022·江苏·扬州中学三模)液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH 。NH 中
3
的一个H原子若被-NH 取代可形成NH(联氨),若被-OH取代可形成NH OH(羟胺)。在有NH 存在时,
2 2 4 2
Cu(OH) 能溶于氨水形成[Cu(NH )]2+。NH 经过一定的转化可以形成N、NO、NO 、NO(无色)、HNO 等。
2 3 4 3 2 2 2 4 3
对于反应2NO (g) NO(g),下列说法正确的是
2 2 4
A.该反应的H >0B.该反应的平衡常数表达式为K=
C.升高温度,该反应的正反应速率减小,逆反应速率增大
D.将反应器容积压缩为原来的一半,气体颜色比压缩前深
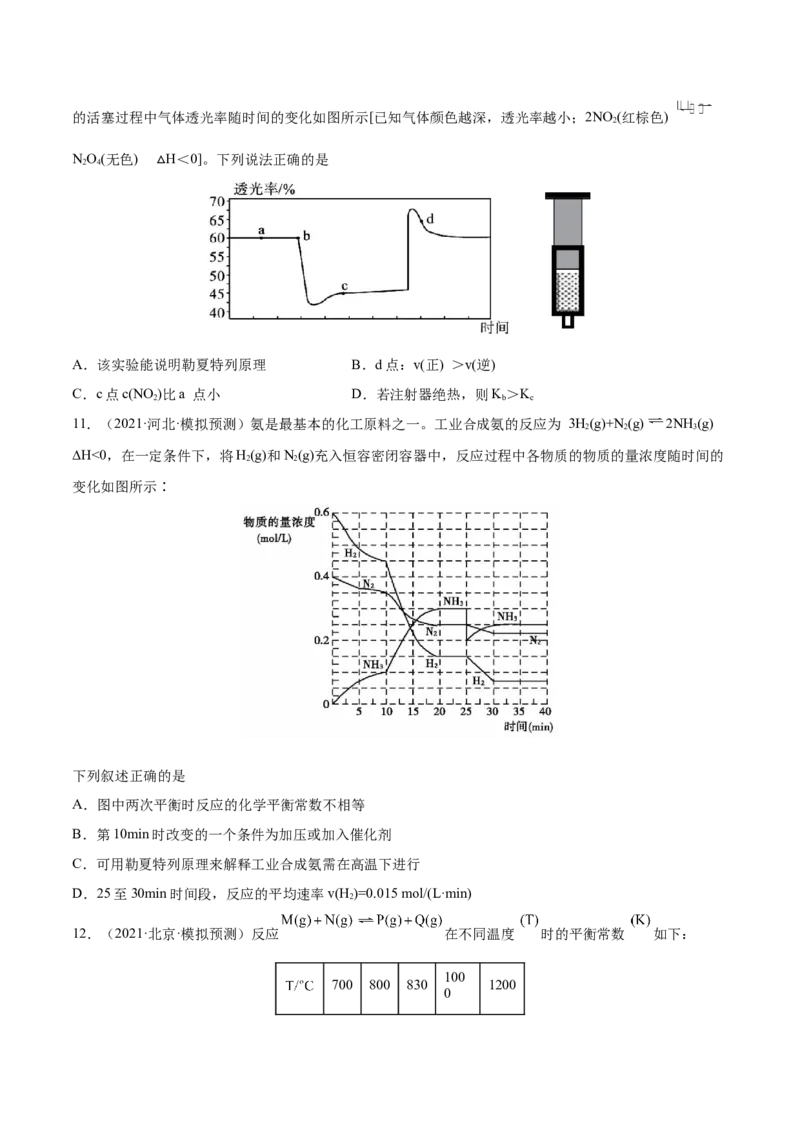
8.(2022·重庆八中模拟预测)氢能是清洁的绿色能源。现有一种太阳能两步法甲烷、水蒸气催化重整制
氢工艺,第I、II步反应原理及反应的lgK -T关系如图所示。下列有关说法正确的是
p
A.CH(g)+HO(g) CO(g)+3H(g) H<0
4 2 2
B.NiFe
2
O
4
改变反⇌应历程,降低了反△应活化能,提升了反应物的平衡转化率
C.1000℃时,反应CH(g)+HO(g) CO(g)+3H(g)平衡常数K=4
4 2 2 p
D.某温度下,向反应体系中通入等⇌体积的CH
4
(g)和H
2
O(g),达到平衡时CH
4
的转化率为60%、则此时混
合气体中H 的体积分数为56.25%
2
9.(2022·云南保山·一模)下列说法正确的是
A.ΔH<0,ΔS >0的反应在任何条件下都可以实际发生
B.O(g) +2SO (g) 2SO (g)在298K时平衡常数K=6.8×1024,说明在该温度下反应速率很快
2 2 3
C.金属单质导电是物理变化,电解质溶液导电是化学变化
D.可用装置证明元素非金属性:N>C>Si
10.(2022·湖南衡阳·一模)常温下某同学将一定量的NO 充入注射器中后封口,测得拉伸和压缩注射器
2的活塞过程中气体透光率随时间的变化如图所示[已知气体颜色越深,透光率越小;2NO (红棕色)
2
NO(无色) H<0]。下列说法正确的是
2 4
△
A.该实验能说明勒夏特列原理 B.d点:v(正) >v(逆)
C.c点c(NO )比a 点小 D.若注射器绝热,则K>K
2 b c
11.(2021·河北·模拟预测)氨是最基本的化工原料之一。工业合成氨的反应为 3H(g)+N(g) 2NH (g)
2 2 3
∆H<0,在一定条件下,将H(g)和N(g)充入恒容密闭容器中,反应过程中各物质的物质的量浓度随时间的
2 2
变化如图所示∶
下列叙述正确的是
A.图中两次平衡时反应的化学平衡常数不相等
B.第10min时改变的一个条件为加压或加入催化剂
C.可用勒夏特列原理来解释工业合成氨需在高温下进行
D.25至30min时间段,反应的平均速率v(H )=0.015 mol/(L·min)
2
12.(2021·北京·模拟预测)反应 在不同温度 时的平衡常数 如下:
100
700 800 830 1200
00.6 0.9 1.0 1.7 2.6
密闭容器中,某温度(T)、某时刻(t)时,反应混合物中M、N、P,Q的浓度分别为 、 、
、 。
下列说法正确的是A.该反应
B.若 ,则t时刻反应向正反应方向进行
C.若t时刻反应达到化学平衡,则
D.当 达到化学平衡时,
二、主观题(共3小题,共40分)
13.(2022·新疆乌鲁木齐·一模)(10分) 与 在高温下发生反应:
。在 时,将 与 充入 的空钢瓶中,
经过 反应达到平衡,平衡时水蒸气的物质的量分数为0.125。
(1)用 的浓度变化表示的反应速率 ________。 的平衡转化率 _______ 。
(2) 时该反应的平衡常数 ,在此温度下按相同投料在相同容器中重复上述反应,经过 ,
测得水蒸气的物质的量为 。判断此时该反应是否达到平衡___________(填“是”“否”或“无法确
定”)。
(3) 时,在体积一定的密闭容器中按原料初始组成 进行该反应,能判断反应达到
化学平衡状态的依据是___________。
A.容器中压强不再改变 B.容器中 的物质的量分数不再改变
C. D.容器中混合气体的密度不再改变
(4)要增大该反应的平衡常数K值,可采取的措施有___________。
A.增大 的起始浓度 B.增大反应体系压强
C.使用高效催化剂 D.升高温度14.(2022·上海上海·二模)(14分)CH-CO 重整反应[CH(g)+CO (g) 2CO(g)+2H(g)-Q(Q>0)]以两种
4 2 4 2 2
温室气体为原料生成了合成气,在“碳中和”的时代背景下,该技术受到更为广泛的关注。
Ⅰ.完成下列填空:
(1)某温度下,在体积2L的容器中加入2molCH 、1molCO 以及催化剂进行重整反应,经过2min达到平衡
4 2
状态时CO 的转化率为50%。此过程中以CH 表示的平均化学反应速率为_______。平衡常数的值为
2 4
_______。达到平衡后,其他条件不变时向容器中充入CO 与CO各1mol,则化学平衡_______移动(选填
2
“正向”“逆向”或“不”)。
Ⅱ.储能是指通过介质或设备把能量存储起来,在需要时再释放的过程。CH-CO 重整反应也可用于高温废
4 2
热的储能。800℃下,研究反应物气体流量、CH 与CO 物质的量比对CH 转化率(α)、储能效率(η)的影响,
4 2 4
部分数据如下所示。
序
加热温度/℃ n(CH)∶n(CO) α/% η/%
号 反应物气体流量/L•min-1 4 2
ⅰ 700 4 2∶2 49.0 42.0
ⅱ 800 4 2∶2 79.6 52.2
ⅲ 800 6 3∶3 64.2 61.9
ⅳ 800 6 2∶4 81.1 41.6
已知储能效率η=Qchem/Q,其中,Qchem是通过化学反应吸收的热量,Q是设备的加热功率。
i i
(2)解释为何可以用CH-CO 重整反应进行储能。_______
4 2
(3)对比实验_______(填序号),可得出结论:气体流量越大,CH 转化率_______。
4
(4)实验ⅳ中CH 转化率比实验ⅲ高,结合相关数据解释为何储能效率却低的原因(两次实验中设备的加热
4
功率Q不变)。_______
i
15.(2022·山东省实验中学模拟预测)以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.
Ⅱ.
回答下列问题:
(1)反应I、II的1nK(K代表化学平衡洋数)随 (温度的倒数)的变化如图所示。据图判断,升高温度时,反
应CO(g)+H(g) CHOH(g)的化学平衡常数将___________(填“增大”“减小”或“不变”)。
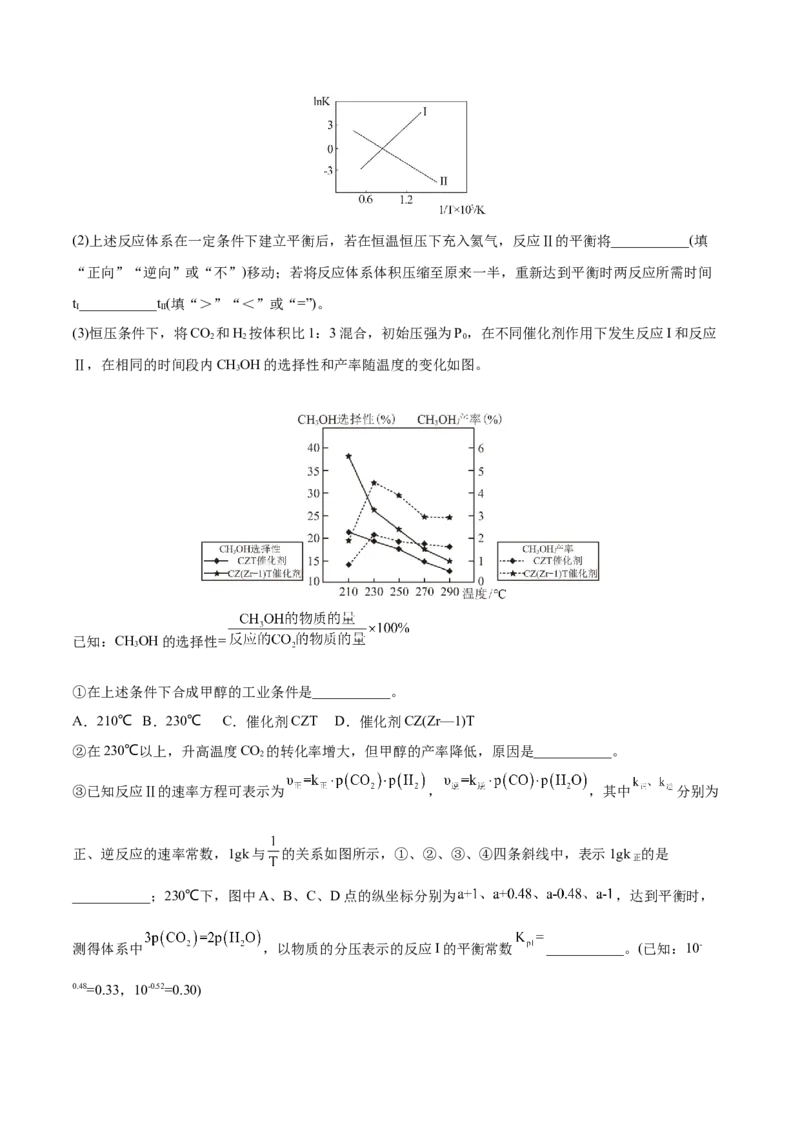
2 3(2)上述反应体系在一定条件下建立平衡后,若在恒温恒压下充入氦气,反应Ⅱ的平衡将___________(填
“正向”“逆向”或“不”)移动;若将反应体系体积压缩至原来一半,重新达到平衡时两反应所需时间
t___________t (填“>”“<”或“=”)。
I II
(3)恒压条件下,将CO 和H 按体积比1:3混合,初始压强为P,在不同催化剂作用下发生反应I和反应
2 2 0
Ⅱ,在相同的时间段内CHOH的选择性和产率随温度的变化如图。
3
已知:CHOH的选择性=
3
①在上述条件下合成甲醇的工业条件是___________。
A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr—1)T
②在230℃以上,升高温度CO 的转化率增大,但甲醇的产率降低,原因是___________。
2
③已知反应Ⅱ的速率方程可表示为 , ,其中 分别为
正、逆反应的速率常数,1gk与 的关系如图所示,①、②、③、④四条斜线中,表示1gk 的是
正
___________;230℃下,图中A、B、C、D点的纵坐标分别为 ,达到平衡时,
测得体系中 ,以物质的分压表示的反应I的平衡常数 ___________。(已知:10-
0.48=0.33,10-0.52=0.30)