文档内容
第三十八讲 原子结构与性质
【基础巩固】
1.某元素+3价离子的电子排布式为1s22s22p63s23p63d5,则该元素在周期表中的位置为( )
A.ⅤB族 B.ⅢB族 C.Ⅷ族 D.ⅤA族
2.元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素原子的外围电子排布式为nsn-1npn+1,则下
列说法不正确的是( )
X
Y
Z
A.Y元素原子的价电子排布式为4s24p4
B.Y元素在元素周期表的第三周期第ⅥA族
C.X元素所在周期中所含非金属元素最多
D.Z元素原子的核外电子排布式为
1s22s22p63s23p63d104s24p3
3.下列电子排布式或电子排布图正确的是( )
①基态 C 原子的电子排布图: ②基态 Cr 原子的电子排布式:
1s22s22p63s23p63d44s2 ③基态O原子的电子排布图: ④基态Br原子的外围电子
排布式:3d104s24p5 ⑤基态B原子的电子排布图:
A.①②③ B.②③④ C.①②④⑤ D.只有③
4..(2021·全国乙卷节选,双选)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着
广泛应用。对于基态Cr原子,下列叙述正确的是 (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
5.下列有关光谱的说法不正确的是( )
A.原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原因
B.原子光谱只有发射光谱
C.通过原子光谱可以发现新的元素
D.通过光谱分析可以鉴定某些元素
6.(2022·江苏卷)工业上电解熔融Al O 和冰晶石(Na AlF)的混合物可制得铝。下列说法正确的是( )
2 3 3 6
A.半径大小:r(Al3+)I(Na),原因是
1 1 1
______________________________________________________________________________。
I(Be)>I(B)>I(Li),原因是____________________________________________________________________。
1 1 1
(2)(2018·全国卷Ⅲ)黄铜是人类最早使用的合金之一,主要由 Zn 和 Cu 组成。第一电离能 I(Zn)
1
I(Cu)(填“大于”或“小于”)。原因是________________________________________________________。
1
(3)(2017·全国卷Ⅲ)元素Mn与O中,第一电离能较大的是 。
【拔高练习】
1.(2022·常州模拟)x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知(
)
A.x的原子半径大于y的原子半径
B.x的电负性小于y的电负性
C.x的氧化性大于y的氧化性
D.x的第一电离能小于y的第一电离能
2.X、Y是同周期的两种主族元素,它们的逐级电离能(I)数据如下表所示:
电离能/kJ·mol-1 I I I I I ……
1 2 3 4 5
X 496 4 562 6 912 9 543 13 353 ……
Y 738 1 451 7 733 10 540 13 630 ……
下列有关说法正确的是( )
A.电负性:X>Y
B.与水反应剧烈程度:XZ>W
5.下列有关光谱的说法不正确的是( )
A.原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原
因
B.原子光谱只有发射光谱
C.通过原子光谱可以发现新的元素
D.通过光谱分析可以鉴定某些元素
6.(2022·烟台模拟)某种具有高效率电子传输性能的有机发光材料的结构简式如图所示。下列关于该材料
组成元素的说法错误的是( )
A.五种组成元素中有四种元素位于p区且均位于同一周期
B.原子半径:Al>C>N>O>H
C.气态氢化物的稳定性:HO>NH >CH
2 3 4
D.基态N原子核外有7种运动状态不同的电子
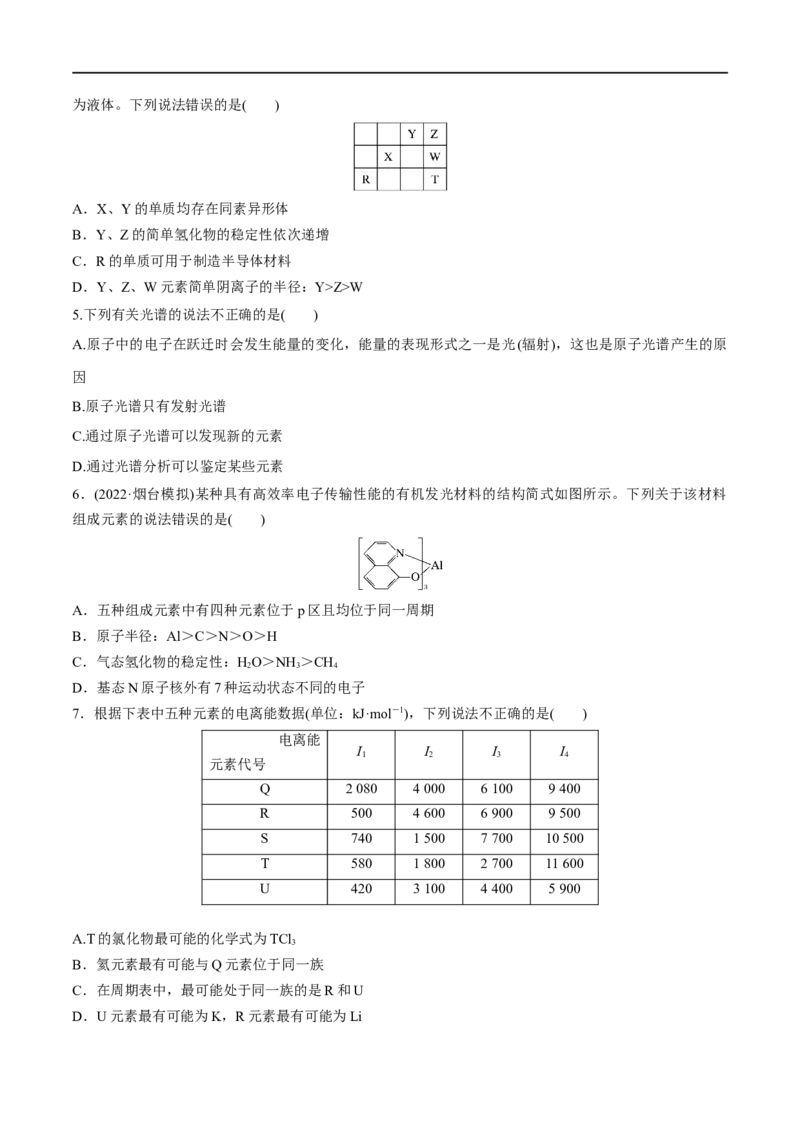
7.根据下表中五种元素的电离能数据(单位:kJ·mol-1),下列说法不正确的是( )
电离能
I I I I
1 2 3 4
元素代号
Q 2 080 4 000 6 100 9 400
R 500 4 600 6 900 9 500
S 740 1 500 7 700 10 500
T 580 1 800 2 700 11 600
U 420 3 100 4 400 5 900
A.T的氯化物最可能的化学式为TCl
3
B.氦元素最有可能与Q元素位于同一族
C.在周期表中,最可能处于同一族的是R和U
D.U元素最有可能为K,R元素最有可能为Li8.(2023·成都模拟)X、Y、Z、W、R属于周期表中前20号主族元素,且原子序数依次增大。X原子中有7
个运动状态完全不同的电子,Z是元素周期表中电负性最大的元素,Z和W同主族,R的最外层电子数是
最内层电子数的一半。下列说法正确的是( )
A.Z的简单氢化物分子间能形成氢键
B.简单离子半径:r(R)>r(W)
C.简单气态氢化物的热稳定性:W>Z
D.第一电离能:I(X)>I(Y)>I(Z)
1 1 1
9.LDFCB是锂离子电池常用的一种离子导体,其阴离子由原子序数依次增大的同周期元素原子W、X、
Y、Z构成,结构如图。基态Y原子的s轨道与p轨道电子数相等,Z的核外电子总数是W的最外层电子
数的3倍。下列说法正确的是( )
A.同周期元素第一电离能小于Y的有5种
B.简单氢化物的沸点:Z>Y>X
C.W的最高价氧化物对应的水化物具有两性
D.W和Z可形成含有极性共价键的非极性分子
10.(1)①基态Cu原子有________种不同能级的电子。
②N原子中最高能级的电子的电子云轮廓图为________。
③ 在 空 气 中 FeO 稳 定 性 小 于 Fe O , 从 电 子 排 布 的 角 度 分 析 , 其 主 要 原 因 是
2 3
_____________________________。
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价层电子排布式是__________;X3+
的价层电子排布式为________。
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子
排布式为________,M+的价层电子排布式为________________,M2+的电子排布式为________。
11.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p为26号元素,请写出其基态原子的核外电子排布式:__________________________。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:__________
_______________________________________________________________________________。
(3)o、p两元素的部分电离能数据如下表:元素
o p
电离能/(kJ·mol-1)
I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
表2
比较两元素的I 、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
2 3
_______________________________________________________________________。
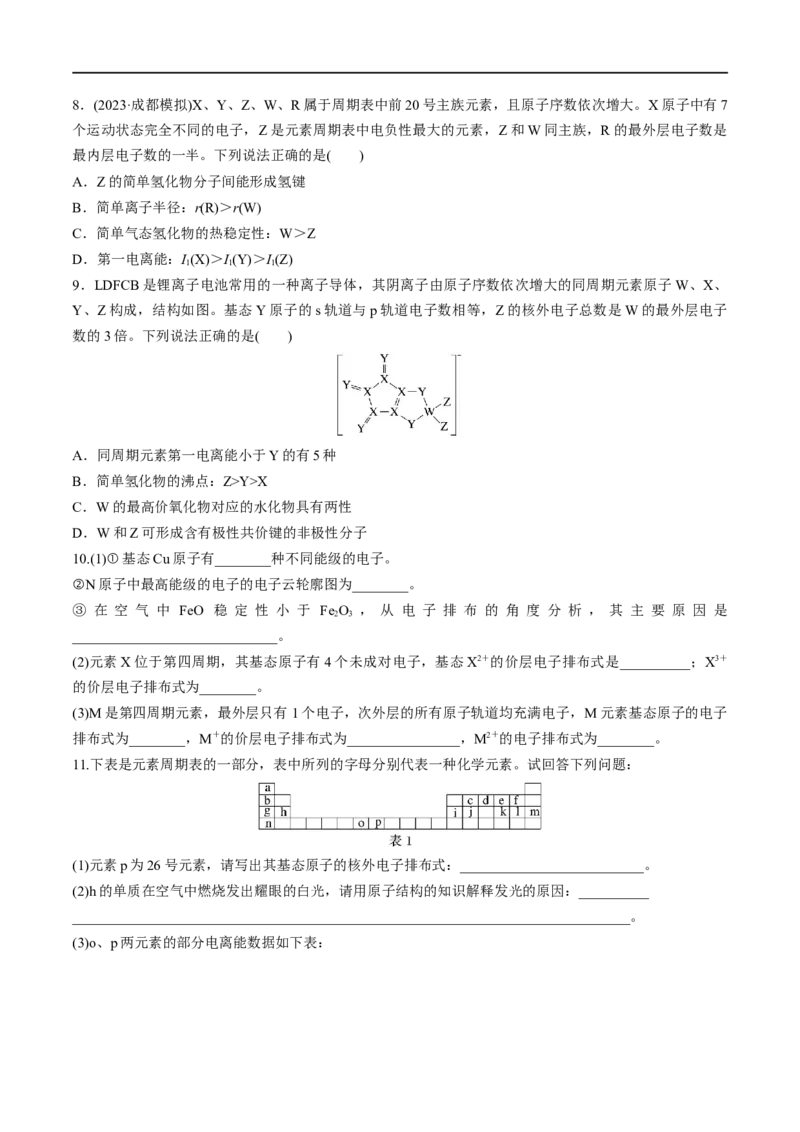
(4)第三周期8种元素单质熔点高低的顺序如图1所示,其中电负性最大的是________(填图1中的序号)。
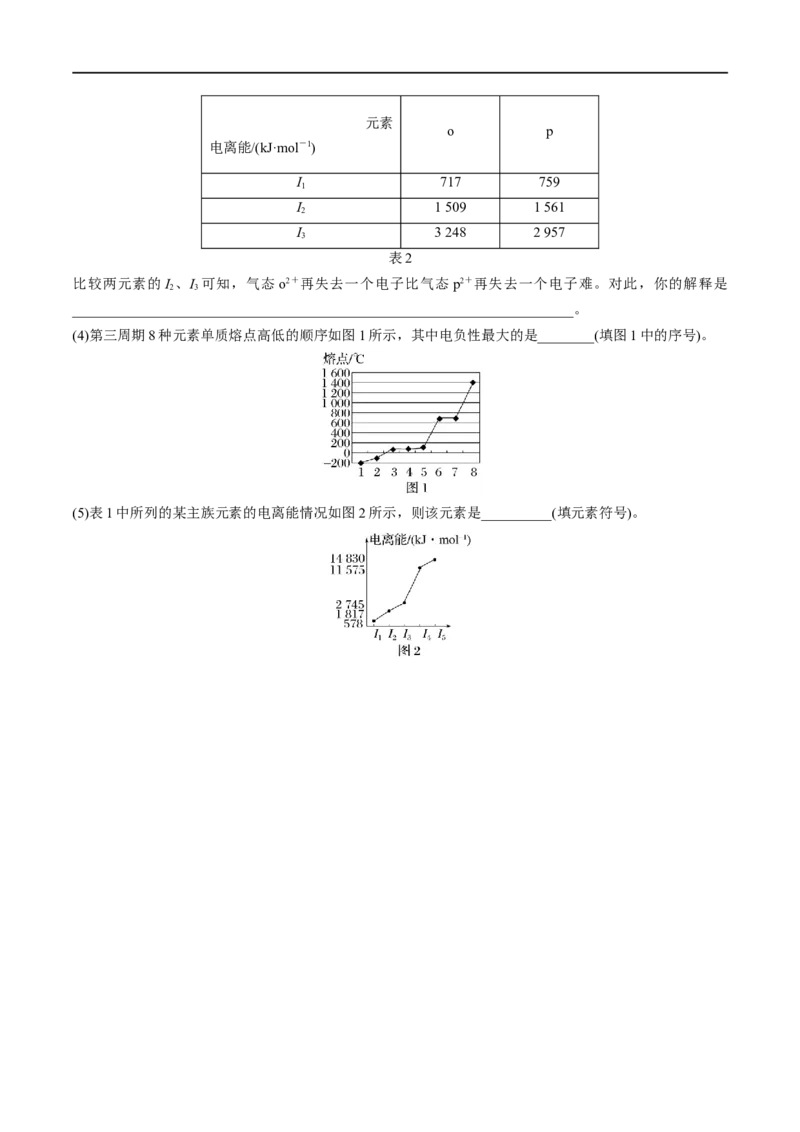
(5)表1中所列的某主族元素的电离能情况如图2所示,则该元素是__________(填元素符号)。