文档内容
训练(五十三) 晶体结构与性质
1.(2021·山东临沂检测)下面有关晶体的叙述中,不正确的是( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO 分子周围紧邻12个CO 分子
2 2
B [氯化钠晶体中,每个Na+周围距离相等的Na+共12个,每个Na+周围距离相等且
最近的Cl-共有6个。]
2.(2021·全国百校联盟联考)氮化硼具有抗化学侵蚀性质,不易被无机酸和水侵蚀,硬度
很高,与金刚石接近。下图是一种纳米立方氮化硼的晶胞结构。以下说法错误的是( )
A.纳米立方氮化硼熔点较低
B.N原子的配位数为4
C.硼原子的2s和2p原子轨道发生sp3杂化
D.纳米立方氮化硼属于共价晶体,可加工制成超硬材料
A [氮化硼的硬度与金刚石相近,则属于共价(或原子)晶体,其熔点很高,A错误;由氮
化硼的晶胞结构可知,N和B原子的配位数均为4,B正确;B原子的核外电子排布式为
1s22s22p1,该晶体中B原子的2s轨道和2p轨道发生sp3杂化,形成4个sp3杂化轨道,形成4
个共价键,C正确;纳米立方氮化硼属于共价晶体,其硬度很高,可加工制成超硬材料,D正
确。]
3.(2021·山东日照检测)现有几组物质的熔点(℃)数据:
A组 B组 C组 D组
金刚石:3 550 ℃ Li:181 ℃ HF:-83 ℃ NaCl:801 ℃
硅晶体:1 410 ℃ Na:98 ℃ HCl:-115 ℃ KCl:776 ℃
硼晶体:2 300 ℃ K:64 ℃ HBr:-89 ℃ RbCl:718 ℃
二氧化硅:1 723 ℃ Rb:39 ℃ HI:-51 ℃ CsCl:645 ℃
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________。(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于____________________________________________。
(4)D组晶体可能具有的性质是__________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D 组 晶 体 的 熔 点 由 高 到 低 的 顺 序 为 NaCl>KCl>RbCl>CsCl , 其 原 因 为
________________________________________________________________________。
解析 (1)A组熔点很高,为原子晶体,是由原子通过共价键形成的。(2)B组为金属晶体,
具有①②③④四条共性。(3)HF中含有分子间氢键,故其熔点反常。(4)D组属于离子晶体,具
有②④两条性质。(5)D组属于离子晶体,其熔点与晶格能有关。
答案 (1)原子 共价键 (2)①②③④
(3)HF分子间能形成氢键,其熔化时需要消耗的能量更多(只要答出HF分子间能形成氢
键即可) (4)②④
(5)D组晶体都为离子晶体,r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电荷数相同的
情况下,半径越小,晶格能越大,熔点就越高
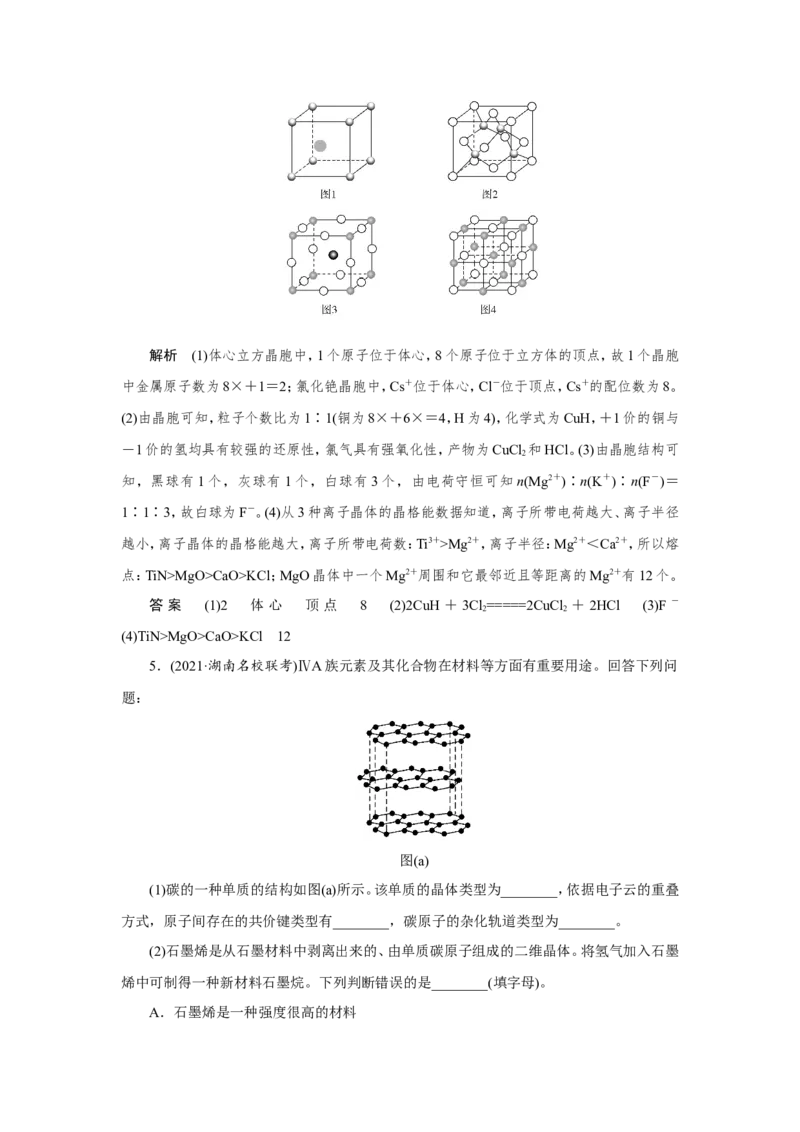
4.(2021·河南六市联考)(1)钠、钾、铬、钼、钨等金属晶体的晶胞属于体心立方,则该晶胞
中属于1个体心立方晶胞的金属原子数目是________。氯化铯晶体的晶胞如图1,则Cs+位
于该晶胞的________,而Cl-位于该晶胞的________________________________,
Cs+的配位数是______。
(2)铜的氢化物的晶胞结构如图2所示,写出此氢化物在氯气中燃烧的化学方程式:
________________________________________________________________________。
(3)图3为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是
________(填离子符号)。
(4)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图4所
示),已知3种离子晶体的晶格能数据如下表:
离子晶体 NaCl KCl CaO
晶格能/kJ·mol-1 786 715 3 401
则这4种离子晶体(不包括NaCl)熔点从高到低的顺序是______________________,其中
MgO晶体中一个Mg2+周围和它最邻近且等距离的 Mg2+有___________________________
个。解析 (1)体心立方晶胞中,1个原子位于体心,8个原子位于立方体的顶点,故1个晶胞
中金属原子数为8×+1=2;氯化铯晶胞中,Cs+位于体心,Cl-位于顶点,Cs+的配位数为8。
(2)由晶胞可知,粒子个数比为1∶1(铜为8×+6×=4,H为4),化学式为CuH,+1价的铜与
-1价的氢均具有较强的还原性,氯气具有强氧化性,产物为CuCl 和HCl。(3)由晶胞结构可
2
知,黑球有1个,灰球有1个,白球有3个,由电荷守恒可知n(Mg2+)∶n(K+)∶n(F-)=
1∶1∶3,故白球为F-。(4)从3种离子晶体的晶格能数据知道,离子所带电荷越大、离子半径
越小,离子晶体的晶格能越大,离子所带电荷数:Ti3+>Mg2+,离子半径:Mg2+<Ca2+,所以熔
点:TiN>MgO>CaO>KCl;MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个。
答 案 (1)2 体 心 顶 点 8 (2)2CuH + 3Cl=====2CuCl + 2HCl (3)F -
2 2
(4)TiN>MgO>CaO>KCl 12
5.(2021·湖南名校联考)ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问
题:
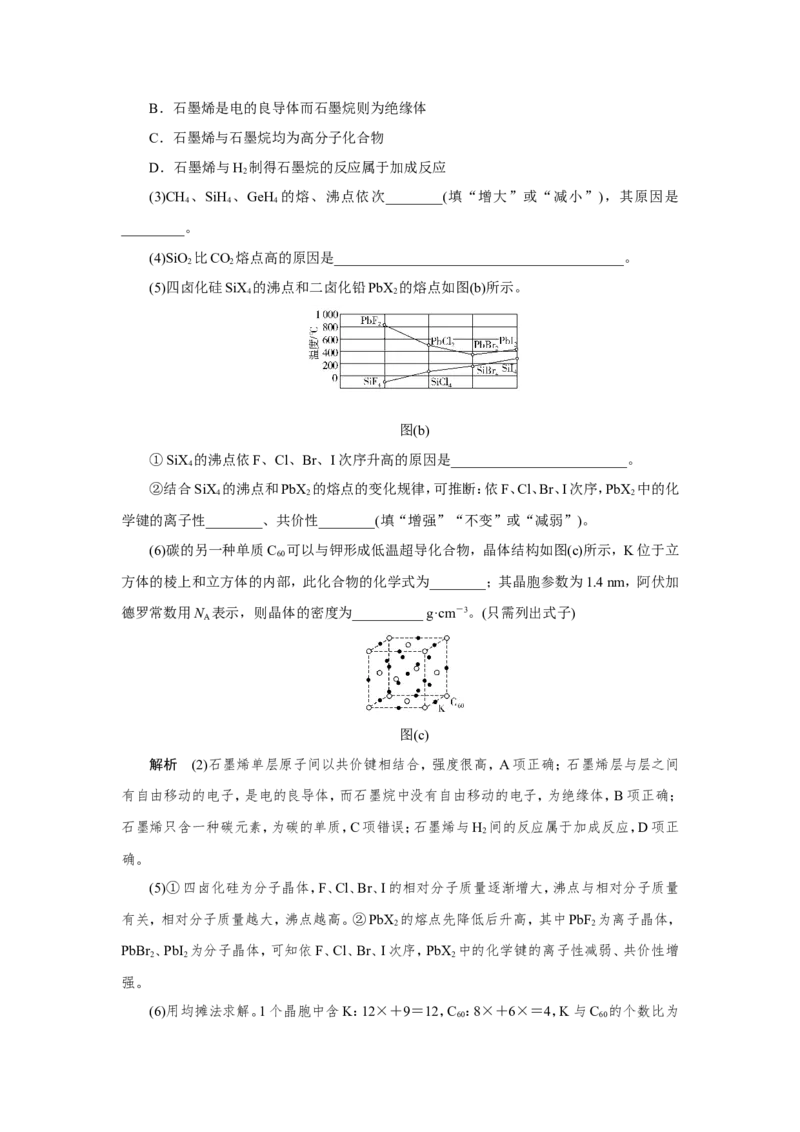
图(a)
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________,依据电子云的重叠
方式,原子间存在的共价键类型有________,碳原子的杂化轨道类型为________。
(2)石墨烯是从石墨材料中剥离出来的、由单质碳原子组成的二维晶体。将氢气加入石墨
烯中可制得一种新材料石墨烷。下列判断错误的是________(填字母)。
A.石墨烯是一种强度很高的材料B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H 制得石墨烷的反应属于加成反应
2
(3)CH 、SiH 、GeH 的熔、沸点依次________(填“增大”或“减小”),其原因是
4 4 4
_________。
(4)SiO 比CO 熔点高的原因是_________________________________________。
2 2
(5)四卤化硅SiX 的沸点和二卤化铅PbX 的熔点如图(b)所示。
4 2
图(b)
①SiX 的沸点依F、Cl、Br、I次序升高的原因是_________________________。
4
②结合SiX 的沸点和PbX 的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX 中的化
4 2 2
学键的离子性________、共价性________(填“增强”“不变”或“减弱”)。
(6)碳的另一种单质C 可以与钾形成低温超导化合物,晶体结构如图(c)所示,K位于立
60
方体的棱上和立方体的内部,此化合物的化学式为________;其晶胞参数为1.4 nm,阿伏加
德罗常数用N 表示,则晶体的密度为__________ g·cm-3。(只需列出式子)
A
图(c)
解析 (2)石墨烯单层原子间以共价键相结合,强度很高,A项正确;石墨烯层与层之间
有自由移动的电子,是电的良导体,而石墨烷中没有自由移动的电子,为绝缘体,B项正确;
石墨烯只含一种碳元素,为碳的单质,C项错误;石墨烯与H 间的反应属于加成反应,D项正
2
确。
(5)①四卤化硅为分子晶体,F、Cl、Br、I的相对分子质量逐渐增大,沸点与相对分子质量
有关,相对分子质量越大,沸点越高。②PbX 的熔点先降低后升高,其中PbF 为离子晶体,
2 2
PbBr 、PbI 为分子晶体,可知依F、Cl、Br、I次序,PbX 中的化学键的离子性减弱、共价性增
2 2 2
强。
(6)用均摊法求解。1个晶胞中含K:12×+9=12,C :8×+6×=4,K与C 的个数比为
60 6012∶4=3∶1,此化合物的化学式为KC 。1个晶胞的体积为(1.4 nm)3=(1.4×10-7)3 cm3,1
3 60
个晶胞中含有4个KC ,则ρ= g·cm-3。
3 60
答案 (1)混合晶体 σ键、π键 sp2 (2)C (3)增大 三种物质均为分子晶体,结构与
组成相似,相对分子质量越大,范德华力越大,熔、沸点越高 (4)SiO 为原子晶体,而CO 为
2 2
分子晶体 (5)①均为分子晶体,范德华力随相对分子质量增大而增大 ②减弱 增强
(6)K C
3 60
6.(2021·湖北武汉部分校联考)铁被称为“第一金属”,铁及其化合物在生产、生活中有
广泛用途。
(1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用______________摄取铁
元素的原子光谱。
(2)FeCl 的熔点为360 ℃,沸点为315 ℃。由此可知FeCl 属于________晶体。FeSO 常作
3 3 4
净水剂和补铁剂,SO的立体构型是__________。
(3)铁氰化钾K[Fe(CN) ]是检验Fe2+的重要试剂。
3 6
①基态N原子的轨道表示式为________________。
②写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式________________。
③铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为______________。
④铁氰化钾中,不存在__________(填字母标号)。
A.离子键 B.σ键 C.π键 D.氢键 E.金属键
(4)有机金属配位化合物二茂铁[(C H)Fe]是汽油中的抗震剂。分子中的大π键可用符号
5 5 2
π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中
的大π键可表示为π),则 中的大∏键应表示为________________,其中碳原子的杂化
方式为____________________。
(5)羰基铁[Fe(CO) ]可用作催化剂、汽油抗爆剂等。1 mol Fe(CO) 分子中含
5 5
__________mol配位键。
解析 (1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取铁元
素的原子光谱。
(2)FeCl 的熔点、沸点较低,故FeCl 属于分子晶体。SO中S原子价层电子对数为4+(6
3 3
+2-2×4)=4,不含孤电子对,则VSEPR模型和SO的立体构型均为正四面体形。(3)①基态N原子核外电子排布式为1s22s22p3,轨道表示式为 。
②铁氰化钾中配体是CN—,与其互为等电子体的极性分子必须含有2个原子,且价电子
总数为4+5+1=10,符合条件的分子有CO等。
③铁氰化钾中涉及的元素有K、Fe、C、N,K、Fe是活泼金属,K更活泼;C、N是非金属元
素,N原子的2p轨道处于半充满的稳定状态,其第一电离能大于 C,故第一电离能:
N>C>Fe>K。
④铁氰化钾由K+和[Fe(CN) ]3—离子构成,故存在离子键、σ键、π键,不存在氢键和金属
6
键。
(4) 中的大π键由5个碳原子参与形成,每个碳原子提供1个电子,并得到1个电
子形成大π键,故大π键表示为π。双键碳原子采取sp2杂化。
(5)Fe(CO) 中配位体是CO,CO分子中含有配位键,则1个Fe(CO) 分子含有10个配位
5 5
键,1 mol Fe(CO) 分子中含有10 mol 配位键。
5
答案 (1)光谱仪 (2)分子 正四面体形
(3)① ②CO ③N>C>Fe>K ④DE
(4) sp2 (5)10
7.(2021·天津滨海新区四校联考)钛有“生物金属”和“未来金属”之称,钛及其化合
物的应用正越来越受到人们的关注。
(1)Ti(BH) 是一种储氢材料,可由TiCl 和LiBH 反应制得。
4 3 4 4
①TiCl 熔点为-24 ℃,沸点为136.4 ℃,室温下为无色液体,可溶于甲苯和氯代烃,固
4
态TiCl 属于________晶体。
4
②LiBH 中BH的空间构型是_________,B原子的杂化轨道类型是________。
4
(2)硫酸氧钛晶体中阳离子为链状聚合形式的离子,部分结构如图所示。该阳离子Ti与O
的原子个数之比为________,其化学式为____________。
(3)钛与卤素形成的化合物的熔、沸点如表所示,分析TiCl 、TiBr 、TiI 的熔点和沸点呈现
4 4 4一定规律的原因:______________________________。
熔点/℃ 沸点/℃
TiCl -25 136.5
4
TiBr 39 230
4
TiI 150 377
4
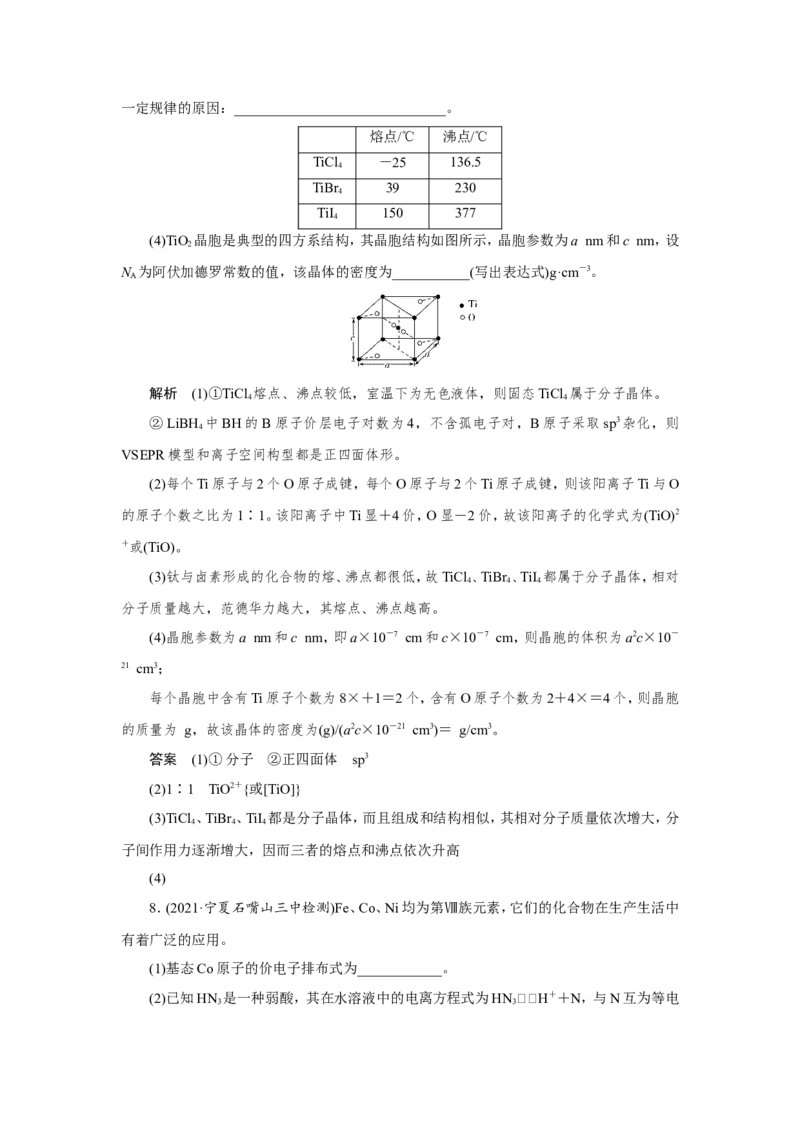
(4)TiO 晶胞是典型的四方系结构,其晶胞结构如图所示,晶胞参数为a nm和c nm,设
2
N 为阿伏加德罗常数的值,该晶体的密度为___________(写出表达式)g·cm-3。
A
解析 (1)①TiCl 熔点、沸点较低,室温下为无色液体,则固态TiCl 属于分子晶体。
4 4
②LiBH 中BH的B原子价层电子对数为4,不含孤电子对,B原子采取sp3杂化,则
4
VSEPR模型和离子空间构型都是正四面体形。
(2)每个Ti原子与2个O原子成键,每个O原子与2个Ti原子成键,则该阳离子Ti与O
的原子个数之比为1∶1。该阳离子中Ti显+4价,O显-2价,故该阳离子的化学式为(TiO)2
+或(TiO)。
(3)钛与卤素形成的化合物的熔、沸点都很低,故TiCl 、TiBr 、TiI 都属于分子晶体,相对
4 4 4
分子质量越大,范德华力越大,其熔点、沸点越高。
(4)晶胞参数为a nm和c nm,即a×10-7 cm和c×10-7 cm,则晶胞的体积为a2c×10-
21 cm3;
每个晶胞中含有Ti原子个数为8×+1=2个,含有O原子个数为2+4×=4个,则晶胞
的质量为 g,故该晶体的密度为(g)/(a2c×10-21 cm3)= g/cm3。
答案 (1)①分子 ②正四面体 sp3
(2)1∶1 TiO2+{或[TiO]}
(3)TiCl 、TiBr 、TiI 都是分子晶体,而且组成和结构相似,其相对分子质量依次增大,分
4 4 4
子间作用力逐渐增大,因而三者的熔点和沸点依次升高
(4)
8.(2021·宁夏石嘴山三中检测)Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中
有着广泛的应用。
(1)基态Co原子的价电子排布式为____________。
(2)已知HN 是一种弱酸,其在水溶液中的电离方程式为HN H++N,与N互为等电
3 3子体的一种分子为_______;N离子杂化类型为___________。
(3)Co3+的一种配离子[Co(N )(NH )]2+中,Co3+的配位数是___________,1 mol该配离
3 3 5
子中所含σ键的数目为____,配位体NH 的空间构型为_________。
3
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均
有一个CN—,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为____________;立
方体中Fe2+间连接起来形成的空间构型是_____________。
(5)NiO的晶体结构如下图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子
坐标参数为_______________。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层
排列,Ni2+填充其中(如下图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量
为__________g(用含a、N 的代数式表示)。
A
解析 (2)与N互为等电子体的一种分子为:CO。N中心氮原子孤电子对数为0,σ键的
2
数目为2,则杂化轨道数为2,故N离子杂化类型为sp。
(3)Co3+的一种配离子[Co(N )(NH )]2+中,氨气分子和N中氮原子中有孤电子对,能够与
3 3 5
Co3+形成配位键,共有5个氨分子和1个N离子,Co3+的配位数是6。5 mol氨气分子提供σ
键为15 mol,1 mol N中含有σ键2 mol,形成配位键有6 mol,则1 mol该配离子中所含σ键
的数目为23N 。配位体NH 的空间构型为三角锥形。
A 3
(4)Fe2+、Fe3+占据立方体的互不相邻的顶点,则每个立方体上有4个Fe2+、4个Fe3+,根
据晶体的空间结构特点,每个顶点上的粒子有属于该立方体,则该立方体中有个Fe2+、个Fe3
+,CN—位于立方体的棱上,棱上的微粒有属于该立方体,该立方体中有3个CN—,则该晶体
的化学式为 [FeFe(CN) ]—。由于物质呈电中性,需要一个钾离子与之结合,故该晶体的化学
6
式为KFe (CN) ;立方体中Fe2+间连接起来形成的空间构型是正四面体形。
2 6
(5)NiO的晶体中离子坐标参数A为(0,0,0),B为(1,1,0),则由图可看出C离子坐标离
x为1,离y为1/2,离z为,则C离子坐标参数为(1,,)。(6)根据结构知,氧离子和相邻的镍离子之间的距离为2a,距离最近的两个阳离子核间的
距离是距离最近的氧离子和镍离子距离的倍,所以其距离是2 am;根据图片知,每个氧化镍
所占的面积=2a m×2a m×sin 60°×10-24,则每平方米含有的氧化镍个数=1/(2a m×2a
m×sin 60°×10-24)=×1024;每个氧化镍的质量为 g,故每平方米含有的氧化镍质量为
(或)g。
答案 (1)3d74s2 (2)CO sp
2
(3)6 23N 三角锥形 (4)KFe (CN) 正四面体形
A 2 6
(5)(1,,) (6)(或×1024)