文档内容
专题 14 分子结构与性质
第 41 练 分子结构与物质的性质
1.下列物质中,由极性键形成的非极性分子是( )
A.CO B.Br
2 2
C.CaCl D.SO
2 2
2.实验测得BeCl 为共价化合物,两个Be—Cl键的夹角为180°,由此可判断BeCl 属于( )
2 2
A.由极性键形成的极性分子 B.由极性键形成的非极性分子
C.由非极性键形成的极性分子 D.由非极性键形成的非极性分子
3.下列各组分子中,都属于含极性键的非极性分子的是( )
A.CO、HS B.C H、CH
2 2 2 4 4
C.Cl、C H D.NH 、HCl
2 2 2 3
4.X、Y为两种不同的元素,下列化学式一定为极性分子的是( )
A.XY B.XY C.XY D.XY
2 3 4
5.下列物质发生状态变化时,克服了范德华力的是( )
A.食盐熔化 B.HCl溶于水
C.碘升华 D.氢氧化钠熔化
6.下列说法中正确的是( )
A.分子间作用力越大,分子越稳定
B.分子间作用力越大,物质的熔、沸点越高
C.相对分子质量越大,其分子间作用力越大
D.分子间只存在范德华力
7.下列叙述与分子间作用力无关的是( )
A.气体物质加压或降温时能凝结或凝固
B.干冰易升华
C.氟、氯、溴、碘单质的熔、沸点依次升高
D.氯化钠的熔点较高
8.下列有机物中含有两个手性碳原子的是( )
A. B.C. D.
9.下列有机物分子中带“*”碳原子就是手性碳原子。该有机物分别发生下列反应,生成的有机物分
子中含有手性碳原子的是( )
A.与乙酸发生酯化反应
B.与NaOH水溶液反应
C.与银氨溶液作用发生银镜反应
D.催化剂作用下与H 反应
2
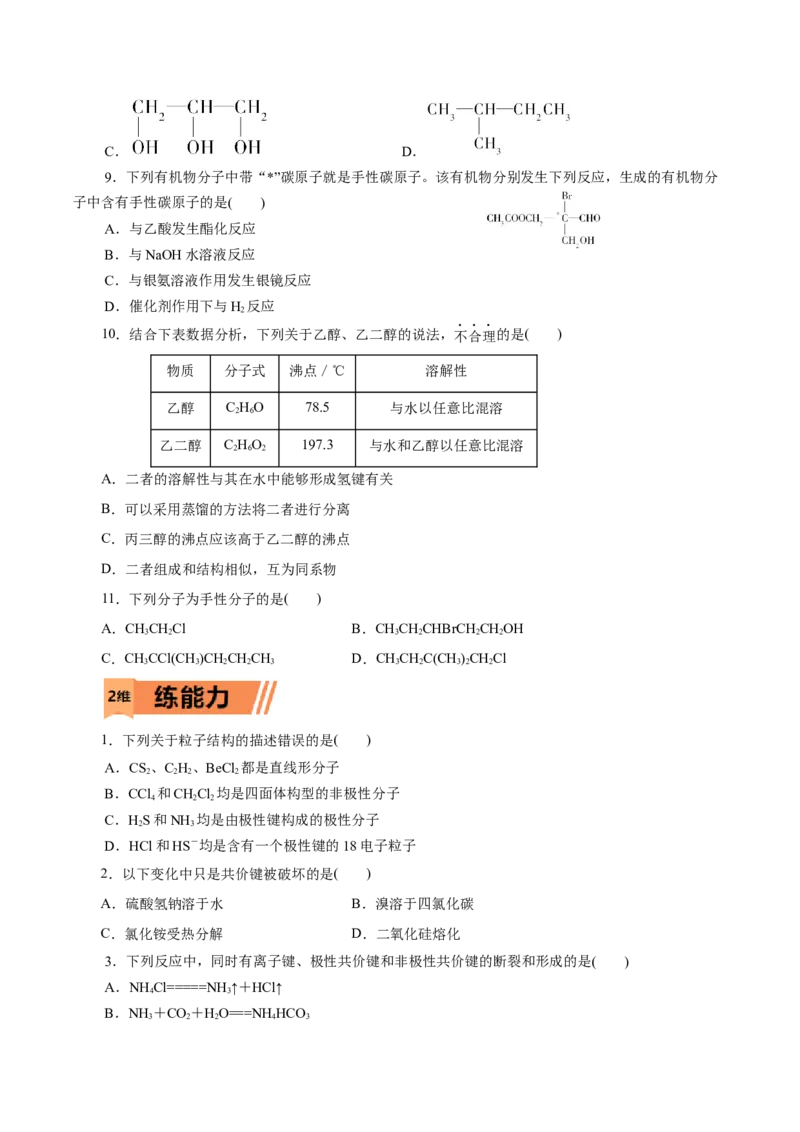
10.结合下表数据分析,下列关于乙醇、乙二醇的说法,不合理的是( )
物质 分子式 沸点/℃ 溶解性
乙醇 C HO 78.5 与水以任意比混溶
2 6
乙二醇 C HO 197.3 与水和乙醇以任意比混溶
2 6 2
A.二者的溶解性与其在水中能够形成氢键有关
B.可以采用蒸馏的方法将二者进行分离
C.丙三醇的沸点应该高于乙二醇的沸点
D.二者组成和结构相似,互为同系物
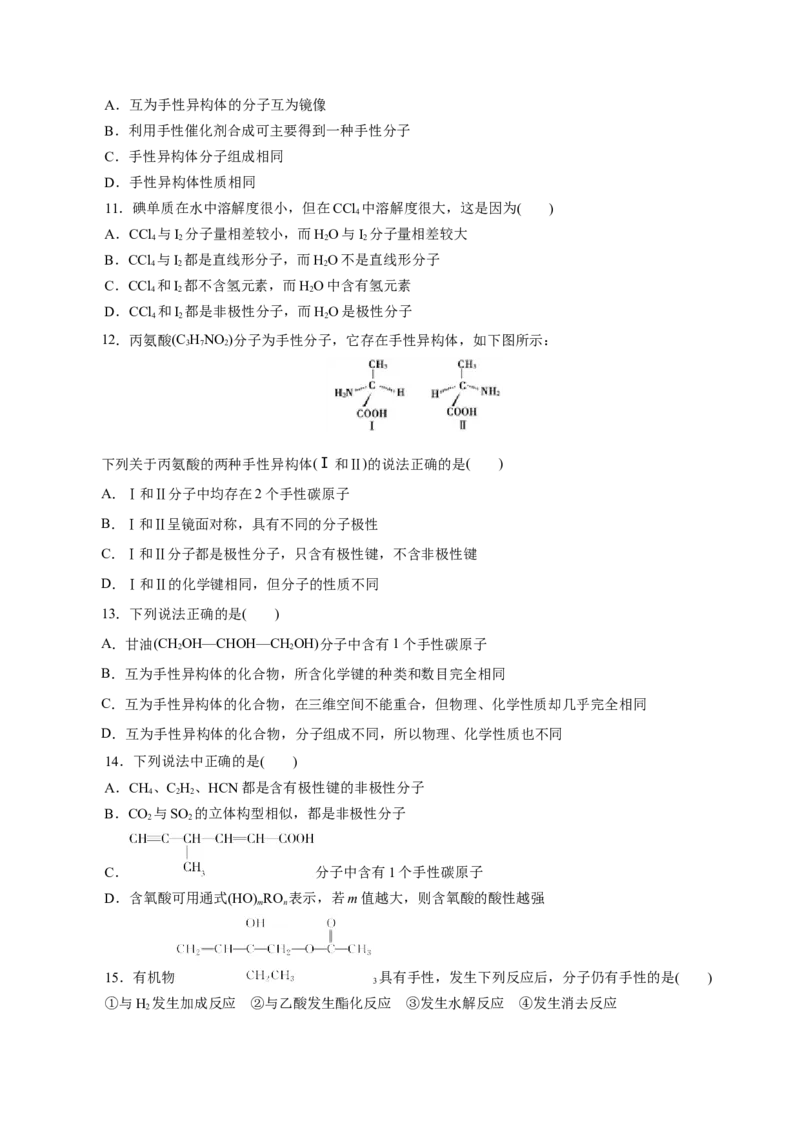
11.下列分子为手性分子的是( )
A.CHCHCl B.CHCHCHBrCH CHOH
3 2 3 2 2 2
C.CHCCl(CH )CHCHCH D.CHCHC(CH)CHCl
3 3 2 2 3 3 2 3 2 2
1.下列关于粒子结构的描述错误的是( )
A.CS、C H、BeCl 都是直线形分子
2 2 2 2
B.CCl 和CHCl 均是四面体构型的非极性分子
4 2 2
C.HS和NH 均是由极性键构成的极性分子
2 3
D.HCl和HS-均是含有一个极性键的18电子粒子
2.以下变化中只是共价键被破坏的是( )
A.硫酸氢钠溶于水 B.溴溶于四氯化碳
C.氯化铵受热分解 D.二氧化硅熔化
3.下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的是( )
A.NH Cl=====NH ↑+HCl↑
4 3
B.NH +CO+HO===NHHCO
3 2 2 4 3C.2NaOH+Cl===NaCl+NaClO+HO
2 2
D.2NaO+2CO===2Na CO+O
2 2 2 2 3 2
4.下列对分子及其性质的解释中,不正确的是( )
A.液态氟化氢分子间存在氢键,所以氟化氢的沸点比氯化氢高
B.CH、CO、BF 都是含有极性键的非极性分子
4 2 3
C.[Cu(NH )]2+ 中含有离子键、极性键、配位键
3 4
D.因为非羟基氧原子数目逐渐减少,所以酸性HClO>H SO >H PO
4 2 4 3 4
5.下列有关范德华力的叙述正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊的化学键
B.范德华力与化学键的区别是作用力的强弱不同
C.任何分子间在任意情况下都会产生范德华力
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
6.下列物质的性质可用范德华力的大小来解释的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.F、Cl、Br 、I 的熔、沸点依次升高
2 2 2 2
C. 、H—O—H、C H—OH中—OH上氢原子的活泼性依次减弱
2 5
D.CH—O—CH 、C HOH的沸点依次升高
3 3 2 5
7.下列物质中不存在氢键的是( )
A.冰醋酸中醋酸分子之间
B.液态氟化氢中氟化氢分子之间
C.氨水中氨分子与水分子之间
D.可燃冰(CH·8H O)中甲烷分子与水分子之间
4 2
8.下列说法正确的是( )
A.氢键是化学键
B.甲烷可与水形成氢键
C.乙醇分子跟水分子之间不只存在范德华力
D.碘化氢的沸点比氯化氢的沸点高是由于碘化氢分子之间存在氢键
9.下列说法正确的是( )
A.乙硫醇(CHCH—SH)比乙醇(CHCH—OH)熔点低,原因是乙醇分子间易形成氢键
3 2 3 2
B.氯化钠易溶于水是因为形成了氢键
C.氨易液化与氨分子间存在氢键无关
D.HO是一种非常稳定的化合物,这是由于氢键所致
2
10.下列现象不能用“相似相溶”原理解释的是( )
3.下列说法不正确的是( )A.互为手性异构体的分子互为镜像
B.利用手性催化剂合成可主要得到一种手性分子
C.手性异构体分子组成相同
D.手性异构体性质相同
11.碘单质在水中溶解度很小,但在CCl 中溶解度很大,这是因为( )
4
A.CCl 与I 分子量相差较小,而HO与I 分子量相差较大
4 2 2 2
B.CCl 与I 都是直线形分子,而HO不是直线形分子
4 2 2
C.CCl 和I 都不含氢元素,而HO中含有氢元素
4 2 2
D.CCl 和I 都是非极性分子,而HO是极性分子
4 2 2
12.丙氨酸(C HNO )分子为手性分子,它存在手性异构体,如下图所示:
3 7 2
下列关于丙氨酸的两种手性异构体(Ⅰ和Ⅱ)的说法正确的是( )
A.Ⅰ和Ⅱ分子中均存在2个手性碳原子
B.Ⅰ和Ⅱ呈镜面对称,具有不同的分子极性
C.Ⅰ和Ⅱ分子都是极性分子,只含有极性键,不含非极性键
D.Ⅰ和Ⅱ的化学键相同,但分子的性质不同
13.下列说法正确的是( )
A.甘油(CHOH—CHOH—CH OH)分子中含有1个手性碳原子
2 2
B.互为手性异构体的化合物,所含化学键的种类和数目完全相同
C.互为手性异构体的化合物,在三维空间不能重合,但物理、化学性质却几乎完全相同
D.互为手性异构体的化合物,分子组成不同,所以物理、化学性质也不同
14.下列说法中正确的是( )
A.CH、C H、HCN都是含有极性键的非极性分子
4 2 2
B.CO 与SO 的立体构型相似,都是非极性分子
2 2
C. 分子中含有1个手性碳原子
D.含氧酸可用通式(HO) RO 表示,若m值越大,则含氧酸的酸性越强
m n
15.有机物 具有手性,发生下列反应后,分子仍有手性的是( )
3
①与H 发生加成反应 ②与乙酸发生酯化反应 ③发生水解反应 ④发生消去反应
2A.①② B.②③
C.①④ D.②④
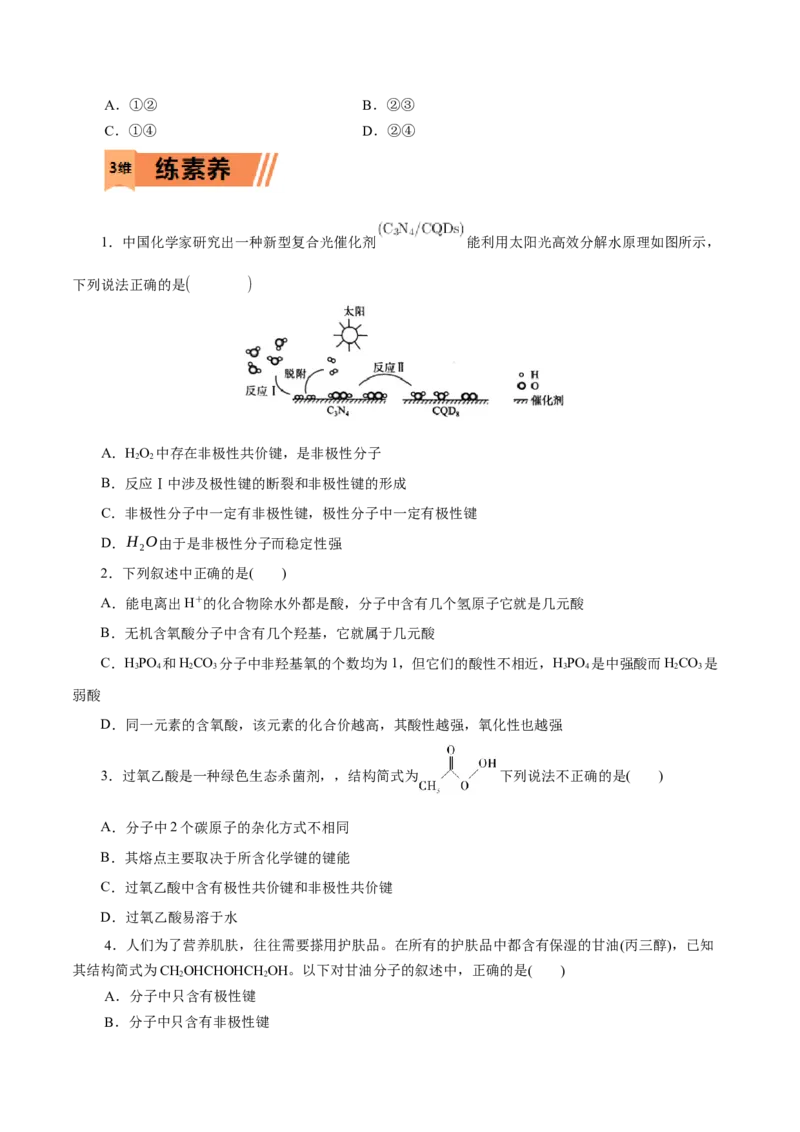
1.中国化学家研究出一种新型复合光催化剂 能利用太阳光高效分解水原理如图所示,
下列说法正确的是( )
A.HO 中存在非极性共价键,是非极性分子
2 2
B.反应Ⅰ中涉及极性键的断裂和非极性键的形成
C.非极性分子中一定有非极性键,极性分子中一定有极性键
D.H O由于是非极性分子而稳定性强
2
2.下列叙述中正确的是( )
A.能电离出H+的化合物除水外都是酸,分子中含有几个氢原子它就是几元酸
B.无机含氧酸分子中含有几个羟基,它就属于几元酸
C.HPO 和HCO 分子中非羟基氧的个数均为1,但它们的酸性不相近,HPO 是中强酸而HCO 是
3 4 2 3 3 4 2 3
弱酸
D.同一元素的含氧酸,该元素的化合价越高,其酸性越强,氧化性也越强
3.过氧乙酸是一种绿色生态杀菌剂,,结构简式为 下列说法不正确的是( )
A.分子中2个碳原子的杂化方式不相同
B.其熔点主要取决于所含化学键的键能
C.过氧乙酸中含有极性共价键和非极性共价键
D.过氧乙酸易溶于水
4.人们为了营养肌肤,往往需要搽用护肤品。在所有的护肤品中都含有保湿的甘油(丙三醇),已知
其结构简式为CHOHCHOHCH OH。以下对甘油分子的叙述中,正确的是( )
2 2
A.分子中只含有极性键
B.分子中只含有非极性键C.分子中既含有σ键又含有π键
D.分子中既含有极性键又含有非极性键
5.关于CS、SO 、NH 三种物质的说法中正确的是( )
2 2 3
A.CS 在水中的溶解度很小,是由于其属于极性分子
2
B.SO 和NH 均易溶于水,原因之一是它们都是极性分子
2 3
C.CS 为非极性分子,所以在三种物质中熔沸点最低
2
D.NH 在水中溶解度很大只是由于NH 分子有极性
3 3
6.下列说法中正确的是( )
A.极性分子组成的溶质一定易溶于极性分子组成的溶剂之中,非极性分子组成的溶质一定易溶于非
极性分子组成的溶剂中
B.溴分子和水分子是极性分子,四氯化碳分子是非极性分子,所以溴难溶于水而易溶于四氯化碳
C.白磷分子是非极性分子,水分子是极性分子,而二硫化碳是非极性分子,所以白磷难溶于水而易
溶于二硫化碳
D.水分子是极性分子,二氧化碳可溶于水,因此二氧化碳是极性分子
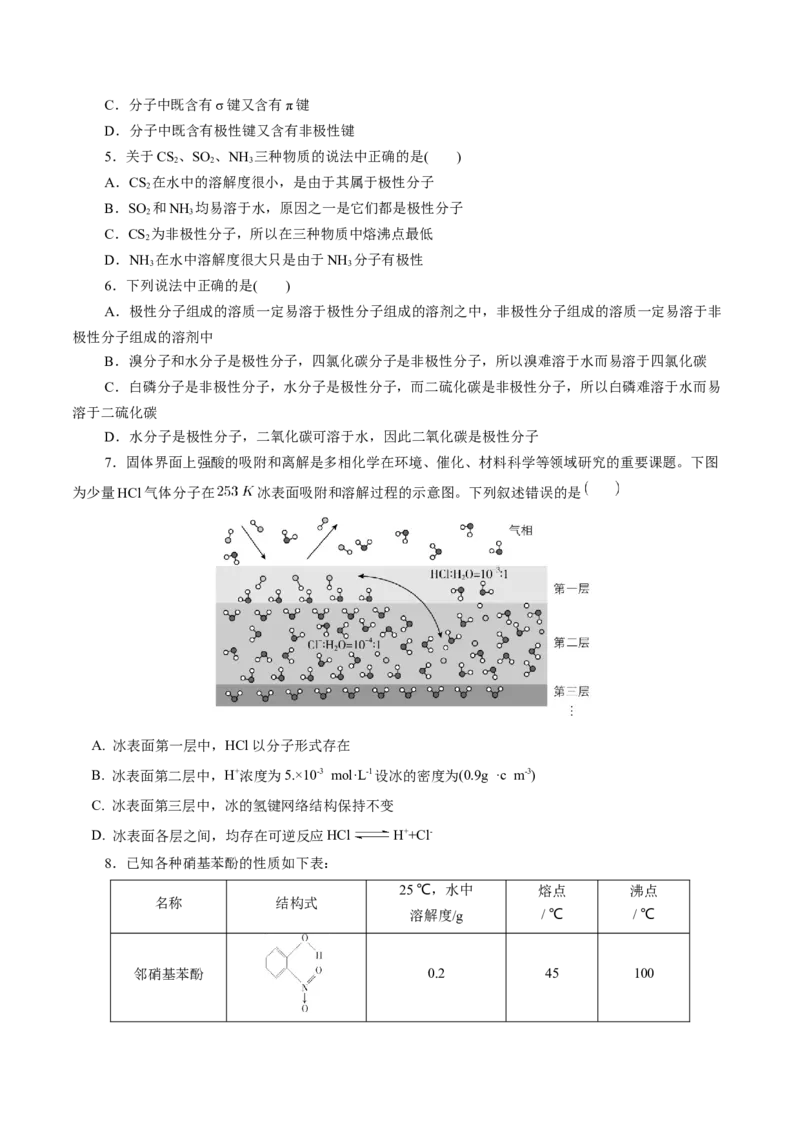
7.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图
为少量HCl气体分子在 冰表面吸附和溶解过程的示意图。下列叙述错误的是
A. 冰表面第一层中,HCl以分子形式存在
B. 冰表面第二层中,H+浓度为5.×10-3 mol·L-1设冰的密度为(0.9g ·c m-3)
C. 冰表面第三层中,冰的氢键网络结构保持不变
D. 冰表面各层之间,均存在可逆反应HCl H++Cl-
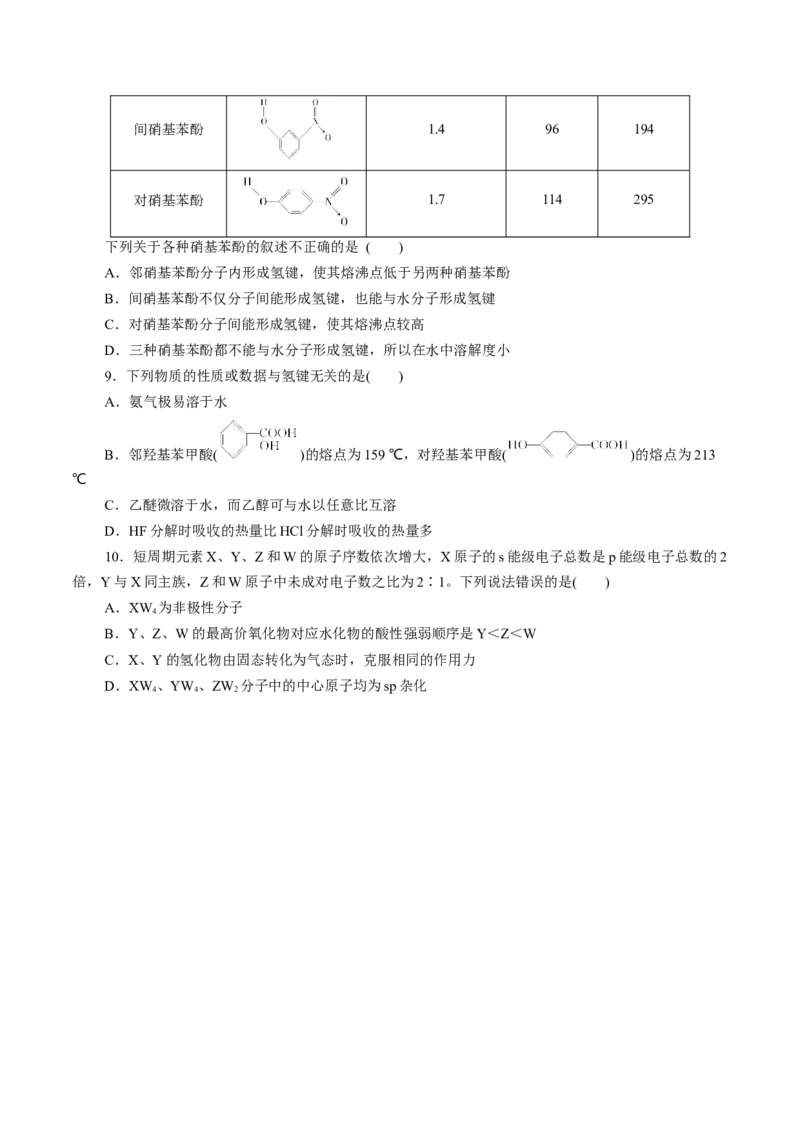
8.已知各种硝基苯酚的性质如下表:
25 ℃,水中 熔点 沸点
名称 结构式
溶解度/g / ℃ / ℃
邻硝基苯酚 0.2 45 100间硝基苯酚 1.4 96 194
对硝基苯酚 1.7 114 295
下列关于各种硝基苯酚的叙述不正确的是 ( )
A.邻硝基苯酚分子内形成氢键,使其熔沸点低于另两种硝基苯酚
B.间硝基苯酚不仅分子间能形成氢键,也能与水分子形成氢键
C.对硝基苯酚分子间能形成氢键,使其熔沸点较高
D.三种硝基苯酚都不能与水分子形成氢键,所以在水中溶解度小
9.下列物质的性质或数据与氢键无关的是( )
A.氨气极易溶于水
B.邻羟基苯甲酸( )的熔点为159 ℃,对羟基苯甲酸( )的熔点为213
℃
C.乙醚微溶于水,而乙醇可与水以任意比互溶
D.HF分解时吸收的热量比HCl分解时吸收的热量多
10.短周期元素X、Y、Z和W的原子序数依次增大,X原子的s能级电子总数是p能级电子总数的2
倍,Y与X同主族,Z和W原子中未成对电子数之比为2∶1。下列说法错误的是( )
A.XW 为非极性分子
4
B.Y、Z、W的最高价氧化物对应水化物的酸性强弱顺序是Y<Z<W
C.X、Y的氢化物由固态转化为气态时,克服相同的作用力
D.XW、YW、ZW 分子中的中心原子均为sp杂化
4 4 2