文档内容
考点 08 物质的量在化学方程式计算中的应用
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 比例法和差量法...........................................................................................................................2
考法02 守恒法和关系式法.......................................................................................................................5
.............................................................................................................................................8
1.高考真题考点分布
考点内容 考点分布
2024·浙江卷;2022·浙江6月30题,4分;2022·浙江1月30题,4分;2021·浙江
无机计算
1月30题,4分;2020·浙江7月,4分;2022·浙江1月30题,4分;
2.命题规律及备考策略
【命题规律】
从近几年全国高考试题来看,通过考查对物质的量在化学方程式中的应用,理解物质的量在高中化学计算
的应用,建立高中使用物质的量及相关概念在方程式计算中的基本运用模型仍是高考命题的热点。
【备考策略】物质的量应用于化学方程式计算类的解题步骤
(1)“审”:审清题目条件和题目要求。
(2)“设”:设出的未知数直接用各物理量的符号表示,并且不带单位。
(3)“写”:依据题意写出并配平化学方程式。
(4)“标”:在化学方程式中有关物质的化学式下面标出已知物质和所求物质有关物理量的关系,并代入已
知量和未知量。比较复杂的数量关系可先化简。
(5)“列”:将有关的几个量列出比例式。
(6)“解”:根据上述比例式求解未知数。
(7)“答”:根据题目要求简明地写出答案。
【命题预测】
预计2025年高考会以工艺流程、化工生产、科学实验为情境载体,进一步理解物质的量在化学计算中的
“桥梁作用”,初步建立化学计算的思维模型,注重化学计算能力、思维能力的考查。考法01 比例法和差量法
1.比例式法
结论:化学方程式中各物质的化学计量数之比等于组成各物质的粒子数之比,也等于各物质的物质的量之
比
【思维建模】
(1)根据题意写出并配平化学方程式。
(2)依据题中所给信息及化学方程式判断过量物质,用完全反应物质的量进行计算。
(3)把已知的和需要求解的量分别写在化学方程式有关化学式的下面,两个量及单位“上下一致,左右相
当”。
(4)选择有关量(如物质的量、气体体积、质量等)的关系作为计算依据,列比例式,求未知量。
2.差量法
(1)差量法是指根据化学反应前后有关物理量发生的变化找出“理论差量”。 这种差量可以是质量、物
质的量、气态物质的体积或压强、反应过程中的热效应等。
(2)差量法解题的关键是找准“理论差量”, 把化学方程式中的对应差量(理论差量)跟差量(实际差量)列
成比例,然后求解。如:
2C(s)+O(g)===2CO(g) Δm(固) /Δn(气) /ΔV(气)
2
2 mol 1 mol 2 mol 24 g 1 mol 22.4 L(标况)
【思维建模】
第一步:准确写出有关反应的化学方程式;
第二步:深入细致地分析题意,关键在于有针对性地找出产生差量的“对象”及“理论差量”。该“理论
差量”可以是质量、物质的量、气体体积、压强等,且该差量的大小与参加反应的物质的有关量成正比;
第三步:根据反应方程式,从“实际差量”寻找比例关系,列比例式求解。
考向01 比例法
【例1】(2024·福建泉州·一模)某红色固体粉末可能是Fe O 、Cu O或二者混合物,为探究其组成,称取
2 3 2
m g该固体粉末样品,用足量的稀HSO 充分反应后,称得固体质量为a g。
2 4
已知:Cu O+2H+===Cu+Cu2++HO
2 2
(1)若a=____________(用含m的最简式表示),则红色固体粉末为纯净物。
(2)若a=,则红色固体粉末中Fe O 的物质的量为______ mol(用含m的最简式表示)。
2 3
【解析】(1)若红色固体粉末只是Fe O ,则与稀HSO 充分反应后,无固体剩余,所以红色固体若为纯净
2 3 2 4
物,只能是Cu O,根据
2
Cu O+2H+===Cu+Cu2++HO
2 2
mol mol所以a=×64=m。
(2)设Fe O、Cu O的物质的量分别为x mol、y mol。
2 3 2
Fe O+6H+===2Fe3++3HO
2 3 2
x 2x
Cu O+2H+===Cu2++Cu+HO
2 2
y y y
2Fe3++Cu===2Fe2++Cu2+
2x x
根据题意
所以x=。
【答案】(1) (2)
考向02 差量法
【例2】(2024·浙江杭州·一模)为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将 w g样品加热,
3 2 3 1
其质量变为 w g,请列式计算该样品中NaCO 的质量分数。
2 2 3
【解析】样品加热发生的反应为
2NaHCO NaCO+HO+CO↑ Δm
3===== 2 3 2 2
168 106 62
m(NaHCO ) (w -w ) g
3 1 2
样品中m(NaHCO )= g,
3
则样品中m(Na CO)=w g- g,
2 3 1
其质量分数为×100%=×100%=×100%。
【易错警示】
注意事项:①x、y可表示物质的质量、物质的量、气体体积等,因而差量可指质量之差( m)物质的量之
差( n)或气体体积之差( V)等。
△
②分清“差量”是增还是△ 减.在较复杂的情况,存在多个反应,可能差量的增减方向并不一致,这就要取其
△
代数和.若方向相同,则总差量等于各个分差量之和。
③正确分析形成差量的原因,找出对应的根据方程式得出的“理论差量”是差量法解题的关键。
【对点1】(2024·河南安阳·模拟)过氧化钙(CaO)是一种安全无毒的物质,带有结晶水,通常还含有
2
CaO。过氧化钙在工农业生产中广泛用作杀菌剂、防腐剂、解酸剂、油类漂白剂等。
(1)称取5.42 g过氧化钙样品,灼烧时发生如下反应:2CaO·xHO=====2CaO+O↑+2xHO,得到O 在标
2 2 2 2 2
准状况下体积为672 mL,则该样品中CaO 的物质的量为________。
2
(2)另取同一样品5.42 g,溶于适量的稀盐酸中,然后加入足量的NaCO 溶液,将溶液中的Ca2+全部转化
2 3
为CaCO 沉淀,得到干燥的CaCO 7.0 g。
3 3
①样品中CaO的质量为________________。
②样品中CaO·xHO中的x为________。
2 2【解析】(1)n(O )==0.03 mol,则
2
解得n(CaO·xHO)=0.06 mol,
2 2
则n(CaO)=n(CaO·xHO)=0.06 mol。
2 2 2
(2)n(CaCO)==0.07 mol。
3
①根据钙原子守恒,可知:n(CaO)=0.07 mol-0.06 mol=0.01 mol,所以 m(CaO)=0.01 mol×56
g·mol-1=0.56 g。
②样品中水的质量为m(H O)=5.42 g-m(CaO)-m(CaO)=5.42 g-0.06 mol×72 g·mol-1-0.56 g=0.54 g,
2 2
所以n(H O)==0.03 mol,
2
则x==0.5。
【答案】(1)0.06 mol (2)①0.56 g ②0.5
【对点2】(2024·江苏扬州·期末)在质量为G g的瓷坩埚里,加入BaCl ·nHO晶体后,称量质量为W
2 2 1
g,加热使结晶水全部失去,冷却后称量为W g,则n的值为( )
2
A. B.
C. D.
【答案】A
【解析】在质量为G g的瓷坩埚里,加入BaCl ·nHO晶体后,称量质量为W g,加热使结晶水全部失去,
2 2 1
冷却后称量为W g,则根据方程式计算:
2
BaCl ·nHO =====BaCl + nHO
2 2 2 2
208+18n 208 18n
W-G W-G W-W
1 2 1 2
故有:=,解得:n=。
考法02 守恒法和关系式法
1.守恒法
(1)含义:所谓“守恒”就是物质在发生“变化”或两物质在发生“相互作用”的过程中某些物理量的
总量保持“不变”。在化学变化中的各种各样的守恒,如质量守恒、元素守恒、原子守恒、得失电子守
恒、电荷守恒、能量守恒等。
(2)守恒类型
①质量守恒(原子守恒)
依据化学反应的实质是原子的重新组合,因而反应前后原子的总数和质量保持不变。
②电荷守恒
依据电解质溶液呈电中性,即阳离子所带正电荷总数等于阴离子所带负电荷总数或离子方程式前后离子所
带电荷总数不变。利用电荷守恒法可以配平离子方程式;巧解某些化学计算题。
③得失电子守恒关系式依据氧化还原反应中电子得失数目相等,即氧化剂得到的电子总数目等于还原剂失去的电子总数目。利用
得失电子守恒法可以计算元素的化合价;计算氧化(或还原)产物的量;计算氧化剂、还原剂的消耗量;计
算混合物的组成。
2.关系式法
关系式是表示两种或多种物质之间量的关系的一种简化的式子。在多步反应中,它可以把始态的反应物与
终态的生成物之间量的关系表示出来,将多步计算简化为一步计算。高考题量大、时间紧,对于涉及多步
计算问题,如滴定实验的有关计算,巧妙运用关系式法,可大大缩短答题时间。
【思维建模】
第一步:准确写出各步反应的化学方程式;
第二步:找出“中介”的物质,并确定最初反应物、中介物质、最终生成物之间量的关系;
第三步:确定最初反应物和最终生成物之间量的关系;
第四步:根据已知条件及关系式列出比例式计算求解。
考向01 守恒法
【例1】(2024·江苏扬州·一模)兴趣小组测定莫尔盐[化学式为(NH )Fe(SO )·wHO(Fe为+2价)]的化学
4 x y 4 z 2
式,过程如下:
①称取两份质量均为1.96 g的该结晶水合物,分别制成溶液。
②一份加入足量BaCl 溶液,生成白色沉淀,用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33 g。
2
③另一份加入含0.001 mol KMnO 的酸性溶液,MnO恰好完全被还原为Mn2+,所发生的反应如下:8H++
4
5Fe2++MnO===5Fe3++Mn2++4HO
2
通过计算得出莫尔盐化学式为( )
A.(NH )Fe(SO )·3H O
4 4 2 2
B.(NH )Fe(SO )·3H O
4 2 4 2 2
C.(NH )Fe(SO )·6H O
4 2 4 2 2
D.(NH )Fe(SO )·H O
4 2 4 2 2
【答案】C
【解析】由操作②可知:n(SO)=n(BaSO)==0.01 mol,由操作③可知,n(Fe2+)=
4
5n(MnO)=5×0.001 mol=0.005 mol,再根据电荷守恒可知:n(NH)+2n(Fe2+)=2n(SO)可得:n(NH)=
2n(SO)-2n(Fe2+)=2×0.01 mol-2×0.005 mol=0.01 mol,再根据质量守恒可知,一份该结晶水合物中结晶
水的物质的量为:
n(H O)==0.03 mol,
2
故x∶y∶z∶w=n(NH)∶n(Fe2+)∶n(SO)∶n(H O)=0.01 mol∶0.005 mol∶0.01 mol∶0.03 mol
2
=2∶1∶2∶6,通过计算得出莫尔盐化学式为(NH )Fe(SO )·6H O。
4 2 4 2 2
【思维建模】
第一步:明确题目要求解的量;
第二步:根据题目要求解的量,分析反应过程中物质的变化,找出守恒类型及相关的量;
第三步:根据守恒原理,梳理出反应前后守恒的量,列式求解。考向02 关系式法
【例2】(2024·河南周口·二模)KMnO 是一种用途广泛的氧化剂,可由软锰矿(主要成分为MnO )通过下
4 2
列方法制备:
a.软锰矿与过量KOH、KClO 固体熔融生成KMnO ;
3 2 4
b.溶解、过滤后将滤液酸化,使KMnO 完全转化为MnO 和KMnO ;
2 4 2 4
c.滤去MnO ,将滤液浓缩、结晶得到深紫色的KMnO 产品。
2 4
测定KMnO 产品的纯度可用标准NaSO 溶液进行滴定。
4 2 2 3
(1)配制250 mL 0.100 mol·L-1标准NaSO 溶液,需准确称取NaSO 固体的质量为 g;
2 2 3 2 2 3
(2)取上述制得的KMnO 产品0.600 0 g,酸化后用0.100 mol·L-1标准NaSO 溶液进行滴定,滴定至终点消
4 2 2 3
耗NaSO 溶液20.00 mL。计算该KMnO 产品的纯度(写出计算过程)。(有关离子方程式为MnO+SO+H+
2 2 3 4 2
―→SO+Mn2++HO未配平)
2
【解析】(1)n=cV=0.100 mol·L-1×0.250 L=0.025 mol,m=nM=0.025 mol×
158 g·mol-1=3.950 g。
【答案】(1)3.950
(2)由化学方程式:8MnO+5SO+14H+===10SO+8Mn2++7HO,设样品中KMnO 物质的量为n mol,可
2 2 4
知
8MnO~ 5SO
2
n 0.100 mol·L-1×20.00×10-3 L
所以n(KMnO)=×0.100 mol·L-1×20.00×10-3 L=3.2×10-3 mol
4
所以m(KMnO)=nM=3.2×10-3 mol×158 g·mol-1=0.505 6 g,KMnO 产品的纯度为×100%≈84.27%。
4 4
【思维建模】
(2)关系式建立的类型
①有关化学方程式的计量数关系式:在化学反应中,任何一种元素的总质量是守恒的,即最初反应物中该
元素的质量等于最终产物中该元素的质量。
②原子守恒关系式:各步反应的化学方程式,找出最初反应物与最终生成物的物质的量的关系式,再进行
一步计算。
③得失电子守恒关系式:根据氧化剂和还原剂得失守恒建立关系式,再进行一步计算。
【对点1】(2024·山东日照·质检)将1.08 g FeO完全溶解在100 mL 1.00 mol·L-1硫酸中,然后加入25.00
mL KCr O 溶 液,恰好使Fe2+全部转化为Fe3+,且Cr O中的铬全部转化为Cr3+。则KCr O 的物质的量
2 2 7 2 2 2 7
浓度是________。
【答案】0.100 mol·L-1
【解析】由电子守恒知,FeO中+2价铁所失电子的物质的量与Cr O中+6价铬所得电子的物质的量相等,
2
×(3-2)=0.025 00 L×c(CrO)×(6-3)×2,得c(CrO)=0.100 mol·L-1。
2 2
【对点2】(2024·江苏宿迁·期末)黄铁矿主要成分是FeS。某硫酸厂在进行黄铁矿成分测定时,取0.100
2
0 g样品在空气中充分灼烧,将生成的SO 气体与足量Fe (SO ) 溶液完全反应后,用浓度为0.020 00 mol·L
2 2 4 3-1的KCr O 标准溶液滴定至终点,消耗KCr O 标准溶液25.00 mL。
2 2 7 2 2 7
已知:SO +2Fe3++2HO===SO+2Fe2++4H+
2 2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(1)样品中FeS 的质量分数是(假设杂质不参加反应) 。
2
(2)煅烧10 t上述黄铁矿,理论上产生SO 的体积(标准状况)为 L,制得98%的硫酸质量为 t。
2
【解析】(1)据方程式4FeS+11O=====2Fe O+8SO
2 2 2 3 2
SO +2Fe3++2HO===SO+2Fe2++4H+
2 2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
得关系式:Cr O~6Fe2+~3SO ~FeS
2 2 2
1
0.020 00 mol·L-1×0.025 00 L
列式计算得:m(FeS )=0.090 00 g
2
样品中FeS 的质量分数为×100%=90.00%。
2
(2)4FeS +11O=====2Fe O+ 8SO
2 2 2 3 2
4 mol 8 mol×22.4 L·mol-1
mol V(SO )
2
列式计算得:V(SO )=3.36×106 L,
2
则n(SO )==1.5×105 mol
2
由SO ~SO ~HSO
2 3 2 4
1 mol 98 g
1.5×105 mol m(H SO )×98%
2 4
列式计算得:m(H SO )=1.5×107 g=15 t。
2 4
【答案】(1)90.00% (2)3.36×106 15
1.(2024·浙江杭州·一模)XSO (aq)与NaOH(aq)反应,定量生成X(OH) SO (s)和NaSO (aq)。1.0mol/L的
4 3 4 4 2 4
XSO 和1.0mol/LNaOH混合,总体积为50mL(体积可加合)。为了得到最大的沉淀量,这两种溶液的体积应
4
取
A.29mLNaOH+21mLXSO B.21mLNaOH+29mLXSO
4 4
C.15mLNaOH+35mLXSO D.20mLNaOH+30mLXSO
4 4
【答案】A
【解析】生成的沉淀为X(OH) SO (s),X2+和OH-的物质的量比为3:4,根据元素守恒,XSO 溶液、NaOH
3 4 4 4
溶液的物质的体积比为3:4,需要XSO 溶液的体积为 ,需要NaOH溶液的体积为 ,故选
4A。
2.(2024·湖南郴州·期末)现有铁及其氧化物粉末7.04g,加入100mL1 的稀硫酸恰好完全溶解,
并收集到标准状况下气体224mL。向反应后的溶液中滴加KSCN溶液,无明显变化。若将等质量的该混合
物在高温下与足量的CO充分反应,生成CO 的质量为
2
A.1.65g B.2.20g C.3.96g D.4.40g
【答案】C
【解析】现有铁及其氧化物粉末7.04克,加入含0.1molHSO 的稀硫酸恰好完全溶解,向反应后的溶液滴
2 4
加KSCN溶液,无明显变化,说明生成物是硫酸亚铁,根据硫酸根离子守恒可知硫酸亚铁的物质的量是
0.1mol,所以混合物中铁元素的物质的量是0.1mol,质量是0.1mol×56g/mol=5.6g,则铁及其氧化物粉末
中氧元素质量为7.04g-5.6g=1.44g,即O元素的物质的量为0.09mol,则该混合物可表示为Fe O,该混合
10 9
物在高温下与足量的CO充分反应,方程式为: ,根据 ,设生成
CO 的质量为xg,可列出: ,解得x=3.96g;故选C。
2
3.(2024·重庆·期中)为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中
的100mL、0.30mol/L的酸性 溶液。已知 与该溶液反应的离子方程式为:
。若管道中空气流量为0.5L/min,经过3min溶液恰好褪色,
假定样品中的 可被溶液充分吸收,则该空气样品中 的含量(单位为g/L)是
A.3.2 B.6.4 C.9.6 D.1.6
【答案】A
【解析】根据题干信息,经过3 min溶液恰好褪色,则通过空气的体积为0.5L·min-1×3min=1.5 L,消耗的酸
性KMnO 的物质的量为0.1L×0.3mol/L=0.03mol,设尾气中SO 的物质的量为nmol,则由离子方程式得
4 2
, ,尾气样品中SO 含量为 ,综上
2
所述A符合题意;故选A。
4.(2024·江西南昌·期末)某稀溶液中含有 和 ,向其中加入 ,充分反
应(已知 被还原为NO),最终溶液体积为 ,下列说法正确的是
A.所得溶液中的溶质只有 、
B.所得溶液中
C.反应后生成NO的体积为 (标准状况下)
D.所得溶液中
【答案】D【分析】铁与氢离子、硝酸根离子反应生成铁离子、一氧化氮和水,反应的离子方程式为Fe+NO
+4H+=Fe3++NO↑+2HO,由方程式可知,5mol氢离子反应消耗1.25mol硝酸根离子和1.25mol铁,生成铁离
2
子和一氧化氮的物质的量都为1.25mol,则反应中氢离子不足量、硝酸根离子和铁过量,过量的铁与溶液
中的铁离子反应生成亚铁离子,反应的离子方程式为2Fe3++Fe=3Fe2+,由方程式可知,0.25mol铁反应消耗
0.5mol铁离子,生成0.75mol亚铁离子,所以充分反应后的溶液中硝酸根离子的物质的量为4mol—
1.25mol=2.75mol、铁离子物质的量为1.25mol—0.5mol=0.75mol、亚铁离子物质的量物质为0.75mol、硫酸
根离子物质的量物质为2.5mo。
【解析】A.由分析可知,充分反应后的溶液中含有3.75mol硝酸根离子,所以所得溶液中的溶质不可能只
有硫酸亚铁和硫酸铁,故A错误;
B.由分析可知,充分反应后的溶液中铁离子和亚铁离子的物质的量都为0.75mol,物质的量比为1:1,故
B错误;
C.由分析可知,反应生成一氧化氮的物质的量为1.25mol,则标准状况下的体积为1.25mol×22.4L/
mol=28L,故C错误;
D.由分析可知,充分反应后的溶液中含有3.75mol硝酸根离子,则溶液中硝酸根离子的浓度为
=2.75mol/L,故D正确;故选D。
5.2024·湖南·期末)将1.52g铜镁合金完全溶解于浓硝酸中,得到 和 的混合气体0.05mol,向反
应后的溶液中加入NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,则 与 的物质的量之比
为
A.1∶1 B.2∶1 C.4∶1 D.1∶2
【答案】C
【解析】由题意可知,铜镁合金完全溶解于浓硝酸中得到含有硝酸铜、硝酸镁的混合溶液,向溶液中加入
氢氧化钠溶液,溶液中铜离子、镁离子完全转化为氢氧化铜、氢氧化镁沉淀,则由原子个数守恒可知,铜
镁合金溶解时失去电子的物质的量为 =0.06mol,设混合气体中二氧化氮为amol,由得失电子
数目守恒可得:a+2(0.05—a)=0.06,解得a=0.04,则混合气体中二氧化氮和四氧化二氮的物质的量之比为
0.04:0.01=4:1,故选C。
6.(2024·四川德阳·期末)把 镁铝合金的粉末放入过量的盐酸中,得到 。下列说法错误的是
A.合金中铝的质量分数约为 B.合金中镁和铝的物质的量之比为
C.镁和铝还原出的 体积之比为 D.在标准状况下, 的体积为
【答案】C
【分析】把 镁铝合金的粉末放入过量的盐酸中,发生反应Mg+2H+=Mg2++H ↑、2Al+6H+=2Al3++3H ↑,
2 2
得到 ,设Mg的物质的量为xmol、Al的物质的量为ymol;则 ,x=0.1mol、y=0.2mol。【解析】A.合金中铝的质量分数约为 ,故A正确;
B.根据以上分析,Mg的物质的量为0.1mol、Al的物质的量为0.2mol,合金中镁和铝的物质的量之比为
,故B正确;
C.Mg的物质的量为0.1mol,还原出0.1mol氢气;Al的物质的量为0.2mol,还原出0.3mol氢气,镁和铝
还原出的 体积之比为1:3,故C错误;
D.在标准状况下, 的体积为 ,故D正确;选C。
7.(2024·浙江杭州·期中)取体积相同的KI、FeCl 、FeBr 溶液,分别通入足量氯气,当恰好完全反应
2 2
时,三种溶液消耗氯气的物质的量相同,则KI、FeCl 、FeBr 溶液的物质的量浓度之比为
2 2
A.1∶1∶1 B.1∶1∶3 C.3∶3∶1 D.2∶2∶1
【答案】C
【解析】碘化钾溶液与氯气反应生成氯化钾和碘,反应的化学方程式为2KI+Cl =2KI+I ,氯化亚铁溶液与
2 2
氯气反应生成氯化铁,反应的化学方程式为2FeCl +Cl=2FeCl ,溴化亚铁溶液与足量氯气反应生成氯化铁
2 2 3
和溴,反应的化学方程式为2FeBr +3Cl=2FeCl +2Br ,若三种溶液都消耗3mol氯气,由方程式可知,体积
2 2 3 2
相同的三种溶液的浓度之比为6∶6∶2=3∶3∶1,故选C。
8.(2024·甘肃兰州·期末)向一定量的铁、氧化铁、氧化亚铁的混合物中,加入200mL0.5mol/L的盐酸,
恰好使混合物完全溶解,放出224mL(标况)气体,所得溶液中加入硫氰化钾无血红色出现,那么用足量CO
还原相同质量的混合物得到铁的质量是
A.11.2g B.5.6g C.2.8g D.10.8g
【答案】C
【解析】盐酸恰好使混合物完全溶解,盐酸没有剩余,向反应所得溶液加KSCN溶液无血红色出现,说明
溶液为FeCl 溶液,根据氯元素守恒可知n(FeCl )=0.5n(HCl)=0.5×0.2L×0.5mol/L=0.05mol;用足量的CO在
2 2
高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeCl )=0.05mol,质量为
2
0.05mol×56g/mol=2.8g;答案选C。
9.(2024·河北衡水·期末)向一定量的Cu、CuO、Fe O 的混合物中加入100mL2mol/L的盐酸,恰好使混
2 3
合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质
量为
A. B. C. D.
【答案】B
【解析】依题意,向一定量的Cu、CuO、Fe O 的混合物中加入100mL2mol/L的盐酸,所得溶液中的溶质
2 3
为CuCl 、FeCl ,混合物中的O元素全部转化为HO;用过量的CO在高温下还原相同质量的原混合物,
2 2 2
固体减少的质量也就是混合物中O元素的质量。由反应可建立关系式:O——2HCl,
n(HCl)=0.100L×2mol/L=0.2mol,则m(O)=0.1mol×16g/mol=1.6g,故选B。
10.(2024·河北邢台·期末)将铜片放入一定体积 溶液A中浸泡,一段时间后取出铜片(经洗涤、干燥)精确称量,铜片质量减轻了 ,得到的溶液B中 ,则下列说法正确的是
A.溶液B中 与 的物质的量之比为1:3 B.原 溶液A中 的物质的量为
C.溶液B中最多可溶解 D.原 溶液A的体积为
【答案】A
【分析】将铜片放入一定体积 溶液A中浸泡,发生 ,铜片质量减轻
了 ,消耗的铜的物质的量为 ,生成的 的物质的量为0.1mol,消耗的 的物质的
量为0.2mol,生成的 的物质的量为0.2mol,得到的溶液B中剩余 的物质的量为0.3mol,
溶液A中 的物质的量为0.5mol。
【解析】A.溶液B中 与 的物质的量之比为0.1mol:0.3mol=1:3,A正确;
B.原 溶液A中 的物质的量为0.5mol,则 的物质的量为1.5mol,B错误;
C.溶液B中 与 的物质的量分别为0.1mol和0.3mol,加入金属铁可以发生反应 、
,可以分别溶解铁的物质的量是0.1mol和0.15mol,即最多可溶解 ,质量为
,C错误;
D. 溶液A中 的物质的量为0.5mol,体积为 ,即500ml,D错误;
答案选A。
11.(2024·黑龙江哈尔滨·期中)现有A、B、C三种化合物,各取20g相混合,完全反应后,得到9.0g
B、24.5g C,还有D生成,已知D的相对分子质量为106.现将44.0g A和22.0g B反应,能生成D的物质的
量为
A.1.00 B.0.500 C.0.275 D.0.250
【答案】B
【分析】20gA完全反应,参加反应的B的质量为20g-9g=11g,生成的C的质量为24.5g-20g=4.5g,根据质
量守恒定律计算生成的D的质量,根据质量定比定律计算44gA和44gB反应,哪种物质有剩余,根据不足
量的物质利用质量定比关系计算生成D的质量,再n= 计算D的物质的量,据此分析解题。
【解析】20gA完全反应,参加反应的B的质量为20g-9g=11g,生成的C的质量为24.5g-20g=4.5g,根据质
量守恒定律可知生成的D的质量为20+11-4.5=26.5g,22gB反应需要A的质量为22g× =12.1g,则A过
量,B完全反应生成D的质量为22g× =53g,D的相对分子质量为106,则D的物质的量为
=0.5mol,故答案为:B。12.(2024·福建福州·期中)2.48g铁铜合金完全溶解于80mL 4.0 稀硝酸中,得到标准状况下
672mL NO气体(假设此时无其他气体产生),下列说法正确的是
A.反应后溶液中不存在
B.该合金中铁与铜的物质的量之比是1∶2
C.反应后溶液(忽略溶液体积变化)中
D.向反应后的溶液中加入2.0 NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积
是120mL
【答案】C
【分析】反应生成672mL的NO气体, ,转移电子物质的量
=0.03mol×3=0.09mol;由方程式可知,作氧化剂的硝酸是整个硝酸的 ,所以参加反应的硝酸的物质的量
为:0.03mol×4=0.12mol,而80mL4.0mol/L稀硝酸中硝酸的物质的量为:0.32mol,所以硝酸过量,铁与铜
完全反应,铁转化为铁离子,令混合物中铁、铜的物质的量分别为xmol、ymol,根据二者质量与电子转移
守恒,则: ,可求得x=0.01,y=0.03。
【解析】A.据分析,铁转化为三价铁,所以溶液中存在Fe3+,A错误;
B.该合金中铁与铜的物质的量之比是0.01∶0.03=1:3,B错误;
C.反应后溶液中剩余 ,则反应后溶液(忽
略溶液体积变化)中 ,C正确;
D.离子完全沉淀得到硝酸钠溶液,根据硝酸根守恒可知:需加入NaOH的物质的量为
0.32−0.03=0.29mol,所以V=0.29mol÷0.2mol/L=0.145L=145ml,D错误;故选C。
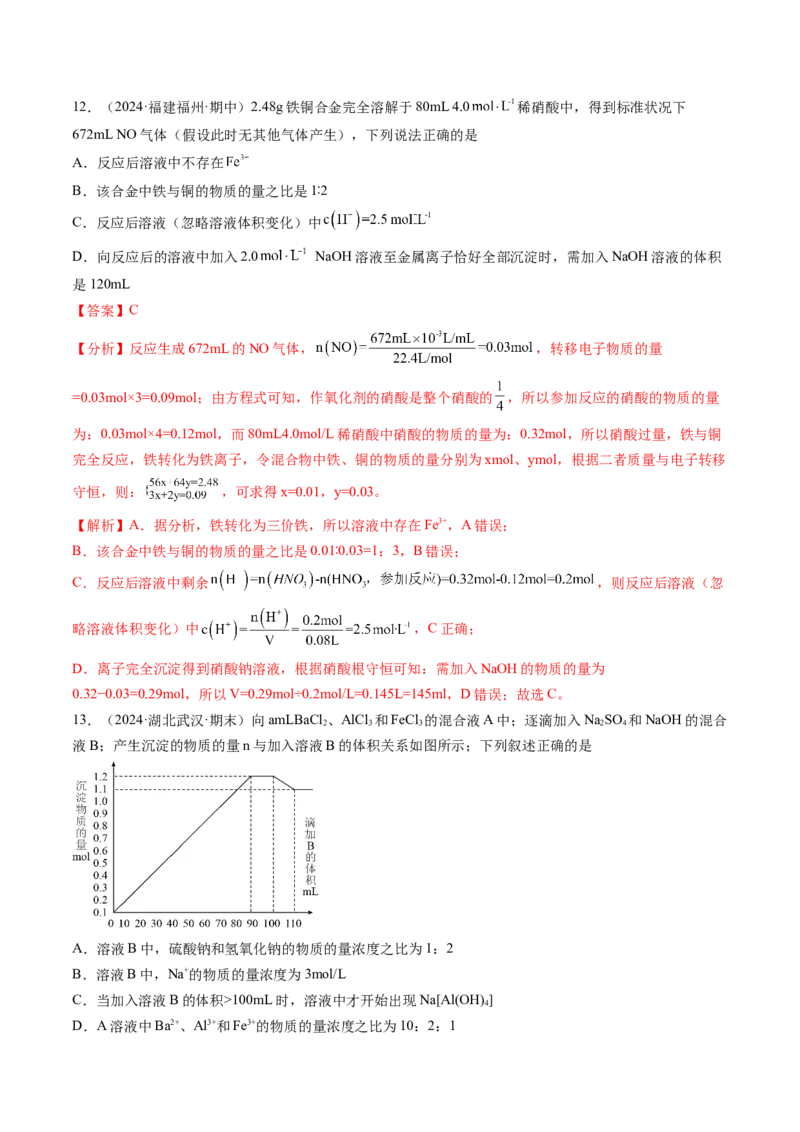
13.(2024·湖北武汉·期末)向amLBaCl 、AlCl 和FeCl 的混合液A中;逐滴加入NaSO 和NaOH的混合
2 3 3 2 4
液B;产生沉淀的物质的量n与加入溶液B的体积关系如图所示;下列叙述正确的是
A.溶液B中,硫酸钠和氢氧化钠的物质的量浓度之比为1:2
B.溶液B中,Na+的物质的量浓度为3mol/L
C.当加入溶液B的体积>100mL时,溶液中才开始出现Na[Al(OH)]
4
D.A溶液中Ba2+、Al3+和Fe3+的物质的量浓度之比为10:2:1【答案】D
【分析】A溶液中含有Ba2+、Fe3+、Al3+、Cl-,B溶液中含有 、OH-、Na+,向A溶液中逐渐滴加B溶
液,一开始产生沉淀为BaSO、Fe(OH) 和Al(OH) ,沉淀的物质的量逐渐增加;当Fe3+、Al3+沉淀完全后,
4 3 3
继续加入B溶液,Al(OH) 逐渐溶解,沉淀的物质的量开始减少,而图像中第二段曲线为平行线,则
3
Al(OH) 溶解的同时,还有BaSO 继续生成,且溶解的Al(OH) 的物质的量和生成的BaSO 的物质的量相
3 4 3 4
等;第三段曲线中,沉淀物质的量逐渐减少,则第三段只有Al(OH) 的溶解过程。根据上述分析,
3
V(B)=90mL时,Fe3+、Al3+恰好沉淀完全;90mL<V(B)<100mL时,Al(OH) 开始溶解,BaSO 继续生成;
3 4
V(B)=100mL时,Ba2+恰好沉淀完全;100mL<V(B)<110mL,Al(OH) 继续溶解;V(B)=110mL,沉淀中
3
Al(OH) 溶解完全。
3
【解析】A.第二段曲线溶解的Al(OH) 的物质的量和生成的BaSO 的物质的量相等,根据反应
3 4
, ,所以NaOH的浓度与NaSO 的浓度相等,故A错
2 4
误;
B.根据分析可知,V(乙)=100mL时,Al(OH)3没有溶解完全,沉淀物应为BaSO4、Fe(OH)3、Al(OH)3,
故B错误;
C.根据A分析,NaOH的浓度与NaSO 的浓度相等,第三段曲线中,消耗了10mL乙溶液,溶解了
2 4
0.1molAl(OH) ,c(NaOH)= ,Na+的物质的量浓度为30mol/L,故C错误;
3
D.第三段曲线中,消耗了10mL乙溶液,溶解了0.1molAl(OH) ,根据 ,可
3
知,c(NaOH)= ;根据分析可知,c(NaOH)=c(Na SO )=10mol/L;100mL乙溶液时,
2 4
BaSO 沉淀完全,则n(Ba2+)=10mol/L×0.10L=1.0mol;第二、三段均有Al(OH) 的溶解,所以
4 3
n(Al3+)=n[Al(OH) ]=10mol/L×0.020L=0.2mol;V(B)=90mL时,Fe3+、Al3+恰好沉淀完全;则
3
n(Al3+)×3+n(Fe3+)×3=10mol/L×0.090L=0.9mol,则n(Fe3+)=0.1mol,所以
n(Ba2+)∶n(Al3+)∶n(Fe3+)=1∶0.2∶0.1=10∶2∶1,则甲溶液中Ba2+、Al3+、Fe3+的物质的量浓度之比为:10:2:1,故
D正确;
故答案为:D。
14.(2024·广东深圳·期末)将6.4g铜投入30mL一定浓度的硝酸中,恰好完全反应,产生标准状况下的
NO和NO 混合气体共2.24L。则下列叙述正确的是
2
A.反应中失去电子数为0.1mol B.做氧化剂的硝酸为0.1mol
C.NO体积为0.56L D.原硝酸浓度0.3mol/L
【答案】B
【分析】6.4gCu的物质的量为0.1mol,与硝酸恰好反应,生成标况下NO和NO 共2.24L,为0.1mol,根
2
据电子转移守恒,Cu失去电子=N得到的电子,0.1molCu被氧化失去0.2mol电子,设NO的物质的量为
xmol,NO 的物质的量为ymol,故有3x+y=0.2和x+y=0.1mol,解得x=0.05mol,y=0.05mol。
2
【解析】A.反应中Cu被氧化为Cu2+,0.1molCu失去的电子的物质的量为0.2mol,A错误;
B.做氧化剂的硝酸转化为一氧化氮、二氧化氮,根据氮原子守恒可知,为0.1mol,B正确;C.NO体积为0.05mol×22.4L/mol=1.12L,C错误;
D.根据原子守恒,消耗的硝酸的总物质的量=起氧化剂作用的硝酸的物质的量(还原产物的总物质的量)
+起酸性作用的硝酸的物质的量(生成盐中的硝酸根的物质的量),故有n(HNO)=n(NO)
3
+n(NO)+2n(Cu(NO ))=0.1+0.2=0.3mol,V=30mL,则c(HNO )= =10mol/L,D错误;
2 3 2 3
故选B。
15.(2024·四川绵阳·期末)将20.0 g铜镁合金完全溶解于140mL某浓度的硝酸中,得到NO 和NO的混
2
合气体8.96 L(标准状况),当向反应后的溶液中加入320 mL4.0 mol/LNaOH溶液时,金属离子全部转化为
沉淀,测得沉淀的质量为37 g。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2:3
B.该硝酸中HNO 的物质的量浓度12 mol/L
3
C.NO 和NO的混合气体中,NO 的体积分数25%
2 2
D.若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为11.2 L
【答案】D
【分析】根据题意可知,铜失去2个电子生成铜离子,铜离子与2个氢氧根离子反应生成氢氧化铜沉淀;
镁失去2个电子生成镁离子,镁离子与2个氢氧根离子反应生成氢氧化镁沉淀,据此分析。
【解析】A.根据上述分析:金属阳离子得到氢氧根物质的量等于金属失去电子物质的量,依据质量守
恒,得到氢氧根物质的量为n(OH-)= =l mol,即得失电子物质的量为l mol,因此有2n(Cu)
+2n(Mg)=l mol,根据二者质量和为20.0 g可得关系式64n(Cu)+24n(Mg) =20.0 g,两式联立解得n(Cu)=0.2
mol,n(Mg)=0.3 mol,因此合金中铜和镁的物质的量之比为2 :3,A正确;
B.金属阳离子Cu2+、Mg2+全部沉淀后,溶液中溶质为NaNO ,根据氮原子守恒可得
3
n(HNO)=n(NaNO )+n(NO)+n(NO )=0.32L×4.0 mol/L+ =l.68 mol,溶液的体积是140 mL,则硝酸
3 3 2
的浓度为c(HNO)= mol/L=12 mol/L,B正确;
3
C.根据得失电子数目守恒,3n(NO)+n(NO )=l mol,n(NO)+n(NO )= =0.4 mol,两式联立解得
2 2
n(NO)=0.3 mol,n(NO )=0.1 mol,则相同条件下,二者的体积分数等于物质的量分数,故NO 的体积分数
2 2
为 ×100%=25%,C正确;
D.根据上述分析可知:反应过程中转移电子的物质的量等于沉淀中OH-的物质的量,n(e-)= n(OH-)=1
mol,若将混合气体与水混合完全转化为硝酸,则O 得到电子的物质的量与HNO 变为NO、NO 时失去电
2 3 2
子的物质的量相等,4n(O )=1 mol,n(O )=0.25 mol,其在标准状况下的体积为V(O )=0.25 mol×22.4
2 2 2
L/mol=5.6 L,D错误;故选D。1.(2024·浙江卷1月)HS可用于合成光电材料。某兴趣小组用 与 反应制备液态HS,实验装
2 2
置如图,反应方程式为: 。
(6)取 产品,与足量 溶液充分反应后,将生成的 置于已恒重、质量为
的坩埚中,煅烧生成 ,恒重后总质量为 。产品的纯度为_______。
【解析】根据铜守恒,氧化铜的质量为32.814 g-31.230 g=1.584g,则氧化铜物质的量为0.0198mol,
,硫化铜物质的量为0.0198mol,则HS物质的量为0.0198mol,HS的质量为
2 2
0.6732g,产品纯度为 。
【答案】99%
2.(2023·湖北卷)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。
(2)铜与过量HO 反应的探究如下:
2 2
实验②中Cu溶解的离子方程
式为_______;产生的气体为_______。比较实验①和②,从氧化还原角度说明 的作用是_______。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰
性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为_______。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示
剂,用0.1000mol·L-1 Na SO 标准溶液滴定,滴定终点时消耗NaSO 标准溶液15.00mL。(已知:2Cu2+
2 2 3 2 2 3
+4I-=2CuI↓+I ,I+2S O2-=2I-+S O2-)标志滴定终点的现象是_______,粗品中X的相对含量为_______。
2 2 2 3 4 6
【解析】(1)由图可知,仪器A的名称为具支试管;铜和浓硝酸反应生成硝酸铜和二氧化氮,其中二氧化氮
易溶于水,需要防倒吸,则装置B的作用为防倒吸;(2)根据实验现象,铜片溶解,溶液变蓝,可知在酸性
条件下铜和过氧化氢发生反应,生成硫酸铜,离子方程式为:Cu+H O+2H+= Cu2++2H O;硫酸铜可以催化
2 2 2
过氧化氢分解生成氧气,则产生的气体为O;在铜和过氧化氢的反应过程中,氢元素的化合价没有发生变
2
化,故从氧化还原角度说明H+的作用是:既不是氧化剂,又不是还原剂;(3)在该反应中铜的质量m(Cu)=n× ,因为 ,则m(O)= ,则X的化学式中铜原子和氧原子的物
质的量之比为: ,则X为CuO;(4)滴定结束的时候,单质碘消耗完,则标志滴定终
2
点的现象是:溶液蓝色消失,且半分钟不恢复原来的颜色;在CuO 中铜为+2价,氧为-1价,根据2Cu2+
2
+4I-=2CuI↓+I ,I+2S O2-=2I-+S O2-,可以得到关系式:CuO~2I ~4S O2-,则n(CuO)= ×0.1mol/
2 2 2 3 4 6 2 2 2 3 2
L×0.015L=0.000375mol,粗品中X的相对含量为 。
【答案】(1)①具支试管 ②防倒吸
(2)①Cu+H O+2H+= Cu2++2H O ②O ③既不是氧化剂,又不是还原剂
2 2 2 2
(3)CuO (4)①溶液蓝色消失,且半分钟不恢复原来的颜色 ② 72%
2
3.(2022·湖南卷)某实验小组用重量法测定产品中BaCl ·2H O的含量。步骤如下:
2 2
①称取产品0.500 0 g,用100 mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100 mol·L-1 HSO 溶液;
2 4
③沉淀完全后,60 ℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.466 0 g。
则产品中BaCl ·2H O的质量分数为 (保留三位有效数字)。
2 2
【解析】由题意可知,硫酸钡的物质的量为:=0.002 mol,依据钡原子守恒,产品中BaCl ·2H O的物质的
2 2
量为0.002 mol,质量为0.002 mol×244 g/mol=0.488 g,质量分数为:×100%=97.6%。
【答案】97.6%
4.(2022·辽宁卷)H O 作为绿色氧化剂应用广泛。某实验小组测定产品中HO 的含量,取2.50 g产品,加
2 2 2 2
蒸馏水定容至100 mL摇匀,取20.00 mL于锥形瓶中,用0.050 0 mol·L-1酸性KMnO 标准溶液滴定。平行
4
滴定三次,消耗标准溶液体积分别为19.98 mL、20.90 mL、20.02 mL。假设其他杂质不干扰结果,产品中
HO 质量分数为 。
2 2
【解析】滴定反应的离子方程式为2MnO+5HO+6H+===2Mn2++5O↑+8HO,可得关系式:2KMnO ~
2 2 2 2 4
5HO。三组数据中20.90 mL偏差较大,舍去,故消耗酸性高锰酸钾标准溶液的平均体积为20.00 mL,
2 2
HO 的质量分数w=
2 2
×100%=17%。
【答案】17%
5.(2022·山东卷)现有含少量杂质的FeCl ·nHO,为测定n值进行如下实验:
2 2
实验Ⅰ:称取m g样品,用足量稀硫酸溶解后,用c mol·L-1 KCr O 标准溶液滴定
1 2 2 7
Fe2+达终点时消耗V mL(滴定过程中Cr O转化为Cr3+,Cl-不反应)。
2
实验Ⅱ:另取m g样品,利用上述装置与足量SOCl 反应后,固体质量为m g。
1 2 2
则n= ;下列情况会导致n测量值偏小的是 (填标号)。
A.样品中含少量FeO杂质B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
【解析】滴定过程中Cr O将Fe2+氧化成Fe3+,自身被还原成Cr3+,反应的离子方程式为6Fe2++Cr O+
2 2
14H+===6Fe3++2Cr3++7HO,则m g样品中n(FeCl )=6n(CrO)=6cV×10-3 mol;m g样品中结晶水的
2 1 2 2 1
质量为(m-m) g,结晶水物质的量为 mol,n(FeCl )∶n(H O)=1∶n=(6cV×10-3 mol)∶ mol,解得n=;样品
1 2 2 2
中含少量FeO杂质,溶于稀硫酸后生成Fe2+,导致消耗的KCr O 溶液的体积V偏大,使n的测量值偏
2 2 7
小,A项选;样品与SOCl 反应时失水不充分,则m 偏大,使n的测量值偏小,B项选;实验Ⅰ称重后,
2 2
样品发生了潮解,样品的质量不变,消耗的KCr O 溶液的体积V不变,使n的测量值不变,C项不选;滴
2 2 7
定达到终点时发现滴定管尖嘴内有气泡生成,导致消耗的KCr O 溶液的体积V偏小,使n的测量值偏
2 2 7
大,D项不选。
【答案】 AB
6.[2022·江苏,14(3)]FeS 、FeS在空气中易被氧化,将FeS 在空气中氧化,测得氧化过程中剩余固体的质
2 2
量与起始FeS 的质量的比值随温度变化的曲线如图所示。800 ℃时,FeS 氧化成含有两种元素的固体产物
2 2
为_______________________________________________________________________(填化学式,写出计算
过程)。
【解析】Fe O;设FeS 氧化成含有两种元素的固体产物化学式为FeO,M(FeS )=120 g·mol-1,则M(FeO)
2 3 2 x 2 x
=120 g·mol-1×66.7%=80.04 g·mol-1,则56+16x=80.04,x≈,即固体产物为Fe O
2 3
7.(2022·浙江省6月选考,30)联合生产是化学综合利用资源的有效方法。煅烧石灰石反应:CaCO (s)
3
=CaO(s)+CO(g) ΔH=1.8×102kJ·mol−1,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定
2
比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成CO,其热量有效利用率为50%。石灰窑中产
2
生的富含CO 的窑气通入氨的氯化钠饱和溶液中,40%的CO 最终转化为纯碱。已知:焦炭的热值为30
2 2
kJ·g-l (假设焦炭不含杂质)。请回答:
(1)每完全分解 石灰石(含CaCO 90%,杂质不参与反应),需要投料_______kg焦炭。
3
(2)每生产106kg纯碱,同时可获得_______kgCaO (列式计算)。
【答案】(1)10.8 (2)70
【解析】(1)完全分解100kg石灰石(含CaCO 90%,杂质不参与反应),需要吸收的热量是
3
=162000kJ,已知:焦炭的热值为30 kJ·g-l (假设焦炭不含杂质),其热量有效利用率为50%,所以需要投料焦炭的质量是 =10800g=10.8kg。(2)根据(1)中计算可知消耗焦炭
的物质的量是 =900mol,参加反应的碳酸钙的物质的量是900mol,这说明参加反应的碳酸钙和焦
炭的物质的量之比为1:1,所以根据原子守恒可知生成氧化钙的质量是 =70kg。