文档内容
考点 4 沉淀溶解平衡
1.3年真题考点分布
考点分布
年份 卷区
沉淀溶解平衡 溶度积常数及其应用 沉淀的生成和溶解、转化
辽宁 √
2023
浙江 √
湖南 √
2022
山东 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.沉淀溶解平衡及其影响因素
2.溶度积常数及其应用
3.沉淀的生成和溶解
【备考策略】熟练掌握认识难溶电解质的溶解有一定限度,是可以调控的。能多角度、动态地分析难溶电解质
的沉淀溶解平衡,并运用难溶电解质的沉淀溶解平衡原理解决实际问题(如利用生成沉淀处理污水等)。
【命题预测】预测2024年高考,有关难溶电解质的沉淀溶解平衡的判断问题;能从问题和假设出发,确定探究
目的,设计探究方案,进行沉淀转化等实验探究。
考法 1 沉淀溶解平衡
一、沉淀溶解平衡的基本概念
1.溶解平衡的定义
杨sir化学,侵权必究
在一定温度下,当难溶电解质溶于水形成饱和溶液时,溶质的离子与该固态溶质之间建立的动态平衡,叫作沉
淀溶解平衡。
2. 沉淀溶解平衡方程式
M A(s) mMn+(aq) + nAm-(aq)
m n
如AgCl沉淀溶解平衡:AgCl(s) Ag+(aq) + Cl-(aq)
二、沉淀溶解平衡及应用
1.难溶、可溶、易溶界定:
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
资料整理【淘宝店铺:向阳百分百】2.沉淀溶解平衡
(1)溶解平衡的建立
(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)
3.影响沉淀溶解平衡的因素
(1)内因
难溶电解质本身的性质,这是决定因素。
(2)外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动;
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;
③同离子效应:向平衡体系中加入难溶物溶解产生的离子,平衡向生成沉淀的方向移动;
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向沉淀溶解
的方向移动。
(3)以AgCl(s) Ag+(aq)+Cl-(aq) ΔH>0为例,填写外因对溶解平衡的影响
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度 正向 增大 增大 增大
加水稀释 正向 不变 不变 不变
加入少量AgNO 逆向 增大 减小 不变
3
通入HCl 逆向 减小 增大 不变
通入HS 正向 减小 增大 不变
2
【典例1】(南京师大附中2023届高三模拟)如图所示,有T、T 两种温度下两条BaSO 在水中的沉淀溶解平衡
1 2 4
曲线,在T 温度下,下列说法不正确的是
1
资料整理【淘宝店铺:向阳百分百】A.加入NaSO 可使溶液由a点变到b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
1. (广东省惠州一中2022-2023学年高三模拟)已知常温下K (AgCl)=1.6×10-10,K (AgI)=8.3×10-17,下列有关说法
sp sp
正确的是( )
A.常温下,AgCl在纯水中的K 比在AgNO 溶液中的K 大
sp 3 sp
B.向AgI与AgCl的悬浊液中加入几滴浓NaCl溶液, 不变
C.在AgCl的饱和溶液中通入HCl,有AgCl析出,且溶液中c(Ag+)=c(Cl-)
D.向AgCl与AgI等体积混合的饱和溶液中加入足量浓AgNO 溶液,产生的AgCl沉淀的物质的量少于AgI
3
考法 2 溶度积常数及其应用
二、溶度积常数及其应用
1.溶度积和离子积
以A B (s ) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
K (A B )=cm(An+)·cn(Bm-),式中的浓度 Q(A B )=cm(An+)·cn(Bm-),式中的
表达式 sp m n c m n
都是平衡浓度 浓度都是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有沉淀析出
c sp
应用
②Q=K :溶液饱和,处于平衡状态
c sp
③Q<K :溶液未饱和,无沉淀析出
c sp
2.K 的影响因素
sp
(1)内因:难溶物质本身的性质,这是主要决定因素。
(2)外因
资料整理【淘宝店铺:向阳百分百】①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K 增大。
sp
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,平衡向
溶解方向移动,但K 不变。
sp
3. 意义
对于相同类型的难溶电解质,K 越大,说明难溶电解质在水中的溶解能力越大。
sp
如:K (AgCl) > K (AgBr) > K (AgI),则溶解度:S (AgCl) > S (AgBr) > S (AgI)。
sp sp sp
4.应用
① M m A n (s) ⇌ mMn+(aq) + nAm-(aq),任意时刻的离子积:Q = cm(Mn+)·cn(Am-)
② 根据K 和Q的相对大小,可以判断给定条件下溶液中难溶电解质的沉淀或溶解情况:
sp
Q > K ,溶液中有沉淀析出
sp 杨sir化学,侵权必究
Q = K ,沉淀与溶解处于平衡状态
sp
Q < K ,溶液中无沉淀析出
sp
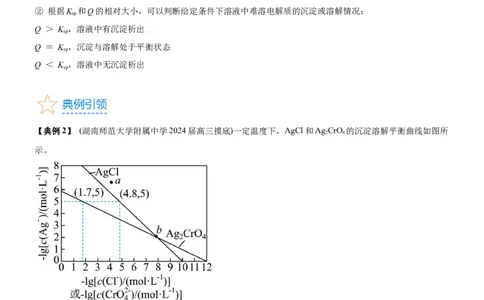
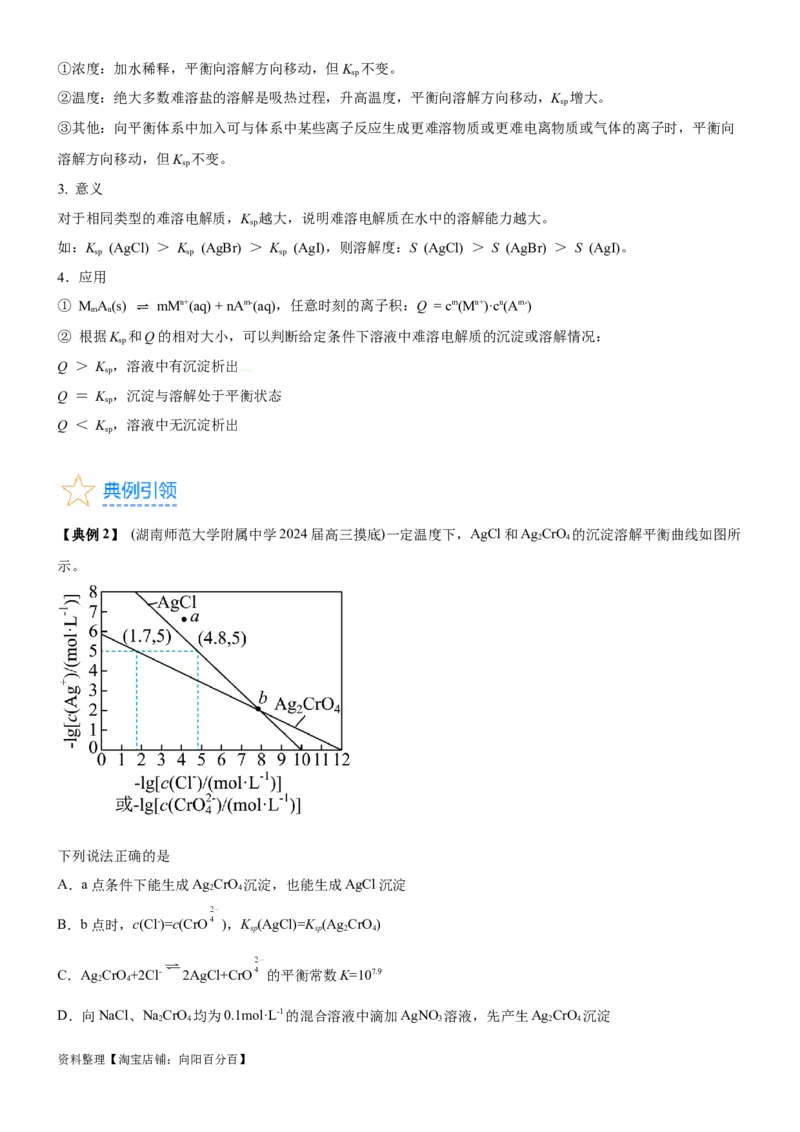
【典例2】 (湖南师范大学附属中学2024届高三摸底)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所
2 4
示。
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO ),K (AgCl)=K (Ag CrO)
sp sp 2 4
C.Ag CrO+2Cl- 2AgCl+CrO 的平衡常数K=107.9
2 4
D.向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
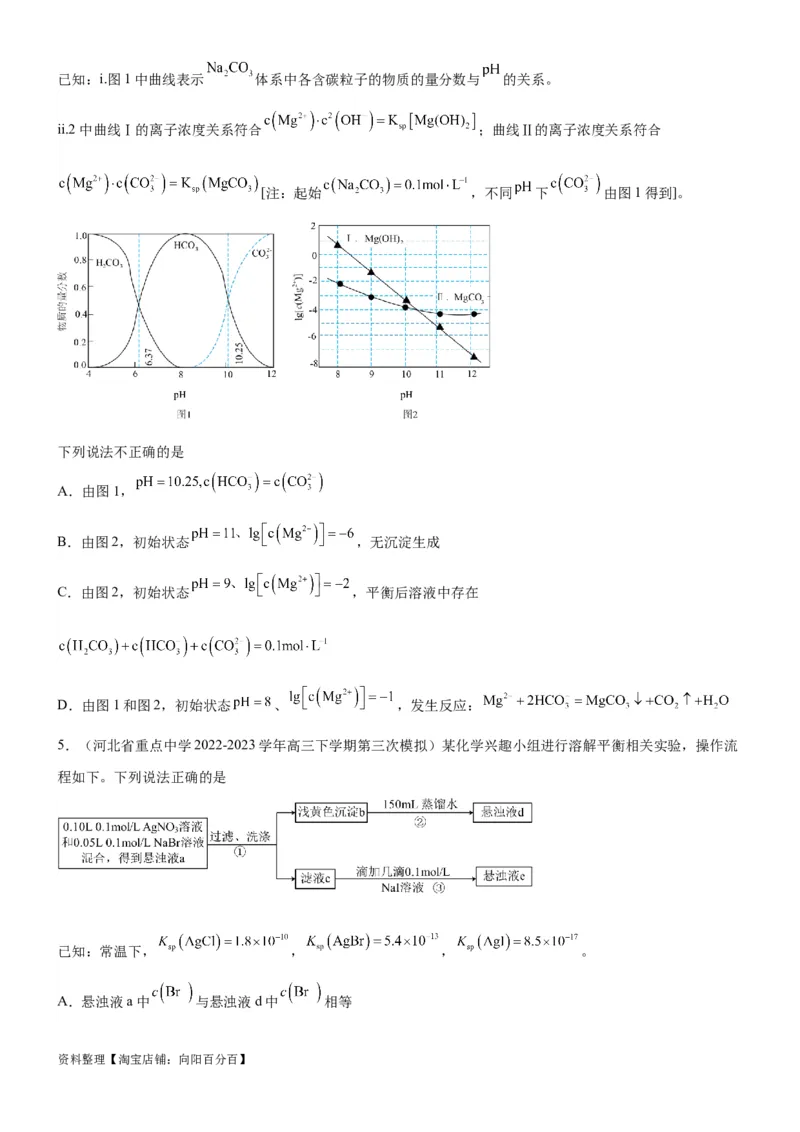
资料整理【淘宝店铺:向阳百分百】1.(江苏省淮阴中学2023届高三下学期最后一模)室温下,将 溶液与过量CaSO 固体混合,溶液pH
4
随时间变化如图所示。
已知: 。
下列说法不正确的是
A. 内上层清液中存在:
B.两者混合发生反应:
C.充分反应后上层清液中 约为
D.随着反应的进行, 逆向移动,溶液pH下降
考法 3 沉淀的溶解和生成
一、沉淀的生成
1.应用
在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。
杨sir化学,侵权必究
2.方法
(1)调节pH法
如:除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至7~8,离子方程式为
4 3
Fe3++3NH ·H O===Fe(OH) ↓+3NH。
3 2 3
(2)沉淀剂法
如:用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
资料整理【淘宝店铺:向阳百分百】二、沉淀的溶解
1.原理
根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去平衡体系中的相应离子,使平衡向沉淀
溶解的方向移动,就可以使沉淀溶解。
(1)酸溶解法
如:CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
(2)盐溶液溶解法
如:Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
(3)氧化还原溶解法
如:不溶于盐酸的硫化物CuS溶于稀HNO。3CuS + 8HNO === 3Cu(NO ) + 3S + 2NO↑+ 4H O
3 3 3 2 2
(4)配位溶解法
如:AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH)]++Cl-+2HO。
3 2 3 2 2
三、沉淀的转化
1. AgCl、AgI、Ag S的转化
2 杨sir化学,侵权必究
如:AgNO 溶液――→AgCl(白色沉淀)――→AgBr(浅黄色沉淀)――→AgI(黄色沉淀)――→Ag S(黑色沉淀)。
3 2
2. 实质、条件、规律
① 实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化)。
② 条件:两种沉淀的溶解度不同。
② 规律:溶解度小的沉淀转化为溶解度更小的沉淀容易实现,溶解度相差越大,转化越容易。
3. 沉淀转化的应用
(1)锅炉除水垢(含有CaSO)
4 杨sir化学,侵权必究
① 操作:先加NaCO 溶液,再加稀盐酸
2 3
② 原理:CaSO 4 (s) + Na 2 CO 3 ⇌ CaCO 3 (s) + Na 2 SO 4 CaCO 3 + 2HCl===CaCl 2 + H 2 O + CO 2 ↑
(2)自然界中矿物的转化
氧化、淋滤 渗透、遇闪锌矿(ZnS)和方铅矿(PbS)
原生铜的硫化物 CuSO 溶液 铜蓝(CuS)
4
CuSO 4 (aq) + ZnS (s) ⇌ CuS(s) + ZnSO 4 (aq);CuSO 4 (aq) + PbS(s) ⇌ CuS (s) + PbSO 4 (s)
(3)氟化物预防龋齿
① 牙齿表面的釉质层,只要成分是难溶的羟基磷灰石[Ca (PO )(OH)]。
5 4 3
② 口腔中的有机酸使釉质层溶解:Ca (PO )(OH) + 4H+ === 5Ca2+ + 3 + HO
5 4 3 HPO2- 2
4
③ 氟离子能与羟基磷灰石反应,生成溶解度更小的氟磷灰石,更能抵抗酸的腐蚀。
资料整理【淘宝店铺:向阳百分百】【典例3】 (浙江省重点中学拔尖学生培养联盟2023届高三适应性考试)某同学模拟工业废水变废为宝,设计了
用沉淀法回收各金属阳离子的实验方案:
模拟工业废水的离子浓度(mol/l)
0.10 0.010 0.0040 0.0010 0.141
已知:
①溶液中某离子浓度小于 ,可认为该离子不存在;
②实验过程中,假设溶液体积、温度不变;
③ ; ; ;
下列说法不正确的是
A.步骤I中加入的
B.步骤II得到的滤液N中 的浓度
C.步骤III得到的沉淀Z为
D.反应 的平衡常数
1.(浙江省宁波市镇海中学2023届高三模拟)从钒铬锰矿渣(主要成分为 、 、MnO)中提取铬的一
种工艺流程如图:
资料整理【淘宝店铺:向阳百分百】已知:Mn(II)在酸性环境中较稳定,在碱性环境中易被氧化;在酸性溶液中钒通常以 、 等存在;
沉铬[生成 ]过程中,当溶液 时,开始出现沉淀,此时铬离子浓度为 。下列说法不正确的
是
A.“沉钒”时, 胶体的作用是吸附
B.“沉铬”过程中,pH升高到约5.7时,沉铬几乎完全
C.“提纯”过程中 的作用是还原铬
D.“转化”过程中发生反应:
【基础过关】
1.(河北省衡水市第二中学2023届高三下学期三模)某污水处理厂用“ 沉淀法”处理含铬废水(主要含
以及少量 、 )的工艺流程如图所示:
已知:①金属离子 、 、 沉淀完全时( )pH分别为6.7、5.6、2.8。
② 。
下列说法错误的是
A.“氧化”时生成 的离子方程式为
B.“沉降”过程中加入NaOH溶液,调节溶液pH>6.7
C.加入 生成 ,说明
D.“沉铬”过程中,增大溶液的pH,沉铬率提高
2.(辽宁省鞍山市2023-2024学年高三上学期第一次质量监测)室温下,向NaCO 和NaHCO 的混合溶液中逐
2 3 3
资料整理【淘宝店铺:向阳百分百】滴加入BaCl 溶液,溶液中-1gc(Ba2+)与 的关系如图所示(已知: 、 ;
2
)。下列说法正确的是
A.a对应溶液pH=6.5
B.b对应溶液的c(HCO )=0.05mol/L
C.a→b的过程中,溶液中 一直增大
D.a对应的溶液中一定存在:
3.(浙江省杭州市强基联盟2023届高三下学期统测)牙齿表面有一薄层釉质保护着,釉质层主要成分是难溶
的羟基磷灰石,存在如下平衡: ,已知
的 。下列说法不正确的是
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用
B.正常口腔的pH接近中性,牙齿不易被腐蚀
C.使用添加 的含氟牙膏,可实现 与 的转化,该反应的平衡常数约为
D.口腔中的食物残渣能产生有机酸,容易导致龋齿,使 增大
4.(山西省晋城市第一中学校2023-2024学年高三第四次调研)利用平衡移动原理,分析一定温度下 在
不同 的 体系中的可能产物。
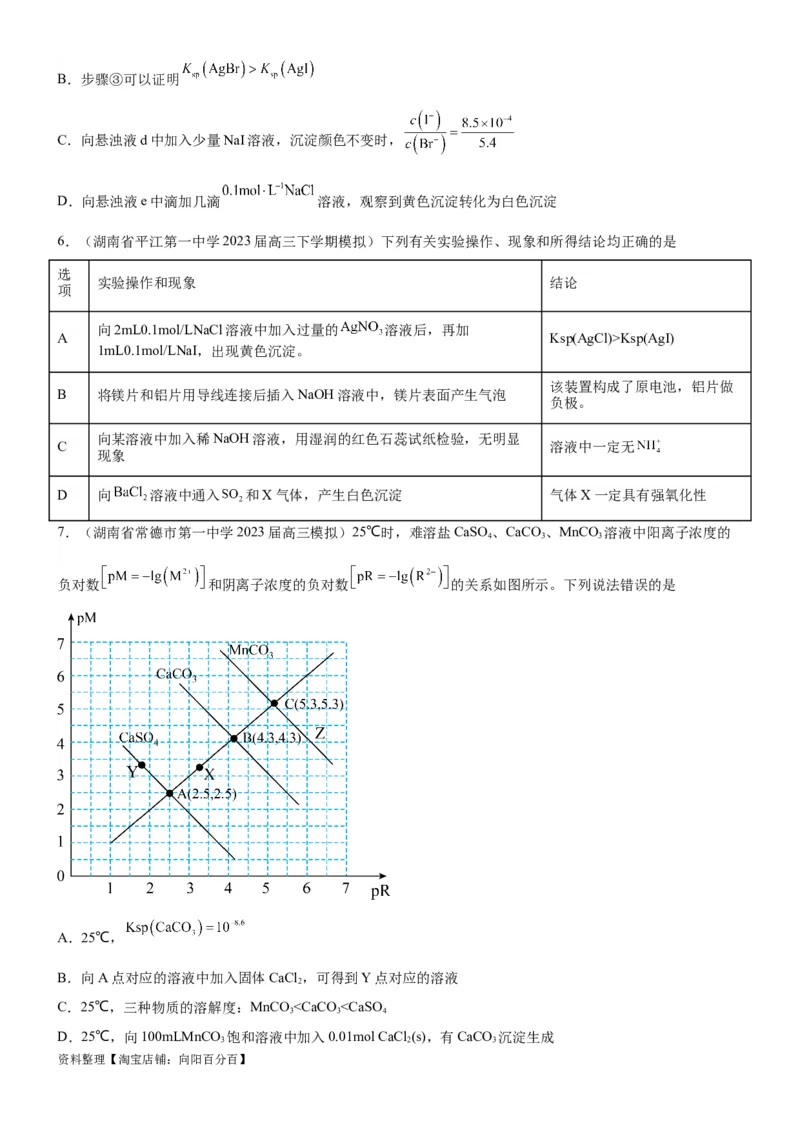
资料整理【淘宝店铺:向阳百分百】已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
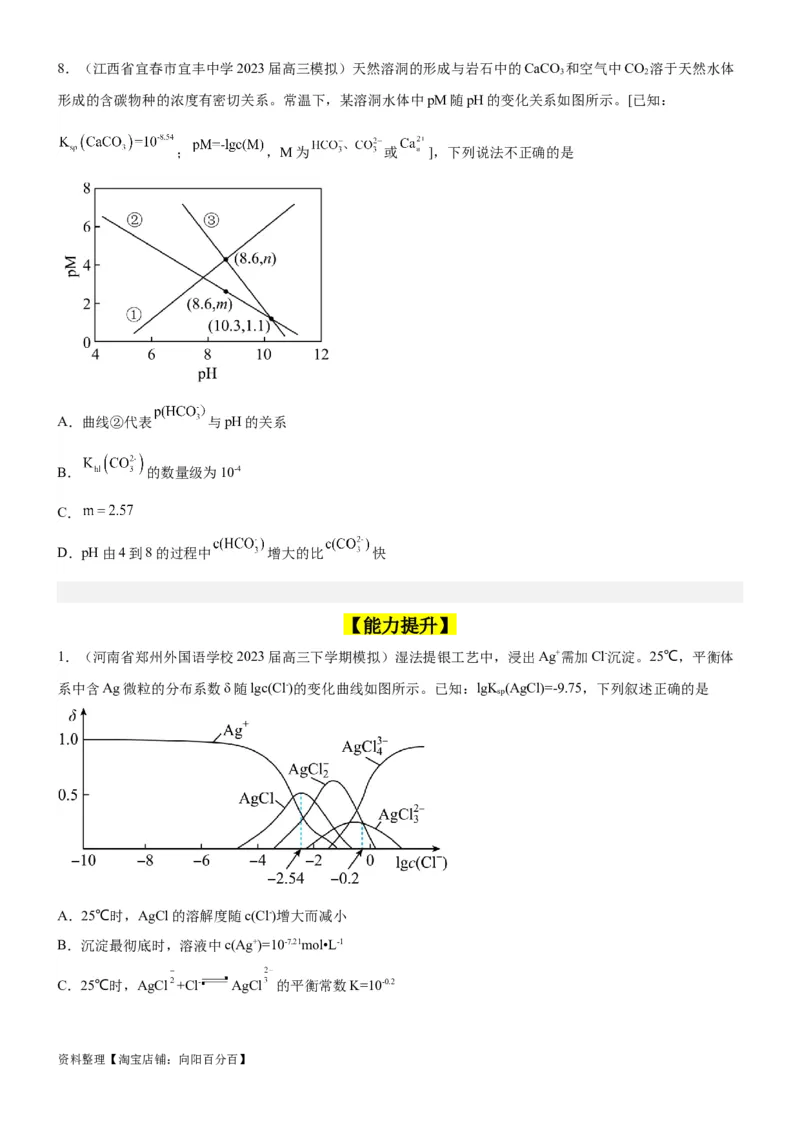
5.(河北省重点中学2022-2023学年高三下学期第三次模拟)某化学兴趣小组进行溶解平衡相关实验,操作流
程如下。下列说法正确的是
已知:常温下, , , 。
A.悬浊液a中 与悬浊液d中 相等
资料整理【淘宝店铺:向阳百分百】B.步骤③可以证明
C.向悬浊液d中加入少量NaI溶液,沉淀颜色不变时,
D.向悬浊液e中滴加几滴 溶液,观察到黄色沉淀转化为白色沉淀
6.(湖南省平江第一中学2023届高三下学期模拟)下列有关实验操作、现象和所得结论均正确的是
选
实验操作和现象 结论
项
向2mL0.1mol/LNaCl溶液中加入过量的 溶液后,再加
A Ksp(AgCl)>Ksp(AgI)
1mL0.1mol/LNaI,出现黄色沉淀。
该装置构成了原电池,铝片做
B 将镁片和铝片用导线连接后插入NaOH溶液中,镁片表面产生气泡
负极。
向某溶液中加入稀NaOH溶液,用湿润的红色石蕊试纸检验,无明显
C 溶液中一定无
现象
D 向 溶液中通入 和X气体,产生白色沉淀 气体X一定具有强氧化性
7.(湖南省常德市第一中学2023届高三模拟)25℃时,难溶盐CaSO、CaCO 、MnCO 溶液中阳离子浓度的
4 3 3
负对数 和阴离子浓度的负对数 的关系如图所示。下列说法错误的是
A.25℃,
B.向A点对应的溶液中加入固体CaCl ,可得到Y点对应的溶液
2
C.25℃,三种物质的溶解度:MnCO