文档内容
考点 50 物质的分离、提纯和检验
本考点考查以依据物质中各成分的特征性质,用不同的试剂,运用不同的方法分离混合物或提纯物质
等,或根据不同的实验现象来检测物质中某成分的存在,题型一直延续选择题与非选择题并存的形式,难
度适中。
预测2023年高考对考点的频率会有所增加,试题将以自然界中的矿石材料或工业生产的废渣为命题背
景,设计物质的分离或提纯路线,关注物质检验、分离和提纯在化学工业生产中的应用,不断强化环保意
识和“变废为宝”意识,实现科学探究、科学态度与社会责任的学科核心素养的提升。
一、物质的分离、提纯
二、物质的检验
物质的分离、提纯
1.物质分离、提纯的区别
(1)物质的分离
将混合物的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯
将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂。
2.依据物理性质选择分离、提纯的方法
(1)“固+固”混合物的分离(提纯)
(2)“固+液”混合物的分离(提纯)(3)“液+液”混合物的分离(提纯)
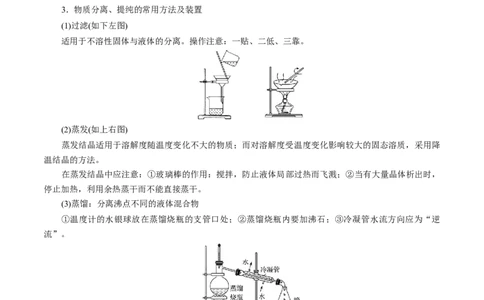
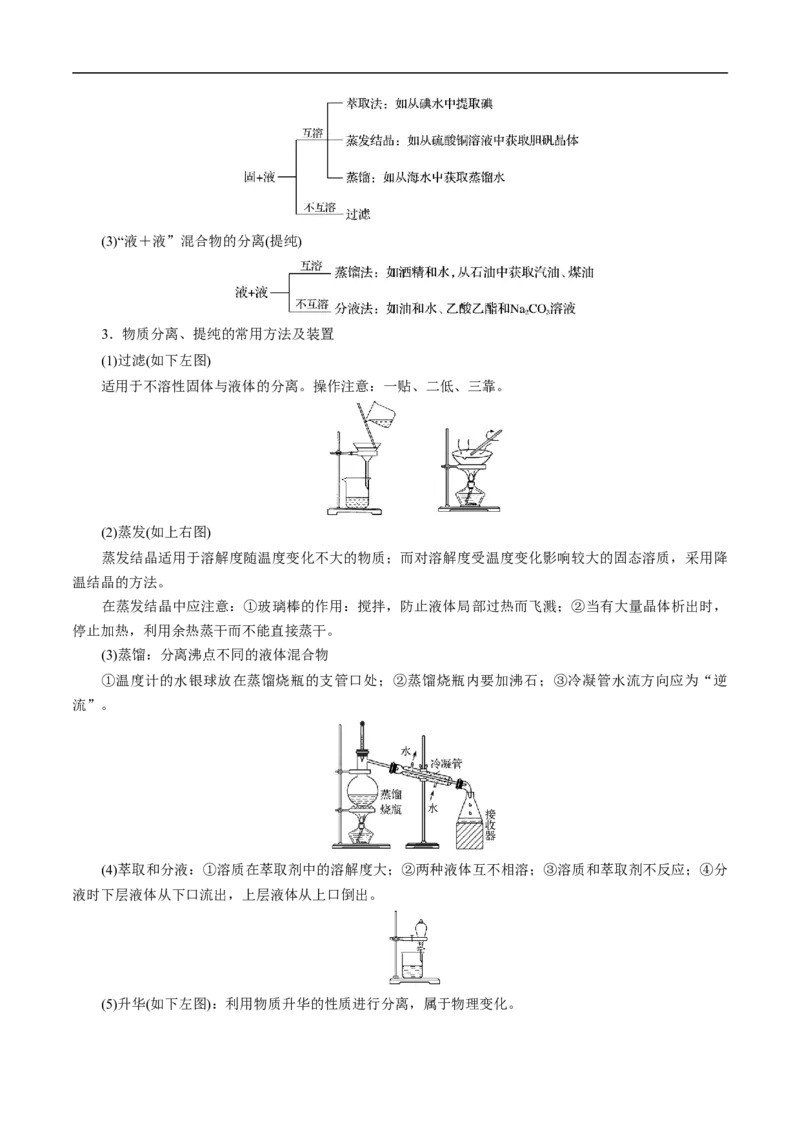
3.物质分离、提纯的常用方法及装置
(1)过滤(如下左图)
适用于不溶性固体与液体的分离。操作注意:一贴、二低、三靠。
(2)蒸发(如上右图)
蒸发结晶适用于溶解度随温度变化不大的物质;而对溶解度受温度变化影响较大的固态溶质,采用降
温结晶的方法。
在蒸发结晶中应注意:①玻璃棒的作用:搅拌,防止液体局部过热而飞溅;②当有大量晶体析出时,
停止加热,利用余热蒸干而不能直接蒸干。
(3)蒸馏:分离沸点不同的液体混合物
①温度计的水银球放在蒸馏烧瓶的支管口处;②蒸馏烧瓶内要加沸石;③冷凝管水流方向应为“逆
流”。
(4)萃取和分液:①溶质在萃取剂中的溶解度大;②两种液体互不相溶;③溶质和萃取剂不反应;④分
液时下层液体从下口流出,上层液体从上口倒出。
(5)升华(如下左图):利用物质升华的性质进行分离,属于物理变化。(6)洗气(如上右图):除去气体中的杂质气体。说明:长管进气短管出气。
4.物质分离、提纯的常用化学方法
方法 原理 实例
当混合物中混有热稳定性差的物质时, 如NaCl中混有NH Cl,
4
加热法 可直接加热,使热稳定性差的物质受热 NaCO 中混有NaHCO 等均可
2 3 3
分解而分离出 直接加热除去杂质
在混合物中加入某种试剂,使其中一种
如加适量的BaCl 溶液可除去
2
沉淀法 以沉淀的形式分离出去的方法。使用该
NaCl中混有的NaSO
2 4
方法一定要注意不能引入新的杂质
如将过量的铁粉加入混有FeCl
3
氧化还原 如果混合物中混有氧化性杂质,可以加
的FeCl 溶液中,以除去FeCl
2 3
反应法 入适当的还原剂使其还原为被提纯物质
杂质
电解法 利用电解原理来分离提纯物质 如电解精炼铜
通过加入试剂来调节溶液的pH,使溶液
调节pH 如CuCl 溶液中含有FeCl 杂
2 3
中某组分沉淀而分离的方法,一般是加
法 质,可向溶液中加入CuO除去
入相应的难溶或微溶物来调节
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热( )
(2)分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出( )
(3)蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处( )
(4)过滤操作时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体( )
(5)根据食用油和汽油的密度不同,可选用分液的方法分离( )
(6)将Cl 与HCl混合气体通过饱和食盐水可得到纯净的Cl( )
2 2
(7)SO 中混有少量SO ,可以将混合气体通过浓硫酸除去( )
2 3
(8)通过灼热的CuO除去H 中的CO( )
2
(9)乙烯中混有的SO 可以通过溴水除去( )
2
(10)除去BaCO 固体中混有的BaSO:加过量盐酸后,过滤洗涤( )
3 4
(11)向MgCl 溶液中加入CaCO 粉末,充分搅拌后过滤可除去杂质FeCl ( )
2 3 3
(12)除去NaCl溶液中少量的NaS:加入AgCl后再过滤( )
2
(13)除去Cu粉中混有CuO的实验操作是加入稀硝酸溶解、过滤、洗涤、干燥( )
(14)提纯混有少量NaCl的KNO 的过程:加热溶解→降温结晶→过滤→洗涤→干燥( )
3(15)提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法(
)
【典例】
例1 (2021•浙江6月选考)下列图示表示灼烧操作的是( )
A. B. C. D.
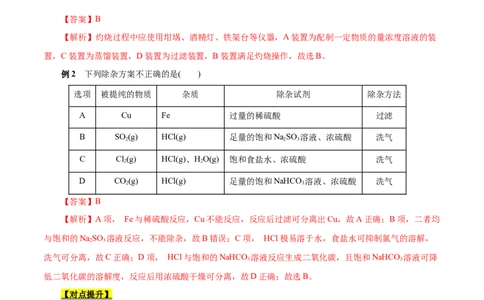
【答案】B
【解析】灼烧过程中应使用坩埚、酒精灯、铁架台等仪器,A装置为配制一定物质的量浓度溶液的装
置,C装置为蒸馏装置,D装置为过滤装置,B装置满足灼烧操作,故选B。
例2 下列除杂方案不正确的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A Cu Fe 过量的稀硫酸 过滤
B SO (g) HCl(g) 足量的饱和NaSO 溶液、浓硫酸 洗气
2 2 3
C Cl(g) HCl(g)、HO(g) 饱和食盐水、浓硫酸 洗气
2 2
D CO(g) HCl(g) 足量的饱和NaHCO 溶液、浓硫酸 洗气
2 3
【答案】B
【解析】A项, Fe与稀硫酸反应,Cu不能反应,反应后过滤可分离出Cu,故A正确;B项,二者均
与饱和的NaSO 溶液反应,不能除杂,故B错误;C项, HCl极易溶于水,食盐水可抑制氯气的溶解,
2 3
洗气可分离,故C正确;D项, HCl与饱和的NaHCO 溶液反应生成二氧化碳,且饱和NaHCO 溶液可降
3 3
低二氧化碳的溶解度,反应后用浓硫酸干燥可分离,故D正确;故选B。
【对点提升】
对点1 下列实验的试剂、装置选用不合理的是( )
选项 实验目的 选用试剂 选用装置
A 除去Cl 中少量的HCl、HO 试剂a为饱和氯化钠溶液 甲
2 2
B 除去NH 中少量的HO 试剂b为无水氯化钙 乙
3 2C 除去H 中少量的HCl、HO 试剂b为碱石灰 乙
2 2
D 除去N 中少量的O 足量铜网 丙
2 2
对点2 为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是( )
序号 物质 杂质 除杂质应选用的试剂或操作方法
① MgCl 溶液 AlCl 在MgCl 溶液中加过量NaOH溶液搅拌、过滤
2 3 2
② FeSO 溶液 CuSO 加入过量铁粉并过滤
4 4
③ CO SO 依次通过盛有NaOH溶液和浓硫酸的洗气瓶
2 2
④ NaNO CaCO 加稀盐酸溶解、过滤、蒸发、结晶
3 3
A.② B.①② C.②③ D.①②③④
【巧学妙记】
1.除杂“四原则”
(1)不增,不得引入新杂质;
(2)不减,尽量不减少被提纯和分离的物质;
(3)易分,应使被提纯或分离的物质与其他物质易分离;
(4)易复原,被提纯物质转化后要易被复原。
2.除杂操作“四注意”
(1)除杂试剂要过量;
(2)过量试剂需除去;
(3)选择的途径要最佳;
(4)除去多种杂质时要考虑加入试剂的先后顺序。
物质的检验
1.常见气体的检验
常见气体 检验方法
氢气 纯净的氢气在空气中燃烧呈淡蓝色火焰,点燃有爆鸣声,生成物只有水
氧气 可使带火星的木条复燃
黄绿色,能使湿润的碘化钾淀粉试纸变蓝(O 、NO 也能使湿润的碘化钾淀粉
氯气 3 2
试纸变蓝)
无色有刺激性气味的气体。在潮湿的空气中形成白雾,能使湿润的蓝色石蕊试
氯化氢 纸变红;用蘸有浓氨水的玻璃棒靠近时冒白烟;将气体通入AgNO 溶液时有
3
白色沉淀生成
无色有刺激性气味的气体。能使品红溶液褪色,加热后又显红色;能使酸性高
二氧化硫
锰酸钾溶液褪色
氨气 无色有刺激性气味的气体。能使湿润的红色石蕊试纸变蓝;用蘸有浓盐酸的玻璃棒靠近时能生成白烟
能使澄清的石灰水变浑浊;能使燃着的木条熄灭。(SO 气体也能使澄清的石灰
二氧化碳 2
水变浑浊,N 等气体也能使燃着的木条熄灭)
2
可燃烧,火焰呈淡蓝色,燃烧后只生成 CO 。能使灼热的CuO由黑色变成红
一氧化碳 2
色
甲烷 无色气体,可燃,在空气中燃烧产生淡蓝色火焰,生成水和CO。
2
2.常见离子的检验
离子 试剂 现象 注意
Cl-、Br-、I AgCl↓白、AgBr↓淡黄、
AgNO 溶液+HNO(稀) —
- 3 3 AgI↓黄
须先用HCl
SO 稀HCl酸化的BaCl 溶液 白色沉淀
2 酸化
沉淀法 白色沉淀→灰绿色→红褐
Fe2+ NaOH溶液 —
色沉淀
Fe3+ NaOH溶液 红褐色沉淀 —
不一定是
Al3+ NaOH溶液 白色沉淀→溶解
Al3+
浓NaOH溶液和湿润的 产生刺激性气体,使试纸
NH 要加热
红色石蕊试纸 变蓝
气体法 SO也有此
CO 稀盐酸+澄清石灰水 澄清石灰水变浑浊
现象
SO 稀HSO 和品红溶液 品红溶液褪色 —
2 4
I- 氯水(少量),CCl 下层为紫色 —
4
先是无变化,滴氯水后变
Fe2+ KSCN溶液,再滴氯水 —
血红色
①KSCN溶液 血红色 —
显色法 Fe3+
②苯酚溶液 紫色 —
K+要透过
Na+、K+ Pt丝+HCl 火焰为黄色、浅紫色 蓝色钴玻
璃
3.常见有机物的检验
常见试剂 现象 被检有机物
烯烃、炔烃等不饱和烃及其衍生物;苯的同系物;含有
酸性高锰酸钾溶液 褪色 羟基或醛基的有机物,如醇、醛、酚、甲酸、甲酸酯、
甲酸盐、葡萄糖、麦芽糖等
因反应而褪色 烯烃、炔烃等不饱和烃及其衍生物
比水重的有CCl 、CS 、氯仿、溴苯等;比水轻的有液
因萃取而褪色 4 2
溴水 态饱和烃、苯及其同系物、液态饱和酯等
因反应而生成白色
苯酚(过量浓溴水)
沉淀
含有醛基的有机物,如醛、甲酸、甲酸酯、甲酸盐、
银氨溶液 有银镜生成
葡萄糖、麦芽糖等含有醛基的有机物,如醛、甲酸、甲酸酯、甲酸盐、
红色沉淀
新制的Cu(OH) 葡萄糖、麦芽糖等
2
蓝色溶液 含羧基的有机物,如羧酸等
FeCl 溶液 发生显色反应 苯酚及其衍生物
3
钠 有气体生成 含有羟基或羧基的有机物,如醇、羧酸等
NaHCO
3
有气体生成 含有羧基的有机物,如羧酸等
或NaCO 溶液
2 3
碘水 变蓝 淀粉
浓硝酸 变黄 含有苯环的蛋白质
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)向某溶液中加入BaCl 溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液中一定存在
2
SO( )
(2)向某溶液中加入Ba(NO ) 溶液,产生不溶于稀HNO 的白色沉淀,则溶液中一定存在SO( )
3 2 3
(3)向某溶液中加入Ca(OH) 溶液,有白色沉淀生成,则溶液中一定存在CO( )
2
(4)加入CaCl 溶液,有白色沉淀生成,溶液中一定存在CO( )
2
(5)加入稀硫酸,产生使品红溶液退色的无色有刺激性气味的气体,则溶液中一定存在SO( )
(6)某溶液的焰色反应呈黄色,则溶液中一定有钠元素,不能确定是否有钾元素( )
(7)无色溶液加入CCl 无现象,滴加氯水后CCl 层呈紫红色,则溶液中一定存在I-( )
4 4
(8)加入AgNO 溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液中一定含有Cl-( )
3
(9)向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体,溶液中一定存在CO( )
(10)区别NaCl、NaSO 时常用到胶头滴管、试管( )
2 4
(11)验证Fe (SO ) 溶液中含Fe2+的方法是加入酸性KMnO 溶液,紫色退去( )
2 4 3 4
(12)向硫酸亚铁溶液中滴加硫氰化钾溶液,溶液变为红色,说明溶液已变质( )
(13)在未知液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知液中存在 SO或
2
SO( )
(14)用新制氢氧化铜悬浊液能够区别葡萄糖溶液和乙醛溶液( )
(15)为将氨基酸混合物分离开,可以通过调节混合溶液pH,从而析出晶体,进行分离( )
【典例】
例1 (2020•天津卷)检验下列物所选用的试剂正确的是( )
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水D 溶液中的NH + NaOH溶液,湿润的蓝色石蕊试纸
4
【答案】C
【解析】A项,淀粉溶液可以检验碘单质,不能检验碘元素,故A错误;B项,能使澄清石灰水变浑
浊的气体可以是二氧化硫或二氧化碳,应该用品红检验二氧化硫气体,故B错误;C项,铜离子遇到氨水
会先产生氢氧化铜蓝色沉淀,继续加氨水会生成四氨合铜离子,检验铜离子可以用氨水,故C正确;D项,
铵根离子遇氢氧化钠溶液(加热)生成氨气,氨气能使湿润的红色石蕊试纸变蓝,不能使用湿润的蓝色石蕊
试纸检验氨气,故D错误;故选C。
例2 (2020•新课标Ⅱ卷)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下
4 3
实验:① 混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液中
加碱,产生白色沉淀。根据实验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO C.KCl、CaCO D.MgSO 、NaCl
4 3 4
【答案】B
【解析】①混合物溶于水,得到澄清透明溶液,则不含CaCO ,排除C选项;②做焰色反应,通过钴
3
玻璃可观察到紫色,可确定含有钾元素,即含有KCl;③向溶液中加碱,产生白色沉淀,则应含有
MgSO ,综合以上分析,混合物由KCl和MgSO 两种物质组成,故选B。
4 4
【对点提升】
对点1 检验下列溶液是否变质,所选试剂或试纸肯定合理的是( )
选项 A B C D
溶液 NaSO 溶液 FeSO 溶液 KI溶液 NaOH溶液
2 3 4
所选试剂或试纸 BaCl 溶液 KSCN溶液 AgNO 溶液 广泛pH试纸
2 3
对点2 下列关于物质或离子检验的叙述正确的是( )
A.向溶液中滴加两滴KSCN溶液,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.将气体通过无水硫酸铜,白色粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.将某气体通入澄清石灰水,溶液变浑浊,证明原气体是CO
2
【巧学妙记】
检验物质的常用方法
检验方法 适用范围 典型物质或离子
观察法 颜色、状态存在差异 Cl 为黄绿色,NO 为红棕色
2 2
物理
嗅试法 气味存在差异 SO 、HCl、NH 等有刺激性气味
2 3
方法
水溶法 溶解性存在差异 如NaCO 与CaCO
2 3 3焰色法 常用于鉴别碱金属 如含钾、钠等元素的单质、化合物
丁达尔效应 鉴别胶体与非胶体 Fe(OH) 胶体与Fe(SCN) 溶液
3 3
沉淀法 待检离子可转化为沉淀
SO2- 、Cl-、CO2-
、Fe2+、Fe3+、Cu2+
4 3
化学
气体法 某些离子可转化为气体
CO2- 、HCO- 、SO2- 、HSO- 、NH+
3 3 3 3 4
方法
待检成分可转化为有特殊颜
显色法 Fe3+、淀粉、I、苯酚、KSCN
色的物质 2
1.在蒸馏操作中,仪器选择及安装都正确的是( )
2.为提纯下列物质(括号内为杂质),选用的试剂或分离方法错误的是( )
选项 物质 试剂 分离方法
A 硝酸钾(氯化钠) 蒸馏水 降温结晶
B 二氧化碳(氯化氢) 饱和NaHCO 溶液 洗气
3
C 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
D 乙醇(水) 生石灰 蒸馏
3.超临界状态下的CO 流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如下。
2
下列说法中错误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.高温条件下更有利于超临界CO 流体萃取
2
C.升温、减压的目的是实现CO 与产品分离
2
D.超临界CO 流体萃取中药材具有无溶剂残留、绿色环保等优点
2
4.依据反应2NaIO +5SO+4H O=I +3H SO +2NaHSO ,利用下列装置从含NaIO 的废液中制取单质碘
3 2 2 2 2 4 4 3
的CCl 溶液并回收NaHSO。其中装置正确且能达到相应实验目的是( )
4 4A.①②③④ B.①②③ C.②③④ D.②④
5.下列说法正确的是( )
A.蒸发结晶操作时,当水分完全蒸干立即停止加热
B.滴定实验中,可以将待测液放到滴定管中,标准液置于锥形瓶中
C.测定NaClO溶液的pH,可用洁净的玻璃棒蘸取液体滴到pH试纸上,再与标准比色卡对照读数
D.用pH计测定同温度同浓度的NaCO 溶液和NaCN溶液的pH,通过比较pH大小比较HCO、
2 3 2 3
HCN的酸性强弱
6.下列实验操作能达到实验目的的是( )
实验目的 实验操作
A 检验粗盐溶液中的Cl- 取少量粗盐溶液,滴加AgNO 溶液,观察现象
3
将Pt丝蘸取盐酸灼烧至无色后,蘸取碳酸钠灼烧,观察现
B 检验碳酸钠
象
C 除去MnO 中的碳粉 反复灼烧至质量不再变化
2
D 检验CO、CO 混合气体 将气体依次通过CuO(灼热)、澄清石灰水
2
7.物质制备过程中离不开物质的提纯。以下除杂方法不正确的是( )
选项 目的 实验方法
A 除去NaCO 固体中的NaHCO 置于坩埚中加热至恒重
2 3 3
B 除去NaCl中少量KNO 将混合物制成热饱和溶液,冷却结晶,过滤
3
C 除去CO 中的 气体 通过饱和NaHCO 溶液,然后干燥
2 3
D 除去Cl 中的HCl气体 通过饱和食盐水,然后干燥
2
8.实验室由MnO 制取KMnO 和KOH的实验流程如下:
2 4下列说法错误的是( )
A.步骤①需要的仪器:玻璃棒、陶瓷坩埚、泥三角、酒精灯及带铁圈的铁架台
B.步骤②、③均涉及过滤操作
C.步骤④实验方案:在搅拌下加入适量石灰乳、静置、过滤、蒸发结晶及干燥
D.步骤②中KMnO 中Mn的实际利用率小于66.7%
2 4
9.实验室由MnO 制取KMnO 和KOH的实验流程如下:
2 4
下列说法错误的是( )
A.步骤①需要的仪器:玻璃棒、陶瓷坩埚、泥三角、酒精灯及带铁圈的铁架台
B.步骤②、③均涉及过滤操作
C.步骤④实验方案:在搅拌下加入适量石灰乳、静置、过滤、蒸发结晶及干燥
D.步骤②中KMnO 中Mn的实际利用率小于66.7%
2 4
10.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
选项 操作 现象 结论
A 滴加BaCl 溶液 生成白色沉淀 原溶液中有SO
2
B 滴加稀硫酸 有刺激性气味的气体产生 原溶液中有SO
用洁净铂丝蘸取溶
C 火焰呈紫色(透过蓝色钴玻璃) 原溶液中有K+
液进行焰色反应
滴加NaOH溶液,
D 将湿润的红色石蕊 试纸不变蓝 原溶液中无NH
试纸置于试管口
11.下列关于物质或离子检验的推断正确的是( )
A.向X溶液中滴加KSCN溶液,溶液显红色,证明X溶液中有Fe3+,无Fe2+
B.用硝酸酸化Y溶液,无现象,再加入硝酸钡溶液,产生白色沉淀,则Y溶液中含有SO
C.用玻璃棒蘸Z溶液在酒精灯上灼烧,火焰呈黄色,再透过蓝色钴玻璃观察火焰无紫色,则 Z溶液
中有Na+,无K+
D.用盐酸酸化W溶液,无现象,再向其中滴加AgNO 溶液,产生白色沉淀,则W溶液中含有Cl-
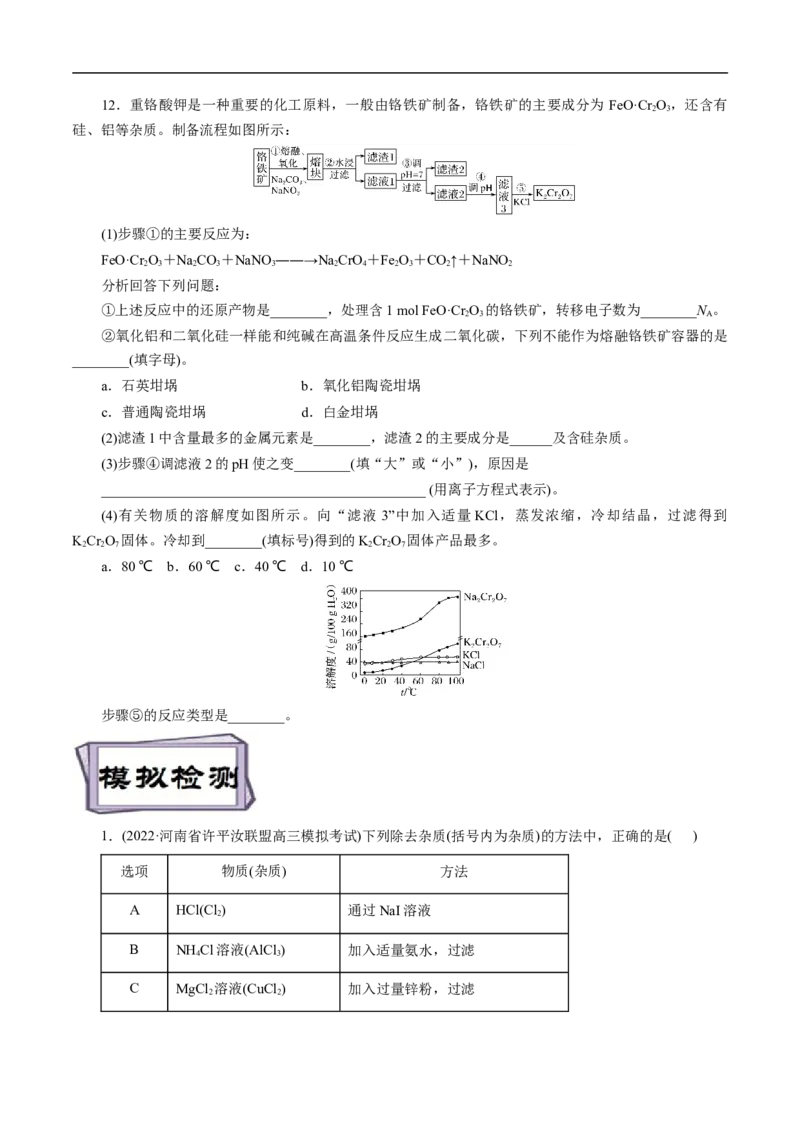
312.重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 FeO·Cr O ,还含有
2 3
硅、铝等杂质。制备流程如图所示:
(1)步骤①的主要反应为:
FeO·Cr O+NaCO+NaNO ――→NaCrO+Fe O+CO↑+NaNO
2 3 2 3 3 2 4 2 3 2 2
分析回答下列问题:
①上述反应中的还原产物是________,处理含1 mol FeO·Cr O 的铬铁矿,转移电子数为________N 。
2 3 A
②氧化铝和二氧化硅一样能和纯碱在高温条件反应生成二氧化碳,下列不能作为熔融铬铁矿容器的是
________(填字母)。
a.石英坩埚 b.氧化铝陶瓷坩埚
c.普通陶瓷坩埚 d.白金坩埚
(2)滤渣1中含量最多的金属元素是________,滤渣2的主要成分是______及含硅杂质。
(3)步骤④调滤液2的pH使之变________(填“大”或“小”),原因是
______________________________________________ (用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液 3”中加入适量 KCl,蒸发浓缩,冷却结晶,过滤得到
KCr O 固体。冷却到________(填标号)得到的KCr O 固体产品最多。
2 2 7 2 2 7
a.80 ℃ b.60 ℃ c.40 ℃ d.10 ℃
步骤⑤的反应类型是________。
1.(2022·河南省许平汝联盟高三模拟考试)下列除去杂质(括号内为杂质)的方法中,正确的是( )
选项 物质(杂质) 方法
A HCl(Cl ) 通过NaI溶液
2
B NH Cl溶液(AlCl ) 加入适量氨水,过滤
4 3
C MgCl 溶液(CuCl ) 加入过量锌粉,过滤
2 2D CO(SO ) 通过浓的碳酸钠溶液
2 2
2.(2022·上海市金山区二模)除去下列物质中的杂质,所选试剂与分离方法均能达到目的的是( )
物质(杂质) 除杂试剂 分离方法
A NaCl(aq)(I ) CCl 分液
2 4
B C HOH(CHCOOH) NaOH(aq) 蒸馏
2 5 3
C HCl(Cl ) 饱和食盐水 洗气
2
D CaSO(CaCO) 稀硫酸 过滤
4 3
3.(2022·山西省晋城市二模)为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法均正确的是(
)
选项 被提纯的物质(杂质) 除杂试剂 分离方法
A 乙酸乙酯(乙醇) 饱和NaCO 溶液 分液
2 3
B Mg(OH) [Al(OH) ] 氨水 过滤
2 3
C C H(C H) 酸性高锰酸钾溶液 洗气
2 6 2 4
D FeCl (Na CO) 水 重结晶
3 2 3
4.(2022·四川省泸州市高三第三次教学质量诊断考试)下列物质的除杂实验中,不能实现除杂目的的
是( )
选项 物质(杂质) 除杂实验
加入饱和NaCO 溶液充分振荡,分液、
A CHCOOC H(CHCOOH) 2 3
3 2 5 3 洗涤、干燥
B KNO(NaCl) 加AgNO 溶液,过滤,洗涤
3 3
C NaCO (NaHCO ) 加热分解
2 3 3
D C HOH(HO) 加CaO充分混合,蒸馏
2 5 2
5.(2022·河北省五个一名校联盟模拟考试)下列关于溶液中所含离子检验的说法正确的是( )
A.取少量某溶液于试管中,向其中先滴加稀硝酸,再滴加硝酸钡溶液,有白色沉淀生成,说明该溶
液中含有SO 2-
4
B.取少量某溶液于试管中,向其中加入少量新制氯水,再滴加KSCN溶液,若溶液变红,说明该溶
液中含有Fe3+
C.取少量某溶液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体,若红色石蕊试纸变蓝,说明该溶液中含有NH +
4
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有CO2-
3
6.(2022·河北省保定市高三调研考试)下列除杂的操作或方法中,不能达到实验目的的是( )
选项 主要成分(杂质) 操作或方法
A 甲烷(乙烯) 将混合气体通过盛有酸性高锰酸钾溶液的洗气瓶
B 碳酸氢钠溶液(碳酸钠) 向混合溶液中通入过量二氧化碳
C 乙酸乙酯(乙酸) 将混合液加入饱和氢氧化钠溶液中,振荡、静置、分液
D 二氧化碳(氯化氢) 将混合气体通过盛有饱和碳酸氢钠溶液的洗气瓶
7.(2022·广东省“六校联盟”高三第三次大联考)侯氏联合制碱法是我国化工专家侯德榜先生创立的,
其原理是:NH +H O+CO+NaCl=NaHCO ↓+NHCl和2NaHCO NaCO+H O+CO↑,实验室模拟制取
3 2 2 3 4 3 2 3 2 2
NaCO 时不需要的装置是( )
2 3
A. B. C. D.
8.(2022·江苏省如皋中学高三模拟)侯德榜将氨碱法制取碳酸钠和合成氨联合起来,将制碱技术发展
到新的水平。氨碱法的反应原理为NaCl+NH +CO +H O=NaHCO ↓+NHCl,过滤所得NaHCO 可用于制纯
3 2 2 3 4 3
碱。现对过滤所得滤液进行如下实验,所得结论正确的是( )
A.用铂丝蘸取少量滤液进行焰色反应,观察到火焰呈黄色,说明滤液中含有Na+
B.取少量滤液于试管中,加热试管,将湿润的红色石蕊试纸置于试管口,试纸未变蓝,说明滤液中
不含NH +
4
C.取少量滤液,向其中加入足量稀盐酸,再加入硝酸银溶液,观察到有白色沉淀生成,说明滤液中
含有Cl-
D.取少量滤液,向其中加入适量澄清石灰水,观察到有白色沉淀生成,说明滤液中含有CO2-
3
9.(2022·浙江省镇海中学高三选考模拟)下图是实验室中制取KMnO 的流程图,已知KMnO 显墨绿
4 2 4
色,下列说法中错误的是( )A.第①步在铁坩埚中进行,第⑥步中加热浓缩在蒸发皿中进行
B.第②步加入的MnO 作还原剂,第④步通CO 发生反应:3 MnO2-+2CO =2 MnO -+MnO↓+2CO 2-,
2 2 4 2 4 2 3
MnO 是氧化产物
2
C.第③步分批浸取可提高浸取率
D.第⑤步加热趁热过滤,说明KMnO 的溶解度随温度变化比较大
4
10.(2022·浙江省金华一中高三选考模拟)洋葱所含的微量元素硒( Se)是一种很强的抗氧化剂,能消除
34
体内的自由基,增强细胞的活力和代谢能力,具有防癌抗衰老的功效。工业上用精炼铜的阳极泥(硒主要以
CuSe存在,含有少量Ag、Au)为原料与浓硫酸混合焙烧,将产生的SO 、SeO 混合气体用水吸收即可得Se
2 2
固体,其工艺流程如图,下列有关说法错误的是( )
A.实验室中过滤用到的玻璃仪器为:玻璃棒、烧杯、普通漏斗
B.SeO 既有氧化性又有还原性,其还原性比SO 强
2 2
C.“焙烧”时的主要反应为:CuSe+4H SO (浓) CuSO +SeO ↑+3SO↑+4H O
2 4 4 2 2 2
D.生产过程中产生的尾气SeO 可以用NaOH溶液吸收
2
11.(2022·山东省普通高中名校高三大联考)绿原酸具有抗病毒、降血压、延缓衰老等保健作用。利用
乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进一步提取绿原酸的流程如图,下列说法不正确的是( )
A.从“提取液”获取“有机层”的操作为分液
B.绿原酸溶解度随温度升高而减小
C.减压蒸馏的目的是防止温度过高绿原酸变质
D.绿原酸粗产品可通过重结晶的方法提纯
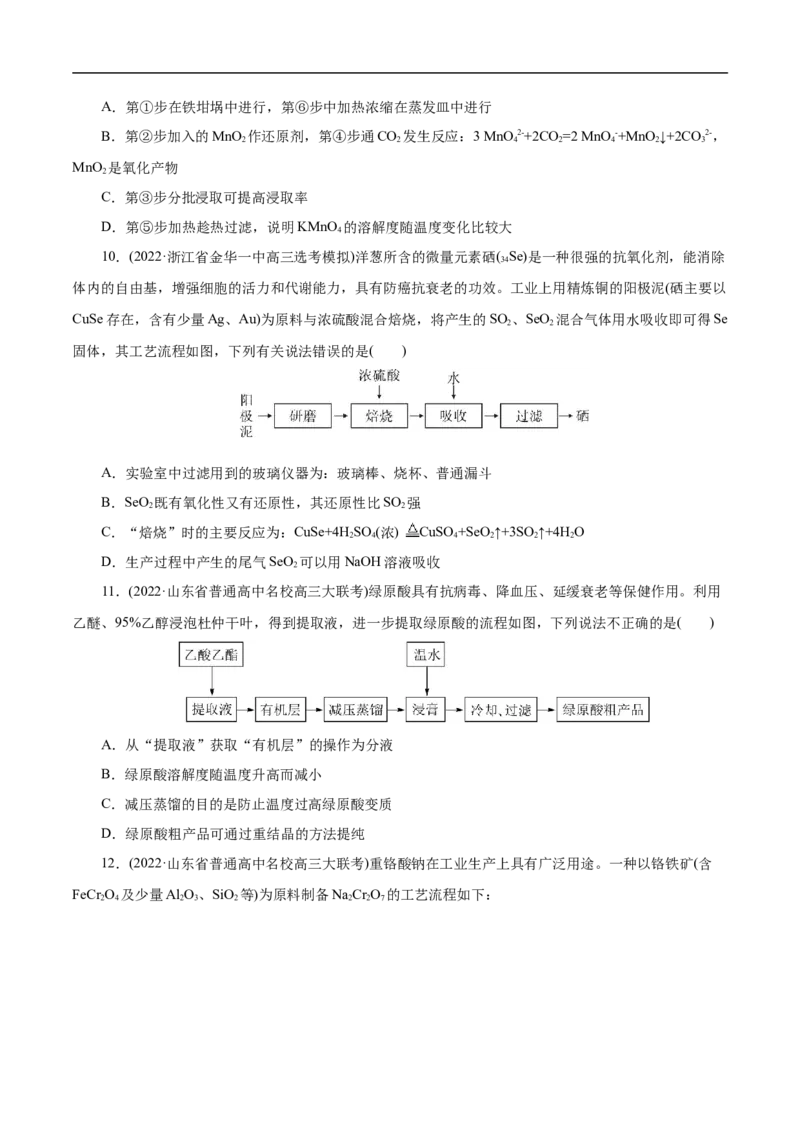
12.(2022·山东省普通高中名校高三大联考)重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含
FeCr O 及少量Al O、SiO 等)为原料制备NaCr O 的工艺流程如下:
2 4 2 3 2 2 2 7已知滤渣1为Fe O。下列说法错误的是( )
2 3
A.流程中可循环使用的物质有CO
2
B.滤渣2的成分是Al(OH) 和HSiO
3 2 3
C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行
D.“高温焙烧"发生的主要反应为4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO
2 4 2 2 3 2 3 2 4 2
13.(2022·江苏省高邮市高三学情调研)工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),
2 4
再经高温煅烧NiC O 制取Ni O 的流程如图所示。已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH
2 4 2 3 2 4 2 4
约为3.7。下列说法正确的是( )
A.酸溶时,可加入大量硫酸来提高“酸溶”效率
B.调pH时,加入NaCO 溶液,目的是使Fe3+转化为Fe (CO) 沉淀
2 3 2 3 3
C.沉镍时,发生反应的离子方程式为:Ni2++C O2-=NiC O↓
2 4 2 4
D.煅烧时,反应的化学方程式为:2NiC O Ni O+3CO↑+CO ↑
2 4 2 3 2
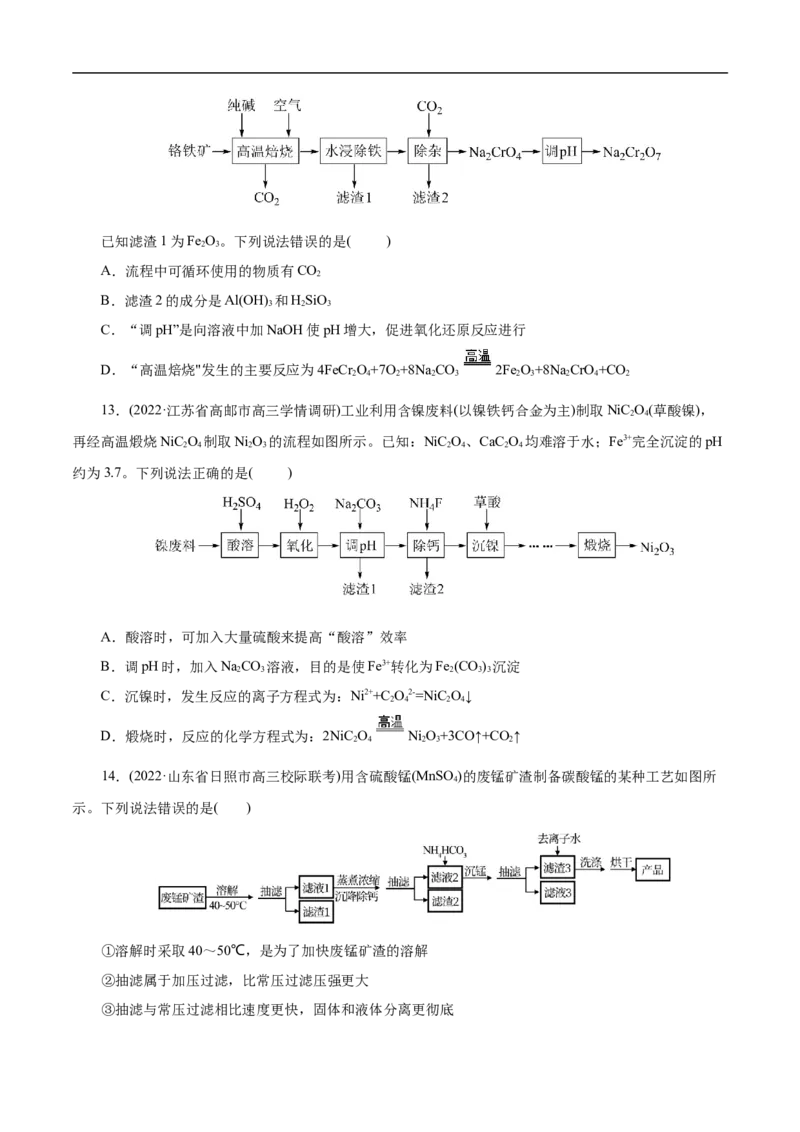
14.(2022·山东省日照市高三校际联考)用含硫酸锰(MnSO )的废锰矿渣制备碳酸锰的某种工艺如图所
4
示。下列说法错误的是( )
①溶解时采取40~50℃,是为了加快废锰矿渣的溶解
②抽滤属于加压过滤,比常压过滤压强更大
③抽滤与常压过滤相比速度更快,固体和液体分离更彻底④沉锰的离子方程式为:Mn2++2HCO-=MnCO↓+CO ↑+H O
3 3 2 2
⑤采用高温烘干,可得到纯净干燥的产品
A.②④ B.①③⑤ C.②⑤ D.②③⑤
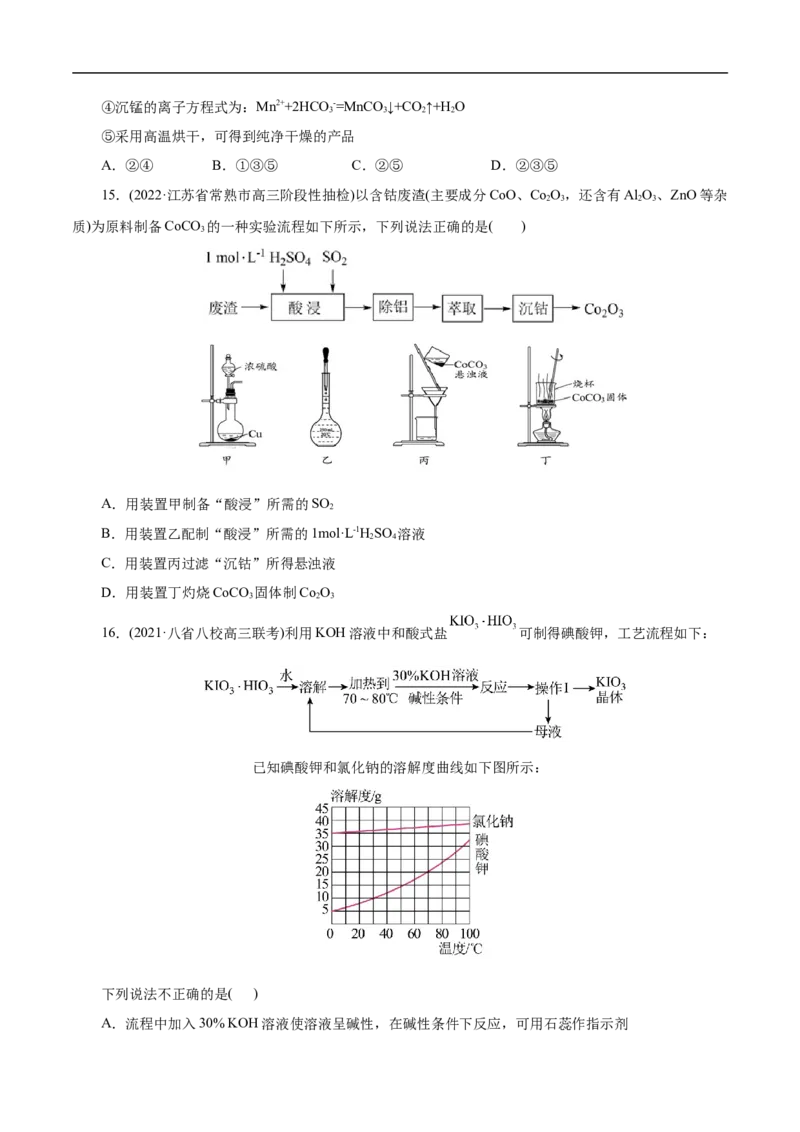
15.(2022·江苏省常熟市高三阶段性抽检)以含钴废渣(主要成分CoO、Co O,还含有Al O、ZnO等杂
2 3 2 3
质)为原料制备CoCO 的一种实验流程如下所示,下列说法正确的是( )
3
A.用装置甲制备“酸浸”所需的SO
2
B.用装置乙配制“酸浸”所需的1mol·L-1HSO 溶液
2 4
C.用装置丙过滤“沉钴”所得悬浊液
D.用装置丁灼烧CoCO 固体制Co O
3 2 3
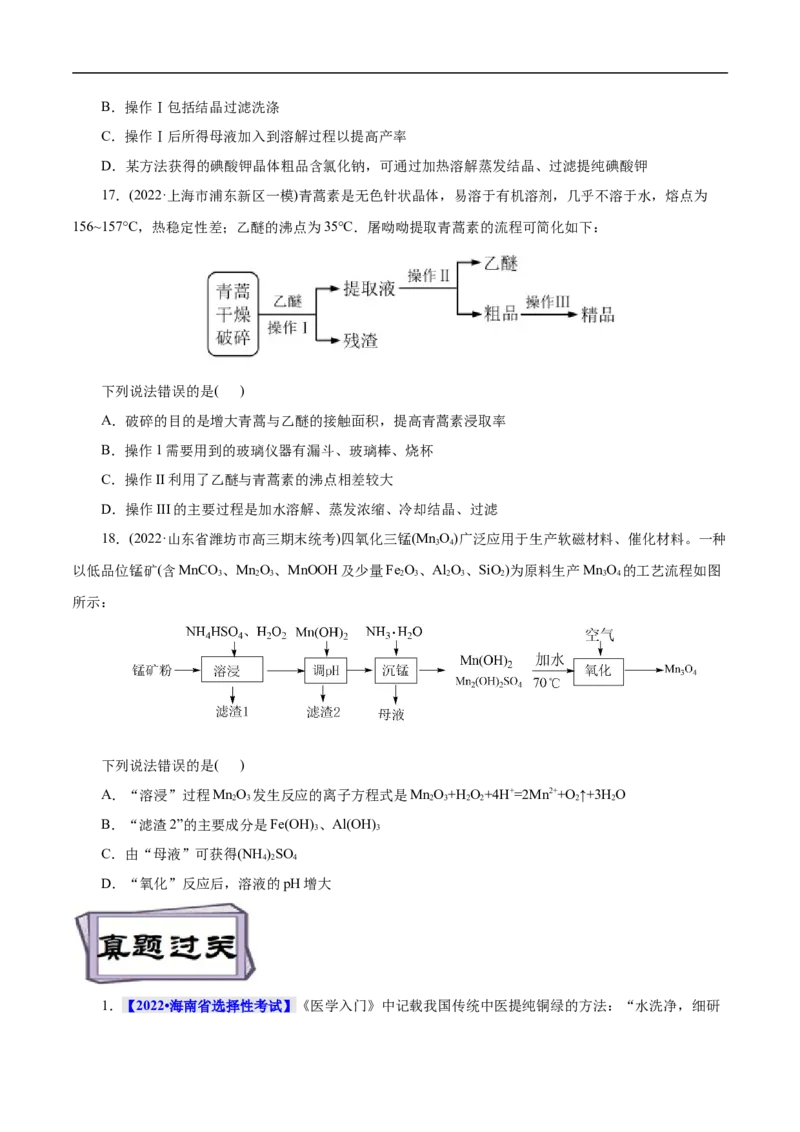
16.(2021·八省八校高三联考)利用KOH溶液中和酸式盐 可制得碘酸钾,工艺流程如下:
已知碘酸钾和氯化钠的溶解度曲线如下图所示:
下列说法不正确的是( )
A.流程中加入30% KOH溶液使溶液呈碱性,在碱性条件下反应,可用石蕊作指示剂B.操作Ⅰ包括结晶过滤洗涤
C.操作Ⅰ后所得母液加入到溶解过程以提高产率
D.某方法获得的碘酸钾晶体粗品含氯化钠,可通过加热溶解蒸发结晶、过滤提纯碘酸钾
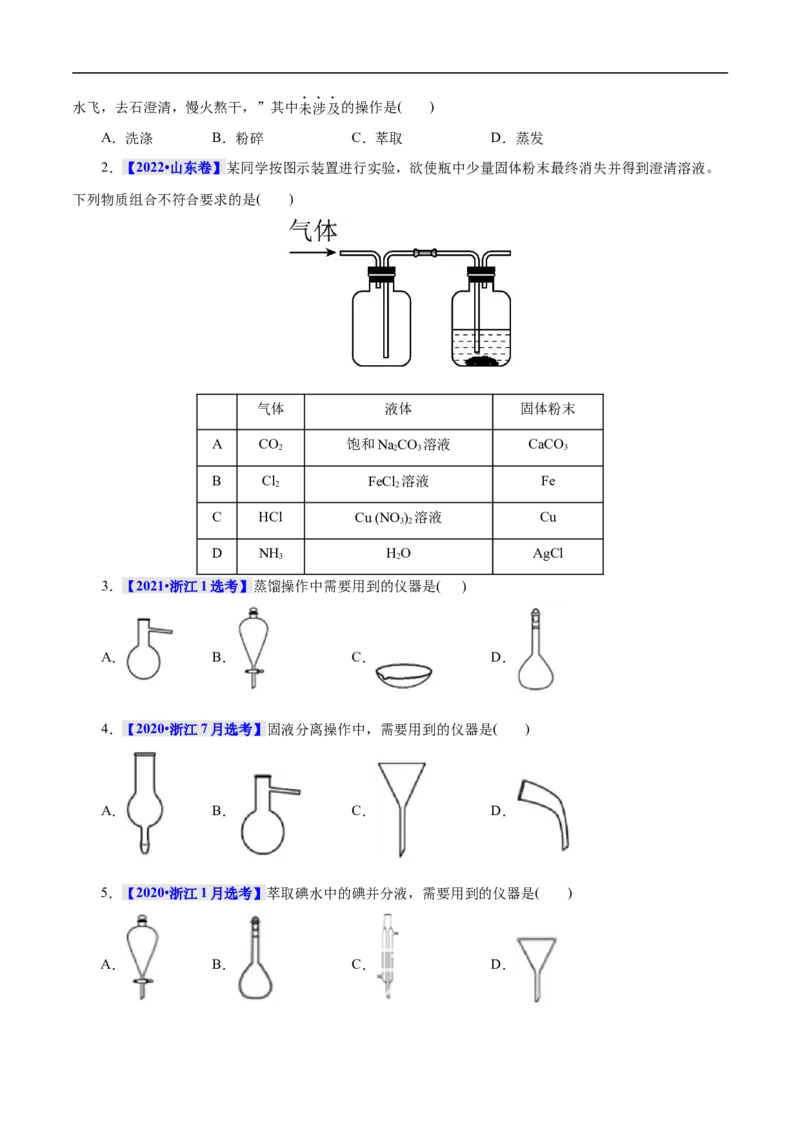
17.(2022·上海市浦东新区一模)青蒿素是无色针状晶体,易溶于有机溶剂,几乎不溶于水,熔点为
156~157°C,热稳定性差;乙醚的沸点为35°C.屠呦呦提取青蒿素的流程可简化如下:
下列说法错误的是( )
A.破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率
B.操作1需要用到的玻璃仪器有漏斗、玻璃棒、烧杯
C.操作II利用了乙醚与青蒿素的沸点相差较大
D.操作III的主要过程是加水溶解、蒸发浓缩、冷却结晶、过滤
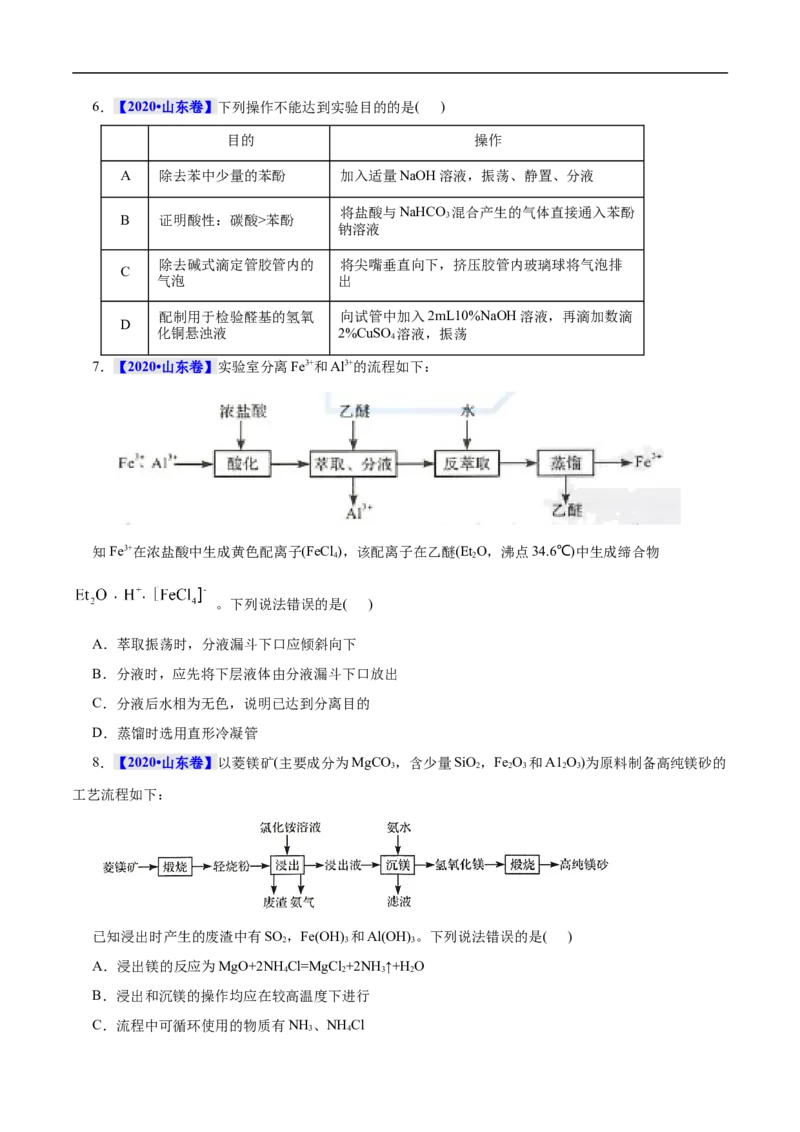
18.(2022·山东省潍坊市高三期末统考)四氧化三锰(Mn O)广泛应用于生产软磁材料、催化材料。一种
3 4
以低品位锰矿(含MnCO 、MnO、MnOOH及少量Fe O、Al O、SiO)为原料生产MnO 的工艺流程如图
3 2 3 2 3 2 3 2 3 4
所示:
下列说法错误的是( )
A.“溶浸”过程MnO 发生反应的离子方程式是MnO+H O+4H+=2Mn2++O ↑+3H O
2 3 2 3 2 2 2 2
B.“滤渣2”的主要成分是Fe(OH) 、Al(OH)
3 3
C.由“母液”可获得(NH )SO
4 2 4
D.“氧化”反应后,溶液的pH增大
1.【2022•海南省选择性考试】《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中未涉及的操作是( )
A.洗涤 B.粉碎 C.萃取 D.蒸发
2.【2022•山东卷】某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。
下列物质组合不符合要求的是( )
气体 液体 固体粉末
A CO 饱和NaCO 溶液 CaCO
2 2 3 3
B Cl FeCl 溶液 Fe
2 2
C HCl Cu (NO) 溶液 Cu
3 2
D NH HO AgCl
3 2
3.【2021•浙江1选考】蒸馏操作中需要用到的仪器是( )
A. B. C. D.
4.【2020•浙江7月选考】固液分离操作中,需要用到的仪器是( )
A. B. C. D.
5.【2020•浙江1月选考】萃取碘水中的碘并分液,需要用到的仪器是( )
A. B. C. D.6.【2020•山东卷】下列操作不能达到实验目的的是( )
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的气体直接通入苯酚
B 证明酸性:碳酸>苯酚 3
钠溶液
除去碱式滴定管胶管内的 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排
C
气泡 出
配制用于检验醛基的氢氧 向试管中加入2mL10%NaOH溶液,再滴加数滴
D
化铜悬浊液 2%CuSO 溶液,振荡
4
7.【2020•山东卷】实验室分离Fe3+和Al3+的流程如下:
知Fe3+在浓盐酸中生成黄色配离子(FeCl ),该配离子在乙醚(Et O,沸点34.6℃)中生成缔合物
4 2
。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
8.【2020•山东卷】以菱镁矿(主要成分为MgCO ,含少量SiO,Fe O 和A1 O)为原料制备高纯镁砂的
3 2 2 3 2 3
工艺流程如下:
已知浸出时产生的废渣中有SO ,Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl=MgCl +2NH↑+H O
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
9.【2019•浙江4月选考】下列图示表示过滤的是( )
A. B. C. D.
10.【2019 上海等级考】能证明亚硫酸钠中部分变质所需要的试剂是( )
A. 硝酸钡,稀硫酸 B. 稀盐酸,氯化钡
C. 稀硫酸,氯化钡 D. 稀硝酸,氯化钡
11.【2019•上海等级考】下列物质分离(括号内的物质为杂质)的方法错误的是( )
A. 硝基苯(苯)--蒸馏
B. 乙烯(SO )--氢氧化钠溶液
2
C. 己烷(己烯)--溴水,分液
D. 乙酸乙酯(乙醇)--碳酸钠溶液,分液
12.【2019•新课标Ⅲ卷】下列实验不能达到目的的是( )
选项 目的 实验
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸
13.【2019• 北京卷】下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
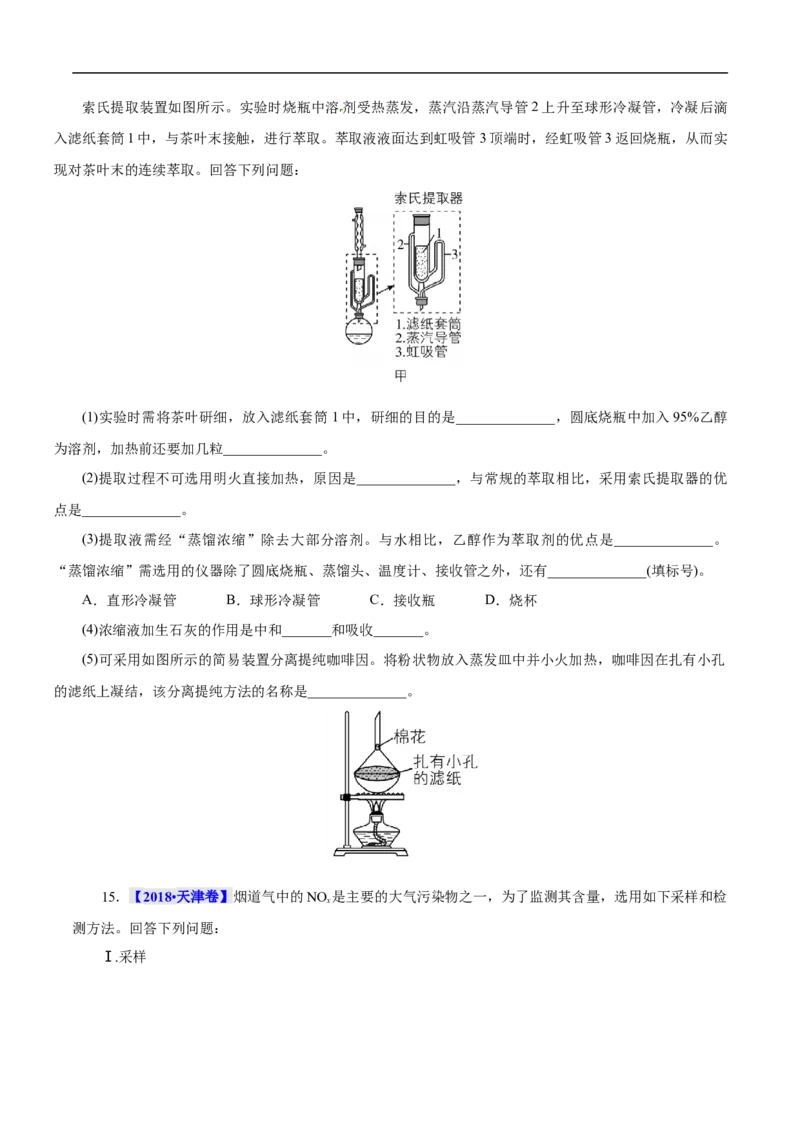
14.【2019•新课标Ⅱ卷】咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),
有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(K 约为10−6,易溶于水及乙醇)约
a
3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如下图所示。索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴
入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实
现对茶叶末的连续萃取。回答下列问题:
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________,圆底烧瓶中加入95%乙醇
为溶剂,加热前还要加几粒______________。
(2)提取过程不可选用明火直接加热,原因是______________,与常规的萃取相比,采用索氏提取器的优
点是______________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是______________。
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________(填标号)。
A.直形冷凝管 B.球形冷凝管 C.接收瓶 D.烧杯
(4)浓缩液加生石灰的作用是中和_______和吸收_______。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔
的滤纸上凝结,该分离提纯方法的名称是______________。
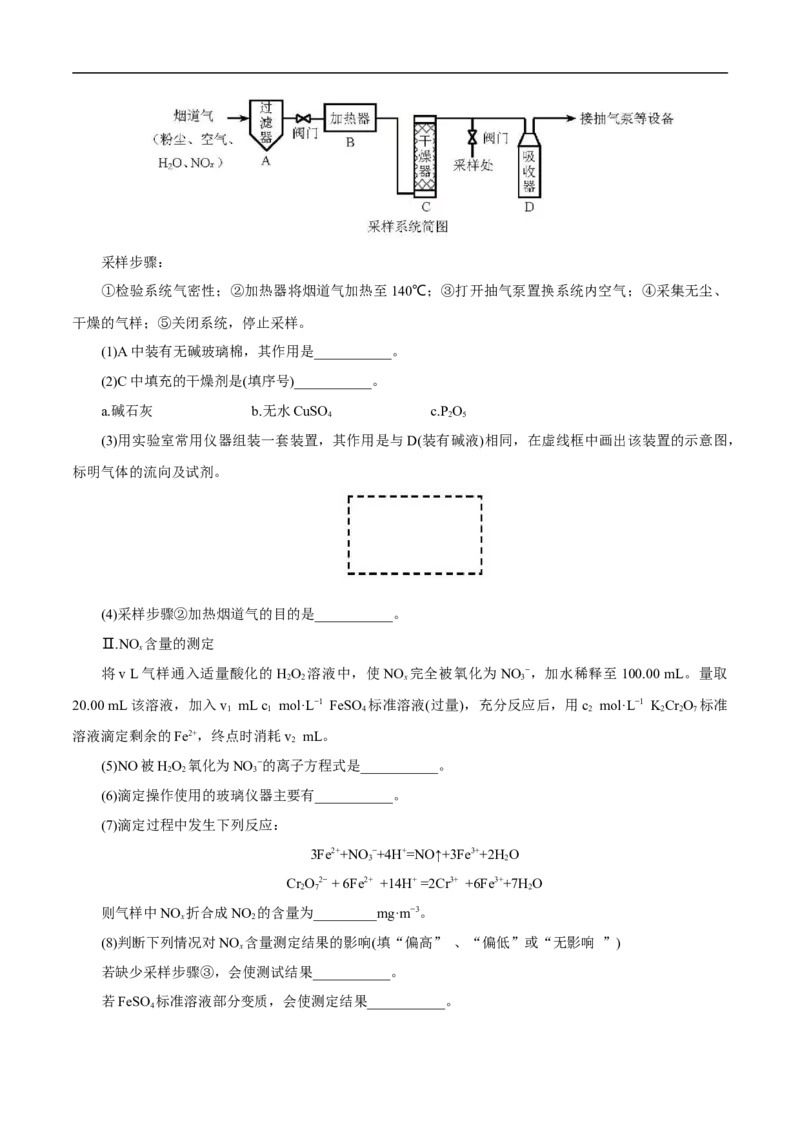
15.【2018•天津卷】烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下采样和检
x
测方法。回答下列问题:
Ⅰ.采样采样步骤:
①检验系统气密性;②加热器将烟道气加热至140℃;③打开抽气泵置换系统内空气;④采集无尘、
干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用是___________。
(2)C中填充的干燥剂是(填序号)___________。
a.碱石灰 b.无水CuSO c.P O
4 2 5
(3)用实验室常用仪器组装一套装置,其作用是与D(装有碱液)相同,在虚线框中画出该装置的示意图,
标明气体的流向及试剂。
(4)采样步骤②加热烟道气的目的是___________。
Ⅱ.NO 含量的测定
x
将v L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO −,加水稀释至100.00 mL。量取
2 2 x 3
20.00 mL该溶液,加入v mL c mol·L−1 FeSO 标准溶液(过量),充分反应后,用c mol·L−1 KCr O 标准
1 1 4 2 2 2 7
溶液滴定剩余的Fe2+,终点时消耗v mL。
2
(5)NO被HO 氧化为NO −的离子方程式是___________。
2 2 3
(6)滴定操作使用的玻璃仪器主要有___________。
(7)滴定过程中发生下列反应:
3Fe2++NO−+4H+=NO↑+3Fe3++2H O
3 2
Cr O2− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H O
2 7 2
则气样中NO 折合成NO 的含量为_________mg·m−3。
x 2
(8)判断下列情况对NO 含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)
x
若缺少采样步骤③,会使测试结果___________。
若FeSO 标准溶液部分变质,会使测定结果___________。
4