文档内容
解密 05 物质结构 元素周期律
一、单选题
1.(2022·湖北·沙市中学高三阶段练习)下列关于元素周期表和元素周期律的说法中,正
确的是
A.所含元素种类最多的族是ⅢB
B.元素周期表的p区共包含5列
C.第三周期元素的简单离子半径从左到右逐渐减小
D.卤素单质和它们的氢化物沸点从上到下均依次升高
2.(2022·上海·一模)短周期主族元素W、X、Y、Z在周期表中的位置如图所示。下列说
法不正确的是
W X
Y Z
A.W的最简单氢化物的稳定性比X的弱 B.X、Y形成的化合物水溶液显碱性
C.W与Y形成的化合物中一定含有离子键 D.原子半径:Z>Y>X>W
3.(2021·甘肃·民勤县第四中学高三期末)2016年IUPAC命名117号元素为Ts(中文名“
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素 B.Ts的同位素原子具有相同的质子数
C.Ts在同族元素中非金属性最弱 D.中子数为176的Ts核素符号是 Ts
4.(2022·黑龙江·鹤岗一中高三阶段练习)下列关于元素周期表与化学键的知识叙述错误
的是
A.在周期表中过渡元素可作为催化剂
B.化学键可以使离子结合,也可以使原子结合
C.常温常压下,相同体积的O 和O 具有相同的分子数
2 3
D.F、Cl、Br 、I 共价键逐渐增强,熔点依次升高
2 2 2 2
5.(2022·浙江·高三专题练习)下列关于晶体的说法正确的是
A.分子晶体中都存在共价键
B.金刚石、SiC、NaF、NaCl、HO、HS晶体的熔点依次降低
2 2
C.离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
D.SiO 晶体中每个硅原子与两个氧原子以共价键相结合
2
6.(2022·广东·高三阶段练习)下列性质的比较,不能用元素周期律解释的是
A.原子半径:S>Cl B.稳定性:HSeCl- D.酸性:HSO >H PO
2 4 3 4
7.(2022·湖南·宁乡一中高三期中)A、B、C、D、E、F、G是元素周期表中前四周期元
素且原子序数依次增大。其中A、B、D、F的最外层电子数均等于其电子层数,C在化合
物中无正价,E的价电子排布符合构造原理且其次外层电子数等于D的核外电子总数,G
的游离态在常温常压下是液体。关于以上元素的说法正确的是
A.E的最高价氧化物是一种碱性氧化物
B.C的简单离子半径大于D的简单离子半径
C.在C、F、G三种元素的简单氢化物中,C的简单氢化物热稳定性最好,酸性最强
D.F的最高价氧化物的水化物是一种强酸
8.(2022·全国·高三阶段练习)我国北斗导航卫星使用的是超薄铷 原子钟,该钟的精
度可以达到每3000万年误差1秒。铷是第五周期第ⅠA族元素,下列说法正确的是
A.单质铷不能与水反应 B.碱性:
C.金属性: D. 可溶于水
9.(2022·黑龙江·牡丹江市第二高级中学高三期中)下列事实不能作为实验判断依据的是
( )
A.钠和镁分别与冷水反应,判断金属活动性强弱
B.F 与Cl 分别与H 反应,判断氟与氯的非金属性强弱
2 2 2
C.酸性HCOHI>HBr>HCl
16.(2022·江西·南昌二中高三阶段练习)化学键是高中化学中非常重要的一个概念,它
与物质变化过程中的能量变化息息相关,下列说法正确的是:
①化学键是存在相邻原子(或离子)间强烈的相互作用
②活泼金属元素与活泼非金属元素一定形成离子键
③碳酸钠固体中既存在离子键又存在共价键
④速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
⑤物理变化也可以有化学键的破坏
⑥化学变化中一定有化学键的断裂和形成,所以一定伴随能量的变化
⑦吸热反应一定需要加热
⑧氢键是化学键中的一种,会影响物质的熔沸点
A.①③⑤⑥ B.③④⑤⑧ C.①②③⑤ D.③⑤⑥⑦
二、填空题
17.(2022·湖北·高三阶段练习)根据以下9种元素在元素周期表中的位置,回答下列问
题:
族
IA IIA IIIA IVA VA VIA VIIA
周期
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨
(1)①的原子轨道形状是_______;②③④的第一电离能由大到小的顺序是_______(填编号)。
(2)下列可以判断⑤和⑥金属性强弱的是_______(填序号)。
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化
学式_______,它的熔点高,硬度大,电绝缘性好,化学性质稳定。它的晶体类型是
_______,试推测其可能有哪些用途_______(填序号)。a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定
结构,试写出其结构式_______。
18.(2021·全国·高三专题练习)我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、
硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、
风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富
舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
___________;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化
学方程式为___________。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的
关系如图所示(已知:a为非金属元素)。
①由a、c、d三种元素形成的离子化合物的化学式为___________。
②图中所示元素中金属性最强的是___________(填元素符号),工业上得到该元素的单质的
原理为___________(填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________(用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________(填化学式)。
⑤ad 可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见
2 2
的碱性气体,发生反应的离子方程式为___________。
一、单选题
1.(2022·安徽·高三阶段练习)已知硒(Se)为第ⅥA族元素,下列有关硒元素的化合物的
说法中错误的是
A. 溶液能使酚酞溶液变红 B. 只有还原性
C. 与 相似,均难溶于水 D. 属于酸性氧化物
2.(2022·天津南开·高三期中)下列说法正确的是
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素B.原子最外层电子数为2的元素一定处于周期表第IIA族
C.同主族元素含氧酸的酸性随核电荷数的增加而减弱
D.同周期中金属性最强的元素是IA族的金属元素
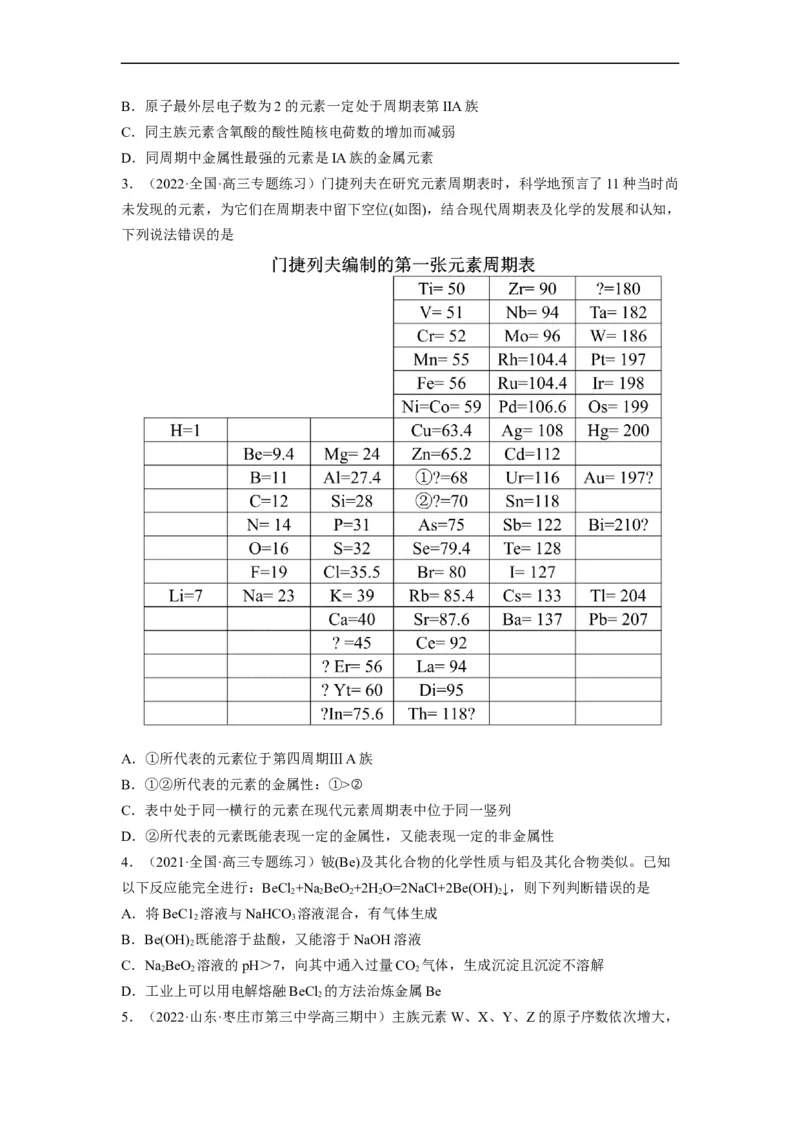
3.(2022·全国·高三专题练习)门捷列夫在研究元素周期表时,科学地预言了11种当时尚
未发现的元素,为它们在周期表中留下空位(如图),结合现代周期表及化学的发展和认知,
下列说法错误的是
A.①所代表的元素位于第四周期ⅢA族
B.①②所代表的元素的金属性:①>②
C.表中处于同一横行的元素在现代元素周期表中位于同一竖列
D.②所代表的元素既能表现一定的金属性,又能表现一定的非金属性
4.(2021·全国·高三专题练习)铍(Be)及其化合物的化学性质与铝及其化合物类似。已知
以下反应能完全进行:BeCl +Na BeO+2H O=2NaCl+2Be(OH) ↓,则下列判断错误的是
2 2 2 2 2
A.将BeC1 溶液与NaHCO 溶液混合,有气体生成
2 3
B.Be(OH) 既能溶于盐酸,又能溶于NaOH溶液
2
C.NaBeO 溶液的pH>7,向其中通入过量CO 气体,生成沉淀且沉淀不溶解
2 2 2
D.工业上可以用电解熔融BeCl 的方法治炼金属Be
2
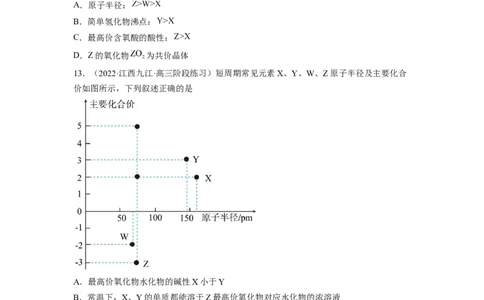
5.(2022·山东·枣庄市第三中学高三期中)主族元素W、X、Y、Z的原子序数依次增大,且均不大于20,W与Y原子的最外层电子数之和等于X原子的最外层电子数。这四种元
素形成的一种食品添加剂的结构如图所示。下列说法正确的是
A.原子半径:
B.X与Y形成的化合物可用作食品干燥剂
C.W与Z形成的化合物中既含有离子键又含有共价键
D.X形成的简单氢化物的沸点和热稳定性均是同族中最高的
6.(2022·北京市第十中学三模)“神州十三号”飞船所使用的砷化镓太阳能电池是我国
自主研发、自主生产的产品,拥有全部知识产权。砷(As)和镓(Ga)都位于第四周期,分别
位于第VA族和第IIIA族。下列说法不正确的是
A.原子半径
B.热稳定性
C.酸性:
D. 的化学性质可能与 相似
7.(2022·安徽安庆·高三阶段练习)如图转化关系中,A、B、C、D是二元化合物,A与
C均含有10个电子。甲、乙、丙是三种常见的非金属单质,下列说法不正确的是
A.化合物A与丙可直接生成D
B.单质乙有多种同素异形体,均具有高熔点、高沸点、硬度大的性质
C.稳定性:A<C
D.组成上述转化关系中的物质的元素种类共有三种
8.(2022·山东临沂·高三期中)1934年,约里奥·居里夫妇用α粒子(即 He)轰击某金属原
子 X得到 Y, Y具有放射性,很快衰变为 Q: He+ X→ Y+ n, Y→
Q+ e。基态Y原子的第一电离能大于同周期相邻元素的第一电离能。下列说法正确的是
A. X原子的中子数为13
B. Y可用作示踪原子研究化学反应历程
C.X、Y均可形成三氯化物D.自然界中不存在 Y 分子是因为其化学键不稳定
4
9.(2022·浙江省杭州学军中学高三阶段练习)根据物质的组成、结构等信息可以预测其
性质或用途。下列预测中,明显不合理的是
A.根据化合价预测,高铜酸钠( )与 可生成硫酸盐
B.根据组成预测,铝酸三钙( )溶于足量盐酸,生成白色沉淀
C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝
色
10.(2022·河南·高三阶段练习)正确掌握化学用语是学好化学的基础,下列化学用语正
确的是
A. +18O→ + 属于化学变化
B.质子数为18、中子数为22的元素符号表示式:22Ar
C.CC1 的球棍模型为
4
D.Mg和Cl形成离子键的过程
11.(2022·甘肃·兰州一中高三期中)下列化学用语使用正确的是
A.质子数为6、中子数为8的核素 C
B.HClO电子式:
C.15N、N 、N 互为同位素
D.MgCl 的形成过程:
2
12.(2022·黑龙江·绥化市第一中学高三期中)下列说法正确的是
①离子化合物一定含离子键,也可能含共价键;
②同位素的性质完全相同;
③含金属元素的化合物不一定是离子化合物;
④由非金属元素组成的化合物一定是共价化合物;
⑤由分子组成的物质中一定存在共价键。
A.①③⑤ B.②④⑤ C.②③④ D.①③
二、填空题
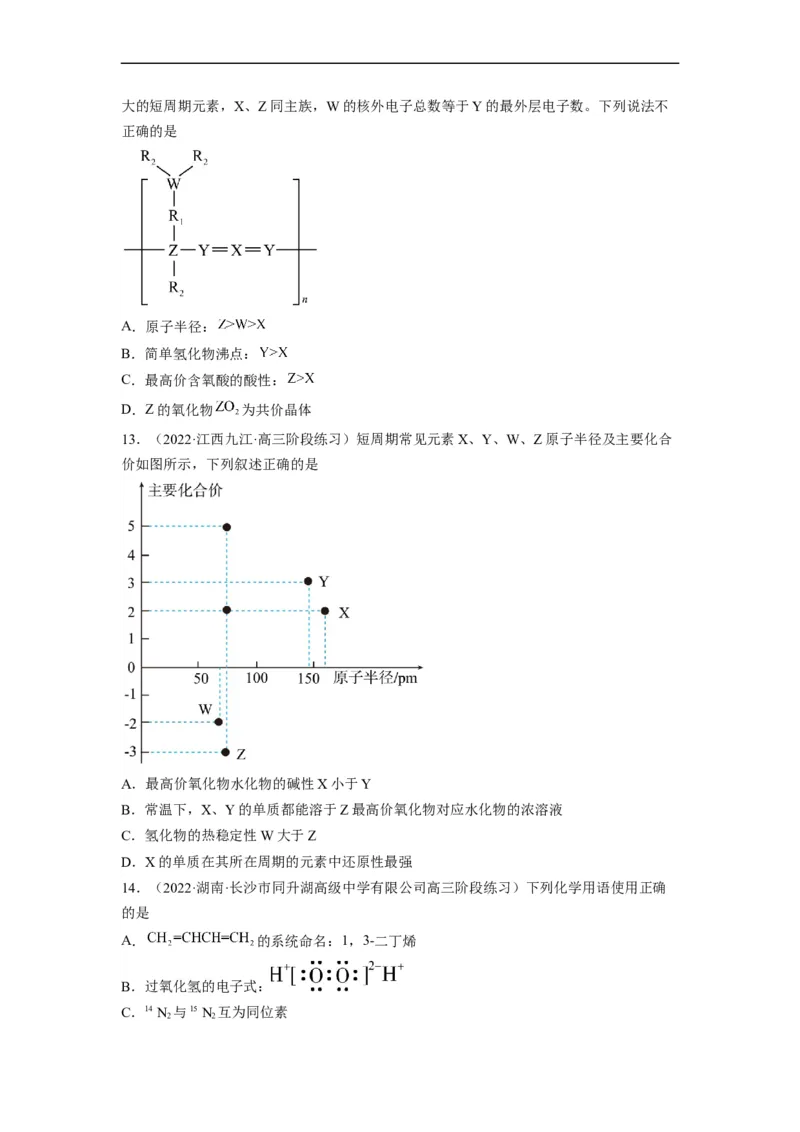
13.(2022·辽宁丹东·高三期中)如图是元素周期表的一部分。回答下列问题:(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①溴在元素周期表中的位置_______。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的是_______(填化学式)。
③类卤素IBr有很多类似于卤素单质的性质,已知IBr能与水发生非氧化还原反应,写出
IBr与水反应的化学方程式_______。IBr中含有的化学键是_______(填“离子键”、“极性
键”或“非极性键”)。
(2)硒能够增强人体免疫力,是人体必需的微量元素。
① 的离子结构示意图为_______。
② 溶于水生成 ,向所得溶液中通入 气体发生反应,生成Se和 。写
出 与 反应的化学方程式_______。
(3)下列说法正确的是_______(填字母)。
a.原子半径:
b.非金属性:
c.气态氢化物稳定性:
14.(2022·湖北·宜城市第一中学高三期中)元素的“价类二维图”体现了化学变化之美。
部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
回答下列问题:(1)写出物质R的电子式。_______。
(2)下列有关图中所示含N、S物质的叙述,正确的是_______(填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与 溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na SO),从氧化还原反应的角度分析,可选择B和D反应
2 2 5
(3)将 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式
是_______。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN ),能
3
用于处理废水中的重金属离子的硫代碳酸钠(Na CS)。根据所学化学知识分析, 晶体
2 3
中所含化学键的类型有_______, 水溶液显_______(填“酸性”、“碱性”或“中
性”)。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物
质R通入 的 溶液中,可制得该物质: ,上述反
应中,物质R体现的性质有_______,该反应每生成 转移电子_______ 。其中被氧
化的元素是_______(填元素符号)。
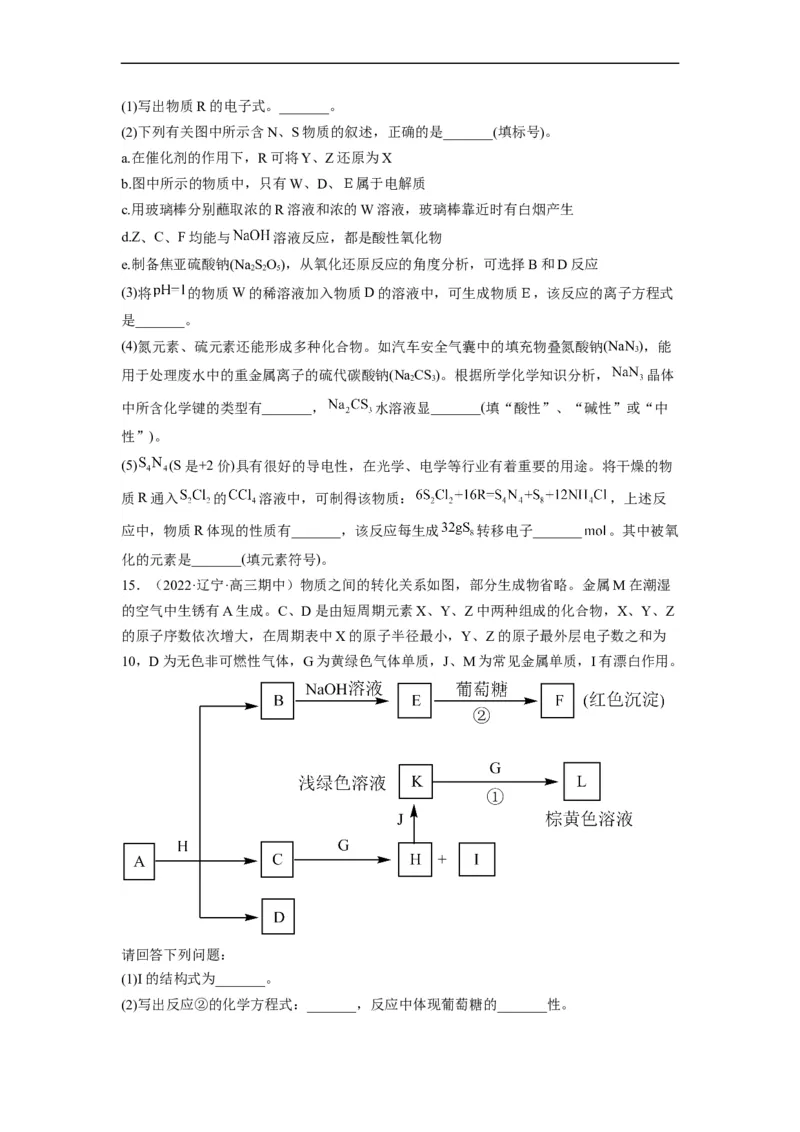
15.(2022·辽宁·高三期中)物质之间的转化关系如图,部分生成物省略。金属M在潮湿
的空气中生锈有A生成。C、D是由短周期元素X、Y、Z中两种组成的化合物,X、Y、Z
的原子序数依次增大,在周期表中X的原子半径最小,Y、Z的原子最外层电子数之和为
10,D为无色非可燃性气体,G为黄绿色气体单质,J、M为常见金属单质,I有漂白作用。
请回答下列问题:
(1)I的结构式为_______。
(2)写出反应②的化学方程式:_______,反应中体现葡萄糖的_______性。(3) 与 中沸点较高的是_______(填化学式)。
(4)写出A的化学式:_______。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体,请写出该反应的离子方程式:
_______。
(6)在含有K和L的混合溶液中,检验K中金属阳离子的方法为_______。
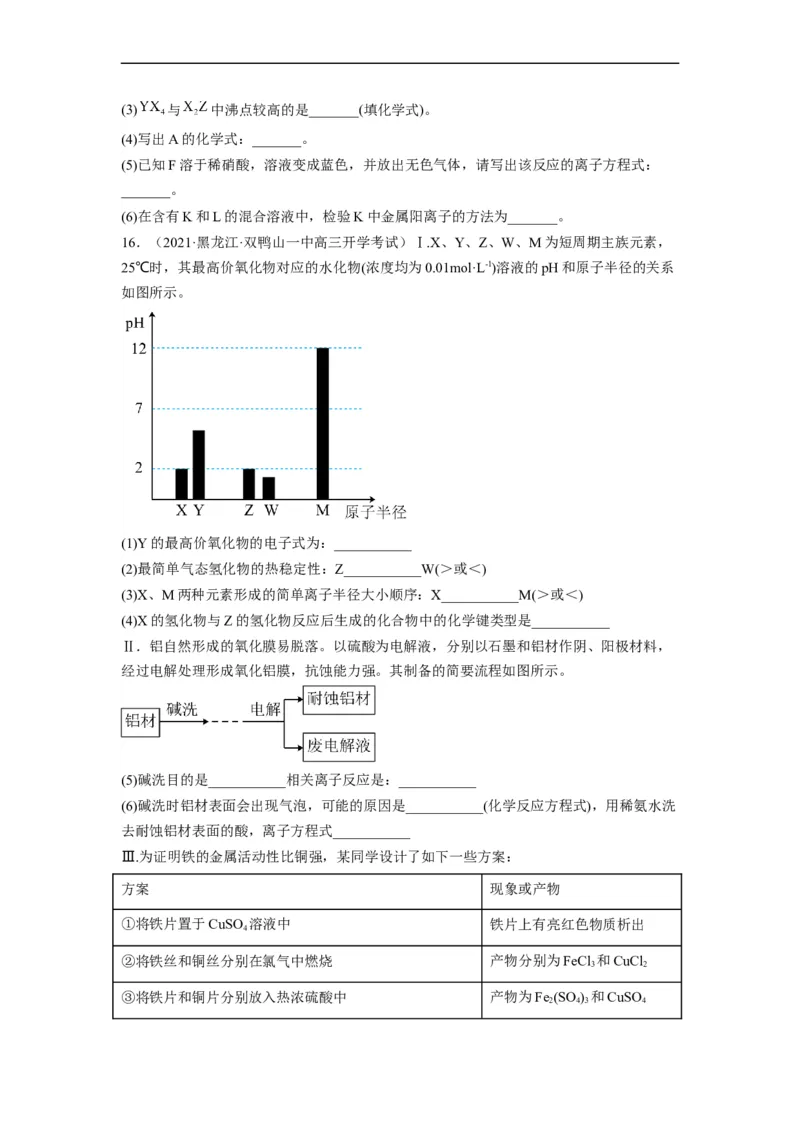
16.(2021·黑龙江·双鸭山一中高三开学考试)Ⅰ.X、Y、Z、W、M为短周期主族元素,
25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol·L-1)溶液的pH和原子半径的关系
如图所示。
(1)Y的最高价氧化物的电子式为:___________
(2)最简单气态氢化物的热稳定性:Z___________W(>或<)
(3)X、M两种元素形成的简单离子半径大小顺序:X___________M(>或<)
(4)X的氢化物与Z的氢化物反应后生成的化合物中的化学键类型是___________
Ⅱ.铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,
经过电解处理形成氧化铝膜,抗蚀能力强。其制备的简要流程如图所示。
(5)碱洗目的是___________相关离子反应是:___________
(6)碱洗时铝材表面会出现气泡,可能的原因是___________(化学反应方程式),用稀氨水洗
去耐蚀铝材表面的酸,离子方程式___________
Ⅲ.为证明铁的金属活动性比铜强,某同学设计了如下一些方案:
方案 现象或产物
①将铁片置于CuSO 溶液中 铁片上有亮红色物质析出
4
②将铁丝和铜丝分别在氯气中燃烧 产物分别为FeCl 和CuCl
3 2
③将铁片和铜片分别放入热浓硫酸中 产物为Fe (SO ) 和CuSO
2 4 3 4④将铜片置于FeCl 溶液中 铜片逐渐溶解
3
⑤将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连
铁片溶解,铜片上有气泡产生
接
(7)能根据现象或产物证明铁的金属活动性比铜强的方案有___________