文档内容
高考解密 05 物质结构与性质
A 组 基础练
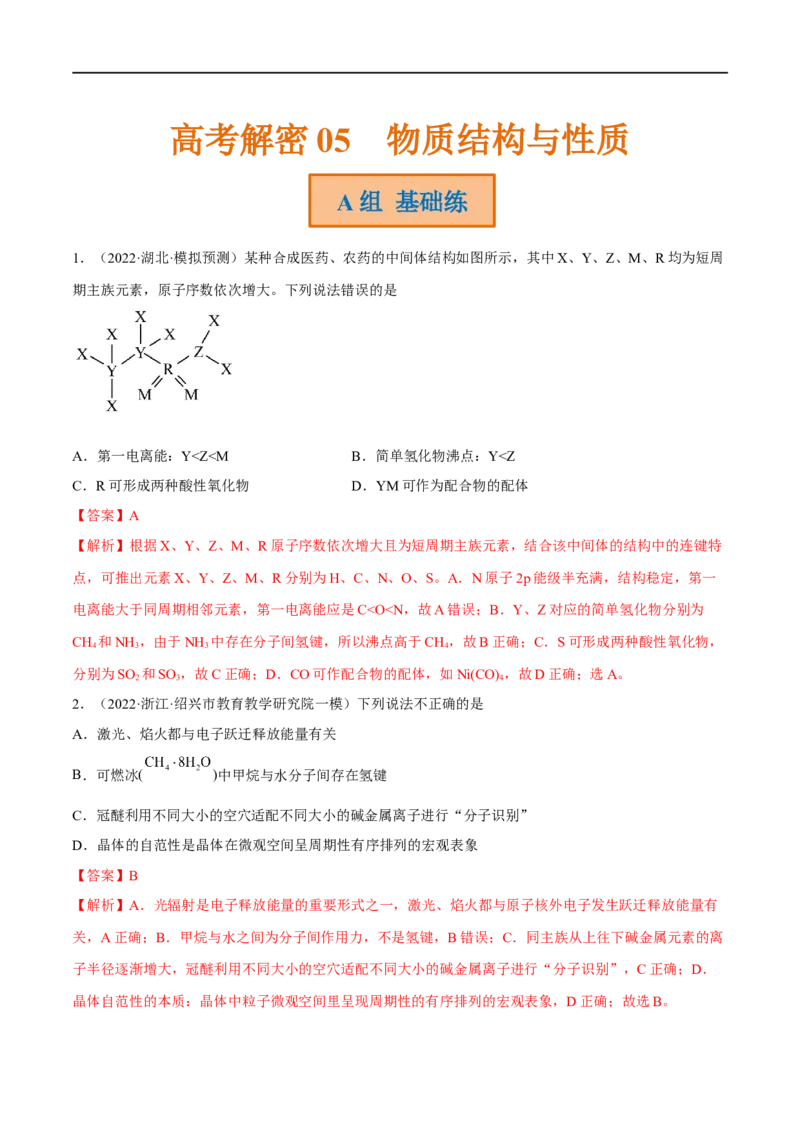
1.(2022·湖北·模拟预测)某种合成医药、农药的中间体结构如图所示,其中X、Y、Z、M、R均为短周
期主族元素,原子序数依次增大。下列说法错误的是
A.第一电离能:YGa,原子半径
Ga>As;同主族自上而下原子半径增大,As在P的下一周期,原子半径As>P,所以原子半径Ga> As>P,
A正确;B.同主族自上而下非金属性减弱,非金属性N>P> As,非金属性越强,氢化物越稳定,所以热
稳定性NH > PH > AsH ,B正确;C.同周期自左而右,非金属性增强,非金属性S>P,同主族自上而下
3 3 3
非金属性减弱,P> As,所以非金属性S>P>As,所以酸性HSO >H PO >H AsO ,C错误;D.镓(Ga)是第
2 4 3 4 3 4
四周期IIIA族元素,与Al同族,与Al具有相似性质,氢氧化铝是两性氢氧化物,Ga金属性虽然比Al强,
但可能具有两性,D正确;故选C。
6.(2022·湖北·模拟预测)科学家近期合成了一种配合物,该物质可以在温和条件下活化H,将N3-转化
2
为NH ,反应过程如图所示。下列说法错误的是A.产物中N原子的杂化轨道类型为sp3
B.NH -的VSEPR模型为四面体形
2
C.电负性大小:N>C>Fe
D.键角:NH >NH
3
【答案】D
【解析】A.产物N连接4根键,为 杂化,A正确;B. 与HO互为等电子体,价层电子对数为
2
4,VSEPR模型为四面体形,B正确;C.一般而言,金属元素的电负性小于1.8,非金属元素电负性大于
1.8,C、N属于同一周期,从左到右电负性逐渐增大,Fe为金属元素,电负性最小,即得N>C>Fe,C正
确;D. 与HO互为等电子体,均存在两对电子对,键角相同,键角:HON>O>C 中第二周期非金属元素为F、C、N、O,同周期主族元素随原子序数增大第
一电离能呈增大趋势,N原子 轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故第一电离能
为F>N>O>C
(4)4 或
【解析】(1) 是25号元素,基态 原子核外电子排布式为 ;原子中运动的电
子有两种相反的自旋状态,若一种自旋状态用 表示,则与之相反的用 表示,称为电子的自旋磁量子
数。对于基态 原子,电子排布式为 ,其核外电子自旋磁量子数的代数和为 或 ;
(2) 中,甲基与碳形成C-C单键,C与N形成三键,含有孤电子对的原子为N原子,其电子排布
式为 ,其能量最高的电子所在的能级符号为 ,配合物 中心原子Mn的配
位数是6;
(3)①根据 结构简式中S的价键可知,S形成6对共用电子对,没有孤电子对,S原子的杂化轨道
类型为sp3杂化;② 中既有单键也有双键,非金属元素之间形成共价键,故存在的作用力为 键、
键 ,不存在金属键、氢键,答案选BC;③ 中第二周期非金属元素为F、C、N、O,同周期主族
元素随原子序数增大第一电离能呈增大趋势,N原子 轨道为半充满稳定状态,第一电离能大于同周期相
邻元素,故第一电离能为F>N>O>C;
(4) 位于晶胞体心, 位于晶胞的棱,若以 为中心,则围在以 为中心的棱为中心的四个晶胞的
中心为距离 最近的 ,总共有4个;根据均摊法,晶胞中含有8 个N,12 个 ,1
个 ,已知阿伏加德罗常数的值为 ,若晶体的密度为 ,该晶胞的质量为 g,体积为 ,则边长为 或 cm。
B 组 提升练
1.(2022·浙江温州·模拟预测)氯化铬酰( )常温下为深红色液体,能与 、 等互溶,沸点
117℃,不存在立体异构,遇水反应并生成两种酸。下列说法不正确的是
A. 中Cr的化合价数与基态原子的价电子数相等
B. 结构为四面体而非平面形
C. 为离子晶体
D. 遇水可发生反应:
【答案】C
【解析】A. 中Cr的化合价数是+6,其基态原子的排布式是3d54s1,价电子数是6,A项正确;
B. 结构式为 ,中心铬原子上的孤电子数是0,价层电子数是4,为四面体而非平
面形,B项正确;C. 为分子晶体,C项错误;D. 遇水可发生反应生成铬酸和盐酸:
,D项正确;故答案选C。
2.(2022·北京·北大附中三模)在一定条件下,[Zn(CN) ]2-与甲醛发生如下反应:[Zn(CN) ]2-
4 4
+4HCHO+4H O=[Zn(OH) ]2-+4HOCH CN
2 4 2
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性ⅱ. Zn2++4CN- [Zn(CN) ]2- K;Zn2++4OH- [Zn(OH) ]2- K
4 1 4 2
下列说法不正确的是
A.反应前后Zn2+均提供4个空轨道容纳4对孤电子对
B.HOCH CN的氰基由CN-与甲醛发生反应而来
2
C.依据上述[Zn(CN) ]2-与甲醛的反应可以证明:KR 且R>R 或R-CH 且-CH->H则该烯烃为顺式,D项错误;故选B。
2 3 2
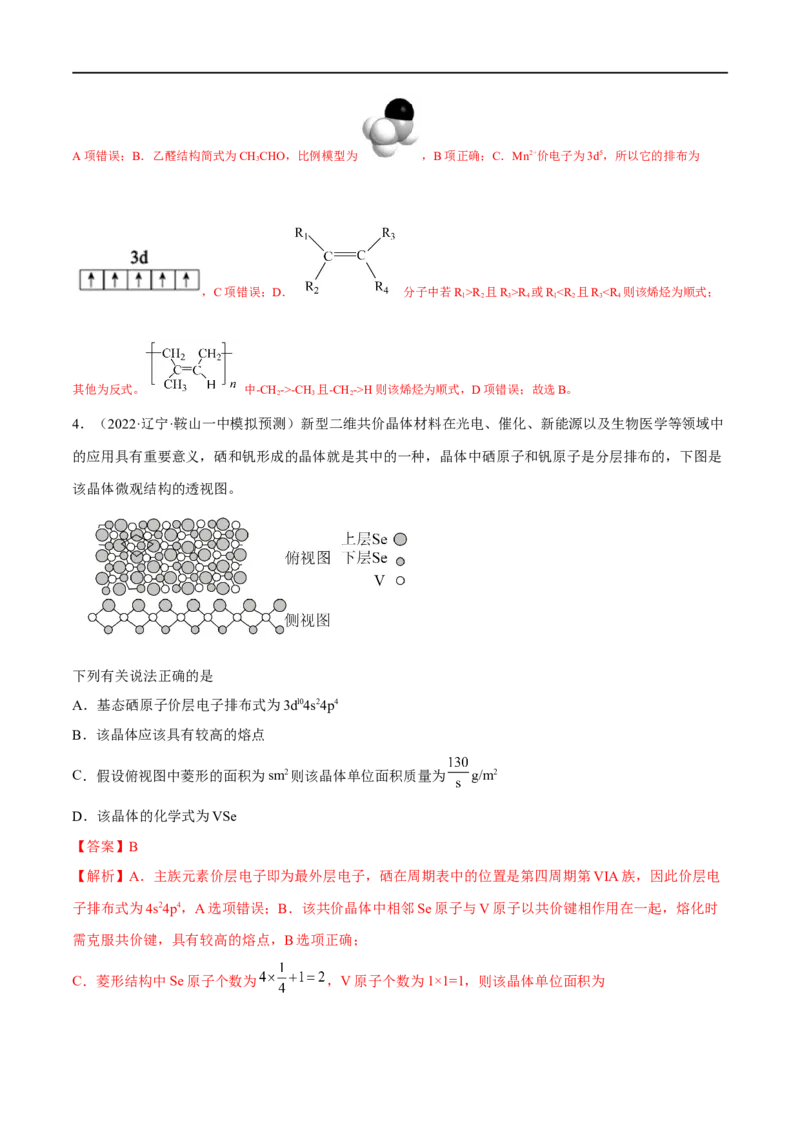
4.(2022·辽宁·鞍山一中模拟预测)新型二维共价晶体材料在光电、催化、新能源以及生物医学等领域中
的应用具有重要意义,硒和钒形成的晶体就是其中的一种,晶体中硒原子和钒原子是分层排布的,下图是
该晶体微观结构的透视图。
下列有关说法正确的是
A.基态硒原子价层电子排布式为3dl04s24p4
B.该晶体应该具有较高的熔点
C.假设俯视图中菱形的面积为sm2则该晶体单位面积质量为 g/m2
D.该晶体的化学式为VSe
【答案】B
【解析】A.主族元素价层电子即为最外层电子,硒在周期表中的位置是第四周期第VIA族,因此价层电
子排布式为4s24p4,A选项错误;B.该共价晶体中相邻Se原子与V原子以共价键相作用在一起,熔化时
需克服共价键,具有较高的熔点,B选项正确;
C.菱形结构中Se原子个数为 ,V原子个数为1×1=1,则该晶体单位面积为,C选项错误;D.俯视图中菱形结构为最小晶胞,Se原子个数为 ,V
原子个数为1×1=1,所以该晶体化学式为VSe ,D选项错误;
2
答案选B。
5.(2022·重庆市育才中学二模)第24届冬奥会于2022年2月4日在北京隆重开幕,“科技冬奥”理念,
体现在方方面面。回答下列有关问题:
(1)冬奥会采用的石墨烯(即单层石墨)材料制造户外保暖穿戴设备,该材料中的碳原子采取_______杂化,属
于元素周期表中_______区,同主族的元素基态Ge原子核外电子的空间运动状态有_______种。
奥运会场馆使用了大量的合金。第VIII族元素Fe、Co、Ni性质相似,称为铁系元素,主要用于制造合金。
(2)基态Fe2+与Fe3+离子的最外层电子数之比为_______,实验室常用A离子来检验Fe3+离子,且又是CO 的
2
某一种等电子体,写出A离子的结构式_______。
(3)Fe(CO) 是一种黄色粘稠状液体化合物,则CO作配体时,配位原子是_______,其原因是_______。
5
(4)写出与Ni同周期元素中,基态原子未成对电子数与Ni相同的元素名称_______。
(5)如表为Co2+、Ni2+不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,
Ni2+比较稳定的配离子配位数是_______(填“4”或“6”)
离 离
配位数 晶体场稳定化能(Dq) 配位数 晶体场稳定化能(Dq)
子 子
6 -8Dq+2p 6 -12Dq+3p
Co2+ Ni2+
4 -5.34Dq+2p 4 -3.56Dq+3p
(6)目前新能源汽车电池主要是磷酸铁锂(LiFePO )和三元锂电池(正极含有Ni、Co、Mn三种元素)。LiFePO
4 4
中阴离子的立体构型名称是_______。三元锂电池的负极材料是石墨,石墨晶体的二维平面结构如图1所示,
晶胞结构如图2所示。根据图2计算石墨晶体的密度是_______g/cm3(写出表达式即可)。【答案】(1)sp2杂化; P; 17;
(2)14:13; [S=C=N]-;
(3)C;C 的电负性小于O,对孤电子对吸引能力弱,给出电子对更容易;
(4)钛、 锗、硒;
(5)6;
(6)正四面体形; 或 或 ;
【解析】(1)石墨每层结构中每个C原子与周围的3个C原子形成3个o键,C原子为sp2杂化,C原子
的核外电子排布为: ,位于周期表中P区,Ge原子核外电子排布 ,有
1s、2s、3s、4s各有1个轨道,2p、3p各有3个轨道,4p有2个轨道含有电子,3d有5个轨道,所以共有
17种空间运动状态,故答案为:sp2;P;17;
(2)基态Fe2+的核外电子排布为: ,最外层电子数为14个,Fe3+离子核外电子排布为
,最外层电子数为13个,基态Fe2+与Fe3+离子的最外层电子数之比为14:13,原子个
数及价电子数相等的微粒是等电子体,故A离子为SCN,结构式为:[S=C=N]-,故答案为:14:13;
[S=C=N]-;
(3)C原子的电负性比O的小,对孤电子对的吸引力更小,更容易给出孤电子对,因此配位原子是C,故
答案为:C;对孤电子对吸引能力弱,给出电子对更容易;
(4)Ni原子的核外电子排布为: ,有2个未成对电子,第四周期含有2个未成对电
子的有钛、锗、硒,故答案为:钛、锗、硒;
(5)由表格可知Ni2+配位数为6时对应的晶体场稳定化能降低的更多,更稳定,故答案为:6;
(6) 中P原子价层电子对数 ,且不含孤电子对, 故 的空间构型为正四面体,
由晶胞结构图可知晶胞含有的C原子个数为 ,C原子之间的距离为anm,则晶胞底
C 组 真题练面边长为 ,晶胞体积: ,晶胞密度
;故答案为: 或 或 ;
1.(2022·江苏·高考真题)下列说法正确的是
A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
【答案】B
【解析】A.金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误;B. 的化学键为
Si-H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为Si-Cl,为极性键,
为正四面体,正负电荷中心重合,为非极性分子,故B正确;C.锗原子( )基态核外电子排布式为
[Ar]3d10 ,故C错误;
D.ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,故D错误;故选B。
2.(2022·北京·高考真题)由键能数据大小,不能解释下列事实的是
化学键
键能/ 411 318 799 358 452 346 222A.稳定性: B.键长:
C.熔点: D.硬度:金刚石>晶体硅
【答案】C
【解析】A.键能越大越稳定, 键能大于 ,所以稳定性: ,故不选A;B.键能越大,
键长越短, 键能大于 ,所以键长: ,故不选B;C.CO 是分子晶体,熔点由分
2
子间作用力决定,SiO 是共价晶体,所以熔点 ,不能用键能解释熔点 ,故选C; D.
2
金刚石、晶体硅都是共价晶体,共价晶体中键能越大,晶体的硬度越大, 的键能大于 ,所以硬
度:金刚石>晶体硅,故不选D;选C。
3.(2022·北京·高考真题)下列化学用语或图示表达不正确的是
A.乙炔的结构简式:
B.顺 丁烯的分子结构模型:
C.基态 原子的价层电子的轨道表示式:
D. 的电子式:
【答案】C
【解析】A.乙炔中含有碳碳三键,其结构简式为 ,A项正确;B.顺 丁烯中两个甲基位于
双键同侧,其结构模型为 ,B项正确;C.基态 原子的价层电子排布式为3s23p2,其轨道表
示式为 ,C项错误;D. 是离子化合物,其电子式为 ,D项正确;答案选C。
4.(2022·湖北·高考真题)磷酰三叠氮是一种高能分子,结构简式为 。下列关于该分子的说法
正确的是
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出 D.分解产物 的电子式为
【答案】C
【解析】A.磷酰三叠氮分子不是对称结构,分子中的正负电荷重心是不重合的,是极性分子,A项错误;
B.磷酰三叠氮分子含有三个P-N键及一个P=O双键,则立体构型为四面体构型,B项错误;C.磷酰三
叠氮是一种高能分子,加热条件下会分解并放出 ,C项正确;D. 为共价化合物,则电子式为
,D项错误;答案选C。
5.(2022·河北·高考真题)含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染
的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_____。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是____,原因是_____。
(3)SnCl 的几何构型为____,其中心离子杂化方式为____。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺
磁性物质的是____(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[Zn(NH )]SO D.Na[Zn(OH) ]
3 2 3 4 4 3 4 4 2 4
(5)如图是硫的四种含氧酸根的结构:
A. B. C. D.根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO 的是____(填标号),理由是____。
(6)如图是CZTS四元半导体化合物的四方晶胞。
①该物质的化学式为_____。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中A原
子的坐标为( , , ),则B原子的坐标为_____。
【答案】(1)1:2或2:1
(2) Cu Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二电离能失去的是4s1
的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大
(3)三角锥形 sp3杂化
(4)B
(5)D D中含有—1价的O元素,具有强氧化性,能将Mn2+转化为MnO
(6)Cu ZnSnS ( , , )
2 4
【解析】(1)基态S的价电子排布是3s23p4,根据基态原子电子排布规则,两种自旋状态的电子数之比为
1:2或2:1,故答案为:1:2或2:1;(2)铜元素的第二电离能失去的是3d10的电子,第一电离能失去
的是4s1电子,锌元素的第二电离能失去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充
满状态,其与4s1电子能量差值更大,所以铜与锌相比,第二电离能与第一电离能差值更大的是铜元素,故答案为:Cu;Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二电离能失
去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大;
(3)三氯化锡离子在锡离子的价层电子对数为4、孤对电子对数为1,所以锡离子杂化方式为sp3杂化,离
子的空间构型为三角锥形,故答案为:三角锥形;sp3杂化;(4)根据题意,具有顺磁性物质含有未成对
电子;A.[Cu(NH )]Cl中亚铜离子外围电子排布是3d10,离子中电子均已成对,该配合物不具有顺磁性,
3 2
故不符合题意;B.[Cu(NH )]SO 中铜离子外围电子排布是3d9,离子中有未成对电子,该配合物具有顺磁
3 4 4
性,故符合题意;C.[Zn(NH )]SO 中锌离子外围电子排布是3d10,离子中电子均已成对,该配合物不具
3 4 4
有顺磁性,故不符合题意;D.Na[Zn(OH) ] 中锌离子外围电子排布是3d10,离子中电子均已成对,该配
2 4
合物不具有顺磁性,故不符合题意;故选B;(5)由四种含氧酸根的结构式可知,只有过二硫酸根离子中
含有过氧链,离子中—1价的氧元素具有强氧化性,则只有过二硫酸根离子能在酸性溶液中将锰离子氧化
为高锰酸根离子,故选D;
(6)①由晶胞结构可知,位于顶点和体心的锌原子个数为8× +1=2,位于面上的铜原子个数为8× =4,
位于面心和棱上的锡原子个数为2× +4× =2,位于体内的硫原子个数为8,则该物质的化学式为
Cu ZnSnS,故答案为:Cu ZnSnS;②若将晶胞先分为上下两个相等的正方体后再将每个正方体继续分为
2 4 2 4
8个相等的小正方体,则B原子位于上面的正方体分割成的8个小立方体中位于右下后方的小立方体的体
心,由A原子的坐标为( , , )可知,B原子的坐标为( , , ),故答案为:( , , )。