文档内容
高频考点 24 电解池工作原理及应用
1.(2022·广东卷)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的再
生。该过程中( )
A.阴极发生的反应为 B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥 D.阳极和阴极的质量变化相等
1. C A.阴极应该发生得电子的还原反应,实际上Mg在阳极失电子生成Mg2+,A错误;B.Al在阳极上
被氧化生成Al3+,B错误;C.阳极材料中Cu和Si不参与氧化反应,在电解槽底部可形成阳极泥,C正确;
D.因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子
生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;故选C。
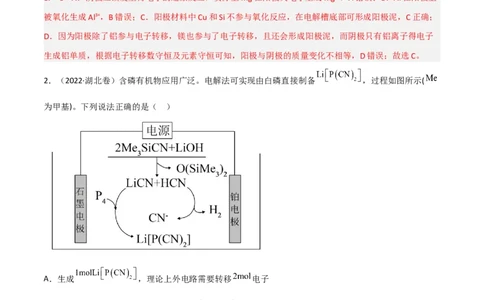
2.(2022·湖北卷)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图所示(
为甲基)。下列说法正确的是( )
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
2.D A.石墨电极发生反应的物质:P → 化合价升高发生氧化反应,所以石墨电极为阳极,对
4应的电极反应式为: ,则生成 ,理论上外电路需要转移 电
子,A错误;B.阴极上发生还原反应,应该得电子, 为阳极发生的反应, B错
误;C.石墨电极:P → 发生氧化反应,为阳极,铂电极为阴极, 应该向阳极移动,即移
4
向石墨电极,C错误;D.由所给图示可知HCN在阴极放电,产生 和 ,而HCN中的H来自 ,
则电解产生的 中的氢元素来自于 ,D正确;故选D。
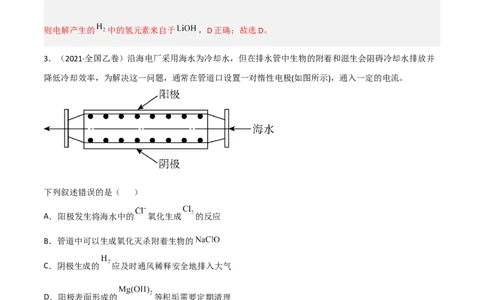
3.(2021·全国乙卷)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并
降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是( )
A.阳极发生将海水中的 氧化生成 的反应
B.管道中可以生成氧化灭杀附着生物的
C.阴极生成的 应及时通风稀释安全地排入大气
D.阳极表面形成的 等积垢需要定期清理
3.D A.根据分析可知,阳极区海水中的Cl-会优先失去电子生成Cl ,发生氧化反应,A正确;B.设置的
2
装置为电解池原理,根据分析知,阳极区生成的Cl 与阴极区生成的OH-在管道中会发生反应生成NaCl、
2
NaClO和H O,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B正确;C.因为H 是易燃性气体,所
2 2
以阴极区生成的H 需及时通风稀释,安全地排入大气,以排除安全隐患,C正确;D.阴极的电极反应式
2
为:2H O+2e-=H ↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极表面会形成Mg(OH) 等积垢需定期清理,
2 2 2
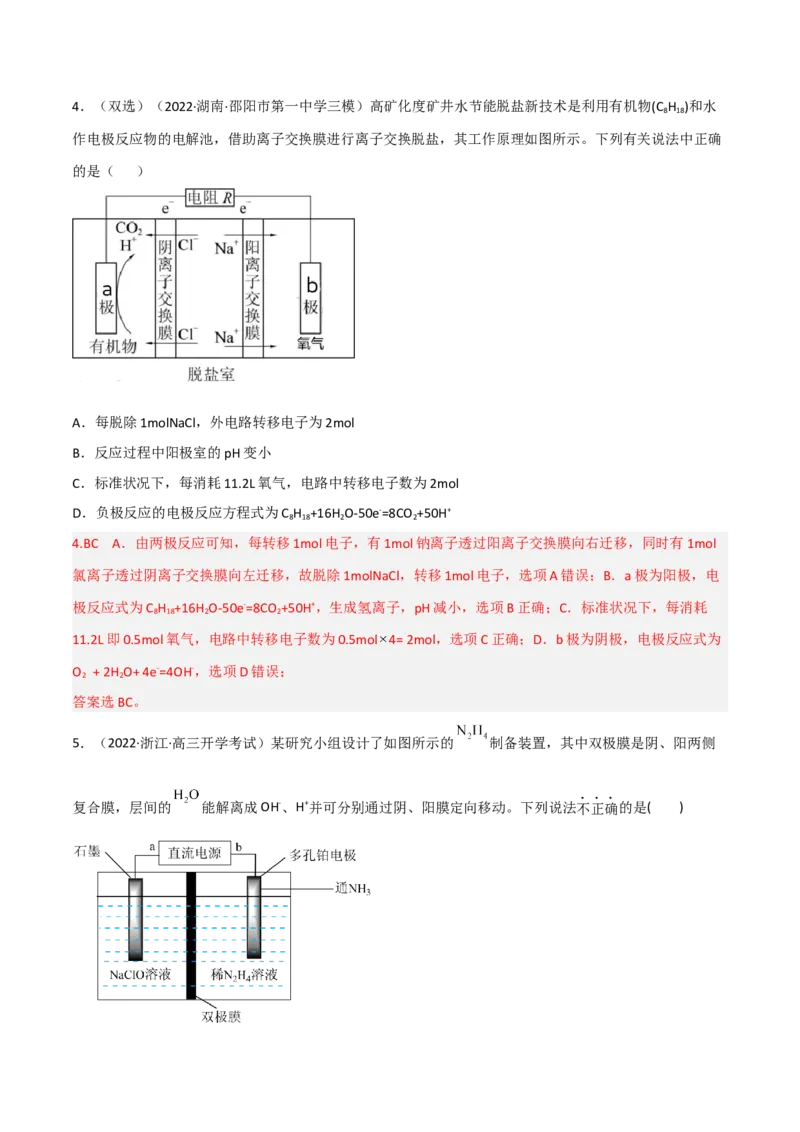
D错误。故选D。4.(双选)(2022·湖南·邵阳市第一中学三模)高矿化度矿井水节能脱盐新技术是利用有机物(C H )和水
8 18
作电极反应物的电解池,借助离子交换膜进行离子交换脱盐,其工作原理如图所示。下列有关说法中正确
的是( )
A.每脱除1molNaCl,外电路转移电子为2mol
B.反应过程中阳极室的pH变小
C.标准状况下,每消耗11.2L氧气,电路中转移电子数为2mol
D.负极反应的电极反应方程式为C H +16H O-50e-=8CO +50H+
8 18 2 2
4.BC A.由两极反应可知,每转移1mol电子,有1mol钠离子透过阳离子交换膜向右迁移,同时有1mol
氯离子透过阴离子交换膜向左迁移,故脱除1molNaCl,转移1mol电子,选项A错误;B.a极为阳极,电
极反应式为C H +16H O-50e-=8CO +50H+,生成氢离子,pH减小,选项B正确;C.标准状况下,每消耗
8 18 2 2
11.2L即0.5mol氧气,电路中转移电子数为0.5mol 4= 2mol,选项C正确;D.b极为阴极,电极反应式为
O + 2H O+ 4e-=4OH-,选项D错误;
2 2
答案选BC。
5.(2022·浙江·高三开学考试)某研究小组设计了如图所示的 制备装置,其中双极膜是阴、阳两侧
复合膜,层间的 能解离成OH-、H+并可分别通过阴、阳膜定向移动。下列说法不正确的是( )A.b端为电源的正极
B.随着反应的进行,阴极室内溶液碱性减弱
C.多孔铂电极上的电极反应式为
D.双极膜的左、右两侧分别属于阴膜和阳膜
5.D A.在电解池的阳极NH 失去电子被氧化成N H ,因此b端为电源的正极,故A项正确;
3 2 4
B.NaClO溶液呈碱性,阴极室内发生的反应为:ClO- + 2e- + H O= Cl- + 2OH-。NaClO浓度降低,因此溶液碱
2
性减弱,故B项正确;C.多孔铂电极上NH 失去电子,电极反应式为:2NH - 2e- +2OH- = N H + 2H O,故
3 3 2 4 2
C项正确; D.在电解池中,阳离子向阴极移动,阴离子向阳极移动,因此双极膜的左右两侧分别为阳膜和
阴膜,故D项错误。故答案选:D。
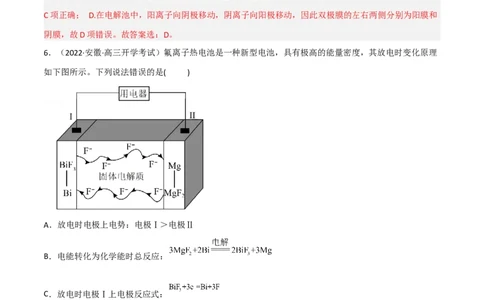
6.(2022·安徽·高三开学考试)氟离子热电池是一种新型电池,具有极高的能量密度,其放电时变化原理
如下图所示。下列说法错误的是( )
A.放电时电极上电势:电极Ⅰ>电极Ⅱ
B.电能转化为化学能时总反应:
C.放电时电极Ⅰ上电极反应式:
D.充电时当电极Ⅱ减少 时,电路中有 电子转移
6.D A.放电时,电极Ⅰ为正极,电极Ⅱ为负极,电极上电势:电极Ⅰ>电极Ⅱ,A正确;
B.充电时,电能转化为化学能,其总反应为 ,B正确;C.放电时,BiF 在电
3极Ⅰ发生得电子的还原反应生成Bi,电极反应式: ,C正确;
D.充电时,电极Ⅱ为阴极,电极反应式为 ,当电路中有 电子转移时,消耗2mol
,生成2mol ,电极Ⅱ质量减少 ,D错误;故答案选
D。
7.(2022·安徽蚌埠·高三阶段练习)铜基配合物电催化还原CO 的装置原理如图所示,下列说法不正确的
2
是( )
A.石墨烯为阳极,发生电极反应为CO +2e-+2H+=HCOOH
2
B.Pt电极附近溶液的pH值减小
C.每转移2mol电子,阳极室、阴极室溶液质量变化量的差值为28g
D.该装置可减少CO 在大气中累积和实现可再生能源有效利用
2
7.A A.石墨烯为阴极,A错误;B.Pt电极上H O失电子转化为O ,电极反应为 ,
2 2
所以电极附近溶液的pH减小,B正确;C.每转移2mol电子,由阴极电极反应式可知生成1molHCOOH,
所以阴极室溶液| |=46g/mol×1mol=46g;根据阳极室反应可知每转移2mol电子时阳极消耗1mol水,生
m阴
成0.5mol氧气,同时有2molH+转移至阴极室,所以| |=18g/mol×1mol=18g,所以| || |
m阳 m阴 m阳
=46g-18g=28g,C正确;
D.该装置可减少CO 在大气中累计和实现可再生能源有效利用,D正确;故选A。
2
8.(2022· 青岛市第一中学二模)某科研团队成功合成了具有拉伸应力的超薄多孔Pd纳米片,以超薄多
孔Pd纳米片作阳极,在常温常压下通过电解将氮气直接转化为硝酸根离子。其工作原理示意图如图所示。
已知:Pd会向PdO 发生转化,在极少量PdO 生成后开始有硝酸根离子生成,Pd溶于硝酸。下列说法错误
2 2的是( )
A.可采用阴离子交换膜
B.电解过程中,Pd、N 均在阳极附近发生反应
2
C.超薄多孔Pd纳米片有助于其转化为PdO ,提高硝酸根离子的产生效率
2
D.开始产生硝酸根离子时,电解的总反应式为
8.D A.由通电于 能溶于硝酸,由此可推测电解质溶液为碱性环境,电解方程式为
, 可通过交换膜进入阳极室,A正确;B.由题意当 产生
时,开始产生硝酸根离子,说明 先在阳极放电,B正确;
C.超薄多孔增大了反应接触面积,有助于转化为 ,由题意可知开始产生 时,开始产生硝酸根离
子,C正确;D.由通电于 能溶于硝酸,由此可推测电解质溶液为碱性环境,电解方程式为
, 可通过交换膜进入阳极室,D项错误。
9.(2022·河南·高三阶段练习)乙醛酸钠(OHC- COONa)是一种精细化工产品。科研工作者设计如图所示装
置制备乙醛酸钠,同时完成CO 的综合利用。该装置工作时,下列说法正确的是( )
2A.电极a上的电势低于电极b上的电势
B.阴极的电极反应式为OHC- CHO+3 +H O- 2e- =OHC- COO-+3
2
C.生成OHC-COO-与生成CO的物质的量相等。
D. 由阳极区移向阴极区
9.C A.电极a连接电解池的阳极,为电源正极,则电势高于电极b上的电势,A错误;
B.阴极发生还原反应,为得到电子的反应,不是失去电子;阳极发生氧化反应,失去电子,电极反应式
为OHC- CHO+3 +H O- 2e- =OHC- COO-+3 ,B错误;C.阴极电子转移情况为:CO ~ 2e- ~CO,根据
2 2
电子守恒可知,OHC-COO-~ 2e- ~CO,则生成OHC-COO-与生成CO的物质的量相等,C正确; D.电解池中
阴离子向阳极运动, 由阴极区移向阳极区,D错误;故选C。
10.(2021·北京卷节选)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯
经电解制备EO的原理示意图如下。(1)阳极室产生Cl 后发生的反应有:_______、CH =CH +HClO→HOCH CH Cl。
2 2 2 2 2
(2)结合电极反应式说明生成溶液a的原理_______。
10.(1) Cl +H O= HCl+ HClO (2) 阴极发生反应: 2H O+2e-=H ↑ + 2OH-生成OH-,K+ 通过阳离子交换膜从
2 2 2 2
阳极迁移到阴极,形成KOH和KCl的混合溶液
解析:阳极产生氯气后,可以和水发生反应生成次氯酸其方程式为:Cl +H O= HCl+ HClO;溶液a是阴极的
2 2
产物,在阴极发生反应2H O+2e-=H ↑ + 2OH-,同时阳极的钾离子会向阴极移动和氢氧根结合形成氢氧化钾,
2 2
故答案为:阴极发生反应: 2H O+2e-=H ↑ + 2OH-生成OH-,K+ 通过阳离子交换膜从阳极迁移到阴极,形成
2 2
KOH和KCl的混合溶液;
11.(2022·北京石景山·高三期末)CO 是一种自然界大量存在的“碳源”化合物,借助零碳能源(太阳能
2
等)制得的H 可将CO 转化为燃料,能缓解温室效应和解决能源危机问题。
2 2
(1)硅太阳能电池可实现太阳能向电能的转化,Si在元素周期表中的位置____。
(2)电解水制H ,阴极电极反应式是____。
2
(3)聚乙烯亚胺捕获CO 并原位氢化为甲醇,反应历程如图1所示。
2
①写出CO 的电子式____。
2
②写出生成甲醇的总反应_____。
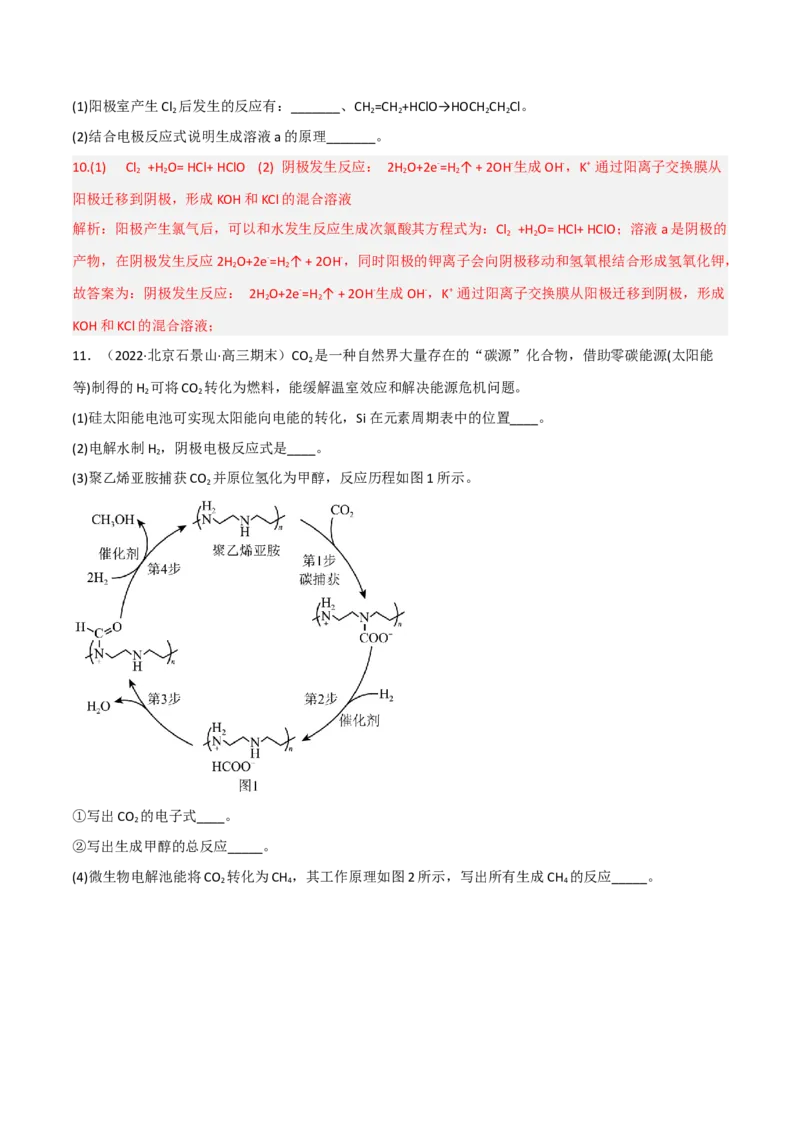
(4)微生物电解池能将CO 转化为CH ,其工作原理如图2所示,写出所有生成CH 的反应_____。
2 4 411.(1)第三周期ⅣA族
(2)2H O+2e-=2OH-+H ↑或2H++2e-=H ↑
2 2 2
(3) CO +3H CH OH+H O
2 2 3 2
(4)CO +4H CH +2H O,CO +8H++8e-= CH +2H O
2 2 4 2 2 4 2
解析:(1)硅原子序数为14,核外电子分3层排布,依次为2、8、4个,Si在元素周期表中的位置第三周
期ⅣA族。
(2)电解水制H ,阴极上水电离产生的氢离子得电子变氢气,阴极电极反应式是2H O+2e-=2OH-+H ↑或
2 2 2
2H++2e-=H ↑。
2
(3)①CO 是共价化合物,分子内每个氧原子和碳原子共用两对电子对、电子式 。
2
②由图知,CO 和H 反应生成CH OH和H O,在生成甲醇的反应中聚乙烯亚胺是催化剂,则生成甲醇的总
2 2 3 2
反应为CO +3H CH OH+H O。
2 2 3 2
(4)由图知,右侧电极上在产甲烷菌的作用下CO 与H 反应生成了CH 和H O,右侧为阴极区,CO 得电
2 2 4 2 2
子被还原为CH ,则所有生成CH 的反应为:CO +4H CH +2H O,CO +8H++8e-= CH +2H O。
4 4 2 2 4 2 2 4 2
12.(2022·全国·高三模拟)根据下列要求回答下列问题。
(1)次磷酸钴[Co(H PO ) ]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,
2 2 2
原理如图:则Co的电极反应式为___________,A、B、C为离子交换膜,其中B为___________离子交换膜(填“阳”
或“阴”)。
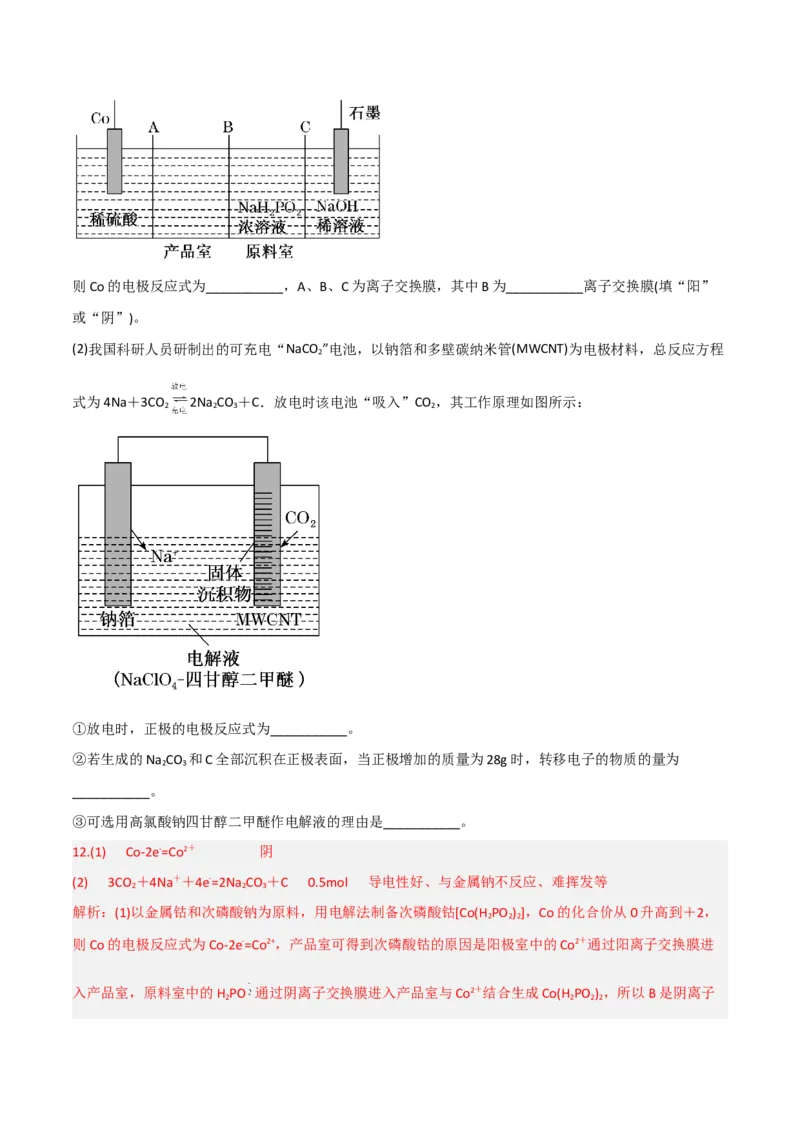
(2)我国科研人员研制出的可充电“NaCO ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程
2
式为4Na+3CO 2Na CO +C.放电时该电池“吸入”CO ,其工作原理如图所示:
2 2 3 2
①放电时,正极的电极反应式为___________。
②若生成的Na CO 和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为
2 3
___________。
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是___________。
12.(1) Co-2e-=Co2+ 阴
(2) 3CO +4Na++4e-=2Na CO +C 0.5mol 导电性好、与金属钠不反应、难挥发等
2 2 3
解析:(1)以金属钴和次磷酸钠为原料,用电解法制备次磷酸钴[Co(H PO ) ],Co的化合价从0升高到+2,
2 2 2
则Co的电极反应式为Co-2e-=Co2+,产品室可得到次磷酸钴的原因是阳极室中的Co2+通过阳离子交换膜进
入产品室,原料室中的H PO 通过阴离子交换膜进入产品室与Co2+结合生成Co(H PO ) ,所以B是阴离子
2 2 2 2交换膜;
(2)①放电时,正极发生得到电子的还原反应,则根据总反应式可知电极反应式为3CO +4Na++4e-
2
=2Na CO +C;
2 3
②根据反应式可知每转移4mol电子,正极质量增加2×106g+12g=224g,所以当正极增加的质量为28g时,
转移电子的物质的量为 ×4mol=0.5mol;
③根据题干信息以及金属钠的化学性质可知可选用高氯酸钠四甘醇二甲醚作电解液的理由是其导电性好、
与金属钠不反应、难挥发等。