文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷08
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、高效光催化剂与碳中和(21分)
AgPO4,具有溶于酸、氰化钾溶液和氨水,微溶于水和稀醋酸。用作照相乳液剂、催
3
化剂、制药和玻璃业。用于制溴化银、碘化银乳剂代替硝酸银制乳剂。具有十八面体结构
的AgPO 晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。
3 4
1. I.配位-沉淀法制备Ag PO 高效光催化剂
3 4
已知:i.Ag PO 难溶于水,可溶于硝酸;
3 4
ii.Ag PO 沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
3 4
iii.银氨溶液中存在:
Ag(NH ) + ⇌ Ag++2NH
。
3 2 3
(1)配制银氨溶液时的反应有 、 。
Ag++NH ⋅H O=AgOH↓+NH+
3 2 4
(2)加入Na HPO 溶液后得到Ag PO 固体,该反应的离子方程式为 。
2 4 3 4
(3)AgNO 和NaPO 在溶液中反应也可制得Ag PO 固体,但制得的Ag PO 固体光催化性能
3 3 4 3 4 3 4
极差。从速率角度解释其原因: 。
II.Ag PO 光催化剂的使用和再生
3 4
已知:Ag PO 晶体在光照条件下发挥催化作用时,首先引发反应S1。
3 4
可见光
S1:Ag 3 PO 4¿[Ag PO ] ⊕+e−
3 4
¿
(4) Ag PO 光催化CO 制备甲醇可实现“碳中和”,S1的后续反应如下。
3 4 2
可见光
2H
2
O+4[Ag
3
PO
4
] ⊕ ¿O
2
+4H++4Ag
3
PO
4
,CO
2
+6e−+6H+=CH
3
OH+H
2
O
¿
则由CO 制备甲醇的总反应的化学方程式为 。
2
(5) Ag PO 光催化降解有机污染物时,有机污染物被氧化成CO 和HO。S1的后续反应如
3 4 2 2下。
S2:
O +e−=O−
,
H O+[Ag PO ] ⊕=H++⋅OH+Ag PO
2 2 2 3 4 3 4
S3:……
注:Ag PO 在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
3 4
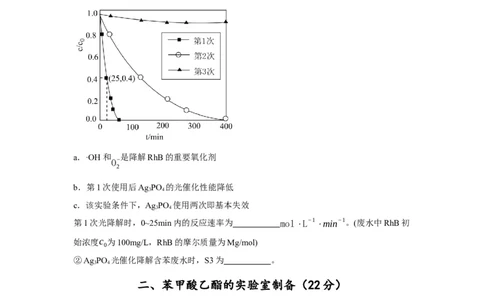
①用Ag PO 依次降解三份相同的含有RhB(一种桃红色有机污染物)的废水,测得3次降解
3 4
过程中RhB的残留率(c/c ,即时浓度与起始浓度之比)随时间变化的曲线如图,下列说法
0
正确的是 (填字母序号)。
a.·OH和 是降解RhB的重要氧化剂
O−
2
b.第1次使用后Ag PO 的光催化性能降低
3 4
c.该实验条件下,Ag PO 使用两次即基本失效
3 4
第1次光降解时,0~25min内的反应速率为 mol⋅L−1 ⋅min−1。(废水中RhB初
始浓度c 为100mg/L,RhB的摩尔质量为Mg/mol)
0
②Ag PO 光催化降解含苯废水时,S3为 。
3 4
二、苯甲酸乙酯的实验室制备(22分)
苯甲酸乙酯可用于配制香水及食用香精,其天然存在于桃、菠萝、醋栗、红茶中。实
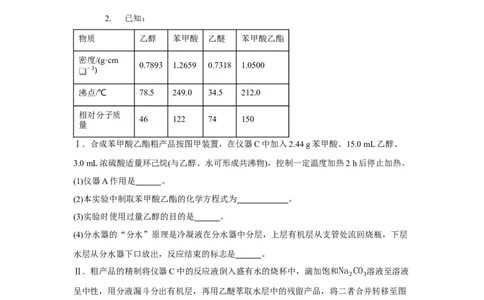
验室可用苯甲酸与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。2. 已知:
物质 乙醇 苯甲酸 乙醚 苯甲酸乙酯
密度/(g·cm
0.7893 1.2659 0.7318 1.0500
❑
−3)
沸点/℃ 78.5 249.0 34.5 212.0
相对分子质
46 122 74 150
量
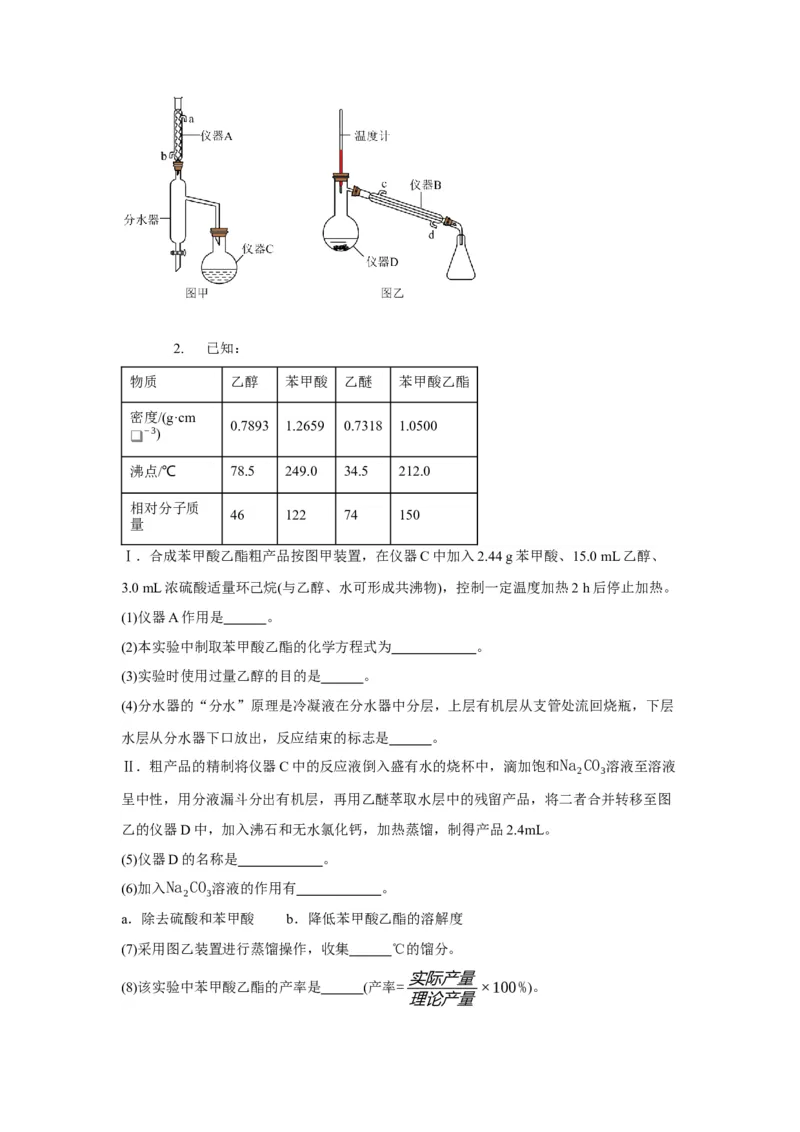
Ⅰ.合成苯甲酸乙酯粗产品按图甲装置,在仪器C中加入2.44 g苯甲酸、15.0 mL乙醇、
3.0 mL浓硫酸适量环己烷(与乙醇、水可形成共沸物),控制一定温度加热2 h后停止加热。
(1)仪器A作用是 。
(2)本实验中制取苯甲酸乙酯的化学方程式为 。
(3)实验时使用过量乙醇的目的是 。
(4)分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层
水层从分水器下口放出,反应结束的标志是 。
Ⅱ.粗产品的精制将仪器C中的反应液倒入盛有水的烧杯中,滴加饱和Na CO 溶液至溶液
2 3
呈中性,用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转移至图
乙的仪器D中,加入沸石和无水氯化钙,加热蒸馏,制得产品2.4mL。
(5)仪器D的名称是 。
(6)加入Na CO 溶液的作用有 。
2 3
a.除去硫酸和苯甲酸 b.降低苯甲酸乙酯的溶解度
(7)采用图乙装置进行蒸馏操作,收集 ℃的馏分。
实际产量
(8)该实验中苯甲酸乙酯的产率是 (产率= ×100%)。
理论产量三、铬基催化剂下丙烷生产丙烯(20分)
丙烯是一种重要的化工原料,其主要产品聚丙烯是生产口罩喷溶布的原料。
3. 铬基催化剂下丙烷生产丙烯相关主要反应有:
Ⅰ.C H (g)⇌ C H (g)+H (g) ΔH =+124.14kJ/mol
3 8 3 6 2 1
Ⅱ.C H (g)⇌ C H (g)+CH (g)
3 8 2 4 4
Ⅲ.C H (g)⇌3C(s)+4H (g)
3 8 2
请回答:
(1)已知键能:E(C−H)=413.4kJ/mol,E(H−H)=436.0kJ/mol。C=C的键能与C-C
的键能相差约 kJ/mol。
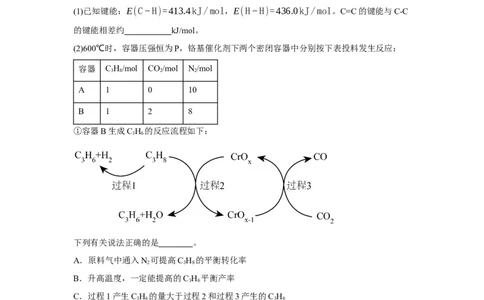
(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
容器 C H/mol CO/mol N/mol
3 8 2 2
A 1 0 10
B 1 2 8
①容器B生成C H 的反应流程如下:
3 6
下列有关说法正确的是 。
A.原料气中通入N 可提高C H 的平衡转化率
2 3 8
B.升高温度,一定能提高的C H 平衡产率
3 6
C.过程1产生C H 的量大于过程2和过程3产生的C H
3 6 3 6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C H 的平衡转化率
3 8
②若容器A中只发生反应Ⅰ和反应Ⅱ,C H 的平衡转化率为α,C H 的选择性(选择性
3 8 3 6
转化为目标产物所消耗丙烷的量
= ×100%)为w,计算反应Ⅰ的平衡常数K =
转化的丙烷的量 p
。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应
器,C H 的转化率和C H 的选择性随时间变化如图所示:
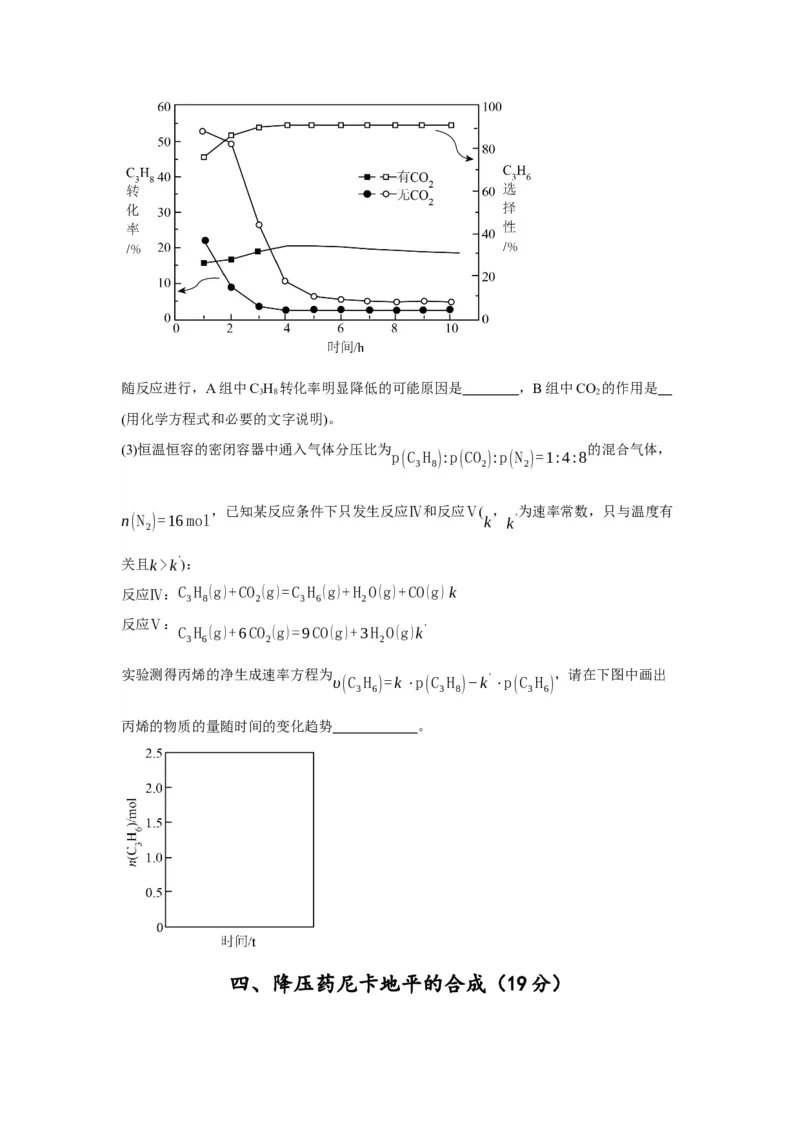
3 8 3 6随反应进行,A组中C H 转化率明显降低的可能原因是 ,B组中CO 的作用是
3 8 2
(用化学方程式和必要的文字说明)。
(3)恒温恒容的密闭容器中通入气体分压比为 的混合气体,
p(C H ):p(CO ):p(N )=1:4:8
3 8 2 2
,已知某反应条件下只发生反应Ⅳ和反应Ⅴ( , 为速率常数,只与温度有
n(N )=16mol k k'
2
关且k>k'):
反应Ⅳ:C H (g)+CO (g)=C H (g)+H O(g)+CO(g) k
3 8 2 3 6 2
反应Ⅴ:
C H (g)+6CO (g)=9CO(g)+3H O(g)k'
3 6 2 2
实验测得丙烯的净生成速率方程为 ,请在下图中画出
υ(C H )=k⋅p(C H )−k' ⋅p(C H )
3 6 3 8 3 6
丙烯的物质的量随时间的变化趋势 。
四、降压药尼卡地平的合成(19分)尼卡地平通过抑制Ca2+流入血管平滑肌细胞而发挥血管扩张作用,而且能抑制磷酸二
酯酶,使脑,冠状动脉及肾血流量增加,起到降压作用。
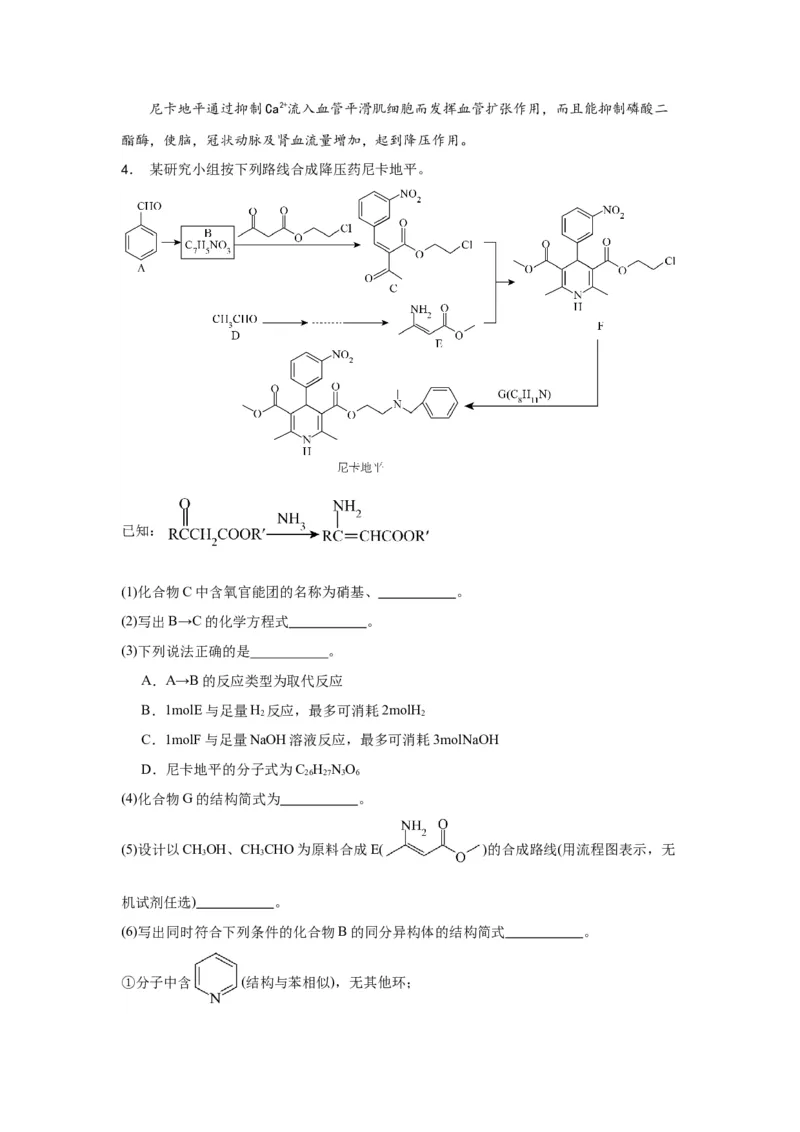
4. 某研究小组按下列路线合成降压药尼卡地平。
已知:
(1)化合物C中含氧官能团的名称为硝基、 。
(2)写出B→C的化学方程式 。
(3)下列说法正确的是___________。
A.A→B的反应类型为取代反应
B.1molE与足量H 反应,最多可消耗2molH
2 2
C.1molF与足量NaOH溶液反应,最多可消耗3molNaOH
D.尼卡地平的分子式为C H NO
26 27 3 6
(4)化合物G的结构简式为 。
(5)设计以CHOH、CHCHO为原料合成E( )的合成路线(用流程图表示,无
3 3
机试剂任选) 。
(6)写出同时符合下列条件的化合物B的同分异构体的结构简式 。
①分子中含 (结构与苯相似),无其他环;②能发生银镜反应;
③1H-NMR谱检测表明:分子中有3种不同化学环境的氢原子。
五、硫及其化合物(18分)
硫单质存在于陨石、火山、温泉等处。 硫是人体内蛋白质的重要组成元素,对人的生
命活动具有重要意义。硫主要用于肥料、火药、润滑剂、杀虫剂和抗真菌剂生产。硫原子
被发现存在于生物分子,如蛋白质、tRNA、抗生素等分子结构中已超过一个多世纪。
5.硫是组成生命的重要元素。回答下列问题:
(1)基态S原子含有 种能量不同的电子,其价层电子排布图是 。
S
(2)S单质的常见形式为 8( ),其中S原子采用的轨道杂化方式是
。
SO F
2 2
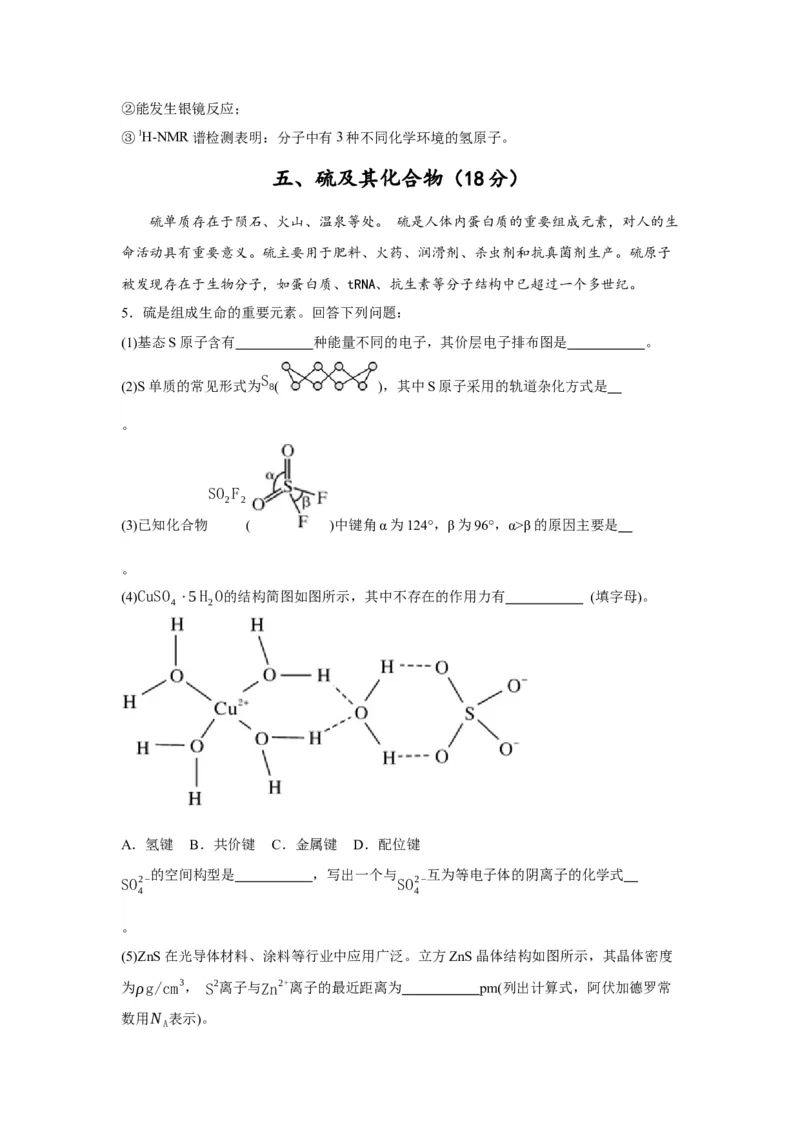
(3)已知化合物 ( )中键角α为124°,β为96°,α>β的原因主要是
。
(4)CuSO ⋅5H O的结构简图如图所示,其中不存在的作用力有 (填字母)。
4 2
A.氢键 B.共价键 C.金属键 D.配位键
的空间构型是 ,写出一个与 互为等电子体的阴离子的化学式
SO2− SO2−
4 4
。
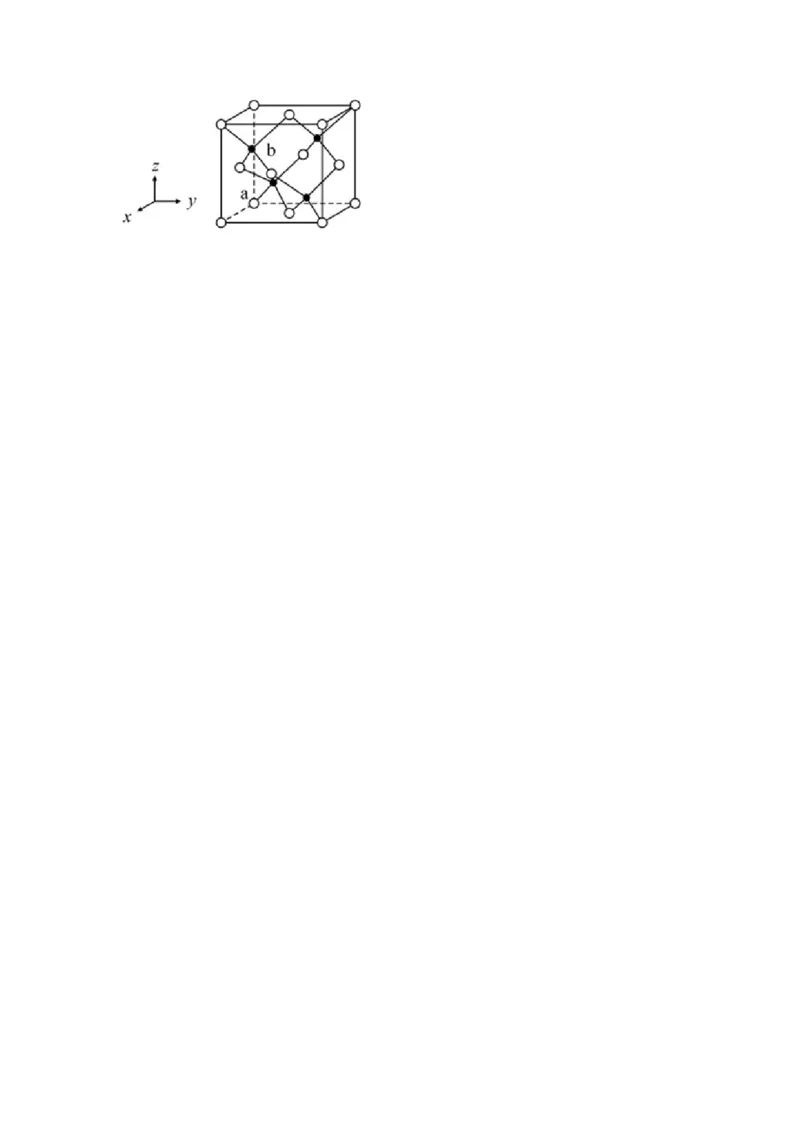
(5)ZnS在光导体材料、涂料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶体密度
为ρg/cm3, S2离子与Zn2+离子的最近距离为 pm(列出计算式,阿伏加德罗常
数用N 表示)。
A