文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟(北京专用)
黄金卷08
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 S 32 Fe 56 Ce 140
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.化学处处呈现美。下列说法不正确的是
A.加热固体碘出现大量紫色蒸气时,共价键断裂
B.降温后水结冰形成晶莹剔透的晶体,氢键数目增加
C.烟花燃放时呈现出五颜六色,是不同金属元素的焰色所致
D.甲烷分子中四个氢原子完美对称,其键角和键长均相等
2.下列图示或化学用语错误的是
A.原子核内有8个中子的碳原子: B.NaClO的电子式:
C. 的VSEPR模型: D.顺-2-丁烯的球棍模型:
3.2023年10月31日8时11分,神舟十六号载人飞船返回舱在东风着陆场成功着陆,神舟十六号载人飞
行任务取得圆满成功。下列有关说法中错误的是。
A.神舟十六号返回舱在着陆前会先抛掉多余的推进剂——水合肼 ,水合肼难溶于水
B.神舟十六号太阳敏感器光学窗口上的石英玻璃主要成分是二氧化硅
C.神舟十六号飞船返回舱侧壁金属壳体用的是铝合金材料,其硬度比纯铝的大
D.神舟十六号飞船返回舱“外衣”中的酚醛树脂属于合成有机高分子化合物
4.向 溶液中通入 气体至饱和,观察到溶液由棕黄色迅速变为红棕色[经检验无 胶体],
较长时间后变为浅绿色。已知:①反应I:
反应II:
②溶液酸性越强, 溶解度越低
下列说法正确的是
A.反应II中 体现漂白性 B.反应II的活化能比反应I的活化能高
C. 在反应I、II中均作氧化剂 D.向红棕色溶液中滴加浓盐酸,颜色加深
5.直接 无膜微流体燃料电池(结构如图所示)利用多股流体在微通道内平行层流的
特性,自然地将燃料和氧化剂隔开,无需使用传统燃料电池中的交换膜,且使用氧化剂 可确
保电池工作过程中无固体析出附着电极表面问题。下列有关说法不正确的是
A.电池工作时,电子由电极a直接经外电路流向电极b
B.电极a上发生的反应为
C.电极b上消耗 时,理论上共转移3mol电子
D.上述无膜微流体技术可降低燃料电池的生产成本,提升电池工作性能
6.下列离子方程式与所给事实不相符的是
A.Cl 制备84消毒液(主要成分是NaClO):
2B.食醋去除水垢中的CaCO :
3
C.向次氯酸钙溶液通入足量二氧化碳:
D.NaS去除废水中的Hg2+:
2
7.化学是以头验为基础的学科。下列根据实验操作和现象能得到相应结论的是
选
实验操作和现象 结论
项
向 溶液KI中加入 溶液( ),溶 和 的反应存在限
A
液呈烹黄色,再滴加几滴KSCN溶液,溶液变为红色 度
常温下,将两块相同的未经打磨的铝片分别投入 饱和的 溶液 能加速破坏铝片表
B
和 溶液中,前者无明显现象,后者迅速反应,现象明显 面的氧化膜
常温下,向 溶液中加入 溶液,将带火星的木条放在试管口,木
C 氧化性:
条复燃
原溶液中一定含有
D 向某无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的的气体
或
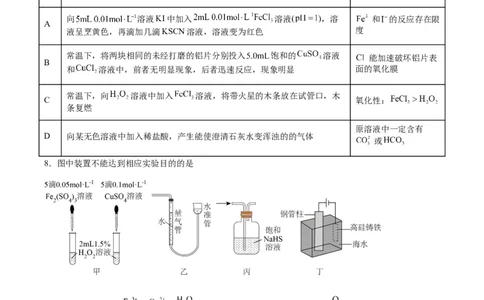
8.图中装置不能达到相应实验目的的是
A.用甲装置探究 、 对 分解的催化效果 B.用乙装置测量 体积
C.用丙装置除去 气体中的 D.用丁装置保护钢管柱不被腐蚀
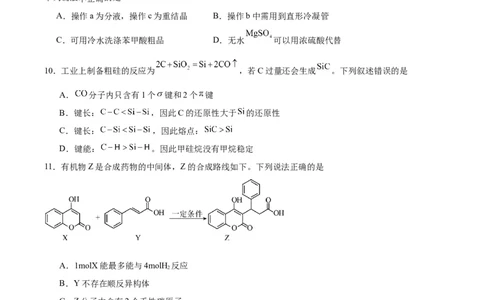
9.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:已知:苯甲酸乙酯的沸点为 ,“乙醚-环己烷-水共沸物”的沸点为 。
下列说法不正确的是
A.操作a为分液,操作c为重结晶 B.操作b中需用到直形冷凝管
C.可用冷水洗涤苯甲酸粗品 D.无水 可以用浓硫酸代替
10.工业上制备粗硅的反应为 ,若C过量还会生成 。下列叙述错误的是
A. 分子内只含有1个 键和2个 键
B.键长: ,因此C的还原性大于 的还原性
C.键长: ,因此熔点:
D.键能: 。因此甲硅烷没有甲烷稳定
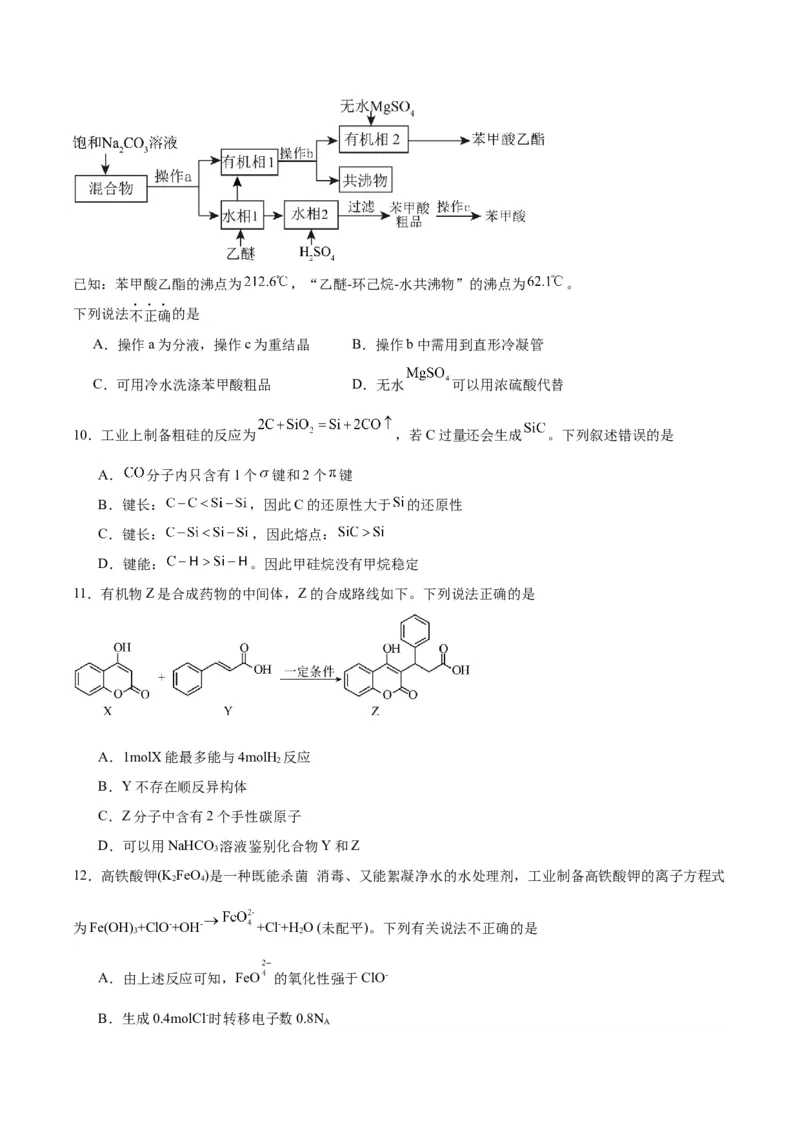
11.有机物Z是合成药物的中间体,Z的合成路线如下。下列说法正确的是
A.1molX能最多能与4molH 反应
2
B.Y不存在顺反异构体
C.Z分子中含有2个手性碳原子
D.可以用NaHCO 溶液鉴别化合物Y和Z
3
12.高铁酸钾(K FeO)是一种既能杀菌 消毒、又能絮凝净水的水处理剂,工业制备高铁酸钾的离子方程式
2 4
为Fe(OH) +ClO-+OH- +Cl-+H O (未配平)。下列有关说法不正确的是
3 2
A.由上述反应可知,FeO 的氧化性强于ClO-
B.生成0.4molCl-时转移电子数0.8N
AC.上述反应中氧化剂和还原剂的物质的量之比为3∶2
D.KFeO 处理水的原理可为:
2 4
13.硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空气的混合气体通入 和
2
HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是
A.历程①发生反应的离子方程式为:
B.历程②中 作氧化剂
C.历程③中
D.该转化历程中可循环的物质有
14.25℃时,向 的氨水中逐滴加入 的盐酸 ,向 的 溶
液中逐滴加入 的 溶液 (无气体逸出),溶液的pH与 [ 或
]的关系如图所示。下列说法错误的是。
A.曲线②中的B.当 时,恒有关系:
C.当 时,两溶液pH均大于9.26
D.25℃时, 的 溶液的pH约为4.63
第二部分
本题共5题,共58分。
15.(11分)完成下列问题。
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NO 、HCOOH、
x
(PAN)等二次污染物。
①PAN中除H外其余三种元素的第一电离能由大到小的顺序为 。1molPAN中含有的σ键数目
为 。
②NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO ,该配合物中中心离子的配位数为 ,中
4 2 5 4
心离子的外围电子排布图 。
③相同压强下,HCOOH的沸点比CHOCH (填高或低),其原因是 。
3 3
(2)PM2.5微细粒子包含(NH )SO 、NH NO 等。
4 2 4 4 3
①(NH )SO 晶体中各种微粒间的作用力不涉及 (填序号)。
4 2 4
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
②NH NO 中阳离子的中心原子轨道采用 杂化,阴离子的空间构型为 。
4 3
(3)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构
如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则 =
(填数字)。已知:该晶胞边长为bpm,N 代表阿伏伽德罗常数,则该晶体的密度为 g/cm3(写出
A
计算式即可)。
16.(11分)已知: 是一种重要的化工品,在一定温度下可发生分解反应:①
②
回答下列问题:
(1) (用含 的式子表示)。
(2)在恒温恒容密闭容器中投入足量 ,发生反应 ,下列叙述正确
的是___________(填标号)。
A.增大 质量时,反应速率增大
B. 体积分数不变时,该反应达到平衡状态
C.平衡后,再充入 ,达到新平衡时, 增大
D.平衡后,再充入少量 质量增大
(3) 的速率方程为 ( 为速率常数,只与温度、
压强有关)。
①某温度下,该反应的平衡常数K为10, ,则 。
②已知: (式中,R为常数, 单位为 ,温度T单位为K,E表示反应的活化
能,单位为 )。 与不同催化剂( 为催化剂)、温度(T)关系如图所示。
相同条件下,催化效率较高的是 (填“ ”或“ ”),判断依据是 。在催化
剂 作用下,正反应的活化能为 。
(4)一定温度下,向密闭容器中充入足量 ,达到平衡时测得生成 和 。则该温度下,反应 的压强平衡常数 ( 为用分压表示的平衡常数,分压=
总压×物质的量分数)。
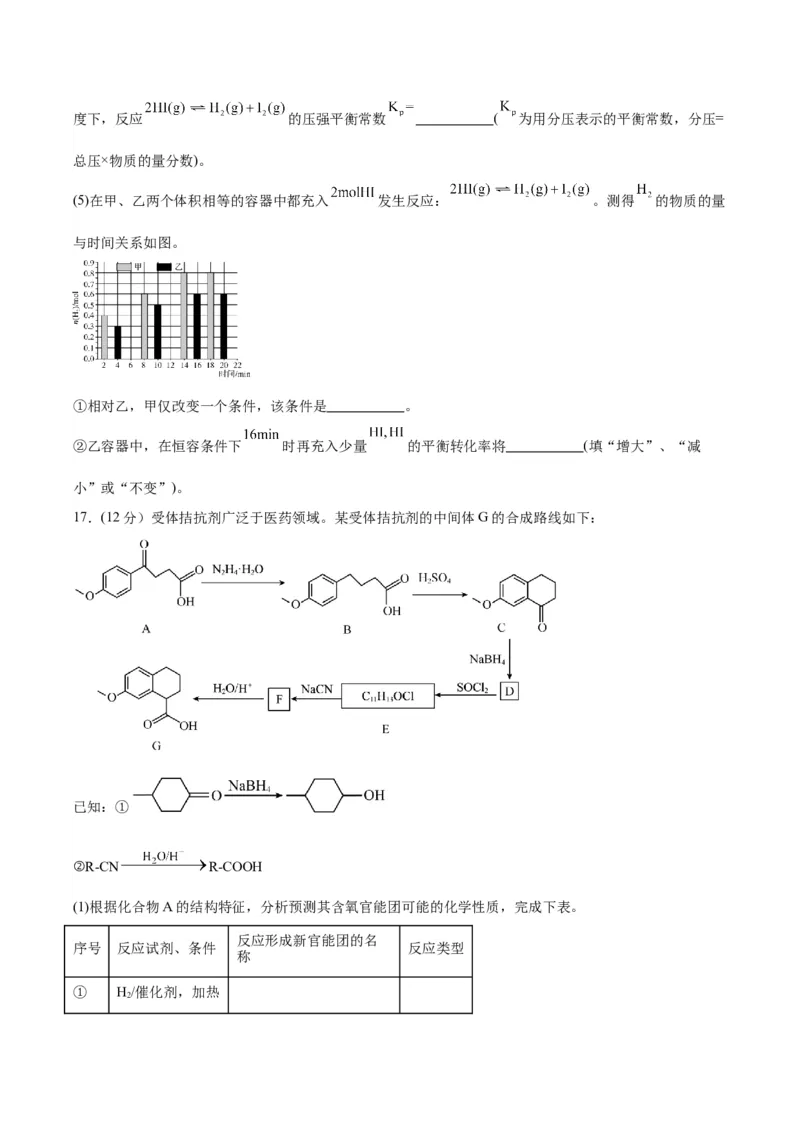
(5)在甲、乙两个体积相等的容器中都充入 发生反应: 。测得 的物质的量
与时间关系如图。
①相对乙,甲仅改变一个条件,该条件是 。
②乙容器中,在恒容条件下 时再充入少量 的平衡转化率将 (填“增大”、“减
小”或“不变”)。
17.(12分)受体拮抗剂广泛于医药领域。某受体拮抗剂的中间体G的合成路线如下:
已知:①
②R-CN R-COOH
(1)根据化合物A的结构特征,分析预测其含氧官能团可能的化学性质,完成下表。
反应形成新官能团的名
序号 反应试剂、条件 反应类型
称
① H/催化剂,加热
2② 酯化反应
(2)关于C→D的反应,下列相关说法正确的是 (填标号)。
a.NaBH 既含共价键又含离子键
4
b.一个化合物C分子中有4个π键
c.反应过程中只有C=O双键断裂和O-H单键形成
d.化合物D分子中存在手性碳原子,且分子中氧原子均采取sp3杂化
(3)由E→F的反应的化学方程式为 。
(4)化合物X是G的同系物,且比G少2个碳原子。写出同时满足下列条件的X的同分异构体的结构简式
、 (任写两种)。
①苯环上连有两个取代基,且苯环上只有两种化学环境不同的氢原子
②能发生银镜反应
③与NaHCO 反应能生成CO
3 2
(5)根据上述合成路线的原理,以 为有机原料,分四步可合成化合物 。基于
设计的合成路线,回答下列问题:
①第一步的化学方程式为 。
②最后一步反应中,有机反应物的结构简式为 。
18.(12分)钴是重要的战略金属之一,钴粉主要以高温氢还原草酸钴制得。一种利用水钴矿[主要成分为
,还含有少量CuO、 、 、MnO、CaO、 等]制备钴的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表。
金属离子
开始沉淀的pH 2.7 7.6 7.6 4.0 7.7 4.7
完全沉淀的pH 3.7 9.6 9.2 5.2 9.8 6.7
请根据以上信息,回答下列问题:
(1)为加快“酸浸”的速率和效率,可以采取的措施有 (答出1条即可),滤渣1的主要成分为(填化学式)。
(2)在“酸浸”步骤中发生的最主要的氧化还原反应的化学方程式为 。
(3)“转化”步骤中加 的目的是 (用离子方程式表示),该步骤反应温度不宜高于40℃的原
因可能是 。
(4)在“调pH”步骤中加入 调节溶液的pH,其合理范围为 ;“萃取”步骤中萃取的主
要离子是 (填离子符号)。
(5)在“沉钴”步骤中,副产物 在空气中可被氧化成 ,该反应的化学方程式为
。
19.(12分)氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
Ⅰ.为探究氯气与 溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去)
实验操作 实验现象
打开A中分液漏斗活塞,放下部分浓盐酸,加热 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色
(1)装置A中生成氯气的化学反应方程式为 。
(2)装置C中 的作用是 。
(3)能证明氯气的氧化性强于碘的实验现象是 。
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料: 和 在溶液中会发生反应: , 显棕黄色且遇淀粉变蓝; 可被氯气氧化为
(红色)和 (黄色),两种离子可继续被氧化成 (无色)。
进行实验:
实验操作 实验现象Ⅰ.取反应后B中的溶液 分成两等份,第一份滴入1滴碘水;第 第一份溶液变蓝色
二份滴入1滴淀粉溶液 第二份溶液颜色没有变化
Ⅱ.将 溶于 溶液中配制得碘总浓度为 的溶液,取上述溶 加淀粉后溶液变蓝,通入氯气后蓝
液 ,滴加1滴淀粉溶液,再通入氯气 色褪去,溶液显浅棕色
Ⅲ.向Ⅱ所得溶液继续通入氯气 溶液几乎变为无色
①操作Ⅰ的实验目的是 。
②写出 在水溶液中与氯气反应生成 的离子方程式 。
③由以上实验可推断 中溶液颜色变成浅棕色的原因是 。
Ⅱ.84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、 、 ;相同浓度时, 的氧化性强于 ;ORP是
反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。某兴趣小组同学研究84消
毒液的漂白性,实验如下。
a.向 消毒液中加入 水后,放入红色纸片,观察到纸片慢慢褪色。
b.向 消毒液中加入 白醋后,放入红色纸片,观察到纸片迅速褪色。
c.测得84消毒液在不同温度时ORP随时间的变化曲线如图。
(5)①已知白醋显酸性,不具有漂白性。实验a、b现象不同的原因是 。
②由实验c可得出的结论是 。