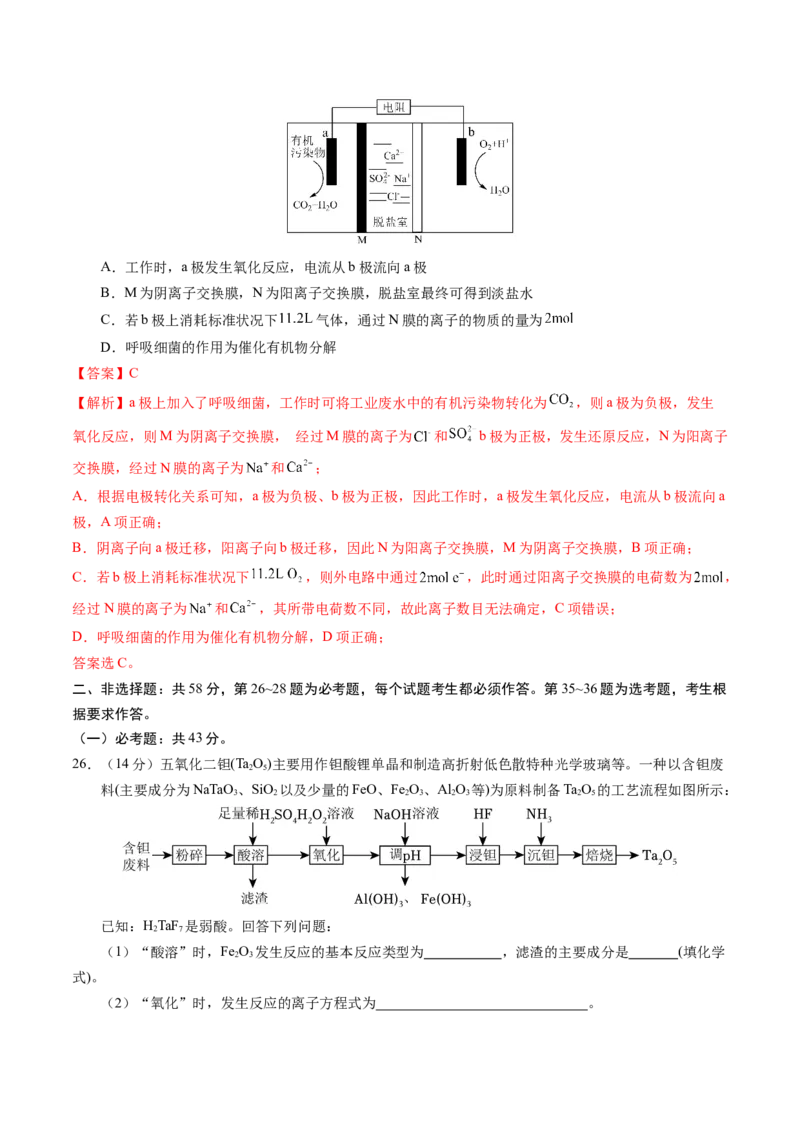
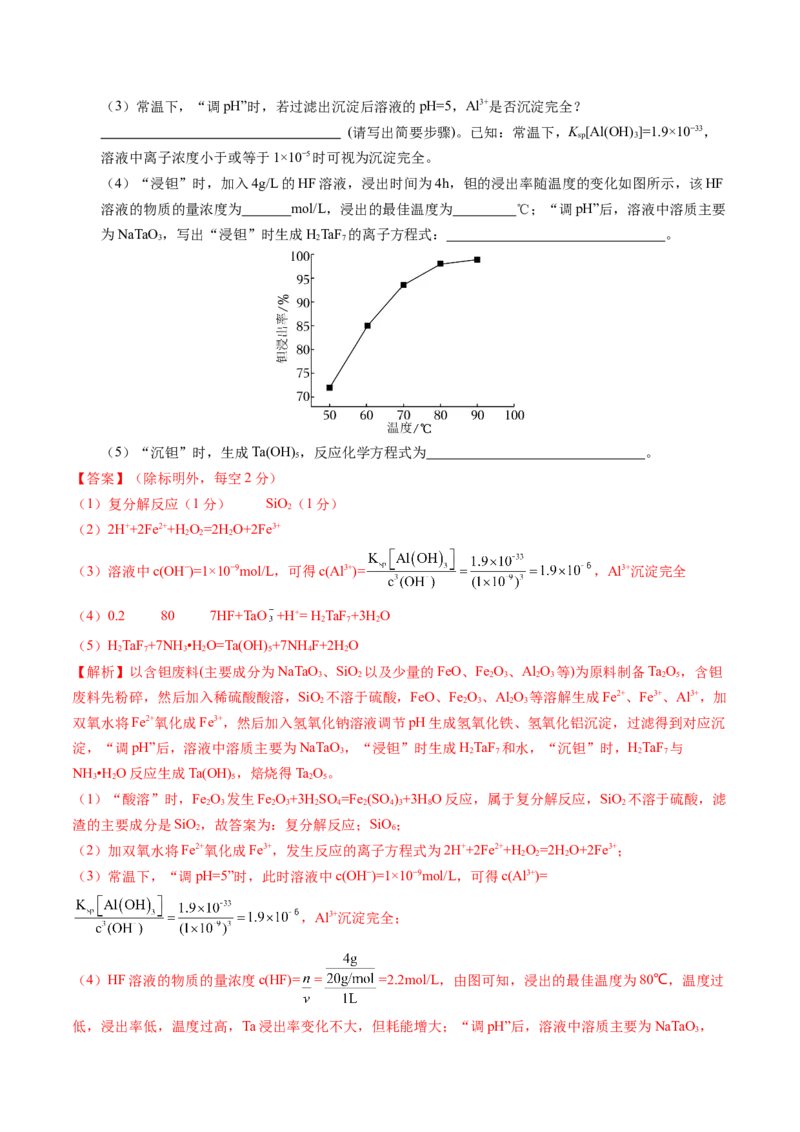
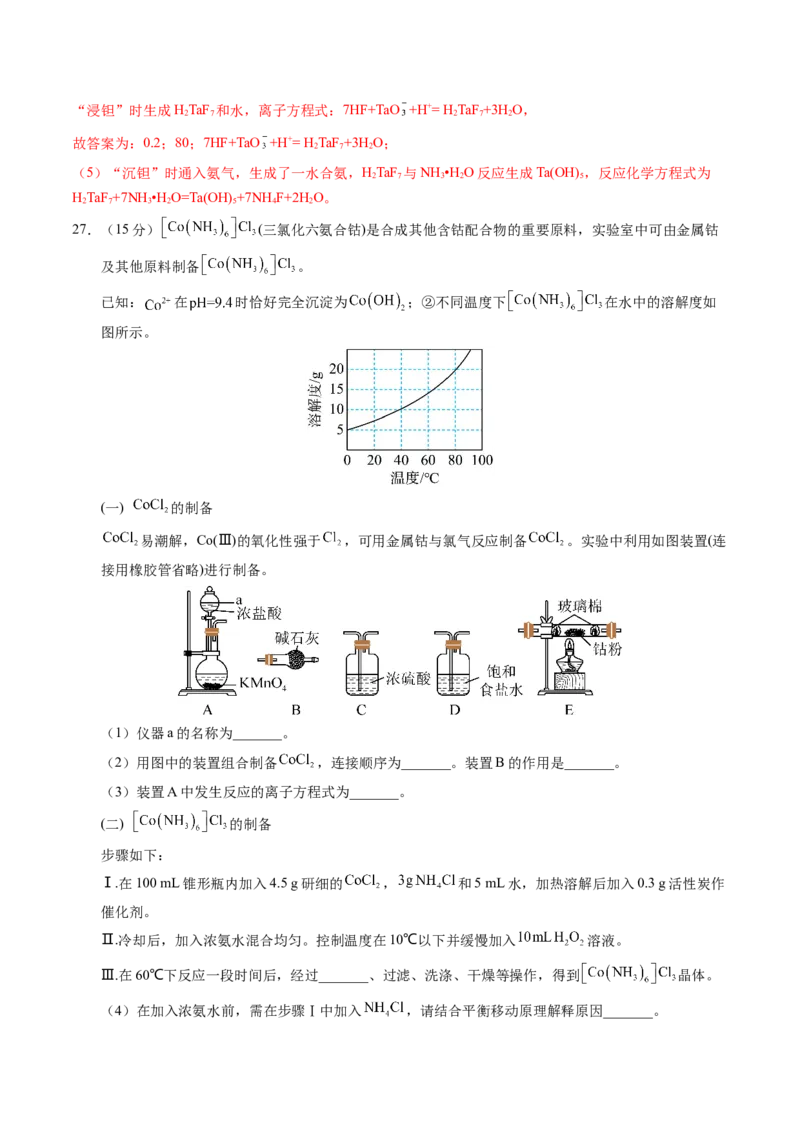
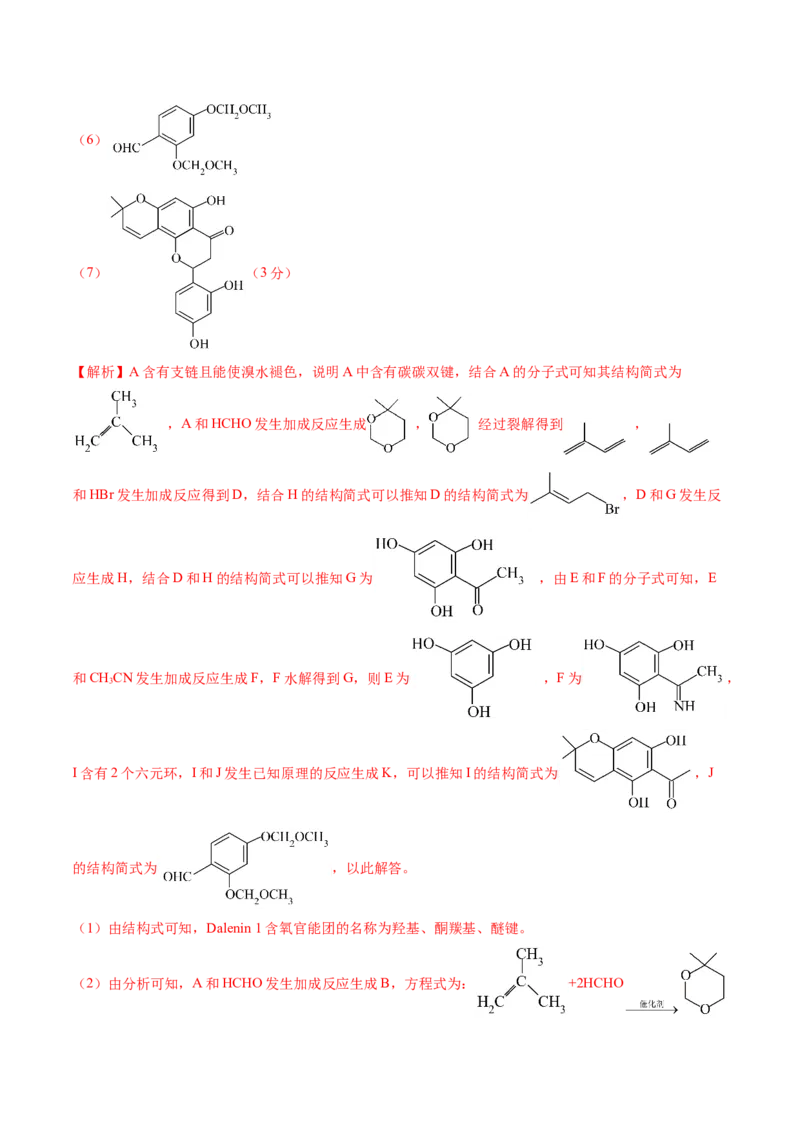
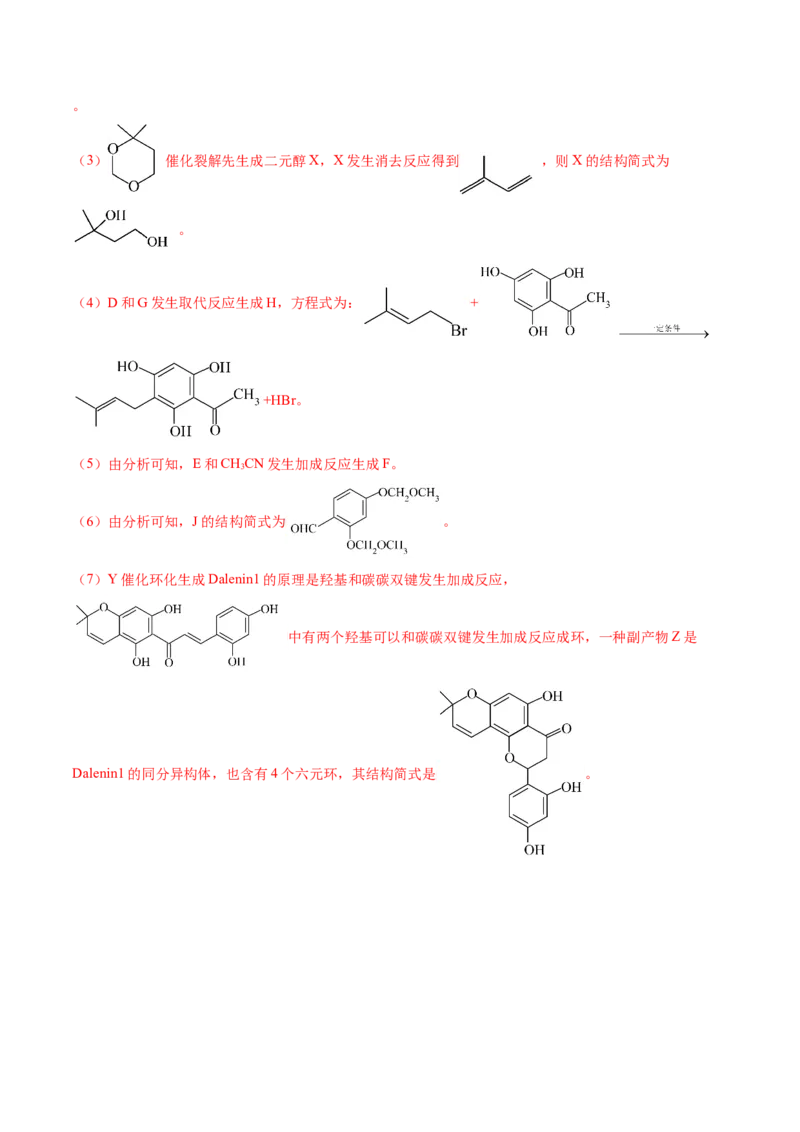
文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷08
(考试时间:50分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Cl 35.5 Fe 56 Ga 70
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.科技发展迅猛离不开材料的不断更新和优化。下列说法正确的是
A.制作火箭所使用的材料均为钢铁
B.新型电池的电极材料石墨烯属于有机高分子化合物
C.天宫二号卫星所使用的高性能计算机芯片含有硅单质
D.新型餐具聚乳酸(聚2-羟基丙酸)的结构为
【答案】C
【解析】A.钢铁是制作火箭所使用的主流材料,故A错误;
B.石墨烯属于新型无机非金属材料,故B错误;
C.硅单质可用于制备计算机芯片,故C正确;
D.聚2-羟基丙酸的结构为 ,故D错误;
故答案选C。
8.设 为阿伏加德罗常数的值。下列说法正确的是
A.在标准状况下, 分子中含氯原子数目为
B.1LpH均为2的硫酸和醋酸溶液,氢离子数均为
C.64g铜与足量硫粉加热充分反应,转移电子数为
D.30g由乙酸和葡萄糖组成的混合物中含氢原子个数为
【答案】D
【解析】A.在标准状况下, 呈液态,不能根据气体摩尔体积计算其物质的量或原子数目,A错误;
B.pH为2的硫酸、醋酸中 ,1L溶液中所含 ,B错
误;
C.Cu与S反应的产物为 ,1molCu参加反应时转移电子数为 ,C错误;D.30g乙酸和葡萄糖的混合物相当于1mol“ ”,含氢原子的物质的量为2mol,D正确;
故选D。
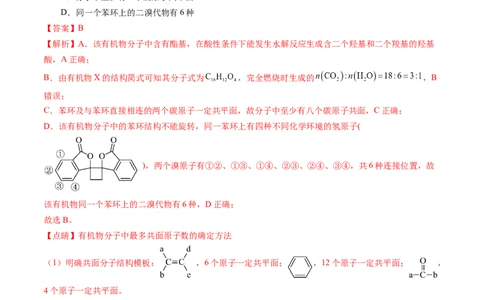
9.有机物X可用于合成抗菌药物,X的结构简式为 。下列有关X的说法错误的是
A.酸性条件下能发生水解反应得到羟基酸
B.完全燃烧时生成的
C.分子中至少有8个碳原子共平面
D.同一个苯环上的二溴代物有6种
【答案】B
【解析】A.该有机物分子中含有酯基,在酸性条件下能发生水解反应生成含二个羟基和二个羧基的羟基
酸,A正确;
B.由有机物X的结构简式可知其分子式为 ,完全燃烧时生成的 ,B
错误;
C.苯环及与苯环直接相连的两个碳原子一定共平面,故分子中至少有八个碳原子共面,C正确;
D.该有机物分子中的苯环结构不能旋转,同一苯环上有四种不同化学环境的氢原子(
),两个溴原子有①②、①③、①④、②③、②④、③④,共6种连接位置,故
该有机物同一个苯环上的二溴代物有6种,D正确;
故选B。
【点睛】有机物分子中最多共面原子数的确定方法
(1)明确共面分子结构模板: ,6个原子一定共平面; ,12个原子一定共平面; ,
4个原子一定共平面。
(2)最多共面原子数的确定:若几个共面模板有共用原子,则几个共面模板上的原子有可能位于同一平
面上。
(3)位于共面模板端点上的“ ”中还有一个氢原子也可能位于相应的平面上。
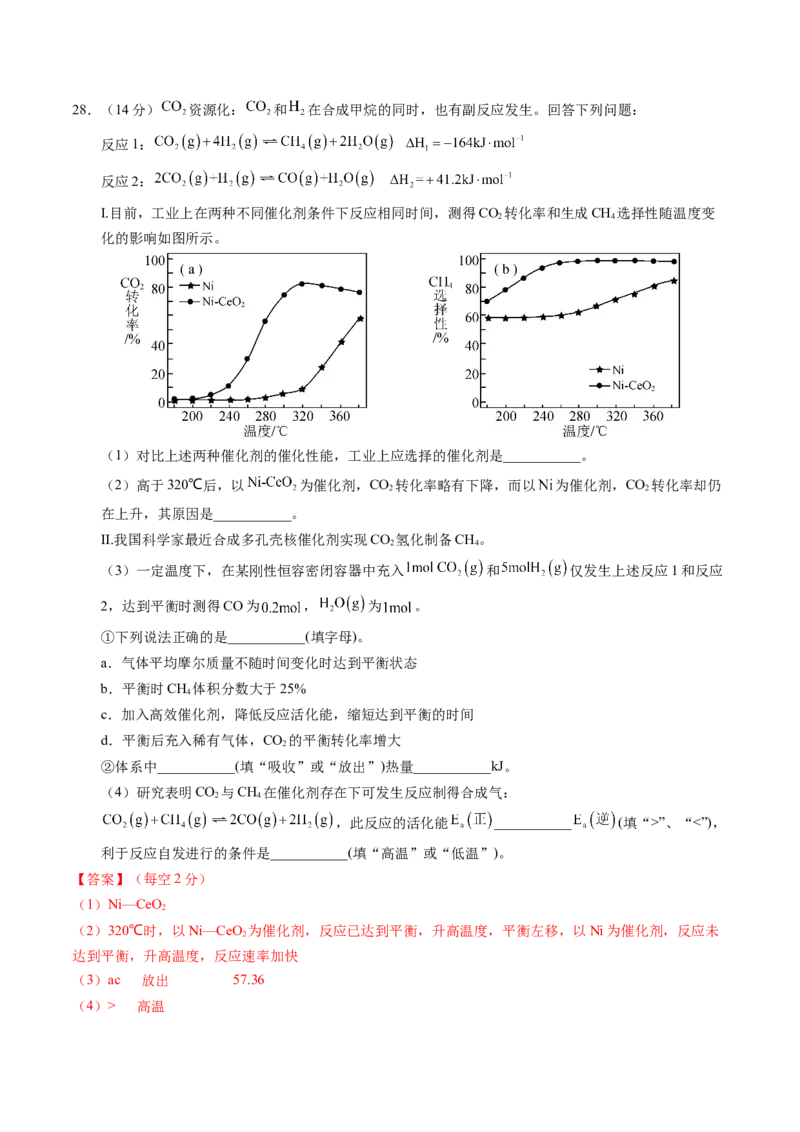
10.N、CO 与 Fe+体系中存在如图 1 所示物质转变关系,已知 Fe+ (s)与中间产物 NO(g) 反应过程中的
2 2 2
能量变化如图2所示。下列说法错误的是A.∆H=-(∆H +∆H +∆H )
1 2 3
B.Fe+在反应中作催化剂,能降低反应的活化能
C.∆H 和∆H 均小于 0
1 2
D.由图 2 可知,反应 Fe+ (s)+NO(g)=FeO+(s) +N (g) ∆H <0
2 2 4
【答案】C
【解析】A.根据图示可知,N(g)+CO (g)=NO(g)+CO(g) ΔH,NO(g)=O(g)+N (g) ΔH ,O(g)+Fe+(s)=FeO+
2 2 2 2 2 1
(s) ΔH,FeO+(s)+CO(g)= Fe+(s)+ CO (g) ΔH ,根据盖斯定律可知,第一个反应=后面三个反应之和的逆反
2 2 3
应,∆H=-(∆H +∆H +∆H ),A正确;
1 2 3
B.从图1中可知,Fe+为反应的催化剂,可降低反应的活化能,B正确;
C.从图2中可知,Fe+(s)+ N O(g)= FeO+(s)+ N (g) ΔH<0,ΔH=(ΔH+ΔH ),只能说明(ΔH +ΔH )<0,不能说
2 2 1 2 1 2
明∆H 和∆H 均小于0,C错误;
1 2
D.ΔH=生成物总能量-反应物总能量,Fe+(s)+ N O(g)= FeO+(s)+ N (g) ΔH<0,D正确;
2 2
故答案选C。
11.北宋名画《千里江山图》历经千年色彩依然,其青色来自青金石,它含有H、O、Si元素,以及X、
Y、Z、M、Q等前20号元素,X、Y、Z、M同周期,Z的原子序数小于M,Z最高价氧化物对应水化
物0.005mol·L-1的pH=2。X、Y、Z、M原子的最外层电子数之和为17,Q与青金石中其他7种元素均
不同周期也不同族。下列说法错误的是
A.X、Y的单质都能形成氧化物保护膜
B.金属活动性强弱:X
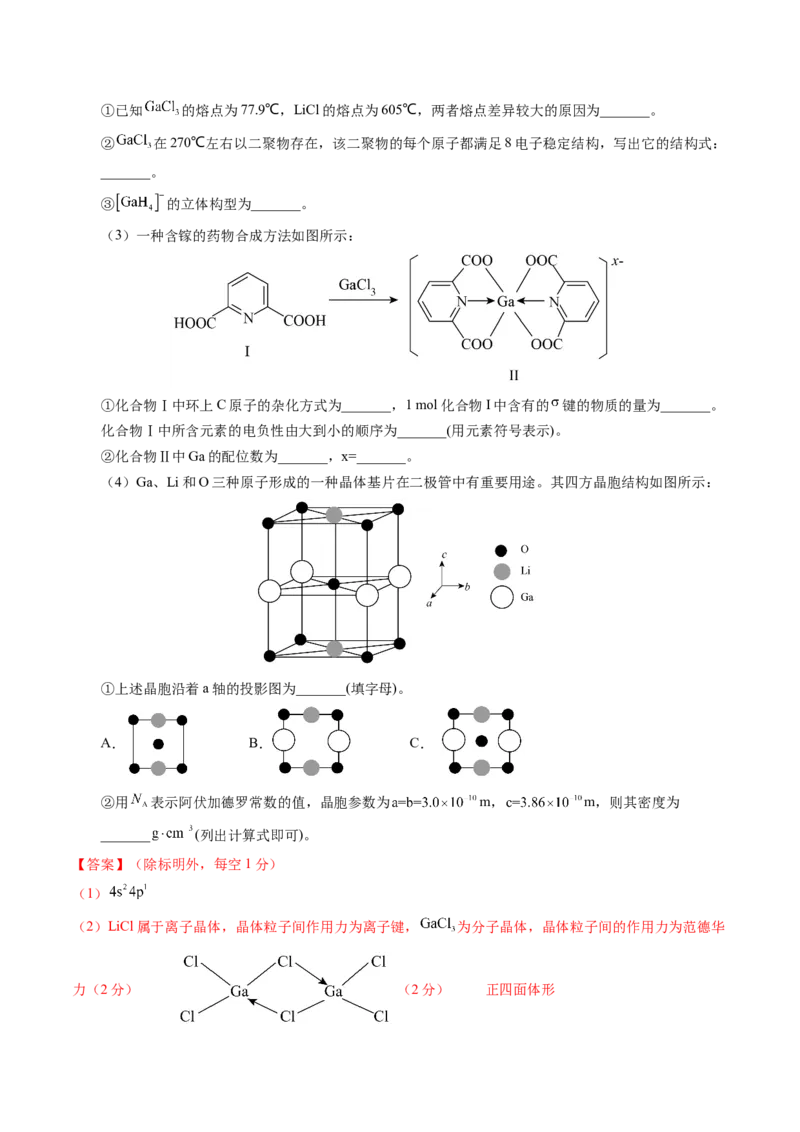
”、“<”), 利于反应自发进行的条件是___________(填“高温”或“低温”)。 【答案】(每空2分) (1)Ni—CeO 2 (2)320℃时,以Ni—CeO 为催化剂,反应已达到平衡,升高温度,平衡左移,以Ni为催化剂,反应未 2 达到平衡,升高温度,反应速率加快 (3)ac 放出 57.36 (4)> 高温【解析】(1)由图可知,相同温度时,以Ni—CeO 为催化剂的反应的二氧化碳转化率和甲烷的选择性均 2 大于以Ni为催化剂,所以工业上应选择的催化剂是Ni—CeO 的反应,故答案为:Ni—CeO; 2 2 (2)由图可知,320℃时以Ni—CeO 为催化剂的反应的二氧化碳转化率达到平衡,该反应为放热反应,高 2 于320℃后,升高温度,平衡向逆反应方向移动,二氧化碳的转化率减小,以Ni为催化剂的反应未达到平 衡,升高温度,化学反应速率加快,二氧化碳的转化率增大,故答案为:320℃时,以Ni—CeO 为催化剂, 2 反应已达到平衡,升高温度,平衡左移,以Ni为催化剂,反应未达到平衡,升高温度,反应速率加快; (3)设平衡时生成甲烷的物质的量为amol,由题意可建立如下三段式: 由水蒸气的物质的量为1可得:2a+0.2=1,解得a=0.4,则平衡时甲烷体积分数为 ×100%≈7.1%; ①a.由质量守恒定律可知,反应前后气体的质量相等,反应1和反应2均为气体体积减小的反应,反应 中气体平均摩尔质量增大,则气体平均摩尔质量不随时间变化说明正逆反应速率相等,反应达到平衡状态, 故正确; b.由分析可知,平衡时甲烷体积分数为7.1%,小于25%,故错误; c.加入高效催化剂,能降低反应活化能,加快反应速率,缩短达到平衡的时间,故正确;d.刚性恒容密 闭容器中,平衡后充入不参与反应的稀有气体,平衡体系中各物质的浓度不变,化学平衡不移动,二氧化 碳的平衡转化率不变,故错误; ②由三段式数据可知,反应1放出的热量为164kJ/mol×0.4mol=65.6kJ,反应2吸收的热量为41.2kJ/ mol×0.2mol=8.24kJ,则反应放出的热量为65.6kJ—8.24kJ=57.36kJ,故答案为:放出;57.36; (4)由盖斯定律可知,反应2—反应1可得反应 ,则反应的焓变 ΔH=(+41.2kJ/mol)— (—164kJ/mol=+205.2kJ/mol,该反应为正反应活化能大于逆反应活化能的吸热反应, 由方程式可知,该反应为气体体积增大的反应,反应的ΔS>0,则高温条件下反应ΔH—TΔS<0,反应能自 发进行,故答案为:>;高温。 (二)选考题:共15分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。 35.[化学——选修3:物质结构与性质](15分) 镓及其化合物在合金工业、制药工业、电池工业有广泛的应用。回答下列问题: (1)基态Ga原子的价层电子排布式为_______。 (2) 是一种温和的还原剂,其可由 和过量的LiH反应制得: 。①已知 的熔点为77.9℃,LiCl的熔点为605℃,两者熔点差异较大的原因为_______。 ② 在270℃左右以二聚物存在,该二聚物的每个原子都满足8电子稳定结构,写出它的结构式: _______。 ③ 的立体构型为_______。 (3)一种含镓的药物合成方法如图所示: ①化合物Ⅰ中环上C原子的杂化方式为_______,1 mol化合物I中含有的 键的物质的量为_______。 化合物Ⅰ中所含元素的电负性由大到小的顺序为_______(用元素符号表示)。 ②化合物Ⅱ中Ga的配位数为_______,x=_______。 (4)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示: ①上述晶胞沿着a轴的投影图为_______(填字母)。 A. B. C. ②用 表示阿伏加德罗常数的值,晶胞参数为 m, m,则其密度为 _______ (列出计算式即可)。 【答案】(除标明外,每空1分) (1) (2)LiCl属于离子晶体,晶体粒子间作用力为离子键, 为分子晶体,晶体粒子间的作用力为范德华 力(2分) (2分) 正四面体形(3) 17 mol O>N>C>H 6 1 (4)C (3分) 【解析】(1)基态Ga原子的价层电子排布式为 ; (2)①镓和铝属于同一主族元素, 和 性质上相似,也为分子晶体,其熔点低于离子晶体 LiCi; ②结合二聚体和每个原子都满足8电子稳定结构的信息,可推测Ga的空轨道应该会与Cl的孤对电子成配 位键,可写出结构式为 ; ③ 的中心原子Ga的价层电子对数为4+ ,没有孤对电子,所以其立体构型为正 四面体形。 (3)①吡啶环的结构与苯环相似,故C原子采用 杂化;化合物Ⅰ除了环上6个 键,其他 键如图所 示: ,1 mol化合物Ⅰ中总共有17 mol 键;Ⅰ中含有四种元素O、N、 C、H,同周期元素,从左到有,半径减小,电负性增大,所以电负性由大到小的顺序为O>N>C>H; ②化合物Ⅱ中Ga的配位数为6,其中4个COOH失去H后显-1,化合物Ⅱ整体带1单位负电荷,所以 ; (4)①由晶胞结构可知,顶点和体心是O,上下面心是Li,棱上是Ga,沿着a轴的投影应为C。 ②晶胞中含有的原子数Li: ,Ga: ,O: ,则晶胞的密度 。 36.[化学——选修5:有机化学基础](15分) Dalenin 1( )对酪氨酸酶有很强的抑制活性,在制药工程和化妆品行业有 巨大的潜在应用价值。已知: (1)Dalenin 1含氧官能团的名称_______。 (2)A含有支链且能使溴水褪色,A生成B的化学方程式是_______。 (3)B催化裂解先生成二元醇X,X转化为C,X的结构简式是_______。 (4)D+G→H的化学方程式是_______。 (5)E→F的反应类型是_______。 (6)I含有2个六元环,J的结构简式是_______。 (7)K先生成中间体Y( ),Y催化环化生成Dalenin1时存在多种 副产物。一种副产物Z是Dalenin1的同分异构体,也含有4个六元环,其结构简式是_______。 【答案】(除标明外,每空2分) (1)羟基、酮羰基、醚键 (2) +2HCHO (3) (4) + +HBr (5)加成反应(6) (7) (3分) 【解析】A含有支链且能使溴水褪色,说明A中含有碳碳双键,结合A的分子式可知其结构简式为 ,A和HCHO发生加成反应生成 , 经过裂解得到 , 和HBr发生加成反应得到D,结合H的结构简式可以推知D的结构简式为 ,D和G发生反 应生成H,结合D和H的结构简式可以推知G为 ,由E和F的分子式可知,E 和CHCN发生加成反应生成F,F水解得到G,则E为 ,F为 , 3 I含有2个六元环,I和J发生已知原理的反应生成K,可以推知I的结构简式为 ,J 的结构简式为 ,以此解答。 (1)由结构式可知,Dalenin 1含氧官能团的名称为羟基、酮羰基、醚键。 (2)由分析可知,A和HCHO发生加成反应生成B,方程式为: +2HCHO。 (3) 催化裂解先生成二元醇X,X发生消去反应得到 ,则X的结构简式为 。 (4)D和G发生取代反应生成H,方程式为: + +HBr。 (5)由分析可知,E和CHCN发生加成反应生成F。 3 (6)由分析可知,J的结构简式为 。 (7)Y催化环化生成Dalenin1的原理是羟基和碳碳双键发生加成反应, 中有两个羟基可以和碳碳双键发生加成反应成环,一种副产物Z是 Dalenin1的同分异构体,也含有4个六元环,其结构简式是 。