文档内容
(5)电化学——2025届高考化学二轮复习易错重难提升【新高考】
一、易错点分析
考点一 原电池 新型化学电源
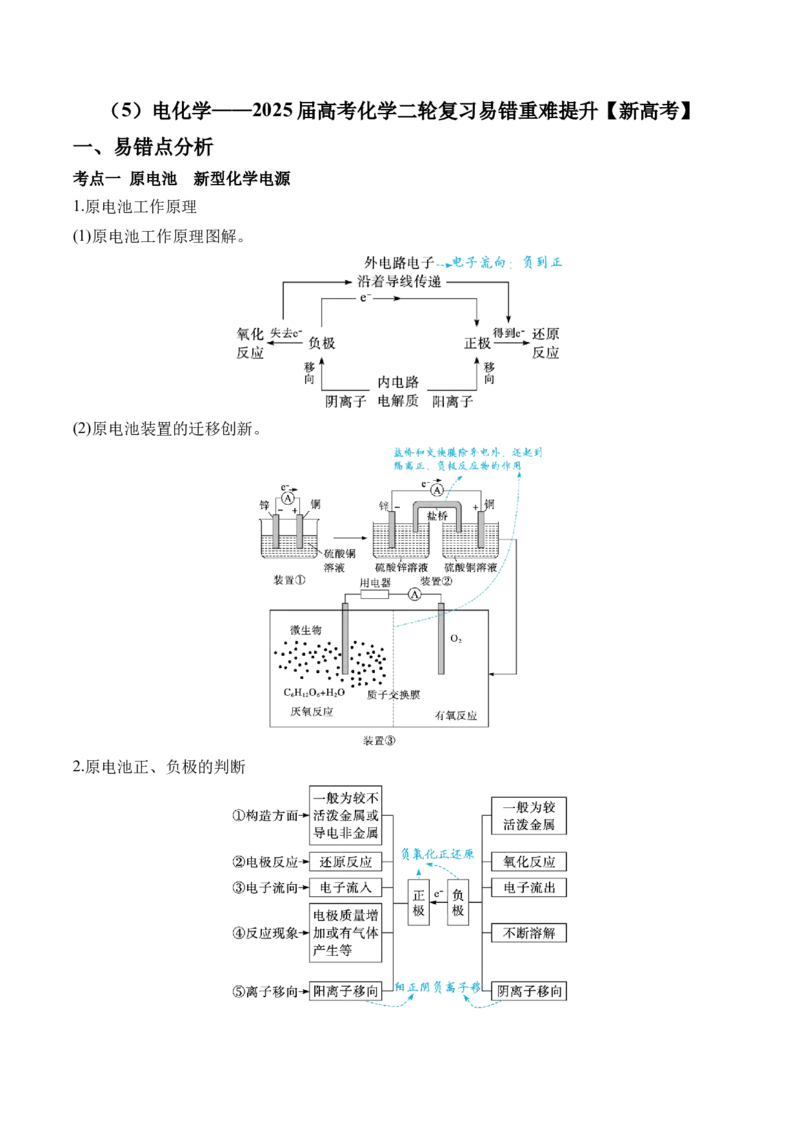
1.原电池工作原理
(1)原电池工作原理图解。
(2)原电池装置的迁移创新。
2.原电池正、负极的判断3.新型化学电源中电极反应式的书写方法
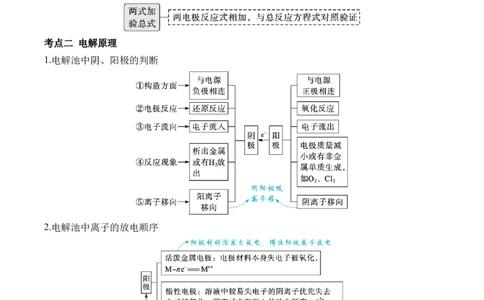
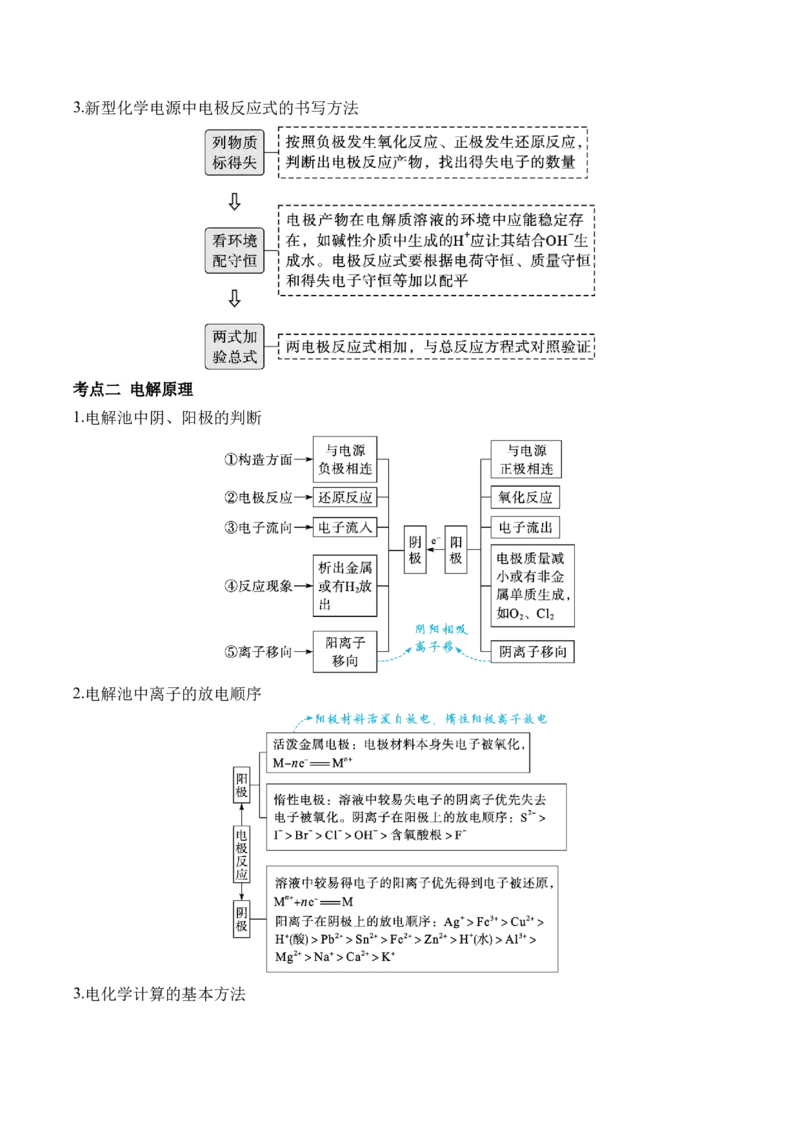
考点二 电解原理
1.电解池中阴、阳极的判断
2.电解池中离子的放电顺序
3.电化学计算的基本方法考点三 金属的腐蚀与防护
1.金属的电化学腐蚀(以铁的电化学腐蚀为例)
2.金属电化学保护的两种方法
二、易错训练
1.某同学设计的原电池装置如图所示。电池工作时,下列说法正确的是( )A.锌片作正极 B.盐酸作为电解质溶液
C.电能转化为化学能 D.电子由铜片经导线流向锌片
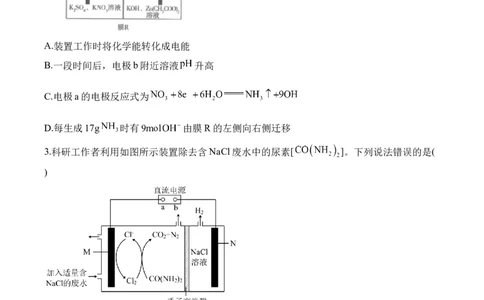
2.香港城市大学科研人员开发一种电极材料 (四氨基苯醌铜)可实现高效率地将硝
酸根转化为氨,工作原理如图所示。下列叙述错误的是( )
A.装置工作时将化学能转化成电能
B.一段时间后,电极b附近溶液 升高
C.电极a的电极反应式为
D.每生成17g 时有9mol 由膜R的左侧向右侧迁移
3.科研工作者利用如图所示装置除去含NaCl废水中的尿素[ ]。下列说法错误的是(
)
A.b为直流电源的负极
B.工作时,废水中NaCl的浓度保持不变
C.工作时,N极区NaCl溶液的质量基本不变
D.若导线中通过6mol电子,则理论上生成1mol
4.一次性纸电池加水就可以激活,可用来驱动低功率电子器件,其基本结构如图所示,下列
说法错误的是( )A.用乙醇代替水也可以激活该电池
B.“油墨混有锌粉”为电池的负极
C.正极电极反应式:
D.激活时水用量过多浸没电池,可能造成电源无法正常工作
5.在直流电场作用下双极膜中间层中的 解离为 和 ,并分别向两极迁移。如图所示
装置,可将捕捉的二氧化碳转化为 而矿化封存,减少碳排放,同时得到氧气、氢气、
高浓度盐酸等产品。下列说法正确的是( )
A.电极a的电势高于电极b的电势
B.两个双极膜中间层的 均向右移动
C.去掉双极膜,两极的电极反应式不变
D.电极b为阴极,电极反应式为
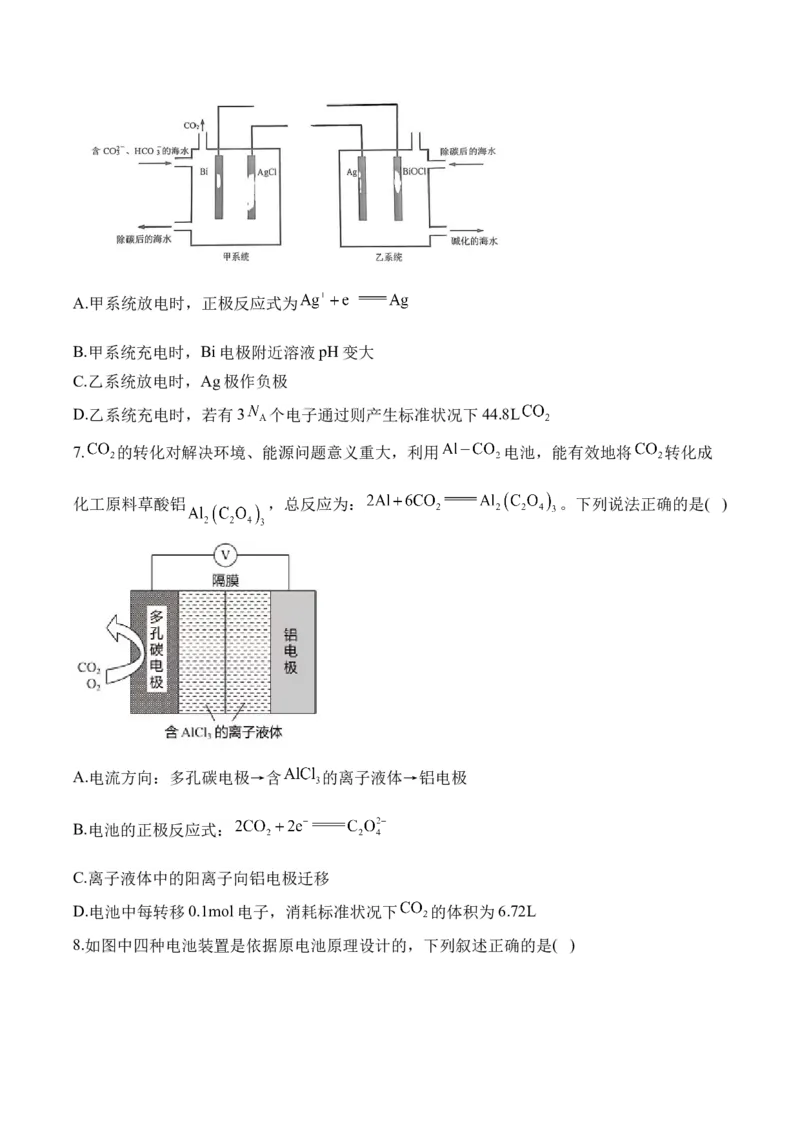
6.最新研究发现一种“氧介导电化学pH变化”系统,通过调节海水的pH去除海水中 ,
电化学原理为 ,甲系统放电时的原理如图所
示,该装置可实现充放电交替运行,达到节约成本的目的;碱化的海水继续吸收空气中的
可缓解温室效应。下列说法正确的是( )A.甲系统放电时,正极反应式为
B.甲系统充电时,Bi电极附近溶液pH变大
C.乙系统放电时,Ag极作负极
D.乙系统充电时,若有3 个电子通过则产生标准状况下44.8L
7. 的转化对解决环境、能源问题意义重大,利用 电池,能有效地将 转化成
化工原料草酸铝 ,总反应为: 。下列说法正确的是( )
A.电流方向:多孔碳电极→含 的离子液体→铝电极
B.电池的正极反应式:
C.离子液体中的阳离子向铝电极迁移
D.电池中每转移0.1mol电子,消耗标准状况下 的体积为6.72L
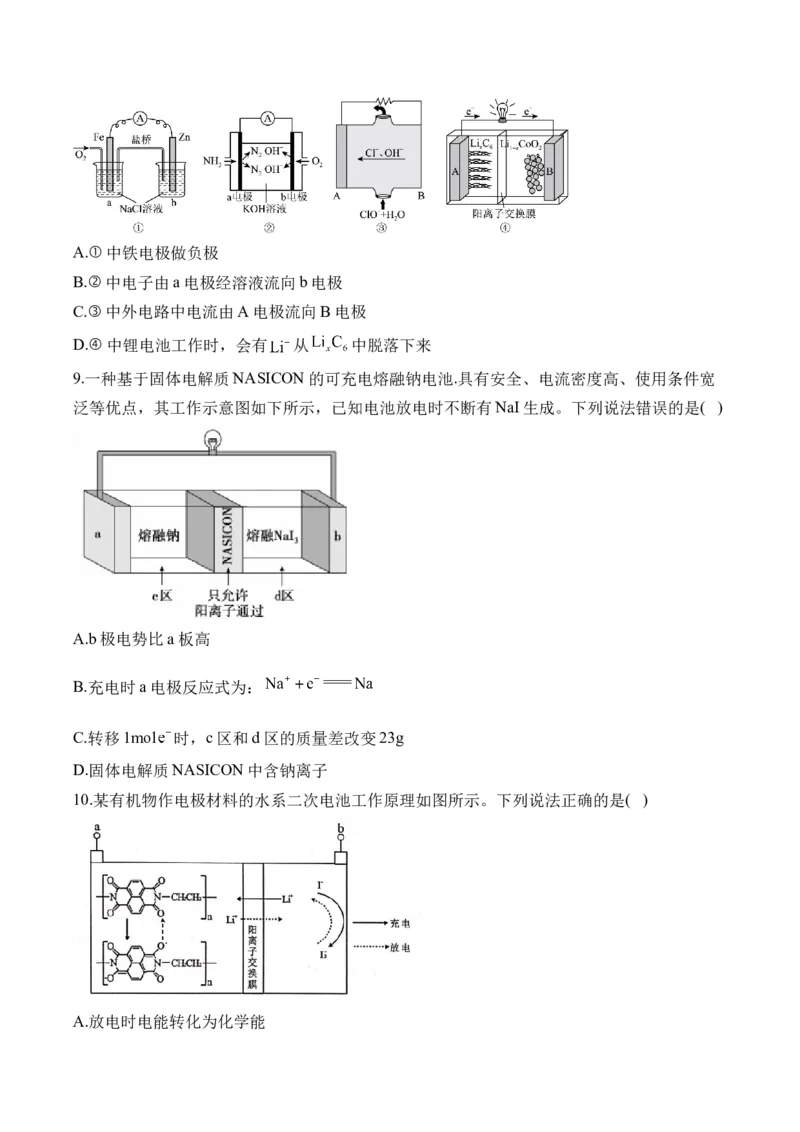
8.如图中四种电池装置是依据原电池原理设计的,下列叙述正确的是( )A.①中铁电极做负极
B.②中电子由a电极经溶液流向b电极
C.③中外电路中电流由A电极流向B电极
D.④中锂电池工作时,会有 从 中脱落下来
9.一种基于固体电解质NASICON的可充电熔融钠电池.具有安全、电流密度高、使用条件宽
泛等优点,其工作示意图如下所示,已知电池放电时不断有NaI生成。下列说法错误的是( )
A.b极电势比a板高
B.充电时a电极反应式为:
C.转移1mol 时,c区和d区的质量差改变23g
D.固体电解质NASICON中含钠离子
10.某有机物作电极材料的水系二次电池工作原理如图所示。下列说法正确的是( )
A.放电时电能转化为化学能B.充电时a接电源正极
C.充电时阴极电极反应为:
D.放电时每转移1mole,右室离子数目增加2mol
11.一种新型电解池如图所示,可实现废水中硝酸根制氨和硫化氢制硫的双污染物的升级回收
利用。下列说法不正确的是( )
A.a为电源正极,电极Ⅰ发生氧化反应
B.阴极电极反应式:
C.若处理含 废水,理论上交换膜通过
D.电解一段时间后,阳极附近的溶液的 不变
12.以普鲁士黄[ ]为代表的新型可充电钠离子电池,其放电工作原理、充放电过程中
正极材料中普鲁士黄晶胞的组成变化如图所示。下列说法错误的是( )A.每个普鲁士黄晶胞转化为普鲁士蓝晶胞时,转移电子数为4, 个数增多
B.充电时阳极反应可能为
C.充电时, 通过离子交换膜从左室移向右室
D.放电时外电路通过 电子时, 箔、 箔质量变化分别为 、
13.1799年意大利物理学家伏打发明了伏打电池,其在早期被称为“电堆”。他把金属条浸入
强酸溶液中时,发现在两个金属条间产生了稳定而又强劲的电流。他又用不同的金属进行实
验,发现铜和锌是最合适的金属,并发明了伏打电池(即为原电池的原型)。如图是伏打电
堆的一种,下列有关该电池的说法正确的是( )
A.若湿布片所含的为饱和食盐水,则在电池工作时,铜片附近会有 产生B.该电池正极电极反应式为
C.电池工作一段时间后,湿布片上可能会有 产生
D.电池工作一段时间后,电池质量一定不会变
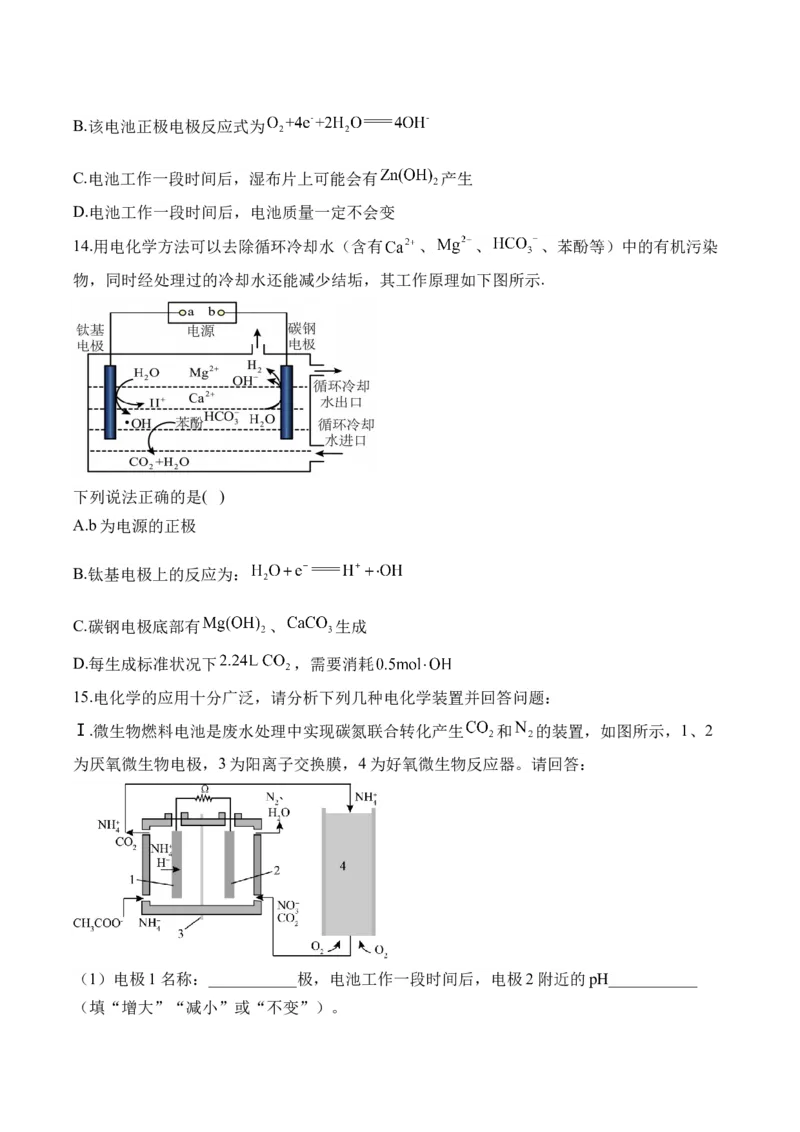
14.用电化学方法可以去除循环冷却水(含有 、 、 、苯酚等)中的有机污染
物,同时经处理过的冷却水还能减少结垢,其工作原理如下图所示.
下列说法正确的是( )
A.b为电源的正极
B.钛基电极上的反应为:
C.碳钢电极底部有 、 生成
D.每生成标准状况下 ,需要消耗
15.电化学的应用十分广泛,请分析下列几种电化学装置并回答问题:
Ⅰ.微生物燃料电池是废水处理中实现碳氮联合转化产生 和 的装置,如图所示,1、2
为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
(1)电极1名称:___________极,电池工作一段时间后,电极2附近的pH___________
(填“增大”“减小”或“不变”)。(2)电极1的电极反应式为___________。
(3)若好氧微生物反应器中消耗 (标准状况)4.48L,理论上电极2生成 物质的量为
___________mol。
Ⅱ.次磷酸钴(Ⅱ) 广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四
室电渗析槽电解法制备次磷酸钴,原理如图。
(4)A、B、C均为离子交换膜,其中为阳离子交换膜的是___________。
(5)石墨电极每生成 时,___________ 向___________迁移(填“阴极室”
“阳极室”或“产品室”)。
(6)该小组同学用图3装置进行实验时发现,Y极溶液逐渐变成紫红色。若氢氧化钠溶液浓
度过高,铁电极区会产生红褐色物质。
查阅资料知:高铁酸根离子( )在溶液中呈紫红色, 只在强碱性条件下稳定。
①电解过程中,X极附近溶液的pH___________(填“增大”“减小”或“不变”)。
②电解过程中,Y极溶液逐渐变成紫红色,则产生该现象对应发生的电极反应式为:
___________。
③ 随初始 的变化如图4,分析 变化趋势不同的原因:
___________。
答案以及解析1.答案:B
解析:A选项:由分析可知Zn作负极,Cu做正极,故A错误;B选项:盐酸作为电解质溶
液,故B正确;C选项:原电池是将化学能转化为电能的装置,故C错误;D选项:电子由
负极经导线流向正极,即电子由Zn片经导线流向Cu片,故D错误;故选B。
2.答案:BD
解析:该装置为原电池装置,工作时将化学能转化为电能,A项正确;电极b的电极反应式
为 , 降低,B项错误;电极a为正极,发生还原反应,
电极反应式为 ,C项正确;根据得失电子数确定迁移电
荷数,为了维持电荷守恒,每生成17g 时有8mol 由膜R的左侧向右侧迁移,D项错
误。
3.答案:B
解析:A.由图知,N极区生成 ,N极作阴极,b为直流电源的负极,故A正确;
B.工作时,阳极区的反应为 、
,氢离子通过质子交换膜进入阴极区,
阳极消耗水而使废水中 的浓度增大,故B错误;
C.工作时, 由M极区通过质子交换膜移向N极区,转移相同量的电子, 极区产生的
质量与 进入N极区的质量相等,N极区NaCl溶液的质量基本不变,故C正确;
D.阳极区的反应为 、
,若导线中通过6 电子,理论上应
生成1 ,故D正确;
选B。
4.答案:A
解析:A.加入乙醇后无法形成电解质溶液,不满足原电池构成条件,A错误;B.“油墨混有锌粉”为电池的负极,发生氧化反应,B正确;
C.“油墨混有石墨”为电池的负极,发生还原反应,电极反应式: ,C
正确;
D.激活时水用量过多浸没电池,空气中氧气无法在正极发生还原反应,可能造成电源无法正
常工作,D正确;
答案选A。
5.答案:B
解析:根据酸室中得到高浓度盐酸可知,中间室的 通过阴离子交换膜移向酸室,判断电极
a为阴极,电极b为阳极,据此分析。A项,电极a的电势低于电极b的电势,A项错误;B
项,由图可知,电极b是阳极,右侧双极膜中 进入酸室生成盐酸, 向右迁移进入阳极
室,电极a为阴极,左侧双极膜中 向左迁移进入阴极室, 向右迁移进入碱室,B项正
确;C项,去掉双极膜,电极b的电极反应变为 失电子,C项错误;D项,电极b是阳极,
应发生氧化反应,电极a为阴极,电极反应式为 ,D项错误。
6.答案:B
解析:B.甲系统充电时,该装置为电解池,BiOCl作阴极电极反应式为
,Bi电极附近溶液pH变大,故B正确。
7.答案:B
解析:该装置为原电池,由方程式知铝电极是负极,电极反应为 ,多孔碳电
极是正极,电极反应为 .多孔碳电极为原电池正极,铝电极为原电池负
极,外电路电流的方向是多孔碳电极→导线→铝电极,A项错误;根据总反应知,正极反应
为 ,B项正确;离子液体中的阳离子应向正极多孔碳电极迁移,C项错
误;根据 ,转移0.1mol电子,消耗标准状况下 为2.24L,D项错误。
8.答案:D
解析:D.根据电子流向,确定A电极 为负极, 电极失电子变为 ,故有 从上脱落,D正确;
故本题选D。
9.答案:C
解析:C选项转移1mol 时,c区和d区的质量差改变46g,错误
10.答案:D
解析:A.放电时化学能转化为电能,故A错误;B.由题干可知,该结构为一种负极材料为固
态聚酰亚胺-水系二次电池,则有机电极为负极发生氧化反应,充电时该极为电解池阴极,与
电源负极相连,故B错误;C.由图可知,充电时阴极反应式为
,故C错误;
D.放电时,右侧电极为正极,发生氧化反应, ,则放电时每转移2mol ,右
侧增加2mol阴离子,同时有2mol 离子进入右室,右室离子数目增加4mol,当转移1mol
时,右室离子数目增加2mol,故D正确。
11.答案:D
解析:D.阳极的电极反应式为 ,每生成1molS,有2mol 经过阴离子
交换膜到达阳极区,与气离子结合生成水,则电解一段时间后,阳极附近的溶液的pH增大,
故D错误。
12.答案:D
解析:D.放电时,Mo箔作正极,电极反应式为 ,外电
路中通过0.2mol电子时,阳极质量减少 ,Mg箔作负极失电子,电极
反应式为 ,通过0.2mol电子时,消耗Mg0.1mol,质量减少
0.1mol×24g/mol= 2.4g,故D错误;故选D。
13.答案:C
解析:当湿布片所含的溶液为饱和食盐水时,铜片为正极, 在铜片上得电子,铜片附近不会生成气体,A项错误;由于无法判断湿布片所含溶液酸碱性,所以无法判断电池具体的电
极反应式,B项错误;当湿布片所含溶液为碱性时,负极会产生 ,由于 在
等于8.1时开始沉淀,所以湿布片上可能会产生沉淀,C项正确;若湿布片所含的是饱和
食盐水,根据该原电池的工作原理可知,原电池在工作一段时间后,总质量会增加,增加的
质量来自于 ,D项错误。
14.答案:C
解析:A.碳电极上水得电子生成氢气,发生还原反应,为电解池的阴极,b为电源的负极,
故A错误;B.阳极失电子,发生氧化反应,钛基电极上的反应为 ,故
B错误;C.碳电极上水得电子生成氢气,
,碳钢电极底部有
生成,故C正确;D.钛基电极上的反应为
,每生成标准状况下2.24L ,需要消
耗0.1mol·OH,故D错误;故选C。
15.答案:(1)负;增大
(2)
(3)0.08
(4)AC
(5)2;产品室
(6)增大;
Fe6e 8OH FeO2 4H O
;随着 增大, 稳定性增强,
4 2
且反应较快,但c
OH
过高,Fe电极上有氢氧化铁生成,使 产率反而降低
解析:(1)由分析可知,电极1为负极;电池工作一段时间后,电极2上发生反应
2NO 10e 12H N 6H O,虽然负极迁移入一部分 ,但仍不能抵销反应消耗的
3 2 2
,所以电极2附近有一部分 被消耗,则电极2附近溶液的pH增大;(2)由分析可知,电极1为负极,反应为 ;
(4)Co电极为阳极,发生反应 , 透过离子交换膜A进入产品室,则
A为阳膜; 透过B膜进入产品室,则B为阴膜;石墨为阴极,水得到电子发生还原反
应生成氢气和氢氧根离子,发生反应 ,则 由原料室透过C膜
进入阴极室得到氢氧化钠,C为阳膜;故阳离子交换膜是AC;
(5)石墨电极反应为 ,石墨电极每生成1mol 时,转移2mol电
子,结合(4)分析可知,由2mol 迁移向产品室。