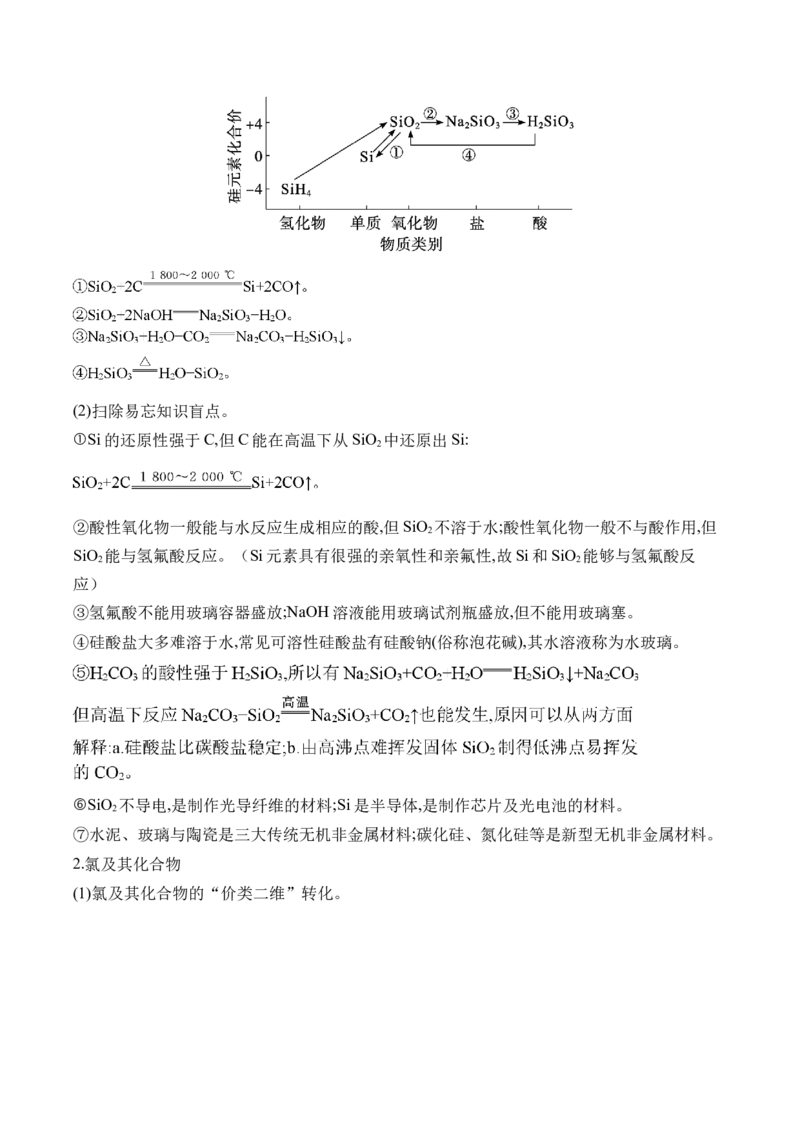文档内容
(6)元素及其化合物——2025届高考化学二轮复习易错重难提升【新高
考】
一、易错点分析
考点一 常见金属及其重要化合物
1.钠及其化合物
(1)钠及其化合物的“价类二维”转化。
(2)扫除易忘知识盲点。
①钠与盐溶液反应,不能置换出盐中的金属,钠与熔融的盐反应才可能置换出盐中的金属。
②Na与足量O 反应无论生成Na O还是Na O ,只要参与反应的Na的质量相等,则转移电子的
2 2 2 2
物质的量一定相等,但得到Na O 的质量大于Na O的质量。
2 2 2
③Na分别与H O和乙醇发生反应均能生成H ,但反应的剧烈程度不同,前者反应剧烈,后者反应
2 2
缓慢。
④1 mol Na O 参与反应转移电子的物质的量不一定为2 mol,如1 mol Na O 与足量CO 的反应
2 2 2 2 2
转移电子应为1 mol。
⑤除去CO 中的HCl气体,应选用饱和NaHCO 溶液;向饱和Na CO 溶液中通入过量CO ,有
2 3 2 3 2
NaHCO 晶体析出。
3
⑥焰色试验体现的是元素的性质,无论元素是游离态还是化合态,同一元素均具有相同的焰色,
焰色试验发生的不是化学变化。在观察钾元素的焰色时,应透过蓝色的钴玻璃片观察。焰色呈
黄色时,一定含有钠元素,但还可能含有钾元素。⑦Na O、Na O 中阴、阳离子个数比均为1∶2。
2 2 2
⑧Na O 与SO 反应的化学方程式是Na O +SO === Na SO ,而非2Na O +2SO ===
2 2 2 2 2 2 2 4 2 2 2
2Na SO +O 。
2 3 2
⑨Na O 投入品红溶液中,因溶液中有强氧化性物质,因而Na O 可使品红溶液褪色。Na O 投入
2 2 2 2 2 2
无色酚酞溶液中,酚酞溶液先变红后褪色
2.铝及其化合物
(1)铝及其化合物的“价类二维”转化。
(2)扫除易忘知识盲点。
①铝是活泼金属,但铝的抗腐蚀性强,因为铝的表面有一层致密的氧化物薄膜。由于Al O 的熔
2 3
点高于Al的熔点,故在酒精灯上加热铝箔直至熔化,熔化的铝并不滴落。
②铝热反应不仅指铝与Fe O 反应,铝热反应置换的金属为金属活动性比铝弱的难熔金属。
2 3
③Al、Al O 、Al(OH) 都既能与盐酸反应,也能与NaOH溶液反应。Al(OH) 不溶于氨水和碳酸,
2 3 3 3
所以实验室常利用铝盐与氨水反应制备Al(OH) ,偏铝酸盐与CO 反应制备Al(OH) 。
3 2 3
④Al(OH) 可用作抗酸药;明矾常用于净水。
3
⑤泡沫灭火器所用试剂为Al (SO ) 溶液和NaHCO 溶液,反应的离子方程式为
2 4 3 3
。
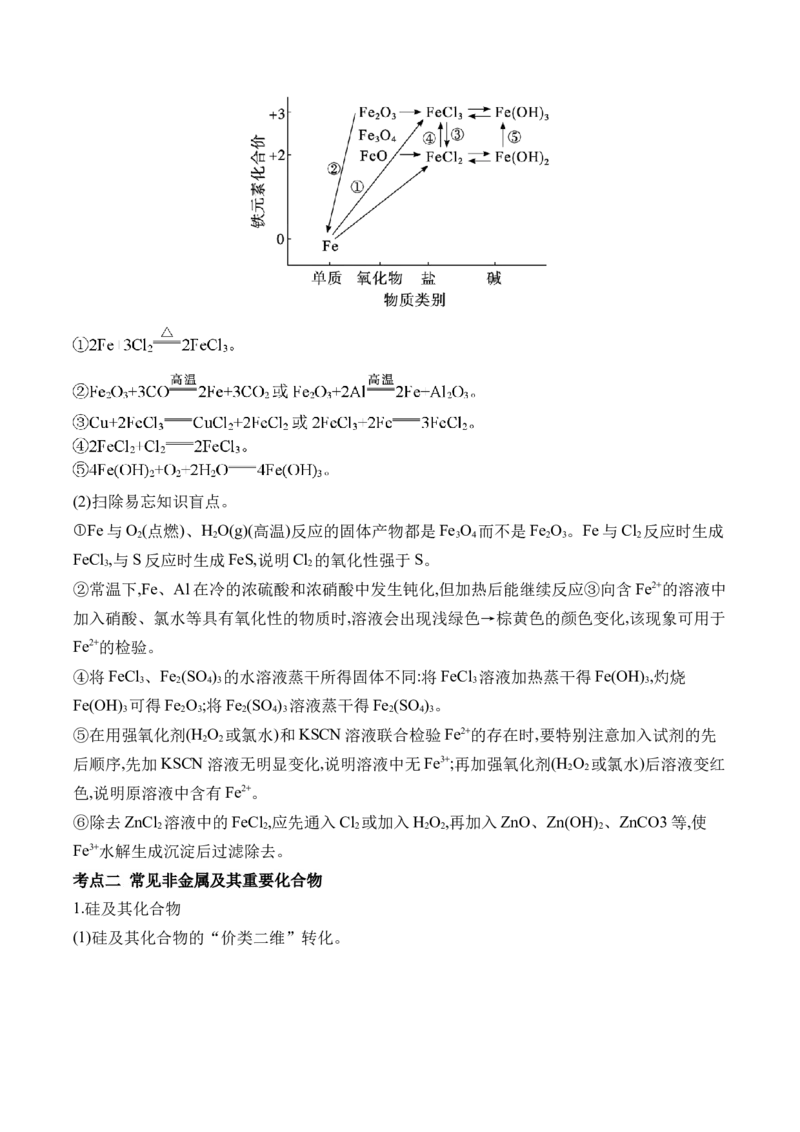
3.铁及其化合物
(1)铁及其化合物的“价类二维”转化。(2)扫除易忘知识盲点。
①Fe与O (点燃)、H O(g)(高温)反应的固体产物都是Fe O 而不是Fe O 。Fe与Cl 反应时生成
2 2 3 4 2 3 2
FeCl ,与S反应时生成FeS,说明Cl 的氧化性强于S。
3 2
②常温下,Fe、Al在冷的浓硫酸和浓硝酸中发生钝化,但加热后能继续反应③向含Fe2+的溶液中
加入硝酸、氯水等具有氧化性的物质时,溶液会出现浅绿色→棕黄色的颜色变化,该现象可用于
Fe2+的检验。
④将FeCl 、Fe (SO ) 的水溶液蒸干所得固体不同:将FeCl 溶液加热蒸干得Fe(OH) ,灼烧
3 2 4 3 3 3
Fe(OH) 可得Fe O ;将Fe (SO ) 溶液蒸干得Fe (SO ) 。
3 2 3 2 4 3 2 4 3
⑤在用强氧化剂(H O 或氯水)和KSCN溶液联合检验Fe2+的存在时,要特别注意加入试剂的先
2 2
后顺序,先加KSCN溶液无明显变化,说明溶液中无Fe3+;再加强氧化剂(H O 或氯水)后溶液变红
2 2
色,说明原溶液中含有Fe2+。
⑥除去ZnCl 溶液中的FeCl ,应先通入Cl 或加入H O ,再加入ZnO、Zn(OH) 、ZnCO3等,使
2 2 2 2 2 2
Fe3+水解生成沉淀后过滤除去。
考点二 常见非金属及其重要化合物
1.硅及其化合物
(1)硅及其化合物的“价类二维”转化。(2)扫除易忘知识盲点。
①Si的还原性强于C,但C能在高温下从SiO 中还原出Si:
2
②酸性氧化物一般能与水反应生成相应的酸,但SiO 不溶于水;酸性氧化物一般不与酸作用,但
2
SiO 能与氢氟酸反应。(Si元素具有很强的亲氧性和亲氟性,故Si和SiO 能够与氢氟酸反
2 2
应)
③氢氟酸不能用玻璃容器盛放;NaOH溶液能用玻璃试剂瓶盛放,但不能用玻璃塞。
④硅酸盐大多难溶于水,常见可溶性硅酸盐有硅酸钠(俗称泡花碱),其水溶液称为水玻璃。
⑥SiO 不导电,是制作光导纤维的材料;Si是半导体,是制作芯片及光电池的材料。
2
⑦水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材料。
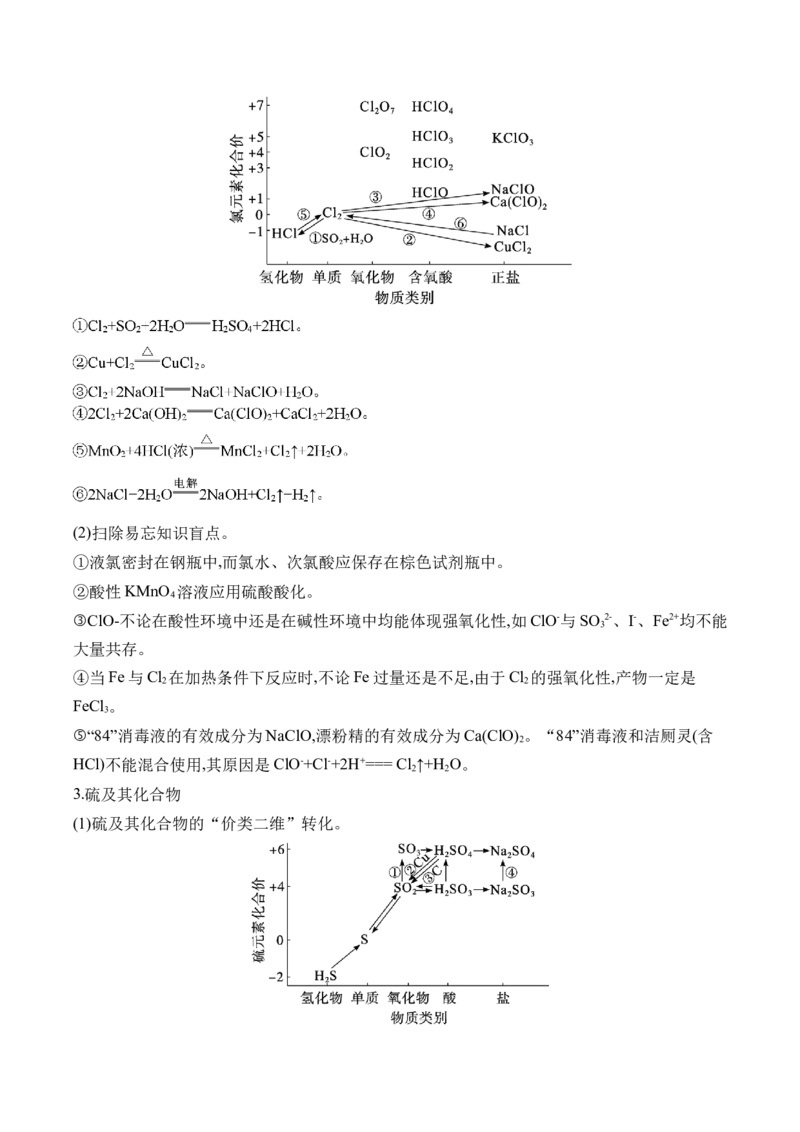
2.氯及其化合物
(1)氯及其化合物的“价类二维”转化。(2)扫除易忘知识盲点。
①液氯密封在钢瓶中,而氯水、次氯酸应保存在棕色试剂瓶中。
②酸性KMnO 溶液应用硫酸酸化。
4
③ClO-不论在酸性环境中还是在碱性环境中均能体现强氧化性,如ClO-与SO 2-、I-、Fe2+均不能
3
大量共存。
④当Fe与Cl 在加热条件下反应时,不论Fe过量还是不足,由于Cl 的强氧化性,产物一定是
2 2
FeCl 。
3
⑤“84”消毒液的有效成分为NaClO,漂粉精的有效成分为Ca(ClO) 。“84”消毒液和洁厕灵(含
2
HCl)不能混合使用,其原因是ClO-+Cl-+2H+=== Cl ↑+H O。
2 2
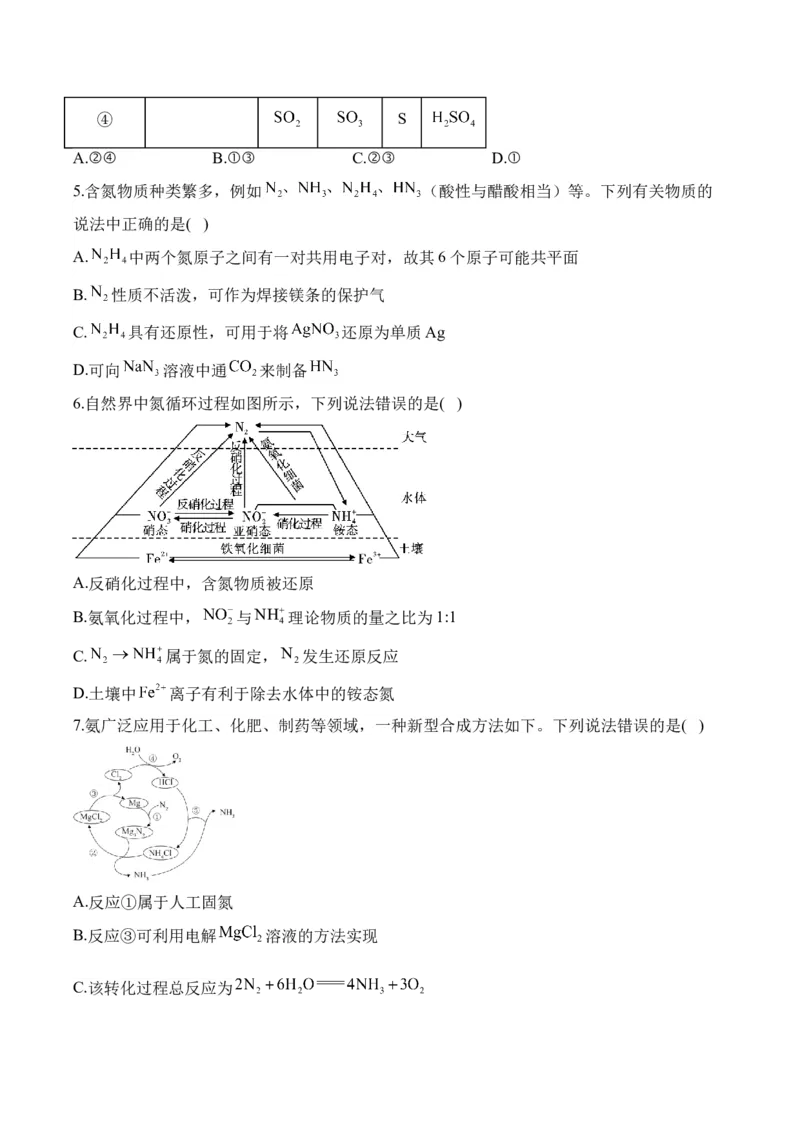
3.硫及其化合物
(1)硫及其化合物的“价类二维”转化。(2)扫除易忘知识盲点。
①除去附着在试管内壁上的硫,除了用热的NaOH溶液,还可以用CS ,但不能用酒精。
2
②SO 使含有酚酞的NaOH溶液褪色,表现SO 酸性氧化物的性质;使品红溶液褪色,表现SO 的
2 2 2
漂白性;使溴水、酸性KMnO4溶液褪色,表现SO 的还原性;SO 与H S反应,表现SO 的氧化
2 2 2 2
性;SO 和Cl 等体积混合通入溶液中,漂白性不但不增强,反而消失。
2 2
③把SO 气体通入BaCl 溶液中,没有沉淀生成,但再通入NH 或加入NaOH溶液,或把BaCl 溶
2 2 3 2
液改成Ba(NO ) 溶液,均有白色沉淀生成,前两者生成BaSO 沉淀,后者生成BaSO 沉淀。
3 2 3 4
④浓硝酸与Cu(足量)、浓硫酸与Cu(足量)、浓盐酸与MnO (足量)在反应时,随反应的进行,产
2
物会发生变化或反应停止。
⑤C与浓硫酸反应时,反应产物的检验应按以下流程进行:无水CuSO 检验水→品红溶液检验
4
SO →酸性KMnO 溶液除去SO →品红溶液检验SO 是否除净→澄清石灰水检验CO 。
2 4 2 2 2
4.氮及其化合物
(1)氮及其化合物的“价类二维”转化。(2)扫除易忘知识盲点。
①NO只能用排水法或气囊法收集;NO2的收集采用向上排空气法。
②在NO 或NO与O 通入水的计算中常用到两个化学方程式:
2 2
4NO+3O +2H O === 4HNO ,4NO +O +2H O === 4HNO 。
2 2 3 2 2 2 3
③浓硝酸显黄色是因为溶有NO ,而工业上制备的盐酸显黄色,是因为溶有Fe3+。
2
④硝酸、浓硫酸、次氯酸均具有强氧化性,属于氧化性酸。
⑤实验室制备NH ,除了用Ca(OH) 和NH Cl反应外,还可用浓氨水的分解(加NaOH固体或加
3 2 4
CaO或加热)制取。而检验NH +需用NaOH溶液并加热,根据湿润的红色石蕊试纸变蓝检验生
4
成的气体是NH ,以确定NH +的存在。
3 4
⑥收集NH 时,把一团干燥的棉花放在试管口,以防止氨与空气对流;收集完毕,进行尾气处理时,
3
应在试管口放一团用稀硫酸浸湿的棉花,以吸收NH 且防止污染空气。
3
二、易错训练
1.氧烛可用于潜艇或密闭空间供氧,由下表中物质压制成形,其原理为受热时,利用d区元
素形成的氧化物催化制氧剂分解产生 。下列说法正确的是( )
成
Al Fe
分
作 产生催化 吸收
燃烧物 制氧剂 定型剂
用 剂 剂
A.氧烛供氧时,Al燃烧为 分解提供能量
B.氧烛成分中的Fe也可以用Cu来代替
C. 吸收氯气时发生反应:
D.氧烛燃尽后残留物可以全部溶解在足量氢氧化钠溶液中
2.实验室用下图装置制备干燥的 并研究其性质。其中,a为湿润的淀粉KI试纸,b、c分别
为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。下列关于实验现象及 性质的说法中,不正确的是( )
A.一段时间后,观察到a变蓝 B.b褪色,说明 具有漂白性
C.b褪色而c不褪色,说明 能与水反应 D.d先变红,一段时间后褪色
3.氯元素是一种重要的“成盐元素”。部分含氯物质的分类与相应化合价关系如图所示。下
列说法不正确的是( )
A.存在f→d→b的转化关系
B.a溶液和f溶液混合可以制得b
C.d的稳定性差,其溶液久置即为a溶液
D.b具有漂白性,能将湿润的有色布条褪色
4.下列各组物质中,物质之间通过一步反应就能实现图示变化的是( )
物质转化关
物质编号 a b c d
系
① Fe
② NO
③ Na NaOH④ S
A.②④ B.①③ C.②③ D.①
5.含氮物质种类繁多,例如 (酸性与醋酸相当)等。下列有关物质的
说法中正确的是( )
A. 中两个氮原子之间有一对共用电子对,故其6个原子可能共平面
B. 性质不活泼,可作为焊接镁条的保护气
C. 具有还原性,可用于将 还原为单质Ag
D.可向 溶液中通 来制备
6.自然界中氮循环过程如图所示,下列说法错误的是( )
A.反硝化过程中,含氮物质被还原
B.氨氧化过程中,
与NH
理论物质的量之比为1:1
4
C. 属于氮的固定,N 发生还原反应
2
D.土壤中 离子有利于除去水体中的铵态氮
7.氨广泛应用于化工、化肥、制药等领域,一种新型合成方法如下。下列说法错误的是( )
A.反应①属于人工固氮
B.反应③可利用电解 溶液的方法实现
C.该转化过程总反应为D.反应⑤在无水环境中进行时有白烟产生
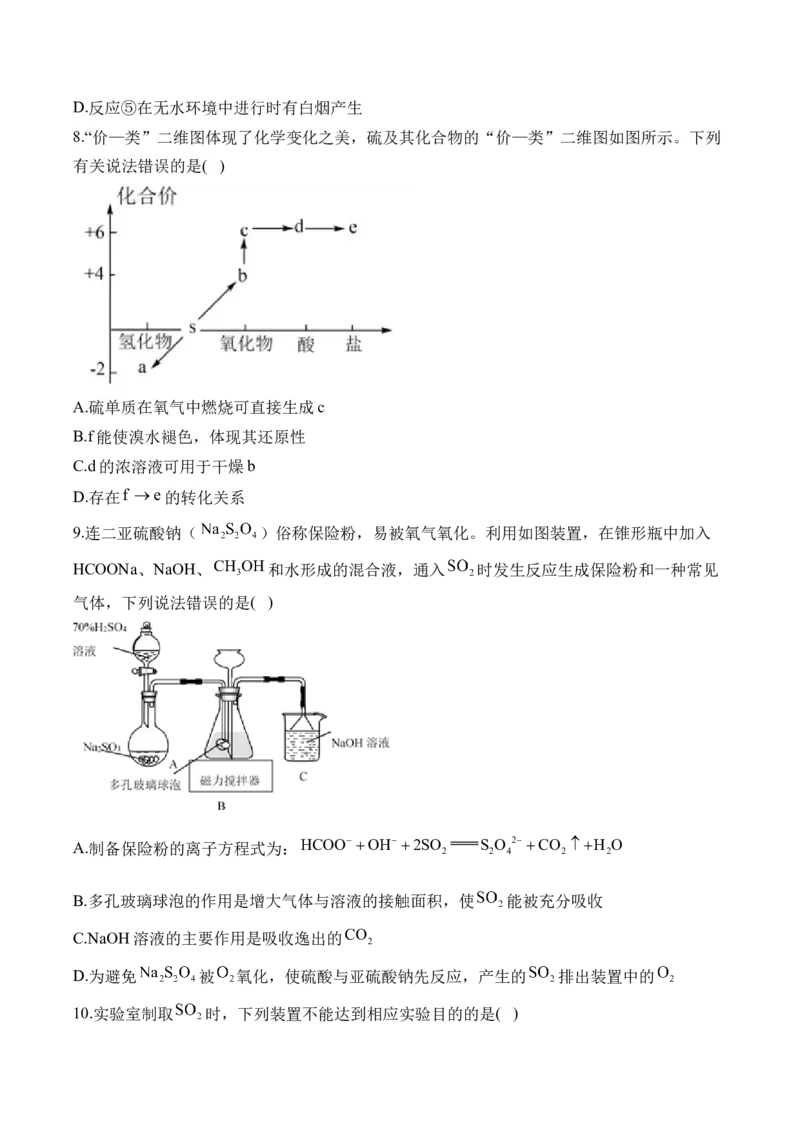
8.“价—类”二维图体现了化学变化之美,硫及其化合物的“价—类”二维图如图所示。下列
有关说法错误的是( )
A.硫单质在氧气中燃烧可直接生成c
B.f能使溴水褪色,体现其还原性
C.d的浓溶液可用于干燥b
D.存在f e的转化关系
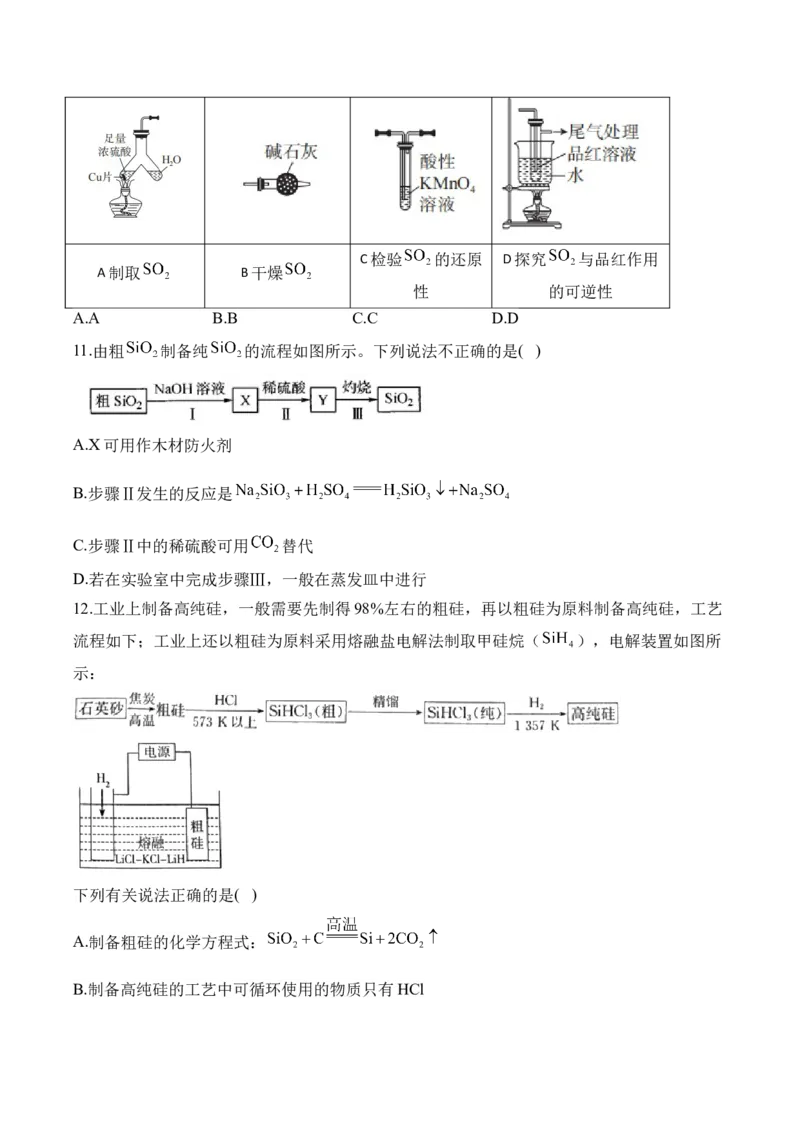
9.连二亚硫酸钠( )俗称保险粉,易被氧气氧化。利用如图装置,在锥形瓶中加入
HCOONa、NaOH、CH OH和水形成的混合液,通入 时发生反应生成保险粉和一种常见
3
气体,下列说法错误的是( )
A.制备保险粉的离子方程式为:HCOO OH 2SO S O 2 CO H O
2 2 4 2 2
B.多孔玻璃球泡的作用是增大气体与溶液的接触面积,使 能被充分吸收
C.NaOH溶液的主要作用是吸收逸出的CO
2
D.为避免 被 氧化,使硫酸与亚硫酸钠先反应,产生的 排出装置中的
10.实验室制取 时,下列装置不能达到相应实验目的的是( )C检验 的还原 D探究 与品红作用
A制取 B干燥
性 的可逆性
A.A B.B C.C D.D
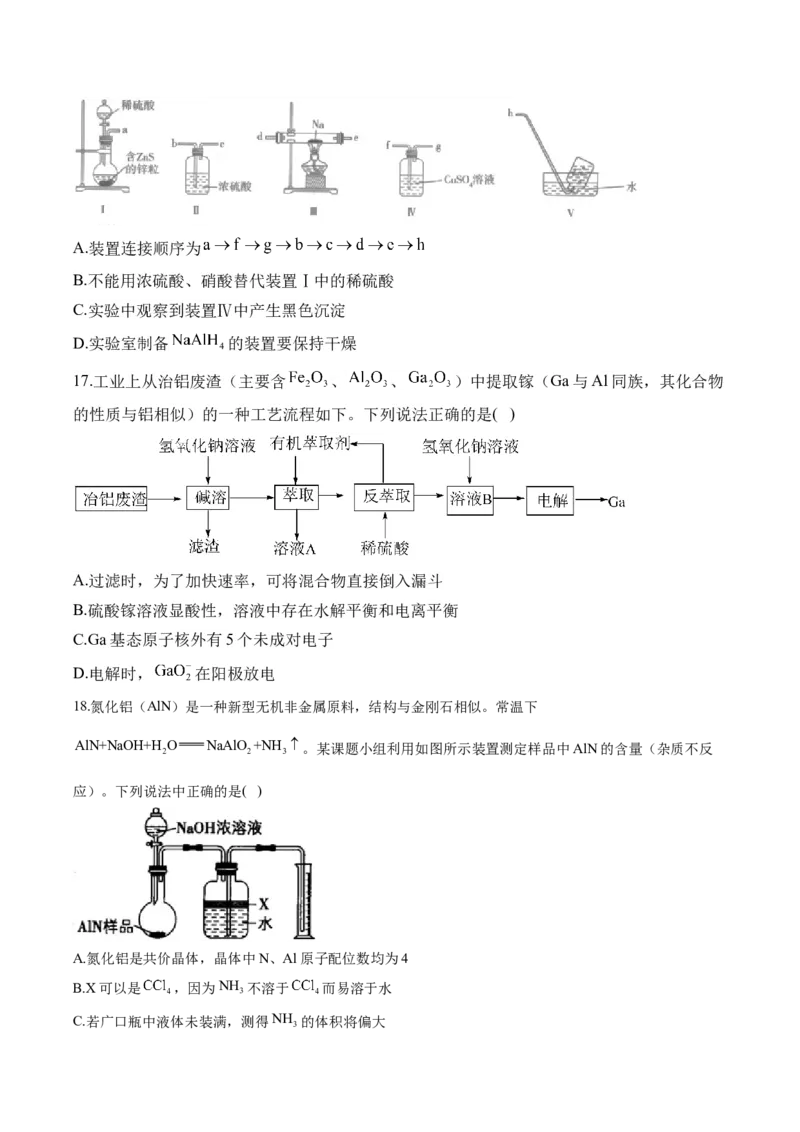
11.由粗 制备纯 的流程如图所示。下列说法不正确的是( )
A.X可用作木材防火剂
B.步骤Ⅱ发生的反应是
C.步骤Ⅱ中的稀硫酸可用 替代
D.若在实验室中完成步骤Ⅲ,一般在蒸发皿中进行
12.工业上制备高纯硅,一般需要先制得98%左右的粗硅,再以粗硅为原料制备高纯硅,工艺
流程如下;工业上还以粗硅为原料采用熔融盐电解法制取甲硅烷( ),电解装置如图所
示:
下列有关说法正确的是( )
A.制备粗硅的化学方程式:
B.制备高纯硅的工艺中可循环使用的物质只有HClC.阴极发生的电极反应:
D. 、Si、 都属于共价晶体
13.实验小组研究Na与 的反应,装置、步骤和现象如下:
实验步骤和现象:
i.先向硬质玻璃管中加一定量钠,再迅速通入 至澄清石灰水浑浊,然后点燃酒精灯。
ii.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验CO的试剂未见
明显变化。
iii.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量 溶液,产
生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
iv.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是( )
A.实验证明Na与 的反应的氧化产物为 ,还原产物为C
B.步骤iii证明Na与 也可以发生类似于Mg与 的反应
C.步骤iv发生反应的化学方程式为
D.根据以上实验推测: 与金属K也可以发生反应并被还原
14.钠及其化合物在工业生产中有重要作用,如图是钠的“价—类”二维图,下列说法正确的
是( )A.Na在空气中燃烧生成
B. 和 与 反应生成物完全相同
C.NaOH固体在空气中易变质,需密封保存
D.相同条件下,等物质的量的 和 分别与足量盐酸反应,生成气体的体积不同
15.以不同类别物质间的转化为线索,构建钠及其化合物的关系如图所示:
下列分析正确的是( )
A.钠在空气中长期放置,最终变成
B.反应②在常温下可发生
C.反应④表明物质M属于碱性氧化物
D.以上反应中只有反应①②属于氧化还原反应
16. (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制
备原理为 (在乙醚中进行,乙醚沸点:34.5℃)。某实验
小组选择下列装置制备 (装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误
的是( )A.装置连接顺序为
B.不能用浓硫酸、硝酸替代装置Ⅰ中的稀硫酸
C.实验中观察到装置Ⅳ中产生黑色沉淀
D.实验室制备 的装置要保持干燥
17.工业上从治铝废渣(主要含 、 、 )中提取镓(Ga与Al同族,其化合物
的性质与铝相似)的一种工艺流程如下。下列说法正确的是( )
A.过滤时,为了加快速率,可将混合物直接倒入漏斗
B.硫酸镓溶液显酸性,溶液中存在水解平衡和电离平衡
C.Ga基态原子核外有5个未成对电子
D.电解时, 在阳极放电
18.氮化铝(AlN)是一种新型无机非金属原料,结构与金刚石相似。常温下
AlN+NaOH+H O NaAlO +NH 。某课题小组利用如图所示装置测定样品中AlN的含量(杂质不反
2 2 3
应)。下列说法中正确的是( )
A.氮化铝是共价晶体,晶体中N、Al原子配位数均为4
B.X可以是 ,因为NH 不溶于 而易溶于水
3
C.若广口瓶中液体未装满,测得NH 的体积将偏大
3D.若实验中测得样品的质量为 ,氨气的体积为 (标况下),则样品中AlN的质量分数为
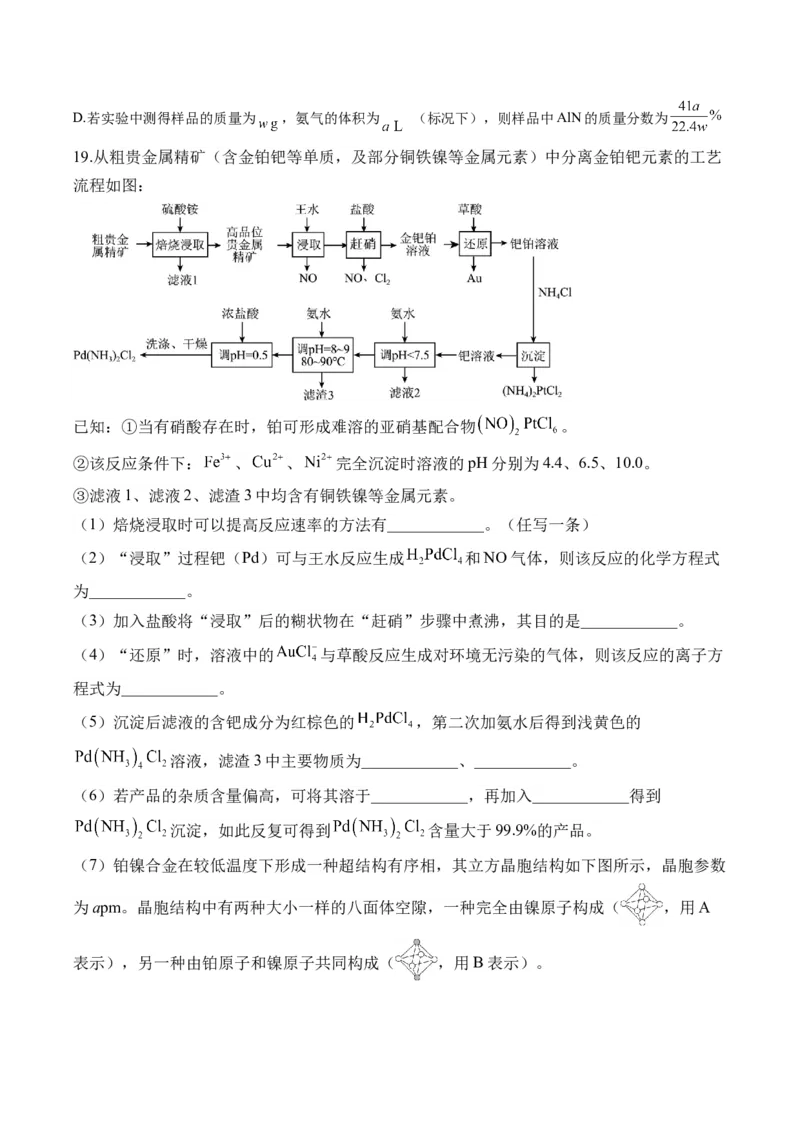
19.从粗贵金属精矿(含金铂钯等单质,及部分铜铁镍等金属元素)中分离金铂钯元素的工艺
流程如图:
已知:①当有硝酸存在时,铂可形成难溶的亚硝基配合物 。
②该反应条件下: 、 、 完全沉淀时溶液的pH分别为4.4、6.5、10.0。
③滤液1、滤液2、滤渣3中均含有铜铁镍等金属元素。
(1)焙烧浸取时可以提高反应速率的方法有____________。(任写一条)
(2)“浸取”过程钯(Pd)可与王水反应生成 和NO气体,则该反应的化学方程式
为____________。
(3)加入盐酸将“浸取”后的糊状物在“赶硝”步骤中煮沸,其目的是____________。
(4)“还原”时,溶液中的 与草酸反应生成对环境无污染的气体,则该反应的离子方
程式为____________。
(5)沉淀后滤液的含钯成分为红棕色的 ,第二次加氨水后得到浅黄色的
溶液,滤渣3中主要物质为____________、____________。
(6)若产品的杂质含量偏高,可将其溶于____________,再加入____________得到
沉淀,如此反复可得到 含量大于99.9%的产品。
(7)铂镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如下图所示,晶胞参数
为apm。晶胞结构中有两种大小一样的八面体空隙,一种完全由镍原子构成( ,用A
表示),另一种由铂原子和镍原子共同构成( ,用B表示)。①该晶体的化学式为____________。
②晶体中A和B的数目之比为____________。
20.某工厂采用如下工艺处理镍钴矿硫酸浸取液(含) 、 、 、 、 和
)。实现镍、钴、镁元素的回收。
已知:
物质
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为____________(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸( ),
中过氧键的数目为___________。
(3)“氧化”中,用石灰乳调节pH=4, 被 氧化为 ,该反应的离子方程式
为________( 的电离第一步完全,第二步微弱);滤渣的成分为 、
_______________(填化学式)。
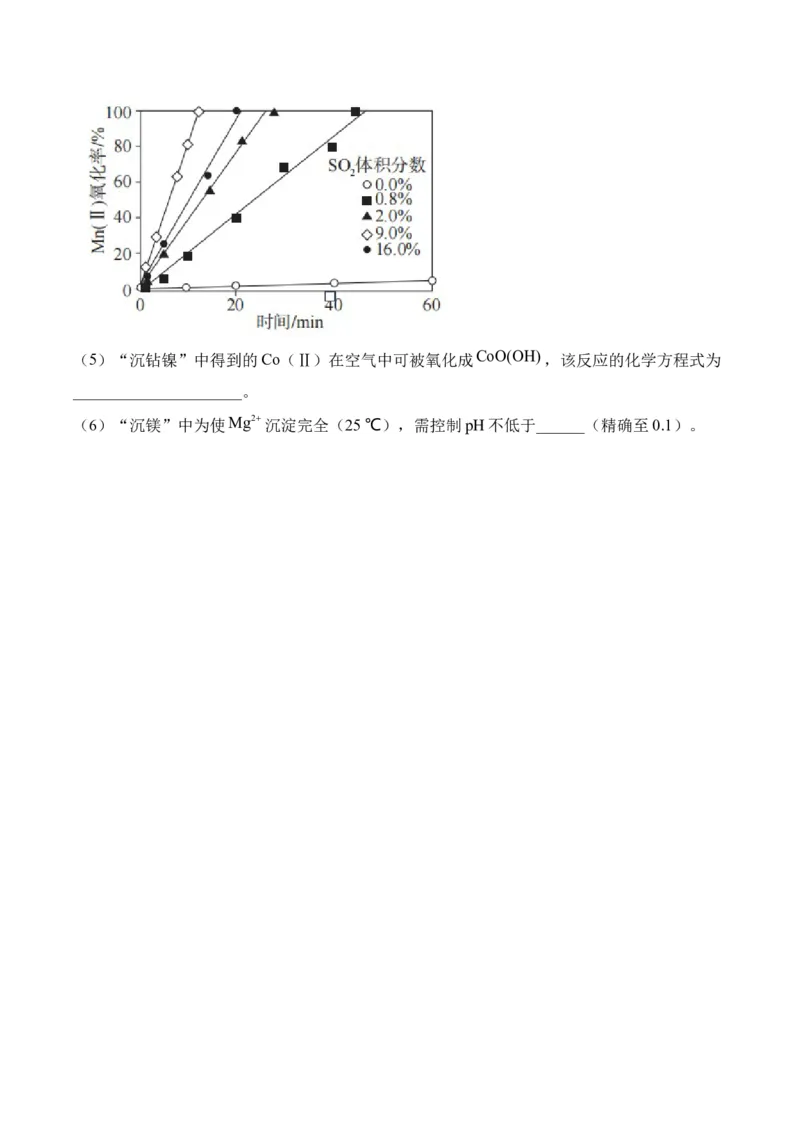
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。 体积分
数为时,Mn(Ⅱ)氧化速率最大;继续增大 体积分数时,Mn(Ⅱ)氧化速率减小的原
因是___________。(5)“沉钻镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为
_____________________。
(6)“沉镁”中为使Mg2沉淀完全(25 ℃),需控制pH不低于______(精确至0.1)。答案以及解析
1.答案:A
解析:A. 分解条件是催化剂、加热,Al燃烧能放出大量热,可为 分解提供能量,
A正确;B.Cu位于周期表的ds区,不符合形成氧化物催化剂的要求,不可代替Fe,B错误;
C. 中氧元素为-1价,吸收 时, 作氧化剂,被还原生成 , 中的氧被氧化
生成 ,反应的化学方程式为: ,C错误;D.氧烛燃烧时,Fe形成
氧化物催化剂,Fe的氧化物不溶于NaOH溶液,D错误;故选A。
2.答案:B
解析:A.氧化性: ,生成氯气将碘离子氧化成碘单质,碘遇淀粉变蓝,可观察到a变
蓝,故A正确;
B. 没有漂白性, 与 生成的HClO具有漂白性,故B错误;
C.HClO具有漂白性、氯气没有漂白性,干燥的 遇干燥的红布条不褪色,遇湿润的红布条
褪色,说明氯气和水发生了反应生成HClO,故C正确;
D.氯气与水生成了盐酸和次氯酸,溶液显示酸性,次氯酸是具有漂白性的物质。所以湿润的
蓝色石蕊试纸先变红后褪色,故D正确;
故选:B。
3.答案:D
解析:A.次氯酸盐与强酸反应生成次氯酸,次氯酸与HCl反应生成氯气,A正确;
B.HCl溶液与次氯酸盐混合,氢离子、氯离子和次氯酸根离子反应生成氯气,B正确;
C.次氯酸光照条件下分解生成HCl和氧气,溶液久置即为盐酸溶液,C正确;
D.氯气本身没有漂白性,氯气能使湿润的有色布条褪色是因为氯气与水反应生成的HClO具
有漂白性,D错误;
故答案选D。
4.答案:D
解析:①发生FeCl Cl 2FeCl CuCuCl FeFeCl ; ,
2 3 2 2
故①可以实现转化关系;
② ; 、 不能一步转化 ,故②不
能实现转化关系;③ 不能一步转化为 ,故③不能实现转化关系;
④ ; ,S不能一步转化为 ,故④不能
实现转化关系。
故答案选D。
5.答案:C
解析:A. 中氮原子是 杂化,呈三角锥形,六个原子不可能共平面,A错误;B. 和
镁条在点燃时会发生反应 ,不能做保护气,B错误;C. 具有还原
性,可以和 反应生成单质Ag, ,C正确;D.已
知 酸性与醋酸相当,其酸性大于碳酸,无法制取,D错误;故选C。
6.答案:D
解析:A.反硝化过程中氮元素化合价降低,做氧化剂被还原,A正确;
B. 中N元素为+3价, 中N元素为-3价,二者反应产物为 ,化合价为0价,根据
转移电子守恒可知,反应过程中二者的理论物质的量之比为1:1,B正确;
C.氮的固定是指游离态氮元素转化为化合态的氮元素,氮气转化为钱根,氮元素化合价降低,
做氧化剂被还原,C正确;
D.由转化图可知,亚铁离子能与水体中的硝酸根反应,可以除去水体中的硝态氮,D错误;
故选D。
7.答案:B
解析:A.反应①是游离态氮转化为化合态氮,A正确;
B.反应③必须是电解无水 ,B错误;
C.分析总的转化过程可看出总反应为 与 的反应,C正确;
D.HCl与 反应会有大量白烟产生,D正确;
故选B。
8.答案:A
解析:硫单质在氧气中燃烧只能生成 ,不能生成 ,A错误; 可以还原溴单质,
使溴水褪色,B正确;浓硫酸不能氧化 ,可以作 的干燥剂,C正确; 可与发生氧化还原反应,生成硫酸盐。D正确。
9.答案:C
解析:根据原子守恒判断生成物还有二氧化碳和水,因此制备保险粉的离子方程式为
,A正确;
多孔玻璃球泡的作用是增大气体与溶液的接触面积,使 能被充分吸收,B正确;
二氧化硫有毒,属于大气污染物,因此NaOH溶液的主要作用是吸收 ,C错误;
保险粉易被氧气氧化,装置内有空气,因此为避免产生的 被O 氧化,应先使硫酸与
2
亚硫酸钠反应,利用产生的 排出装置中残留的O ,D正确。
2
10.答案:B
解析:铜与浓硫酸在加热的条件下可以产生二氧化硫,将反应后的溶液倒入装置右侧的水中,
可观察到溶液变蓝,A项不符合题意;二氧化硫会与碱石灰反应,不能达到相应的实验目的,
B项符合题意;二氧化硫可以与酸性 溶液发生氧化还原反应,酸性 溶液褪色,
可以用来检验二氧化硫的还原性, C项不符合题意;二氧化硫可以使品红溶液褪色,加热后
品红溶液恢复至原色,可以用来探究二氧化硫与品红作用的可逆性,D项不符合题意。
11.答案:D
解析:由流程图可知,粗 与NaOH溶液反应得到的X为 溶液,Na SiO 溶液具
2 3
有阻燃性,可用作木材防火剂,A正确; 溶液与稀硫酸反应得到的Y为Na SiO 沉淀,
2 3
即 ,B正确;碳酸的酸性比硅酸强,故步骤Ⅱ中的稀
硫酸可用CO 替代,C正确;步骤Ⅲ中进行的操作是灼烧硅酸固体,若在实验室中完成步骤
2
Ⅲ,一般在坩埚中进行,D错误。
12.答案:C
解析:制备粗硅的化学方程式为 ,A项错误;
制备高纯硅的工艺中可循环使用的物质有 和HCl,B项错误;
属于分子晶体,D项错误。
13.答案:A
解析:A.由上述分析可知,硬质玻璃管反应后生成了C和 、 ,说明Na与的反应的氧化产物为 和 ,还原产物为C,故A错误;
B.实验iii说明Na与 的反应生成了 ,故Na与 的反应类似于Mg与 的反应;
故B正确;
C.步骤iv反应为C和浓硫酸反应生成SO ,化学方程式为:
2
△
C2H SO (浓) CO 2SO 2H O;故C正确;
2 4 2 2 2
D.K与Na同主族,故可以推测CO 与金属K也可以发生反应并被还原为C,故D正确。
2
答案选A。
14.答案:C
解析:Na在空气中燃烧生成Na O ,A项错误;Na O与H O反应生成NaOH,Na O 与
2 2 2 2 2 2
H O反应生成NaOH和O ,B项错误;NaOH易潮解并与空气中的CO 反应,需要密封保存,
2 2 2
C项正确;相同条件下,等物质的量的Na CO 和NaHCO 分别与足量盐酸反应,生成CO 的
2 3 3 2
体积相同,D项错误。
15.答案:A
解析:A.钠在空气中长期放置,和空气中氧气、水、CO 反应最终生成物为碳酸钠,故A正
2
确;
B.钠氧化生成过氧化钠需要加热或者点燃,常温下生成氧化钠,故B错误;
C.过氧化钠与水反应生成氢氧化钠和氧气,不是碱性氧化物,故C错误;
D.过氧化钠与水反应生成氢氧化钠和氧气,有化合价变化,所以也是氧化还原反应,故D错
误;
故选:A。
16.答案:A
解析:装置连接顺序为制氢、净化、干燥、合成、吸水、收集氢气,装置Ⅱ可使用两次,第
一次干燥氢气,第二次吸收水槽中挥发出来的水蒸气,连接顺序为
,A项错误;锌与浓硫酸反应生成 ,锌与稀硝酸反
应生成 ,与浓硝酸反应生成 ,均不生成 ,故不能用浓硫酸、硝酸替代装置Ⅰ中的
稀硫酸,B项正确;锌粒中含 ,则产生的 中混有 ,用硫酸铜溶液吸收,发生反应:
,产生黑色沉淀,C项正确; 、 均能够与水蒸气反应,D项正确。
17.答案:B
解析:A.过滤时,必须将混合物沿玻璃棒慢慢流入漏斗,A错误;
B.依题意,Ga及其化合物的性质与Al相似,故硫酸稼溶液中存在嫁离子的水解平衡和水的
电离平衡,溶液呈酸性,B正确;
C.Ga和铝同族,核外未成对电子数应为1个,C错误;
D.Ga被还原, 应在阴极放电,D错误;
故选B。
18.答案:A
解析:本题考查氮化铝纯度测定实验。测定原理为AlN和NaOH浓溶液反应产生氨气,氨气不溶于X,广
口瓶中压强增大,将水压入量筒中,量筒中水的体积即为产生氨气的体积,从而计算出AlN的质量,进而
计算其含量。氮化铝结构与金刚石相似,所以为共价晶体,N、Al原子配位数均为4,A正确;CCl 密度
4
大于水,不会浮在水面上,B错误; 的体积等于排出水的体积,与广口瓶中液体是否装满无直接关系,
V aL a
C错误;nNH mol,根据 可知,
3 V 22.4Lmol1 22.4
m
a
n(AlN)nNH mol,则样品中AlN的质量分数为
3 22.4
m(AlN) n(AlN)M(AlN) 4100a
100% 100% %,D错误。
w w 22.4w
19.答案:(1)将固体粉碎,搅拌
(2)3Pd2HNO 12HCl 3H PdCl 2NO4H O
3 2 4 2
(3)将难溶的亚硝基配合物 NO PtCl 溶解,提高铂的浸出率
2 6
(4)2AuCl3H C O 2Au6CO 8Cl 6H
4 2 2 4 2
(5)CuOH ;FeOH
2 3
(6)氨水;盐酸
(7)Ni Pt(或PtNi );1:3
3 3
解析:(1)焙烧浸取时可以提高反应速率的方法有将固体粉碎,搅拌;加热或适当增大浸取
液浓度;(2)“浸取”过程钯(Pd)可与王水反应生成H PdCl 和NO气体,由此可以写出反应为:
2 4
3Pd2HNO 12HCl 3H PdCl 2NO4H O;
3 2 4 2
(3)根据已知②,当有硝酸存在时,铂可形成难溶的亚硝基配合物 NO PtCl ,将“浸
2 6
取”后的糊状物煮沸“赶硝”,目的是将难溶的亚硝基配合物 NO PtCl 溶解,提高铂的浸
2 6
出率;
(4)溶液中的AuCl 与草酸(H C O )反应生成对环境无污染的气体,故产物中应该仅有二氧
4 2 2 4
化碳气体,该反应的离子方程式为2AuCl3H C O 2Au6CO 8Cl 6H ;
4 2 2 4 2
(5)根据题干信息知道Fe3、Cu2、Ni2完全沉淀时溶液的pH分别为4.4、6.5、9,当加
入氨水调pH小于7.5时,主要沉淀的铁离子、铜离子,滤渣3中主要物质为CuOH
、
2
FeOH
;
3
(6)若产品的杂质含量偏高,可将其溶于氨水,使杂质离子充分沉淀,再过滤,滤液中加盐
酸调节pH值得到纯度较高的产品。
20.答案:(1)将镍钴矿粉碎(或浸取时搅拌,延长浸取时间等)
(2)6.021023
(3)Mn2 HSO H O MnO SO2 3H ; 、
5 2 2 4
Fe(OH) CaSO
3 4
(4)9.0%;SO 具有还原性,也能还原
2
(5)
(6)11.1
解析:(1)用硫酸浸取镍钴矿时,提高浸取速率的方法可以是将镍钴矿粉碎、浸取时搅拌、
延长浸取时间等。
(2) 可以看成是 中一个氢原子被磺基 取代的产物,即 ,
故分子中有一个过氧键,1 mol 中过氧键的数目为 。
(3)根据题干信息可知,“氧化”中 被 氧化为 ,则 被还原为 ,结合 的电离第一步完全可知,反应的离子方程式为
;“氧化”中 会被氧化为 ,用石灰乳调
节pH=4时Fe元素沉淀为 , 与 结合生成 沉淀,故滤渣中还含有
、 。
(4)由图可知,当 体积分数为9.0%时,Mn(Ⅱ)氧化率达到100%所用时间最短,氧
化速率最大; 具有还原性,也能还原 ,其体积分数过大时,与 反应,使Mn
(Ⅱ)氧化速率减小。
(5)“沉钴镍”中得到的Co(Ⅱ)以 形式存在,其可被空气中 氧化为 ,
根据氧化还原反应规律可写出反应的化学方程式。
(6) 沉淀完全,则 ,
, ,pH≥11。