文档内容
(7)物质结构与性质——2025届高考化学二轮复习易错重难提升【新高
考】
一、易错点分析
考点一 原子结构、化学用语
1.原子或离子中各粒子间的数量关系
(1)对于原子:质子数=核电荷数=核外电子数=原子序数。
(2)质量数=质子数+中子数。
(3)对于阳离子:质子数=阳离子的核外电子数+阳离子所带正电荷数。
(4)对于阴离子:质子数=阴离子的核外电子数-阴离子所带负电荷数。
2.元素、核素、同位素之间的关系
3.基态原子核外电子排布规律
两原理一规则
(1)能量最低原理。
构建基态原子时,电子将尽可能地占据能量最低的原子轨道,使整个原子的能量最低。
(2)泡利原理。
每个原子轨道最多容纳两个电子且自旋状态必须相反。
(3)洪特规则。
基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。
4.表示基态原子核外电子排布的四种方法PS:对于20号后的第四周期元素的简化电子排布式容易忽视3d轨道上的电子。
考点二 元素周期表、元素周期律
1.原子序数与元素位置的“序数差值”规律
(1)同周期相邻主族元素的“序数差值”规律。
同周期第ⅡA族和第ⅢA族元素,其原子序数差分别是:第二、三周期相差1,第四、五周期相
差11,第六、七周期相差25。其余同周期相邻元素的原子序数差为1。
(2)同族相邻元素的“序数差值”规律。
①第二、三周期的同族元素原子序数相差8。
②第三、四周期的同族元素原子序数相差有两种情况:第ⅠA族、第ⅡA族相差8,其他族相差
18。
③第四、五周期的同族元素原子序数相差18。
④第五、六周期的同族元素原子序数镧系之前的相差18,镧系之后的相差32。
⑤第六、七周期的同族元素原子序数相差32。
2.通过“三看”比较粒子半径大小
在中学化学要求的范围内,可按“三看”规律来比较粒子半径的大小。
“一看”电子层数:一般情况下,当电子层数不同时,电子层数越多,半径越大。
例如:r(Li)r(Na+)。
“二看”核电荷数:当电子层数相同时,核电荷数越大,半径越小。
相同电子层结构的离子半径规律是“序大径小”
例如:r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)、r(O2-)>r(F-)>
r(Na+)>r(Mg2+)>r(Al3+)。
“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
例如:r(Cl-)>r(Cl)、r(Fe2+)>r(Fe3+)。
3.元素金属性、非金属性的多方面比较4.第一电离能、电负性
(1)元素第一电离能的周期性变化规律及应用。
(2)电负性大小的判断。考点三 化学键、分子间作用力
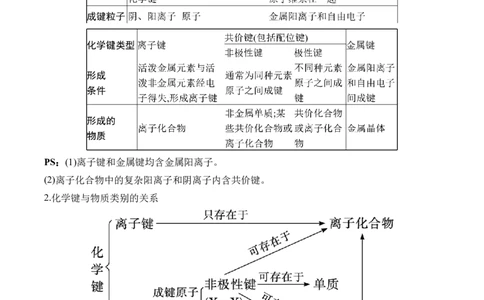
1.离子键、共价键及金属键的比较
PS:(1)离子键和金属键均含金属阳离子。
(2)离子化合物中的复杂阳离子和阴离子内含共价键。
2.化学键与物质类别的关系
3.σ键与π键的判断方法4.三种作用力及对物质性质的影响
考点四 分子结构与性质
1.中心原子杂化轨道数的判断方法
杂化轨道数=σ键电子对数+孤电子对数=价层电子对数
(1)看中心原子有没有形成双键或三键。如形成1个三键,则其中有2个π键,用去了2个p轨道,
碳原子为sp杂化;如形成1个双键,则其中有1个π键,碳原子为sp2杂化;如果全部是单键,碳原
子为sp3杂化。
(2)由分子的空间结构结合价层电子对互斥模型判断。没有填充电子的空轨道一般不参与杂
化,1个孤电子对占据1个杂化轨道。如NH 分子为三角锥形,且N上有1个孤电子对,即4个杂
3
化轨道各指向四面体的四个顶角,氮原子为sp3杂化。
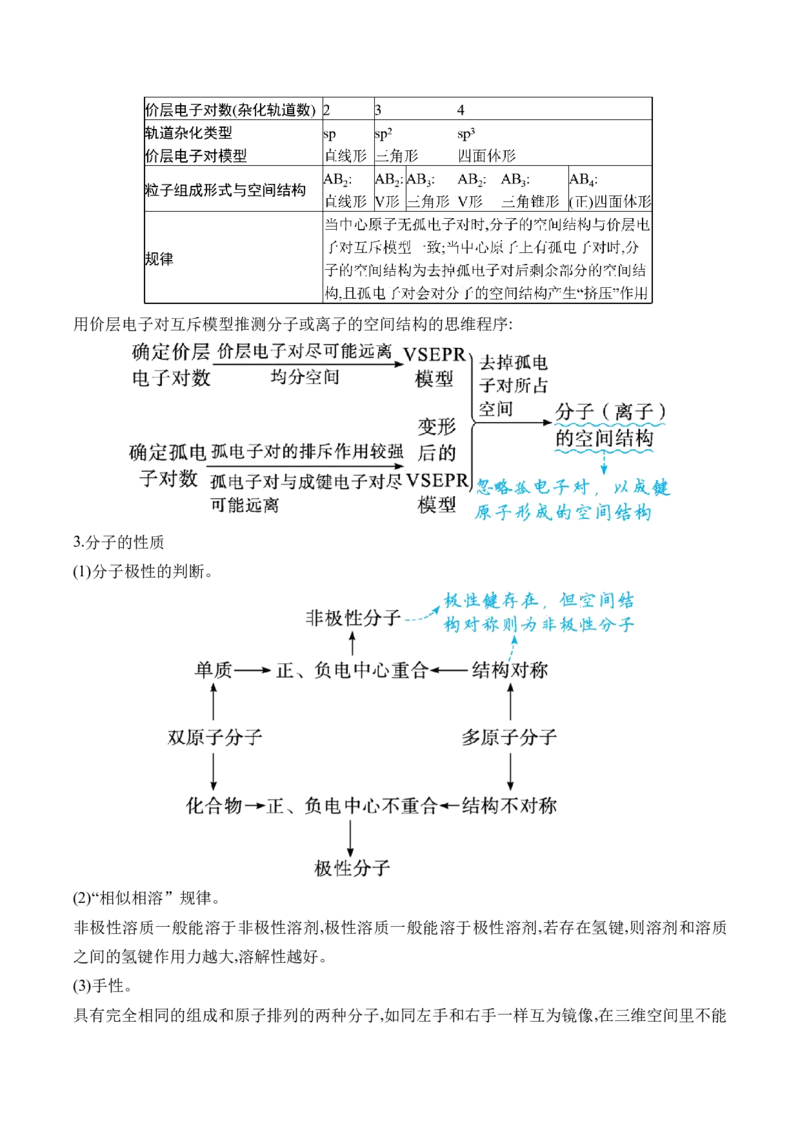
2.中心原子的价层电子对数、杂化类型与粒子的空间结构用价层电子对互斥模型推测分子或离子的空间结构的思维程序:
3.分子的性质
(1)分子极性的判断。
(2)“相似相溶”规律。
非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂,若存在氢键,则溶剂和溶质
之间的氢键作用力越大,溶解性越好。
(3)手性。
具有完全相同的组成和原子排列的两种分子,如同左手和右手一样互为镜像,在三维空间里不能重叠,互为手性异构体,有手性异构体的分子叫作手性分子。在有机物中,如果一个碳原子以4
个单键(σ键)与4个不同的原子(或原子团)连接,该碳原子称为手性碳原子。
考点五 化学键、分子间作用力
1.物质熔、沸点高低的比较规律
(1)一般情况下,不同类型晶体的熔、沸点高低规律:共价晶体>离子晶体>分子晶体,如熔、沸点:
金刚石>NaCl>Cl ;金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如汞。
2
(2)形成共价晶体的原子半径越小、键长越短,则键能越大,其熔、沸点就越高,如熔、沸点:金刚
石>石英>碳化硅>晶体硅。
(3)一般来说,形成离子晶体的阴、阳离子所带的电荷数越多,离子半径越小,则离子键越强,熔、
沸点就越高,如熔、沸点:MgO>MgCl ,NaCl>CsCl。
2
(4)一般来说,金属晶体中金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单
质的熔、沸点就越高,如Al>Mg>Na。
(5)分子晶体的熔、沸点比较规律。
①组成和结构相似的分子,相对分子质量越大,其熔、沸点就越高,如熔、沸点:HI>HBr>HCl。
②相对分子质量相等的分子,分子极性越大,其熔、沸点就越高,如熔、沸点:CO>N 。
2
③互为同分异构体的分子中,支链越少,其熔、沸点就越高,如熔、沸点:正戊烷>异戊烷>新戊烷。
④互为同分异构体的芳香烃及其衍生物,熔、沸点:邻位取代物>间位取代物>对位取代物,如熔、
沸点:邻二甲苯>间二甲苯>对二甲苯。
2.晶胞中粒子数目的计算方法——均摊法
3.晶体密度的计算二、易错训练
1.下列化学用语表示正确的是( )
A.氨气分子的空间填充模型:
B.铍原子最外层原子轨道的电子云轮廓图:
C.铜氨配离子的结构简式:
D.用电子式表示 的形成过程为:
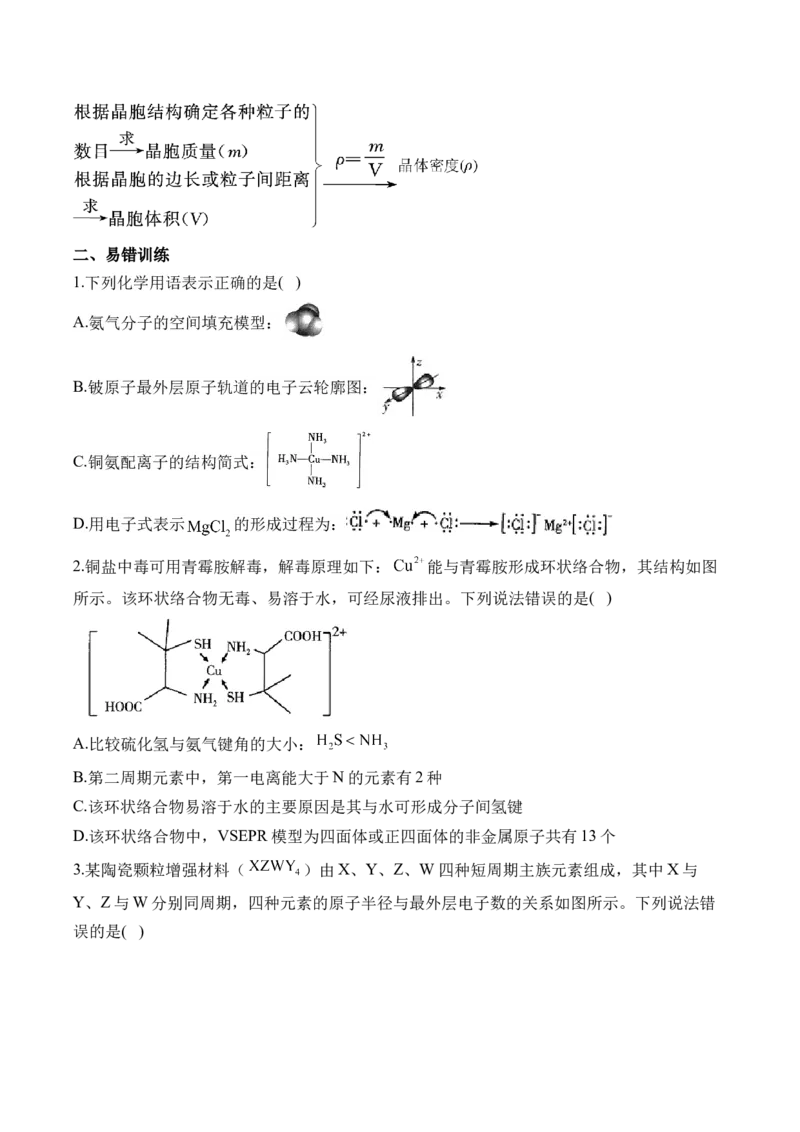
2.铜盐中毒可用青霉胺解毒,解毒原理如下: 能与青霉胺形成环状络合物,其结构如图
所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是( )
A.比较硫化氢与氨气键角的大小:
B.第二周期元素中,第一电离能大于N的元素有2种
C.该环状络合物易溶于水的主要原因是其与水可形成分子间氢键
D.该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有13个
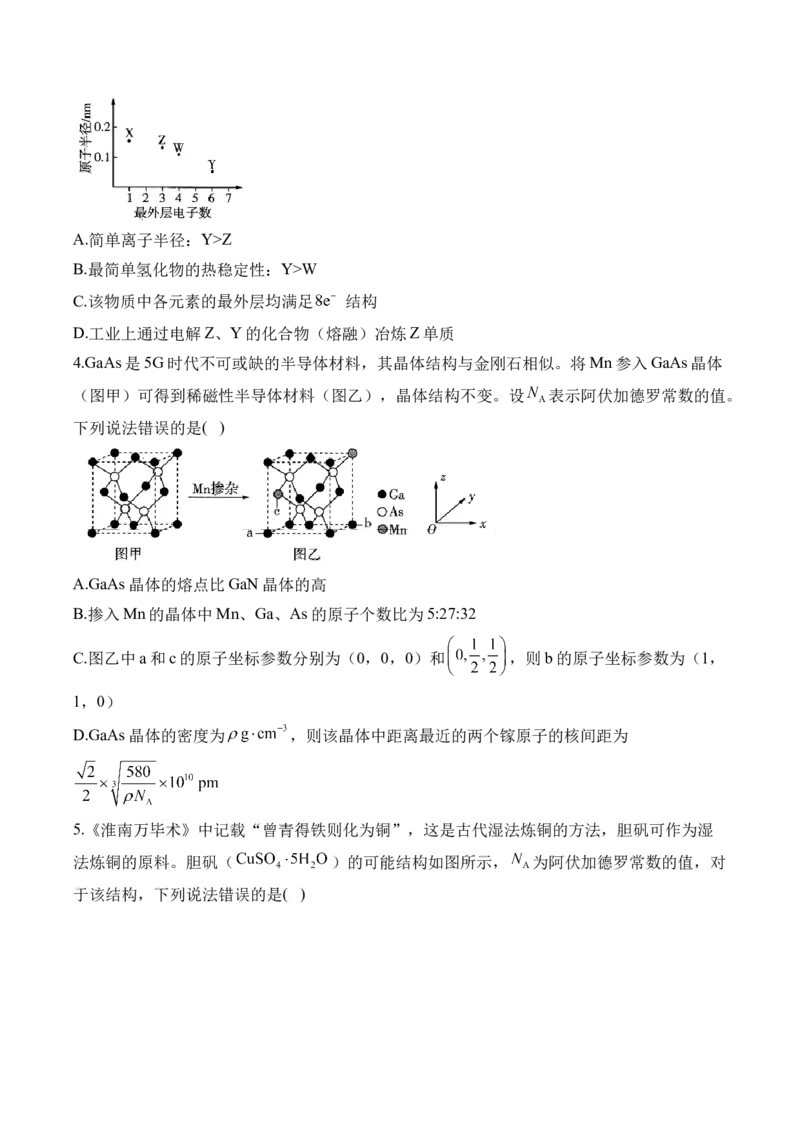
3.某陶瓷颗粒增强材料( )由X、Y、Z、W四种短周期主族元素组成,其中X与
Y、Z与W分别同周期,四种元素的原子半径与最外层电子数的关系如图所示。下列说法错
误的是( )A.简单离子半径:Y>Z
B.最简单氢化物的热稳定性:Y>W
C.该物质中各元素的最外层均满足 结构
D.工业上通过电解Z、Y的化合物(熔融)冶炼Z单质
4.GaAs是5G时代不可或缺的半导体材料,其晶体结构与金刚石相似。将Mn参入GaAs晶体
(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。设 表示阿伏加德罗常数的值。
下列说法错误的是( )
A.GaAs晶体的熔点比GaN晶体的高
B.掺入Mn的晶体中Mn、Ga、As的原子个数比为5:27:32
C.图乙中a和c的原子坐标参数分别为(0,0,0)和 ,则b的原子坐标参数为(1,
1,0)
D.GaAs晶体的密度为 ,则该晶体中距离最近的两个镓原子的核间距为
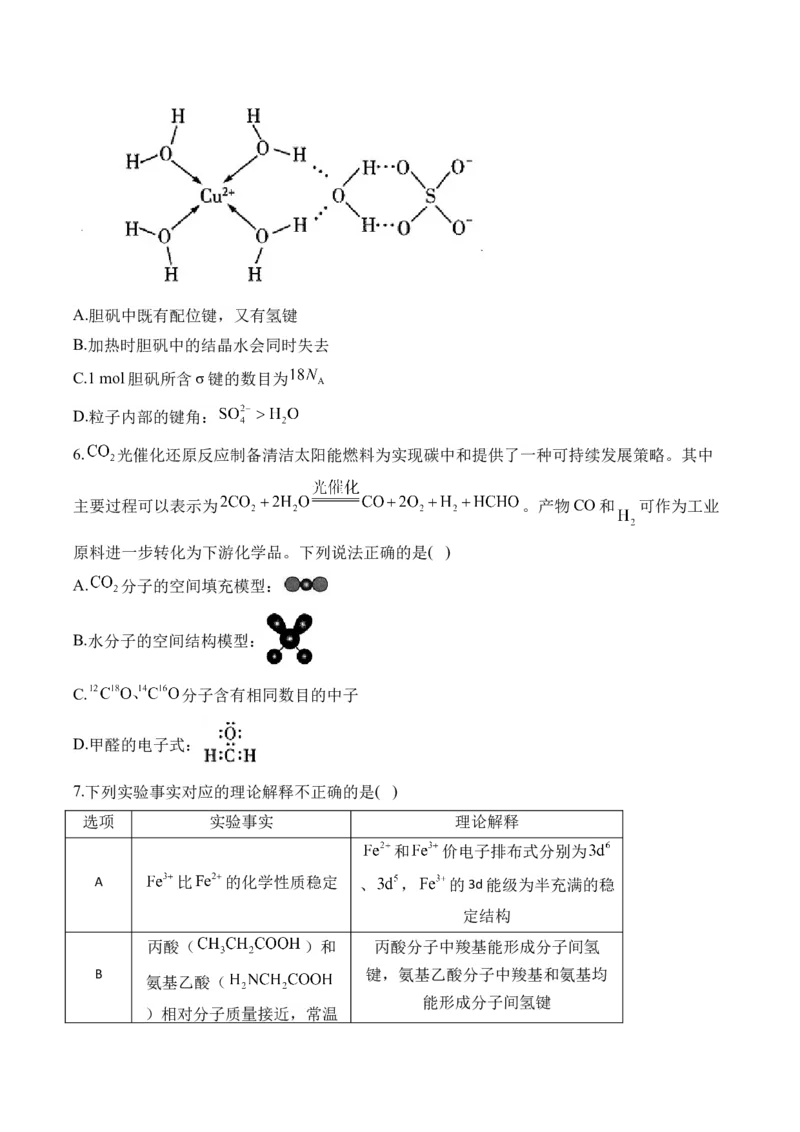
5.《淮南万毕术》中记载“曾青得铁则化为铜”,这是古代湿法炼铜的方法,胆矾可作为湿
法炼铜的原料。胆矾( )的可能结构如图所示, 为阿伏加德罗常数的值,对
于该结构,下列说法错误的是( )A.胆矾中既有配位键,又有氢键
B.加热时胆矾中的结晶水会同时失去
C.1 mol胆矾所含σ键的数目为
D.粒子内部的键角:
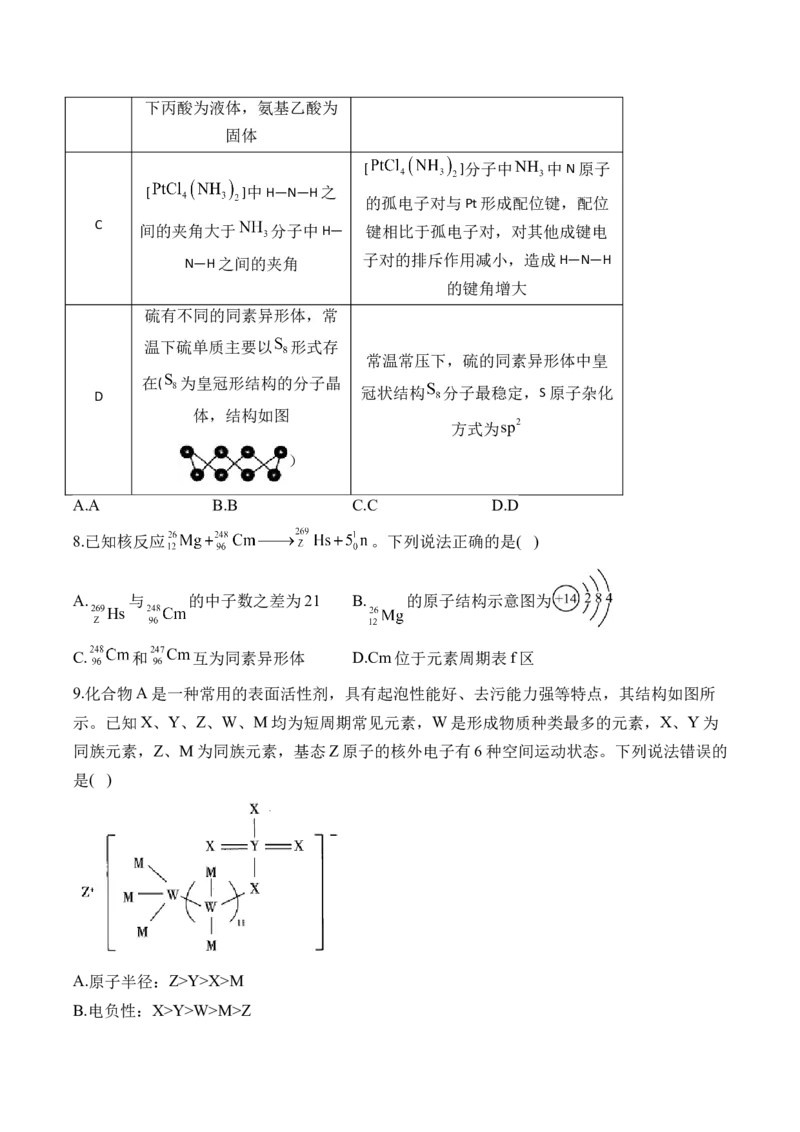
6. 光催化还原反应制备清洁太阳能燃料为实现碳中和提供了一种可持续发展策略。其中
主要过程可以表示为 。产物CO和 可作为工业
原料进一步转化为下游化学品。下列说法正确的是( )
A. 分子的空间填充模型:
B.水分子的空间结构模型:
C. 分子含有相同数目的中子
D.甲醛的电子式:
7.下列实验事实对应的理论解释不正确的是( )
选项 实验事实 理论解释
和 价电子排布式分别为
A 比Fe2的化学性质稳定 、 , 的3d能级为半充满的稳
定结构
丙酸( )和 丙酸分子中羧基能形成分子间氢
B 键,氨基乙酸分子中羧基和氨基均
氨基乙酸(
能形成分子间氢键
)相对分子质量接近,常温下丙酸为液体,氨基乙酸为
固体
[ ]分子中NH 中N原子
3
[ ]中H—N—H之
的孤电子对与Pt形成配位键,配位
C 间的夹角大于 分子中H— 键相比于孤电子对,对其他成键电
N—H之间的夹角 子对的排斥作用减小,造成H—N—H
的键角增大
硫有不同的同素异形体,常
温下硫单质主要以 形式存
常温常压下,硫的同素异形体中皇
在( S 为皇冠形结构的分子晶
8 冠状结构 分子最稳定,S原子杂化
D
体,结构如图
方式为sp2
)
A.A B.B C.C D.D
8.已知核反应 。下列说法正确的是( )
A. 与 的中子数之差为21 B. 的原子结构示意图为
269Hs
Z
C. 和
247Cm互为同素异形体
D.Cm位于元素周期表f区
96
9.化合物A是一种常用的表面活性剂,具有起泡性能好、去污能力强等特点,其结构如图所
示。已知X、Y、Z、W、M均为短周期常见元素,W是形成物质种类最多的元素,X、Y为
同族元素,Z、M为同族元素,基态Z原子的核外电子有6种空间运动状态。下列说法错误的
是( )
A.原子半径:Z>Y>X>M
B.电负性:X>Y>W>M>ZC.X、Y、Z、W的简单氢化物中稳定性最强、熔沸点最高的为X的氢化物
D.均由X、Y、Z、M四种元素组成的两种盐可以发生反应
10.红砷镍是一种六方晶体,晶胞结构如图所示(设 为阿伏加德罗常数的值)。下列说法
正确的是( )
A.As位于元素周期表s区
B.红砷镍的化学式是
C.Ni的配位数是6
D.红砷镍晶体密度为
11.下列说法正确的是( )
A. 分子中心原子As的杂化方式为 ,分子的空间结构为平面三角形
B.第一电离能
C. 与 原子总数相同、价电子总数相同
D.金属羰基化合物 中含有σ键和π键的个数比为
12.我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆
炸时发生的反应为 ,生成物 的晶胞结构如图所示。
下列说法正确的是( )
A.NO
的空间结构为三角锥形
33
B. 晶胞中距离最近的 与 的核间距为 anm
S2 4
C. 晶体中阴离子和阳离子的配位数之比为1:2
D.反应物中两种单质(S、C)的晶体类型分别为分子晶体和共价晶体
13.[化学——选修3:物质结构与性质]
铁及其化合物有着极其广泛的用途。回答下列问题:
(1)基态铁原子的核外电子中有________对成对电子。若其价电子发生如下四种不同形式的
转化,其中能够产生发射光谱的是__________。
A.3d64s2 4s24p6
B.
C.
D.
(2)基态铁原子的五级电离能数据如图1所示,其中I 到 的电离能差值较大,其主要原
3
因是____________。
(3)甘氨酸亚铁是一种具有口服活性的铁强化剂和补充剂。其制备反应如下:
①甘氨酸分子中各元素的电负性大小顺序是__________。
②甘氨酸亚铁分子中Fe2的配位数是__________,配体的化学式是__________,分子中碳原
子的杂化类型是__________。(4)氯化亚铁的熔点为674 ℃,而氯化铁的熔点仅为282 ℃,二者熔点存在差异的原因是
____________。
(5)磁性氮化铁的晶胞结构如图2所示,沿z轴方向的投影如图3所示,则该化合物的化学
式为____________。晶体的密度为__________
[用含a、b、N
(阿伏加德罗常数的
A
值)的代数式表示]。
14.[化学——选修3:物质结构与性质]
氮及其化合物在工农业生产、生活和科研中有着广泛的应用。回答下列问题:
(1)基态N原子的价层电子排布式为_________;C、N、O的第二电离能由大到小的顺序是
____________。
(2)已知 的键能分别为 性
质稳定的原因是___________;工业上曾用氰氨基法固氮,先将 和纯 在1100 ℃下反
应得 ,然后水解 得到 中含有的化学键类型为___________(填标
号)。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键
(3) 中的键角 ___________(填“>”“<”或“=”) 中的键角
中N原子能通过配位键与 结合而使其具有碱性,且碱性:
,试从物质结构角度进行解释____________。
(4) 可用于制备汽车安全气囊, 的中心原子的杂化方式为__________, 的空间
结构为___________。
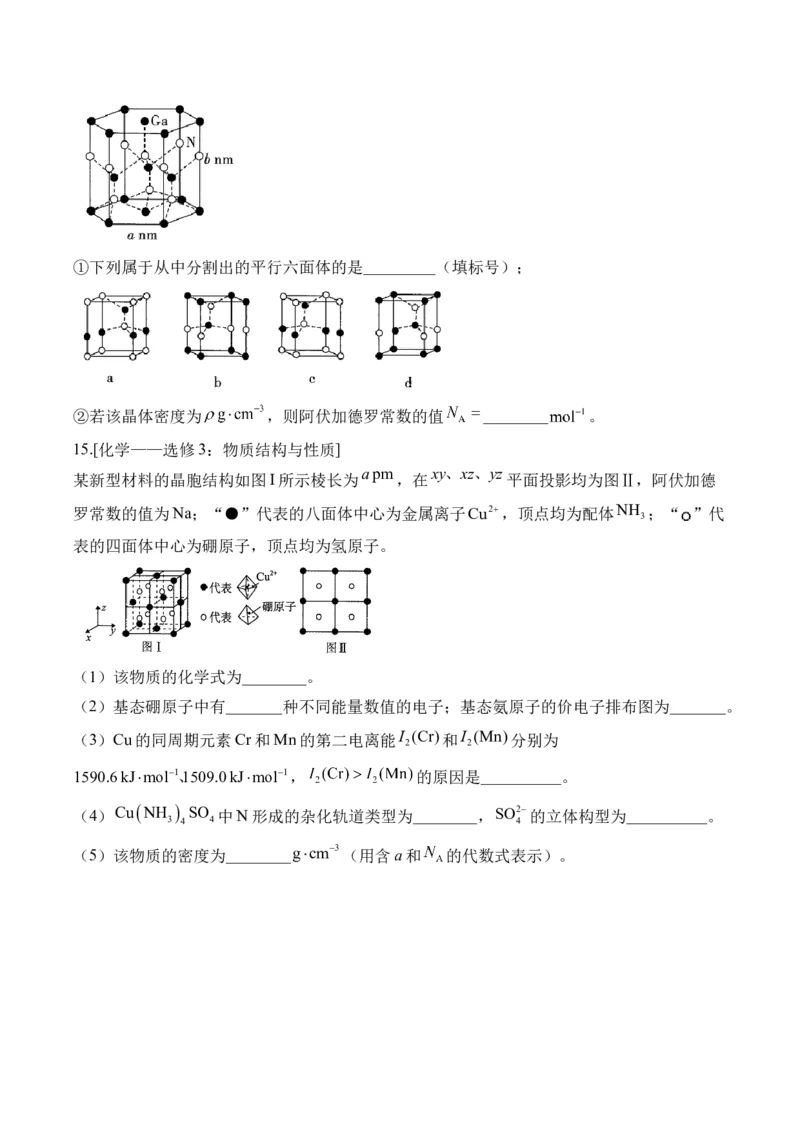
(5)氮化傢(GaN)为六方晶胞,其晶胞结构如图所示:①下列属于从中分割出的平行六面体的是_________(填标号);
②若该晶体密度为 ,则阿伏加德罗常数的值 ________ 。
15.[化学——选修3:物质结构与性质]
apm xy、xz、yz
某新型材料的晶胞结构如图I所示棱长为 ,在 平面投影均为图Ⅱ,阿伏加德
罗常数的值为Na;“●”代表的八面体中心为金属离子Cu2,顶点均为配体NH ;“ ”代
3
表的四面体中心为硼原子,顶点均为氢原子。
(1)该物质的化学式为________。
(2)基态硼原子中有_______种不同能量数值的电子;基态氨原子的价电子排布图为_______。
(3)Cu的同周期元素Cr和Mn的第二电离能I (Cr)和I (Mn)分别为
2 2
1590.6kJmol1、1509.0kJmol1, 的原因是__________。
(4)CuNH SO 中N形成的杂化轨道类型为________,SO2的立体构型为__________。
3 4 4 4
(5)该物质的密度为________gcm3(用含a和 的代数式表示)。答案以及解析
1.答案:C
解析:氨气分子的电子式为 ,含有孤电子对,则氨气分子的空间结构为三角锥,氨气
分子的空间填充模型为 ,A错误;基态铍原子核外电子排布式为 ,最外层为s
能级电子,s能级电子的电子云轮廓图为球形,不是哑铃形,B错误;铜氨配离子中 与
分子间形成配位键,结构简式为 ,C正确; 为离子化合物,
Cl得电子带负电,Mg失电子带正电,用电子式表示 的形成过程为:
,D错误。
2.答案:D
解析:氨分子的孤电子对数为1, 的孤电子对数为2, 中孤电子对对成键电子对的排
斥力比 的大,所以 的键角比硫化氢的大,A正确;同周期元素自左至右第一电离能
呈增大趋势,但由于N原子的2p能级为半充满状态,第一电离能大于相邻的O原子,所以
第二周期中第一电离能大于N的有F、Ne,B正确;该化合物容易与水分子之间形成分子间
氢键,提高其在水中的溶解度,C正确;该环状络合物中的N原子、饱和C原子和S原子及
羧基中—OH中的O原子的价层电子对数都为4,则该络合物分子中VSEPR模型为四面体或
正四面体形的非金属原子有14个,D错误。
3.答案:C
解析:简单离子半径: ,A项正确;元素的非金属性越强,最简单氢化物的热稳定
性越强,B项正确;该物质中Li元素的最外层为 结构,C项错误;工业上通过电解熔融
的 冶炼Al单质,D项正确。
4.答案:A
解析:GaAs和GaN都属于共价晶体,但前者所含共价键键长长,键能小,熔点低,A错误;
利用均摊法可知,每个图乙晶胞中Mn的个数为5/8,Ga的个数为27/8,As的个数为4,
Mn、Ga、As的个数比为5:27:32,B正确;a和c原子坐标参数分别为(0,0,0)和,则b原子坐标参数为(1,1,0),C正确;设GaAs晶胞的边长为 ,则距离
最近的两个镓原子的核间距为 ,该晶胞中的Ga位于顶点和面心,个数为4,As位于
体内,个数为4,则晶胞的质量为 ,解得
,故距离最近的两个镓原子的核间距为 ,D正确。
5.答案:B
解析:由胆矾的结构可知其中含有配位键和氢键,A项正确。由胆矾的结构可知,胆矾中有
1个水分子和其他微粒通过氢键结合,有4个水分子和 通过配位键结合,作用力不同,
加热时结晶水分步失去,B项错误。l mol胆矾所含σ键的数目为 [易错:氢键不是σ键],
C项正确。 的空间结构为正四面体形,键角约为109°28′, 的空间结构为V形,中
心O原子上孤电子对数为2,键角小于 的,D项正确。
6.答案:C
解析:一般地,同周期主族元素原子半径从左到右逐渐增大,原子半径:C>O,A项错误;
水分子中一个氧原子与两个氢原子形成共价键,空间结构模型为 ,O的价电子对数为
4,含有2个孤电子对,所以 为水分子的VSEPR模型,B项错误;一个
分子中均含有16个中子,C项正确;甲醛分子中H、C原子间共用1对电子对,O、C原子间
共用2对电子对,其电子式为 ,D项错误。
7.答案:D
解析: 和 的价电子排布式分别为 、 ,离子的核外电子排布处于半充满或全满
状态时较为稳定,故 比 的化学性质稳定,A项正确;丙酸分子中,只有羧基形成分
子间氢键,而氨基乙酸分子中,羧基和氨基均能形成分子间氢键,氢键越多,沸点越高,B
项正确; 中N原子形成3个N—H和1个N→Pt配位键,N→Pt配位键相比于
孤电子对,对其他成键电子对的排斥作用减小,故其H—N—H之间的夹角大于 分子中的H—N—H键角,C项正确;在环状 分子结构中,每个S原子与相邻2个S原子形成2个
σ键,其原子上还含有2个孤电子对,故S原子杂化类型为 杂化,D项错误。
8.答案:D
解析:根据质量守恒定律可知 ,则 的中子数为
的中子数为 ,二者中子数之差为9,A项错误;Mg的原子
序数为12, 的原子结构示意图为 ,B项错误; 和 互为同位素,
C项错误;Cm为96号元素,基态Cm原子的核外电子排布式为 ,Cm位于元素
周期表f区,D项正确。
9.答案:C
解析:同周期主族元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,
原子半径Na>S>O>H,A项正确;一般来说,同周期主族元素从左到右电负性逐渐增大,同
主族元素从上到下电负性逐渐减小,电负性O>S>C>H>Na,B项正确;X、Y、Z、W的简单
氢化物分别为 ,NaH为离子化合物,熔沸点最高,C项错误;
和 可以发生反应 ,D项正确。
10.答案:C
解析:As位于元素周期表的第四周期ⅤA族,位于p区,A错误;晶胞中Ni原子位于顶点
和棱上,1个晶胞中含有Ni原子的个数为 ,1个晶胞中含有As
原子的个数为2,故化学式为NiAs,B错误;由图中晶胞可知,As的配位数为6,则Ni的配
位数也是6,C正确;红砷镍晶体密度
,D错误。
11.答案:C
解析: 分子中心原子As的价层电子对数为 ,中心原子As的杂化方式
为 杂化,分子的空间结构为三角锥形,A项错误;同周期从左到右元素的第一电离能呈增大趋势,但N的2p轨道半充满,较稳定,N的第一电离能大于O的,同主族元素从上到下第
一电离能逐渐减小,第一电离能 ,B项错误; 与 都为3原子、价电子总数
为22的微粒,C项正确;1个 中含有σ键和π键的个数均为10,个数比为 ,D项
错误。
12.答案:B
解析: 的中心N原子的价层电子对数为3,无孤电子对, 的空间结构为平面三角形,
A错误;由图可知, 与 的最小核间距为晶胞体对角线长的1/4,B正确; 晶体中阴
离子的配位数为8,阳离子的配位数为4,阴离子和阳离子的配位数之比为2:1,C错误;反
应物中的S属于分子晶体,但木炭粉不属于共价晶体,D错误。
13.答案:(1)11;BD
(2)铁失去三个电子后,价电子排布为 为半充满稳定状态,再失去一个电子需要的
能量较高
(3)①O>N>C>H
②4; ;
(4)氯化亚铁为离子晶体,熔化时需要破坏离子键,而氯化铁为分子晶体,熔化时需要破坏
分子间作用力
(5) ;
解析:(1)基态铁原子的核外电子排布式是 ,只有3d轨道上有4个未
成对电子,故成对电子对数是 。电子由能量高的轨道跃迁到能量低的轨道会产生
发射光谱,由此可以得出B、D转化过程中会产生发射光谱。
(2)铁原子失去的第1、2个电子是最外层的4s轨道上的电子,电离能差值小,失去的第
3~5个电子是3d轨道上的电子,失去第3个电子时达到 半充满稳定状态,再失去一个电
子吸收的能量最多。
(3)①元素的非金属性越强,其电负性越强,故电负性:O>N>C>H。②配体中的 与N通
过孤电子对与 之间形成配位键,故配位数是4,配体是 ;分子中碳原子有
两种杂化类型。
(4)氯化亚铁是离子晶体,熔化时需要破坏离子键,氯化铁是分子晶体,熔化时需要破坏分子间作用力,所以二者熔点存在差异。
(5)晶胞中8个N位于顶角、1个N位于体心,N的个数是 ,8个Fe位于棱上、
16个Fe位于面上、6个Fe位于体内,Fe的个数为 ,故该化合物的化学式
是 。其密度 。
14.答案:(1) ;O>N>C
(2) 键能大,且断裂第一个π键需消耗较多能量;AB
(3)<;电负性:O>N>H, 中N的电子云密度逐渐减小,与 形成配
位键的能力逐渐减弱,则碱性逐渐减弱
(4)sp;直线形
(5)①abc
②
解析:(1)基态N原子的核外电子排布式为 ,故其价层电子排布式为 。基
态原子O、N、C失去最外层一个电子后,其核外电子排布式分别为
,+1价O的p轨道处于半充满稳定状态,故C、N、O的第二电
离能:O>N>C。
(2)由题给数据可知, 键能大,而且 的键能相差 ,即断裂
第一个π键需消耗较多能量,故 性质稳定。 经水解得到 ,发生非氧化还
原反应,则 中N为-3价,C为+4价,其电子式为 ,故 中含有离
子键、极性共价键。
(3) 分子中N的价层电子对中含有一对孤电子对,而 分子与 通过配位键形成
后,N原子的价层电子中不含孤电子对,孤电子对与成键电子对之间的斥力大
于成键电子对之间的斥力,故键角 。 分
子的N原子均含有孤电子对,能通过配位键与 结合, 在结构上分别可看作—OH、 取代了 分子中的一个H,电负性:O>N>H,因而N的电子云密度:
,N的电子云密度越小,与 形成配位键的能力越弱,物质的碱性就
越弱,所以碱性: 。
(4) 的中心原子的价层电子对数=σ键电子对数+中心原子的孤电子对数
,根据价层电子对互斥理论,可知 的中心原子N采取sp杂
化, 的空间结构为直线形。
(5)①根据晶胞结构特点,可以得出a、b、c符合题意;②根据六方晶胞的结构特点,可以
得出Ca原子位于晶胞顶点、面心和体内,个数为 ,N原子位于棱上和体
内,个数为 ,该晶胞的体积 ,则晶胞的密度
,则 。
15.答案:(1)
(2)3;
(3)铬的第二电离能是失去半充满的3d能级上的电子;锰的第二电离能是失去4s能级上的
电子,更容易失去,所需能量更少
(4) ;正四面体
(5)
解析:(1)每个八面体中有1个 、6个 ,而八面体处在晶胞的顶点和面心,所以1
个晶胞中所含 的个数为 的个数为 ;四面体中心为硼原子,
顶点均为氢原子,8个四面体都处在晶胞内部,所以一个晶胞中所含 的个数为8,所以该
物质的化学式为 。
(2)基态硼原子的核外电子排布式为 ,三个能级上有电子,基态硼原子中有3种不同能量数值的电子;基态氮原子的价电子排布式为 ,所以价电子排布图为
。
(3)铬的第二电离能是失去半充满的3d能级上的一个电子;锰的第二电离能是失去4s能级
上的一个电子,更容易失去,所需能量更少。
(4) 中,N原子周围有一个孤电子对和三个N—H键,共四个价层电子对,
所以N形成的杂化轨道类型为 ;在 中,硫原子周围的孤电子对数
,有四个σ键电子对,根据价层电子对互斥模型, 的立体构型为正
四面体。
(5)由题意可知,晶胞棱长 ,所以一个晶胞的体积为 ,一
个 的质量为 ,而一个晶胞里含有四个 ,所以该物质
的密度为 。