文档内容
(4)氧化还原反应——2025届高考化学二轮复习易错重难提升【新高
考】
一、易错点分析
考点一 氧化还原反应基本概念
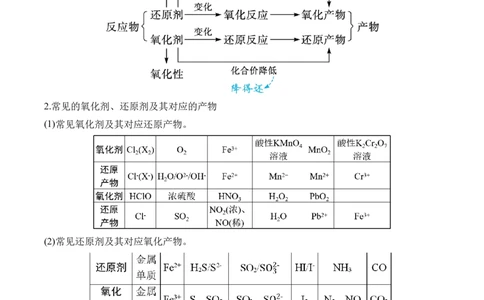
1.理清两条概念线索
2.常见的氧化剂、还原剂及其对应的产物
(1)常见氧化剂及其对应还原产物。
(2)常见还原剂及其对应氧化产物。
考点一 氧化还原反应的规律
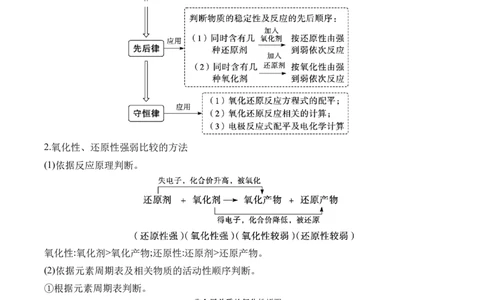
1.氧化还原反应中的“四大规律”2.氧化性、还原性强弱比较的方法
(1)依据反应原理判断。
氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
(2)依据元素周期表及相关物质的活动性顺序判断。
①根据元素周期表判断。
②根据金属活动性顺序判断。③根据非金属活动性顺序判断。
(3)依据电化学原理判断。
①原电池:一般情况下,两种不同的金属构成原电池的两极,还原性:负极>正极。
特例:Al、Mg和NaOH溶液构成原电池,因Mg不能与NaOH溶液反应,负极是相对不活泼的Al
②电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的
阴离子的还原性较强。
3.氧化还原反应方程式的配平步骤及方法
二、易错训练
1.下列实验中的现象及现象过程中与氧化还原反应无关的是( )选项 A B C D
过量的硫酸亚铁溶 向碳酸钠溶液中边 紫色石蕊试液
漂白粉长期暴露在潮
实验 液加入到高锰酸钾 振荡边滴加稀盐酸 滴入新制氯水
湿的空气中
溶液中 直至过量 中
现象及 最初没有现象,继 白色粉末失效最终变
紫色褪去,溶液最 溶液变红,随
现象过 续滴加稀盐酸产生 成团块,无法均匀地
终变为浅黄色 后迅速褪色
程中 气泡 溶解在水中
A.A B.B C.C D.D
2.硝酸工业尾气中的NO、 可用火碱溶液吸收,有关化学反应为:
① ;
② 。
下列说法错误的是( )
A.反应①、②均为氧化还原反应
B.反应①中氧化产物与还原产物的物质的量之比为1:1
C.若尾气可以被完全吸收,则尾气中 与NO的体积之比可能大于1:1
D.反应②中,生成2mol 共转移电子的物质的量为2mol
3.电视剧中美轮美奂的“仙境”,其中所需的烟雾是在置于温热石棉网上的 和Zn粉
混合物中滴几滴水后能持续产生白烟,涉及反应: 。下
列有关说法中错误的是( )
A.上述反应属于氧化还原反应
B.氮气既是氧化产物也是还原反应
C.在标准状况下,11.2L 中所含电子的物质的量为6mol
D.每生成1molZnO共转移5mol电子
4.常温下,实验室可用 和浓盐酸反应制取 ,反应原理为,下列说法正确的是( )
A.该反应中 是氧化剂,发生还原反应
B.该反应中氧化剂与还原剂的物质的量之比为1:8
C.该反应说明氧化性:
D.该反应中每消耗 ,生成
5.锅炉水内溶解的氧气易对锅炉造成腐蚀,为了保证锅炉的安全正常使用,常使用联氨(
)处理锅炉水中溶解的氧,部分转化关系如图所示。下列说法错误的是( )
A.液态 不能导电
B.反应①②③④均属于氧化还原反应
C.反应②中,每生成23.2g ,生成0.1mol
D.反应①的电子转移可表示为
6.某运载火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈
反应产生大量气体并释放出大量的热,该反应的化学方程式为
,则下列叙述错误的是( )
A.此反应是氧化还原反应 B.反应瞬间产生大量高温气体,推动火箭飞行
C.R的分子式为 D.在反应中 作还原剂
7.以太阳能为热源分解 ,铁氧化合物循环分解水制 的过程如图所示。下列说法错误
的是( )A.过程Ⅰ、Ⅱ发生的反应均属于氧化还原反应
B.该制氢过程中,固体的颜色不会发生变化
C.过程Ⅰ中每消耗116gFe O 理论上转移2mol电子
3 4
△
D.过程Ⅱ的化学方程式为3FeOH O(g) Fe O H
2 3 4 2
8.CuCl在有机合成中常用作催化剂或还原剂,其一种制备方法为
,下列说法错误的是( )
A.氧化剂和还原剂的物质的量之比为2∶1
B.还原产物为CuCl
C.电子转移的方向和数目可表示为
D.每转移1mol ,生成 的质量为142g
9.根据下列反应判断,有关物质的氧化性由强到弱的顺序正确的( )
① ② ③
A. B.ClO Cl Fe2 Cu2
2
C.ClO Cl Cu2 Fe2 D.
2
10.在特定碱性条件下,过量 可将Cr(Ⅲ)完全氧化成Cr(Ⅵ),其反应为
(未配平),下列有关说法正确的是( )
A.Y为
B.上述反应中氧化剂和还原剂的物质的量之比为2:3C.1mol 参加反应时,转移电子的物质的量为6mol
D.在酸性条件下 可以转化为
11.常温下,可混合制备氯气,其化学方程式为:
,下列说法错误的是( )
A.与 和浓盐酸制 比较可知,氧化性:
B.标准状况下,生成5.6L 时,转移的电子数目为0.5
C.该反应中HCl只表现出还原性
D.该反应中1mol 被还原,则有5molHCl被氧化
12.溶液中有如下反应(未配平): ,有
关叙述正确的是( )
A.当有1mol电子转移时,消耗硫酸1mol
B.消耗3mol ,有0.5mol 被还原
C.反应中氧化剂和还原剂物质的量之比为6∶1
D.若用 代替 ,上述反应的离子方程式不变
13. 去除酸性废水中 的反应机理如图所示(图中“HS・”为自由基)。下列
说法正确的是( )
A.X的化学式为
B.1molHS・自由基含18mol电子
C.步骤Ⅲ反应中氧化产物与还原产物的物质的量比为8:1
D.步骤Ⅳ生成1mol 需要67.2L 气体
14.化学与生产、生活、环境息息相关。从化学视角回答下列问题:
(1)钠在空气中的燃烧产物A可用于呼吸面具或潜水艇中氧气的来源,涉及的主要反应的
化学方程式为_______(写一种即可)。(2)家庭的厨卫管道内常因留有油脂、毛发、菜渣、纸棉纤维等而造成堵塞,此时可用固体
管道疏通剂进行疏通。管道疏通剂主要成分为铝和氢氧化钠,疏通管道时发生反应的离子方
程式是_______。
(3)亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防
微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用。已知 能发生反应:
。
①配平上述化学方程式,并用“双线桥”标明电子转移的方向和数目_______。
②氧化剂与还原剂的物质的量之比为_______;反应中转移0.3mol电子时生成标准状况下的
NO_______L。
③误食 会导致血红蛋白中的 转化为 而中毒,可服用维生素C解毒,维生素C
在解毒过程中作_______剂。
15.双氧水是工业上常用的绿色氧化剂,也是治疗创伤伤口的消毒剂以及环境消毒剂,贮存时
见光、受热或有杂质进入会加快分解速率。氨水具有部分碱的通性,受热易分解,实验室中
密封保存。回答下列问题。
(1)双氧水用于伤口的消毒,是利用 的___________性(填“强氧化”或“强还原”)。
(2)向双氧水中滴加酸性 溶液,溶液的紫红色褪去,说明 具有___________性
(填“氧化”或“还原”)。
(3)过氧化钙( )是一种水产养殖增氧剂。一种过氧化钙的制备方法如下:在冰水浴
的环境下,向饱和 溶液中加入双氧水和氨水,不断搅拌,析出纯度较高的
晶体。
①该反应在冰水浴环境下进行的目的是___________。
② 作增氧剂,与水反应的化学方程式为___________。
(4)酸性条件下,向双氧水中加入 或 ,发生反应的过程表示如图所示:
① 在过程ⅰ、ⅱ中表现出氧化性的是___________(填“ⅰ”或“ⅱ”)。②过程ⅰ中发生反应的化学方程式为 ,用单线桥法表示
该反应中电子转移的方向和数目:___________,该反应中每生成标准状况下 ,转移
电子的物质的量为___________。
③过程ⅱ中发生反应的化学方程式为___________。答案以及解析
1.答案:B
解析:B.向碳酸钠溶液中边振荡边滴加稀盐酸直至过量,起初生成 和NaCl,
与HCl继续反应生成NaCl、 等,有气泡产生,B符合题意。
2.答案:D
解析:A.反应①、②中均有元素化合价变化,均为氧化还原反应,故A正确;
B.反应①中氧化产物 与还原产物 的物质的量之比为1:1,故B正确;
C.若尾气可以被完全吸收,则尾气中 与NO的体积之比可能大于1:1或等于1:1,故C
正确;
D.反应②中,生成2mol 共转移电子的物质的量为1mol,故D错误;
故选D。
3.答案:C
解析:锌元素的化合价升高,锌作还原剂,ZnO是氧化产物, 中氮元素的化合价既
升高又降低,故氨气既是氧化产物也是还原产物,A、B两项均正确;标准状况下,11.2L
的物质的量为0.5 mol,其所含电子的物质的最为0.5 mol×14-7 mol,C项错误;由元素的化合
价变化可知。每生成1 mol ZnO共转移5 mol电子,D项正确。
4.答案:AC
解析:A.该反应中 是氧化剂,发生还原反应,故A正确;
B.该反应中氧化剂与还原剂的物质的量之比为 ,故B错误;
C.该反应中氧化剂是 ,氧化产物是 ,氧化剂的氧化性大于氧化产物,所以氧化性:
,故C正确;
D.该反应中每消耗2mol ,生成5mol ,但是没有说明气体所处的温度和压强,无法
计算气体的体积,故D错误;
故选AC。
5.答案:C
解析:C.反应②的化学方程式为 , 的物质
的量为 ,根据方程式可知生成0.025mol ,故C错误。6.答案:D
解析:A.N元素在反应物中以化合态存在,反应生成氮气,N元素化合价变化,反应是氧化
还原反应,故A正确;
B.偏二甲肼和四氧化二氮剧烈反应产生大量气体并释放出大量的热,瞬间产生大量高温气体,
推动火箭飞行,故B正确;
C.根据原子守恒可知,偏二甲肼的分子式为 ,故C正确;
D. 中N元素化合价降低, 是氧化剂,偏二甲肼中所含元素化合价一定有升高,故
偏二甲肼作还原剂,故D错误;
故选:D。
7.答案:C
解析:过程Ⅰ、Ⅱ发生的反应均有单质生成,元素化合价一定发生了变化,发生了氧化还原
反应,A项正确;FeO和 均为黑色固体,固体的颜色不会发生变化,B项正确;116g
的物质的量为0.5mol,生成FeO时,理论上转移1mol电子,C项错误;根据流程中给
出的信息,判断反应物和生成物,过程Ⅱ的化学方程式为 ,D项
正确。
8.答案:D
解析:每转移1mol ,生成的 的质量为71g,D项错误。
9.答案:C
解析:氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;反应①中氧化剂为 ,
氧化产物为 ,则氧化性: ;反应②中氧化剂为 ,氧化产物为 ,则氧
化性: ;反应③中氧化剂为 ,氧化产物为 ,则氧化性: ,所以
氧化性由强到弱的顺序为 ,故C正确;
故选:C。
10.答案:D
解析:配平该反应为 ,可知Y为 ,A错误;该反应
氧化剂为 ,还原剂为 ,二者物质的量之比为3:2,B错误;1mol 参加反应时,
转移电子的物质的量为2mol,C错误;在酸性条件下 可以转化为 ,离子方程式为,D正确。
11.答案:C
解析:A. 和浓盐酸制 ,需要加热,用高锰酸钾与浓盐酸制备氯气常温就可以,所以
氧化性: ,故A说法正确;
B.根据化学方程式中Mn元素的化合价变化,可知生成5mol 需转移电子数目为10 ,所
以当生成5.6L 时,即0.25mol ,则转移的电子数为0.5 ,故B说法正确;
C.该反应中HCl不仅表现出还原性,还表现出酸性,因为该反应还生成了KCl、
,故C说法错误;
D.通过化学方程式可知,2mol 被还原,有10molHCl被氧化,故1mol 被还原,
则有5molHCl被氧化,故D说法正确;
本题答案C。
12.答案:B
解析:A.由分析可知,反应消耗3mol硫酸时,反应转移6mol电子,则有1mol电子转移时,
消耗硫酸的物质的量为1mol× =0.5mol,故A错误;
B.由分析可知,反应消耗6mol亚铁离子时,被还原氯酸根离子的物质的量为1mol,则反应
消耗3mol亚铁离子时,被还原氯酸根离子的物质的量为1mol× =0.5mol,故B正确;
C.由分析可知,反应中氧化剂氯酸钠和还原剂硫酸亚铁的物质的量之比为1∶6,故C错误;
D.硝酸具有强氧化性,也能与亚铁离子发生氧化还原反应,则用硝酸代替硫酸,题给反应的
反应的离子方程式会发生变化,故D错误;
故选B。
13.答案:A
解析:A.正确;B.1molHS・自由基含17mol电子,B错误;C.氧化产物与还原产物的物质的
量比为1:8,C错误;D.没有标准状况,D错误。
14.答案:(1) 或
(2)(3) ;1∶1;6.72;还原
解析:(1)钠在空气中的燃烧产物A为过氧化钠,可用于呼吸面具或潜水艇中氧气的来源,
涉及的主要反应是过氧化钠与水或二氧化碳反应生成氧气,化学方程式为
或 。故答案为:
或 ;
(2)管道疏通剂主要成分为铝和氢氧化钠,反应生成偏铝酸钠和氢气,疏通管道时发生反应
的离子方程式是 。故答案为:
;
(3)①在反应中,N元素的化合价从+3价降低到了+2价,得到了1mol电子,I元素的化合
价从-1价升高到了0价,共失去电子2mol,根据电子守恒,所含以氮元素的物质前边都乘以
系数2,碘单质系数是1,根据原子守恒,NaI前边式系数2,HI前边式系数4,水的前边是
系数2, ,用“双线桥”标明电子转移的方向和
数目 。故答案为:
;
②氧化剂 与还原剂HI的物质的量之比为1∶1;由方程式每转移1mol电子生成
1molNO,反应中转移0.3mol电子时生成标准状况下的0.3mol×22.4L/mol=6.72LNO。故答案为:1∶1;6.72;
③误食 会导致血红蛋白中的 转化为 而中毒,可服用维生素C解毒,将 还
原为 ,维生素C在解毒过程中作还原剂。故答案为:还原。
15.答案:(1)强氧化
(2)还原
(3)①防止温度过高, 和NH H O分解
3 2
②2CaO 2H O 2Ca(OH) O
2 2 2 2
(4)①ⅱ
② ;1mol
③5H O I 2HIO 4H O
2 2 2 3 2
解析:(1)H O 具有强氧化性,能用来消毒杀菌;
2 2
(2)酸性KMnO 溶液的紫红色褪去转化为 ,元素的化合价降低,KMnO 作氧化剂,
4 4
则 作还原剂,表现还原性;
(3)①H O 和NH H O受热易分解,在冰水浴环境下反应的目的是防止温度过高,H O
2 2 3 2 2 2
和NH H O分解;
3 2
②CaO 与水的反应类似Na O 与水的反应,CaO 与水反应生成 和O ,反应的化学
2 2 2 2 2
方程式为 。