文档内容
氯气的性质
(40分钟 70分)
一、选择题(本题包括12小题,每小题3分,共36分)
1.烟是由固体小颗粒分散到空气中形成的分散系。下列反应中,能产生白烟的
是
( )
A.铜在氯气中燃烧
B.钠在氯气中燃烧
C.氢气在氯气中燃烧
D.氢气在氧气中燃烧
2.生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有
效的方法保护自己。如果发生了氯气泄漏,以下自救得当的是 ( )
A.用湿毛巾或蘸有肥皂水的毛巾捂住口鼻撤退
B.向地势低的地方撤离C.观察风向,顺风撤离
D.在室内放一盆水
3.下列现象不属于H 在Cl 中燃烧现象的是 ( )
2 2
A.苍白色火焰 B.瓶口有白雾
C.集气瓶内气体颜色变浅 D.爆炸
4.下列氯化物既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的
是 ( )
A.CuCl B.FeCl
2 2
C.NaCl D.FeCl
3
5.下列物质中,同时含有氯气分子和氯离子的是 ( )
A.氯水 B.液态氯化氢
C.液氯 D.氯酸钾溶液
6.(2019·德州高一检测)将适量物质分别加到干燥的红色布条上,不能使其褪
色的是 ( )
A.新制的氯水 B.84消毒液
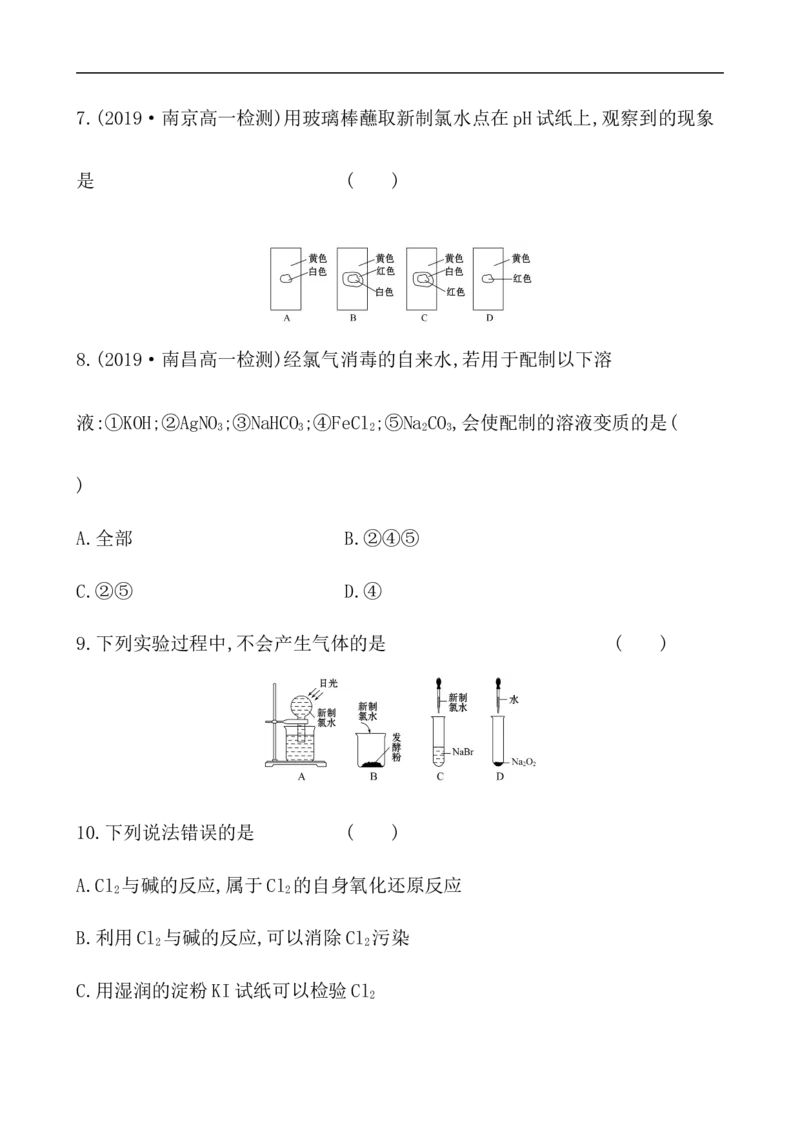
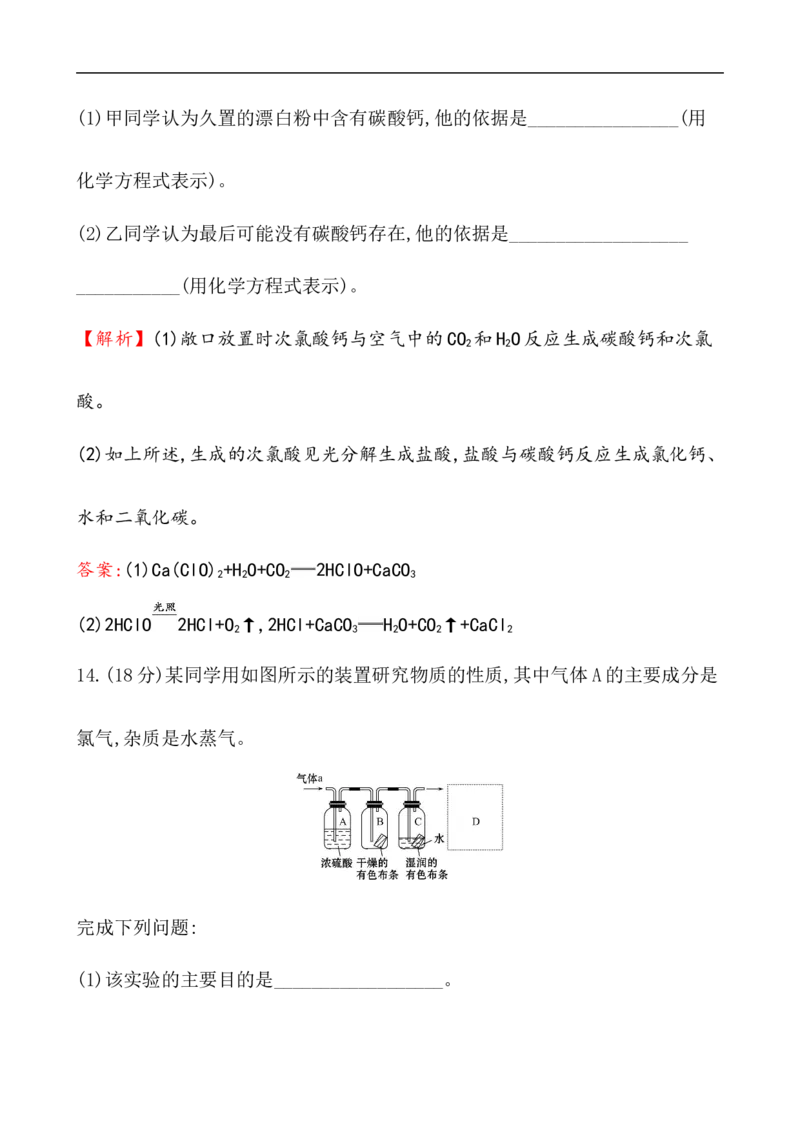
C.液氯 D.次氯酸溶液7.(2019·南京高一检测)用玻璃棒蘸取新制氯水点在pH试纸上,观察到的现象
是 ( )
8.(2019·南昌高一检测)经氯气消毒的自来水,若用于配制以下溶
液:①KOH;②AgNO ;③NaHCO ;④FeCl ;⑤Na CO ,会使配制的溶液变质的是(
3 3 2 2 3
)
A.全部 B.②④⑤
C.②⑤ D.④
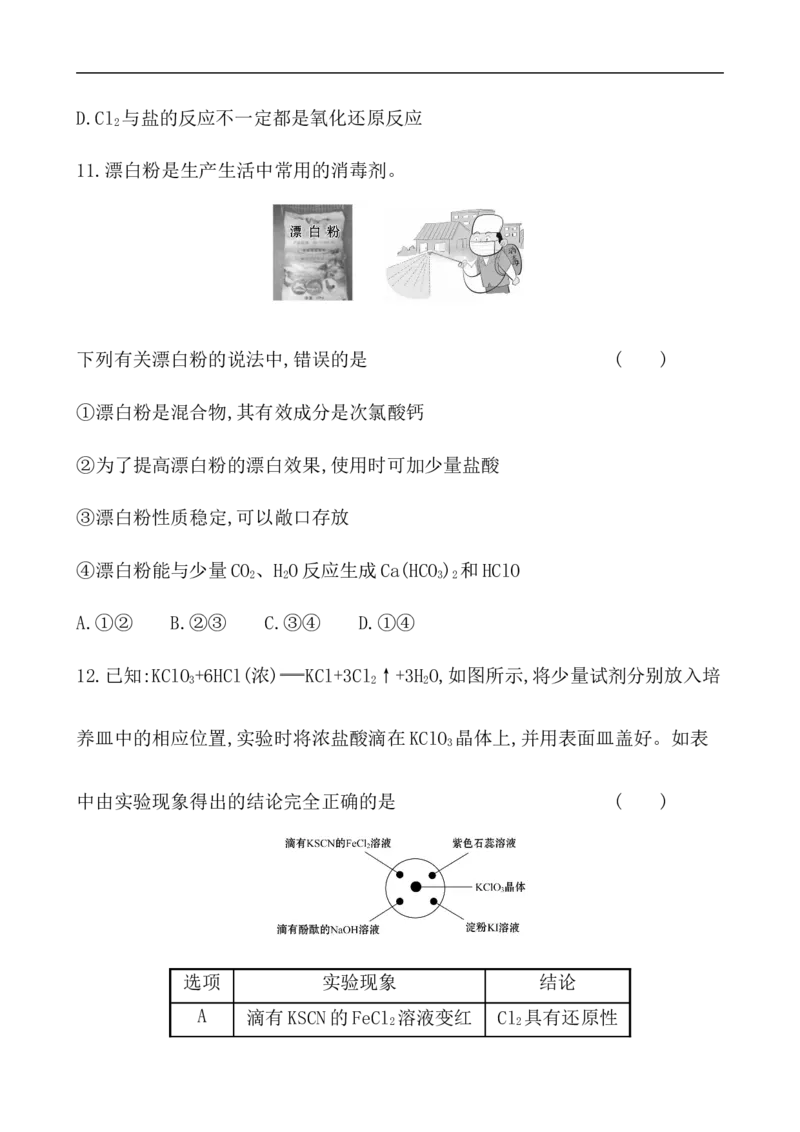
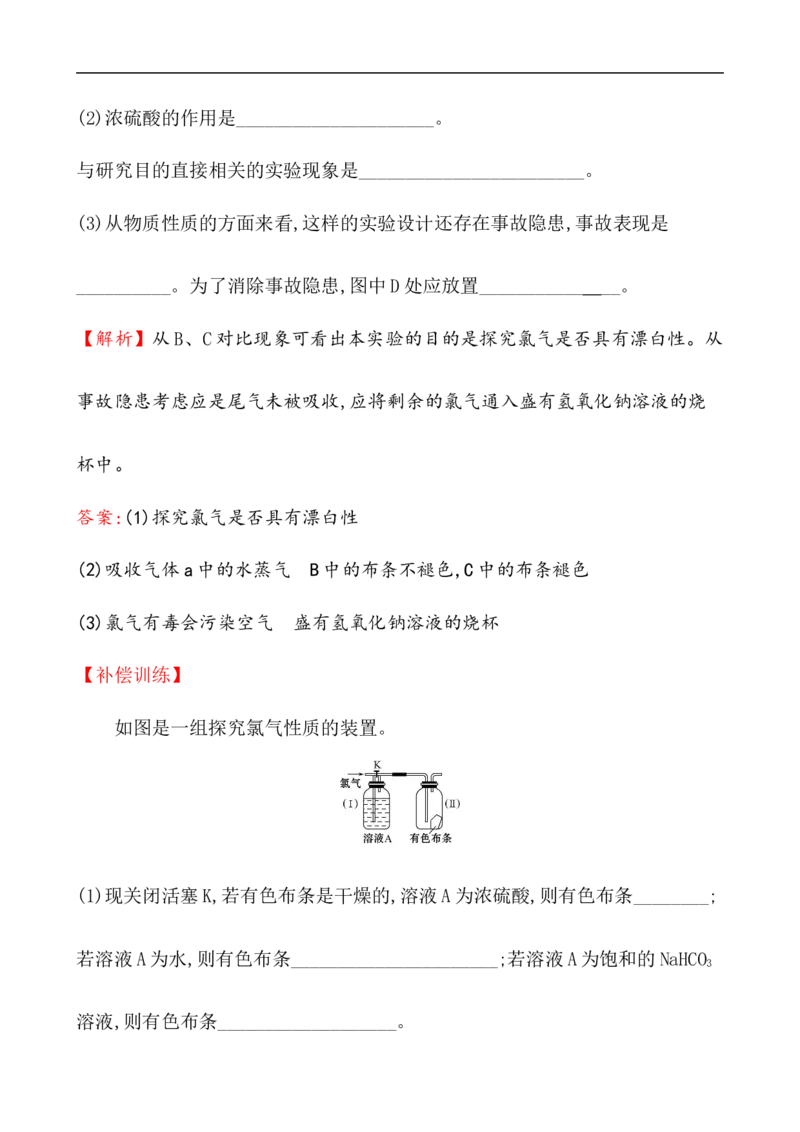
9.下列实验过程中,不会产生气体的是 ( )
10.下列说法错误的是 ( )
A.Cl 与碱的反应,属于Cl 的自身氧化还原反应
2 2
B.利用Cl 与碱的反应,可以消除Cl 污染
2 2
C.用湿润的淀粉KI试纸可以检验Cl
2D.Cl 与盐的反应不一定都是氧化还原反应
2
11.漂白粉是生产生活中常用的消毒剂。
下列有关漂白粉的说法中,错误的是 ( )
①漂白粉是混合物,其有效成分是次氯酸钙
②为了提高漂白粉的漂白效果,使用时可加少量盐酸
③漂白粉性质稳定,可以敞口存放
④漂白粉能与少量CO 、H O反应生成Ca(HCO ) 和HClO
2 2 3 2
A.①② B.②③ C.③④ D.①④
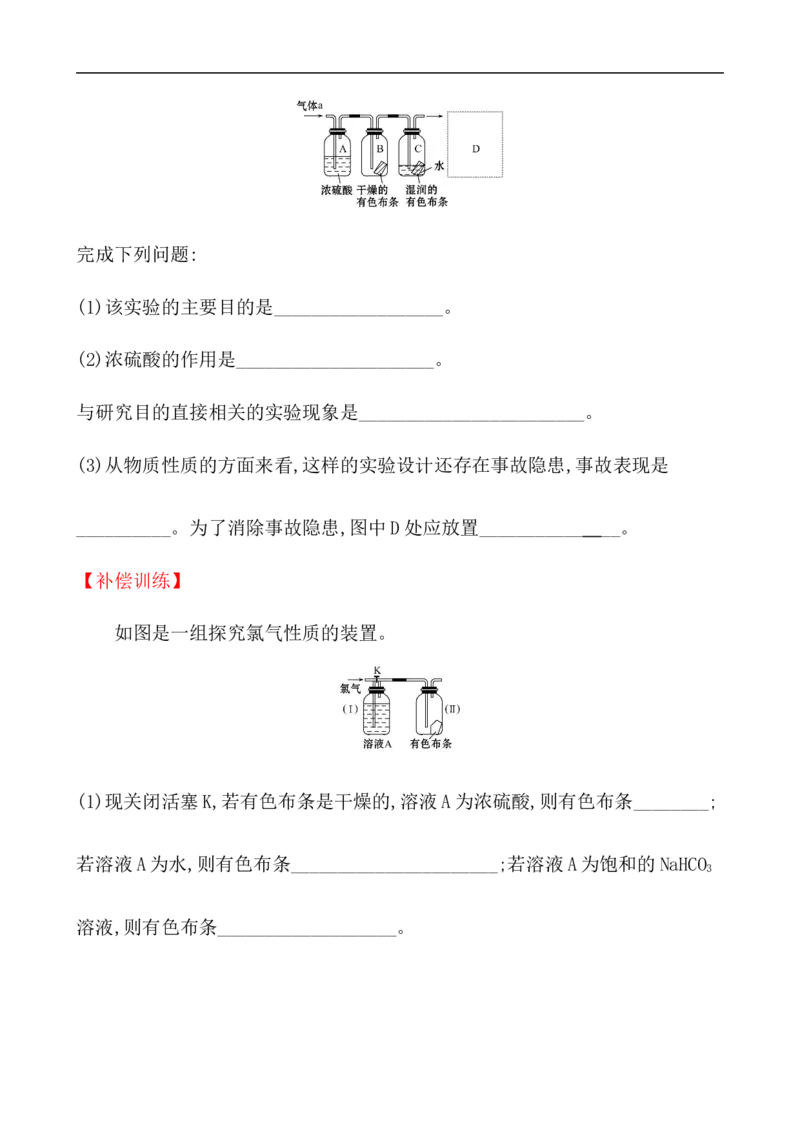
12.已知:KClO +6HCl(浓) KCl+3Cl ↑+3H O,如图所示,将少量试剂分别放入培
3 2 2
养皿中的相应位置,实验时将浓盐酸滴在KClO 晶体上,并用表面皿盖好。如表
3
中由实验现象得出的结论完全正确的是 ( )
选项 实验现象 结论
A 滴有KSCN的FeCl 溶液变红 Cl 具有还原性
2 2B 滴有酚酞的NaOH溶液褪色 Cl 具有酸性
2
C 紫色石蕊溶液先变红后褪色 Cl 具有漂白性
2
D 淀粉KI溶液变为蓝色 Cl 具有氧化性
2
二、非选择题(本题包括2小题,共34分)
13.(16分)漂白粉是一种有较强氯臭的白色粉末,其主要成分是次氯酸钙。漂白
粉主要用于游泳池、工业循环水、饮用水、杀菌卫生防疫、纸浆纱布等的消毒,
其用途非常广泛。
某化学兴趣小组对一瓶敞口放置的漂白粉产生了浓厚的兴趣。
(1)甲同学认为久置的漂白粉中含有碳酸钙,他的依据是________________(用
化学方程式表示)。
(2)乙同学认为最后可能没有碳酸钙存在,他的依据是___________________
___________(用化学方程式表示)。
14.(18分)某同学用如图所示的装置研究物质的性质,其中气体A的主要成分是
氯气,杂质是水蒸气。完成下列问题:
(1)该实验的主要目的是__________________。
(2)浓硫酸的作用是_____________________。
与研究目的直接相关的实验现象是________________________。
(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是
__________。为了消除事故隐患,图中D处应放置___________ __。
【补偿训练】
如图是一组探究氯气性质的装置。
(1)现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条________;
若溶液A为水,则有色布条______________________;若溶液A为饱和的NaHCO
3
溶液,则有色布条___________________。(2)现打开K,溶液a为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有
色布条 ______________________________。
(20分钟 30分)
一、选择题(本题包括2小题,每小题7分,共14分)
15.(2019·东营高一检测)下列物质转化不能通过一步反应直接实现的是
( )
FeCl Cl Ca(ClO) HClO O
2 2 2 2
A.① B.②
C.③ D.④
16.(2019·襄阳高一检测)现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来
区别它们的一种试剂是 ( )
A.AgNO 溶液 B.酚酞溶液
3
C.紫色石蕊溶液 D.饱和食盐水
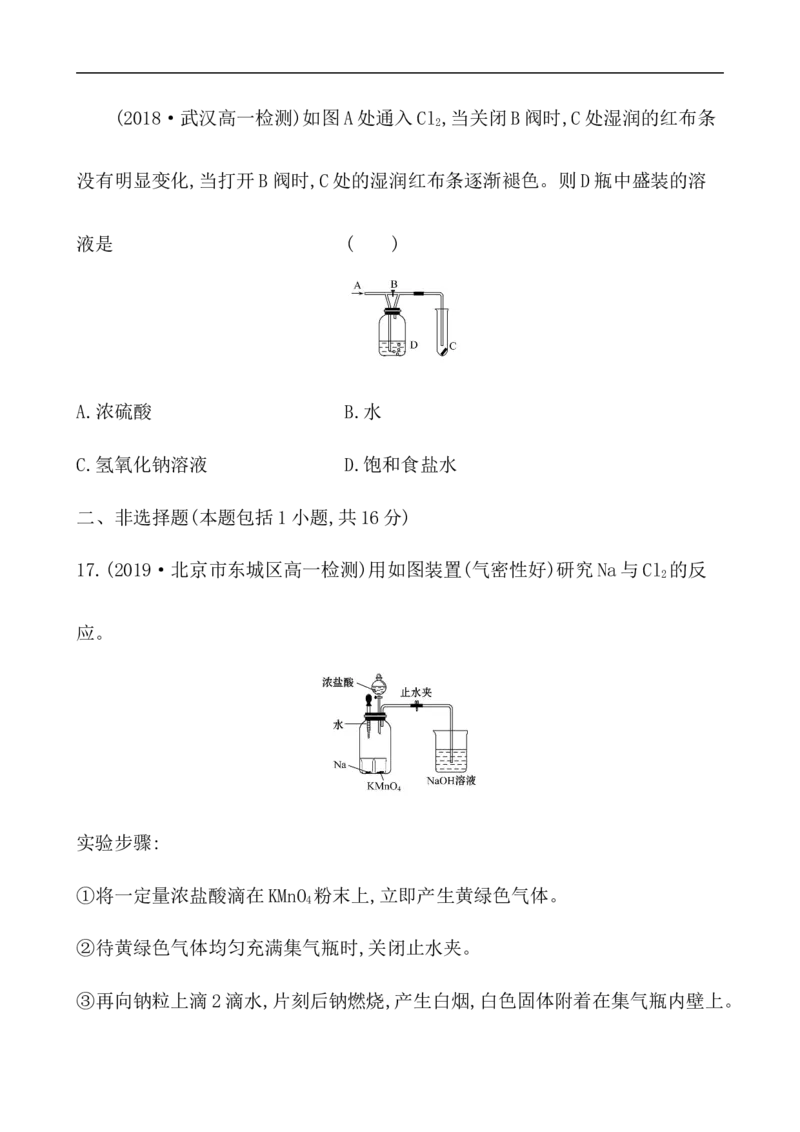
【补偿训练】(2018·武汉高一检测)如图A处通入Cl ,当关闭B阀时,C处湿润的红布条
2
没有明显变化,当打开B阀时,C处的湿润红布条逐渐褪色。则D瓶中盛装的溶
液是 ( )
A.浓硫酸 B.水
C.氢氧化钠溶液 D.饱和食盐水
二、非选择题(本题包括1小题,共16分)
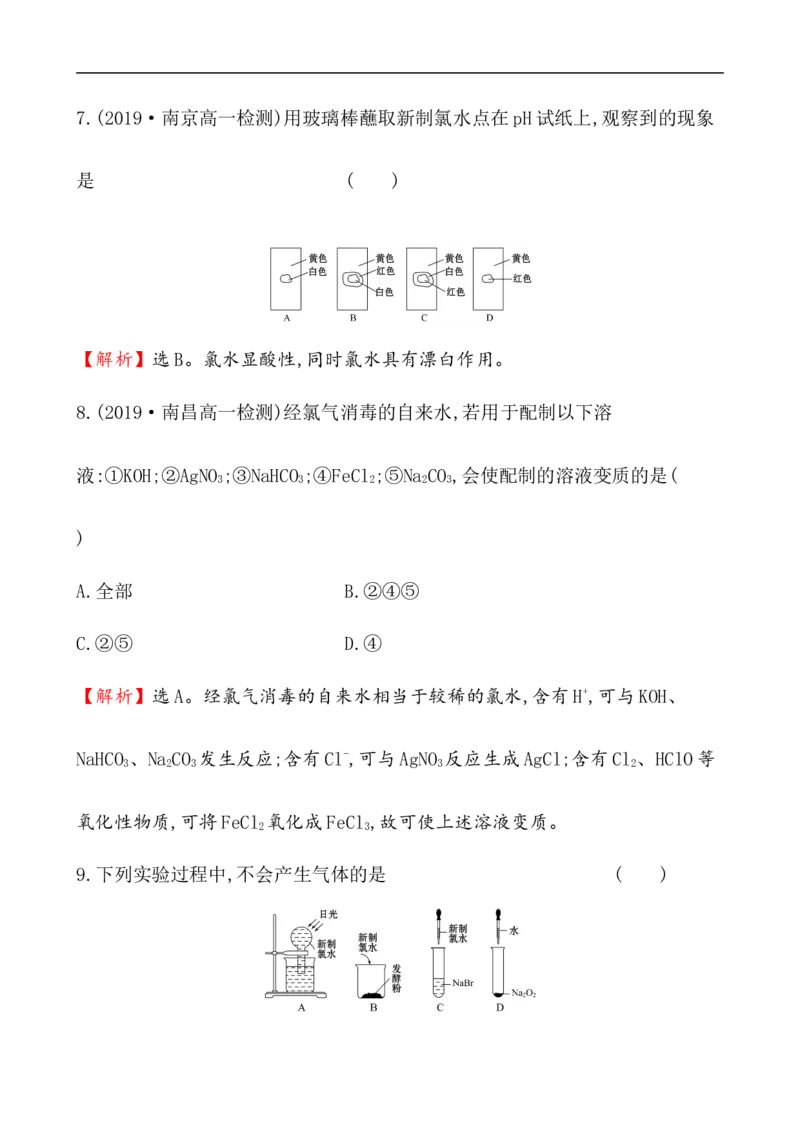
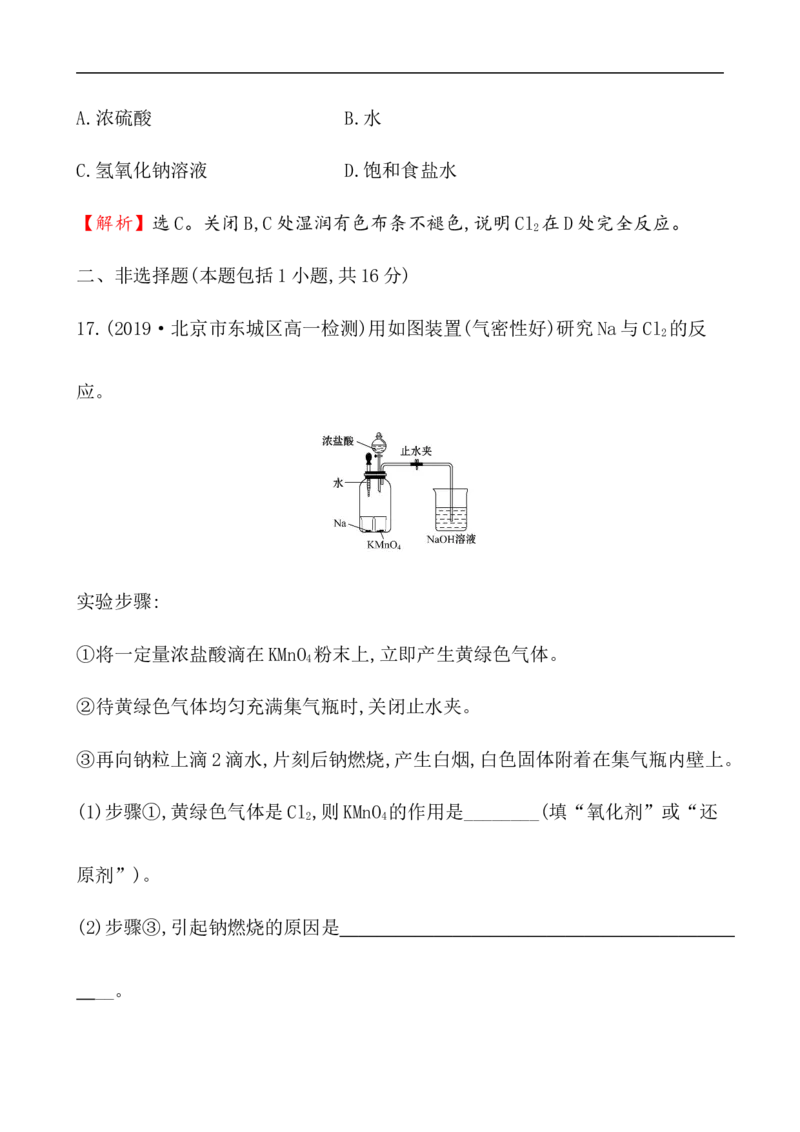
17.(2019·北京市东城区高一检测)用如图装置(气密性好)研究Na与Cl 的反
2
应。
实验步骤:
①将一定量浓盐酸滴在KMnO 粉末上,立即产生黄绿色气体。
4
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。(1)步骤①,黄绿色气体是Cl ,则KMnO 的作用是________(填“氧化剂”或“还
2 4
原剂”)。
(2)步骤③,引起钠燃烧的原因是
__。
(3)生成白色固体的化学方程式是 __。
(4)结合离子方程式说明NaOH溶液的作用是
__。
【补偿训练】
为了探究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄
绿色褪去并同时产生气体。
实验二:取实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。
②该清液中滴加碳酸钠溶液产生白色沉淀。
③该清液中滴加盐酸可产生大量气体。
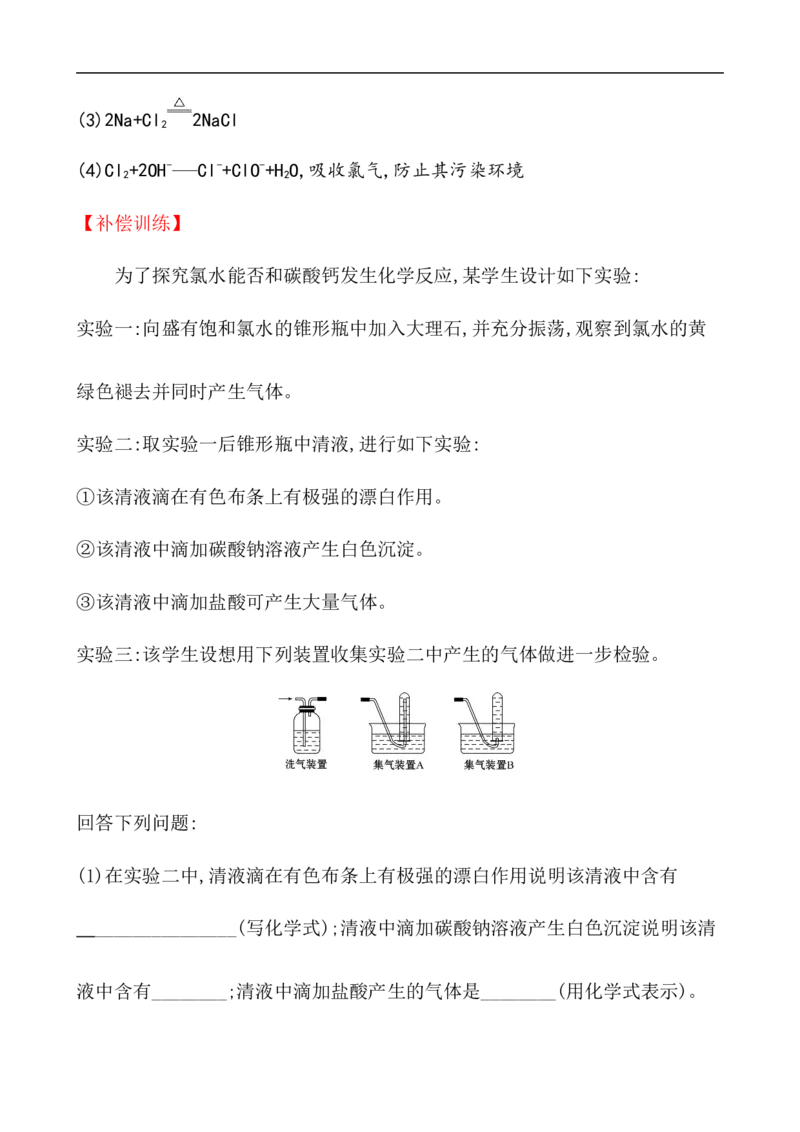
实验三:该学生设想用下列装置收集实验二中产生的气体做进一步检验。回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有
_______________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清
液中含有________;清液中滴加盐酸产生的气体是________(用化学式表示)。
(2)实验三中,洗气装置内的洗涤液一般用______溶液,用________装置收集。
(3)该学生通过上述实验,写出了氯水和碳酸钙反应的化学方程式:__。氯气的性质
(40分钟 70分)
一、选择题(本题包括12小题,每小题3分,共36分)
1.烟是由固体小颗粒分散到空气中形成的分散系。下列反应中,能产生白烟的
是
( )
A.铜在氯气中燃烧
B.钠在氯气中燃烧
C.氢气在氯气中燃烧
D.氢气在氧气中燃烧
【解析】选B。化学反应中能产生白烟的现象说明有白色固体生成,A项虽有固
体产生但不是白色;C项无固体生成,生成的氯化氢在瓶口有白雾现象。
2.生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有
效的方法保护自己。如果发生了氯气泄漏,以下自救得当的是 ( )A.用湿毛巾或蘸有肥皂水的毛巾捂住口鼻撤退
B.向地势低的地方撤离
C.观察风向,顺风撤离
D.在室内放一盆水
【解析】选A。因肥皂水显弱碱性,可以吸收氯气,A正确;氯气的密度大于空气,
故应向地势高的地方跑,B错误;逆风跑,才可以脱离氯气的笼罩,C错误;氯气与
水反应,其速度慢且反应不充分,D错误。
3.下列现象不属于H 在Cl 中燃烧现象的是 ( )
2 2
A.苍白色火焰 B.瓶口有白雾
C.集气瓶内气体颜色变浅 D.爆炸
【解析】选D。H 在Cl 中燃烧,发出苍白色火焰,瓶口因生成的HCl吸收空气中
2 2
的H O形成盐酸小液滴而形成白雾,瓶内气体颜色因Cl 的消耗而变浅,但不发生
2 2
爆炸。
4.下列氯化物既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的
是 ( )
A.CuCl B.FeCl
2 2
C.NaCl D.FeCl
3【解析】选C。A项,铜与盐酸不反应,错误;B项,铁与氯气反应生成氯化铁,与
盐酸反应生成氯化亚铁,错误;C项,钠与氯气或盐酸反应均生成氯化钠,正确;D
项,根据B中分析可知D错误。
5.下列物质中,同时含有氯气分子和氯离子的是 ( )
A.氯水 B.液态氯化氢
C.液氯 D.氯酸钾溶液
【解析】选A。氯气能与水反应生成盐酸和次氯酸,氯水中含有氯气分子、次氯
酸分子、氢离子、氯离子、次氯酸根离子等微粒;液态氯化氢由氯化氢分子构
成,不含氯分子、氯离子;液氯是液态氯分子,不含氯离子;氯酸钾能电离出钾离
子和氯酸根离子(Cl ),不存在氯分子、氯离子。
6.(2019·德州高一检测)将适量物质分别加到干燥的红色布条上,不能使其褪
色的是 ( )
A.新制的氯水 B.84消毒液
C.液氯 D.次氯酸溶液
【解析】选C。液氯为液态Cl ,不能使干燥的红色布条褪色;新制的氯水、84消
2
毒液、次氯酸溶液中都含具有强氧化性的HClO,可使干燥的红色布条褪色。7.(2019·南京高一检测)用玻璃棒蘸取新制氯水点在pH试纸上,观察到的现象
是 ( )
【解析】选B。氯水显酸性,同时氯水具有漂白作用。
8.(2019·南昌高一检测)经氯气消毒的自来水,若用于配制以下溶
液:①KOH;②AgNO ;③NaHCO ;④FeCl ;⑤Na CO ,会使配制的溶液变质的是(
3 3 2 2 3
)
A.全部 B.②④⑤
C.②⑤ D.④
【解析】选A。经氯气消毒的自来水相当于较稀的氯水,含有H+,可与KOH、
NaHCO 、Na CO 发生反应;含有Cl-,可与AgNO 反应生成AgCl;含有Cl 、HClO等
3 2 3 3 2
氧化性物质,可将FeCl 氧化成FeCl ,故可使上述溶液变质。
2 3
9.下列实验过程中,不会产生气体的是 ( )【解析】选C。A项,新制氯水中的HClO见光分解生成氧气,不符合题意;B项,
新制氯水中的H+与发酵粉中的NaHCO 反应生成CO ,不符合题意;C项,新制氯水
3 2
中的Cl 与NaBr反应生成Br 和NaCl,没有气体产生,符合题意;D项,H O与Na O
2 2 2 2 2
反应生成O ,不符合题意。
2
10.下列说法错误的是 ( )
A.Cl 与碱的反应,属于Cl 的自身氧化还原反应
2 2
B.利用Cl 与碱的反应,可以消除Cl 污染
2 2
C.用湿润的淀粉KI试纸可以检验Cl
2
D.Cl 与盐的反应不一定都是氧化还原反应
2
【解析】选D。Cl 与碱(NaOH)溶液反应的化学方程式为Cl +2NaOH NaCl+
2 2
NaClO+H O,该反应前后只有氯元素化合价发生变化,属于Cl 的自身氧化还原反
2 2
应,A、B项正确。因为Cl 的氧化性大于I ,可以发生反应Cl +2KI 2KCl+I ,
2 2 2 2
淀粉遇I 变蓝,故C项正确。Cl 参与的反应,氯元素均有价态变化,都是氧化还
2 2
原反应,故D错误。
11.漂白粉是生产生活中常用的消毒剂。下列有关漂白粉的说法中,错误的是 ( )
①漂白粉是混合物,其有效成分是次氯酸钙
②为了提高漂白粉的漂白效果,使用时可加少量盐酸
③漂白粉性质稳定,可以敞口存放
④漂白粉能与少量CO 、H O反应生成Ca(HCO ) 和HClO
2 2 3 2
A.①② B.②③ C.③④ D.①④
【解析】选C。漂白粉的性质相对于HClO来说比较稳定,但在敞口存放过程中,
会发生反应:Ca(ClO) +CO +H O CaCO +2HClO,2HClO 2HCl+O ↑,使漂白粉逐
2 2 2 3 2
渐失效,故③错误;与少量CO 反应:Ca(ClO) +CO +H O CaCO +2HClO,与过量CO
2 2 2 2 3 2
反应时才生成Ca(HCO ) ,故④错误。
3 2
12.已知:KClO +6HCl(浓) KCl+3Cl ↑+3H O,如图所示,将少量试剂分别放入培
3 2 2
养皿中的相应位置,实验时将浓盐酸滴在KClO 晶体上,并用表面皿盖好。如表
3
中由实验现象得出的结论完全正确的是 ( )选项 实验现象 结论
A 滴有KSCN的FeCl 溶液变红 Cl 具有还原性
2 2
B 滴有酚酞的NaOH溶液褪色 Cl 具有酸性
2
C 紫色石蕊溶液先变红后褪色 Cl 具有漂白性
2
D 淀粉KI溶液变为蓝色 Cl 具有氧化性
2
【解析】选D。A项说明Cl 具有氧化性。B项是Cl 与H O反应生成了有漂白性
2 2 2
的次氯酸。C项是Cl 与H O反应生成的HCl具有酸性,HClO具有漂白性。D项的
2 2
反应为Cl +2KI 2KCl+I ,说明Cl 具有氧化性。
2 2 2
二、非选择题(本题包括2小题,共34分)
13.(16分)漂白粉是一种有较强氯臭的白色粉末,其主要成分是次氯酸钙。漂白
粉主要用于游泳池、工业循环水、饮用水、杀菌卫生防疫、纸浆纱布等的消毒,
其用途非常广泛。
某化学兴趣小组对一瓶敞口放置的漂白粉产生了浓厚的兴趣。(1)甲同学认为久置的漂白粉中含有碳酸钙,他的依据是________________(用
化学方程式表示)。
(2)乙同学认为最后可能没有碳酸钙存在,他的依据是___________________
___________(用化学方程式表示)。
【解析】(1)敞口放置时次氯酸钙与空气中的CO 和H O反应生成碳酸钙和次氯
2 2
酸。
(2)如上所述,生成的次氯酸见光分解生成盐酸,盐酸与碳酸钙反应生成氯化钙、
水和二氧化碳。
答案:(1)Ca(ClO) +H O+CO 2HClO+CaCO
2 2 2 3
(2)2HClO 2HCl+O ↑,2HCl+CaCO H O+CO ↑+CaCl
2 3 2 2 2
14.(18分)某同学用如图所示的装置研究物质的性质,其中气体A的主要成分是
氯气,杂质是水蒸气。
完成下列问题:
(1)该实验的主要目的是__________________。(2)浓硫酸的作用是_____________________。
与研究目的直接相关的实验现象是________________________。
(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是
__________。为了消除事故隐患,图中D处应放置___________ __。
【解析】从B、C对比现象可看出本实验的目的是探究氯气是否具有漂白性。从
事故隐患考虑应是尾气未被吸收,应将剩余的氯气通入盛有氢氧化钠溶液的烧
杯中。
答案:(1)探究氯气是否具有漂白性
(2)吸收气体a中的水蒸气 B中的布条不褪色,C中的布条褪色
(3)氯气有毒会污染空气 盛有氢氧化钠溶液的烧杯
【补偿训练】
如图是一组探究氯气性质的装置。
(1)现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条________;
若溶液A为水,则有色布条______________________;若溶液A为饱和的NaHCO
3
溶液,则有色布条___________________。(2)现打开K,溶液a为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有
色布条 ______________________________。
【解析】(1)关闭K通入Cl ,若A为浓硫酸,则进入(Ⅱ)的是干燥的Cl ,有色布
2 2
条不褪色;若A为水,则进入(Ⅱ)的是湿润的Cl ,有色布条褪色;若A是饱和
2
NaHCO 溶液,则Cl 在(Ⅰ)中被消耗,有色布条不褪色。
3 2
(2)打开K,尽管A是NaOH溶液,湿润的Cl 还是直接进入(Ⅱ),有色布条褪色。
2
答案:(1)不褪色 褪色 不褪色 (2)褪色
(20分钟 30分)
一、选择题(本题包括2小题,每小题7分,共14分)
15.(2019·东营高一检测)下列物质转化不能通过一步反应直接实现的是
( )
FeCl Cl Ca(ClO) HClO O
2 2 2 2
A.① B.②
C.③ D.④
【解析】选A。A.①氯气与铁在点燃条件下反应生成氯化铁,不能一步到位生成
氯化亚铁,选项A符合题意; B.②氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水,可以一步反应直接实现,选项B不符合题意;C.③次氯酸钙与二氧化碳和
水反应生成碳酸钙和次氯酸,可以一步反应直接实现,选项C不符合题意;D.④
次氯酸溶液在光照条件下分解生成盐酸和氧气,可以一步反应直接实现,选项D
不符合题意。
16.(2019·襄阳高一检测)现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来
区别它们的一种试剂是 ( )
A.AgNO 溶液 B.酚酞溶液
3
C.紫色石蕊溶液 D.饱和食盐水
【解析】选C。盐酸遇紫色石蕊溶液变红,NaCl溶液遇紫色石蕊溶液无明显现象,
NaOH溶液遇紫色石蕊溶液变蓝,新制氯水遇紫色石蕊溶液先变红后褪色。
【补偿训练】
(2018·武汉高一检测)如图A处通入Cl ,当关闭B阀时,C处湿润的红布条
2
没有明显变化,当打开B阀时,C处的湿润红布条逐渐褪色。则D瓶中盛装的溶
液是 ( )A.浓硫酸 B.水
C.氢氧化钠溶液 D.饱和食盐水
【解析】选C。关闭B,C处湿润有色布条不褪色,说明Cl 在D处完全反应。
2
二、非选择题(本题包括1小题,共16分)
17.(2019·北京市东城区高一检测)用如图装置(气密性好)研究Na与Cl 的反
2
应。
实验步骤:
①将一定量浓盐酸滴在KMnO 粉末上,立即产生黄绿色气体。
4
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
(1)步骤①,黄绿色气体是Cl ,则KMnO 的作用是________(填“氧化剂”或“还
2 4
原剂”)。
(2)步骤③,引起钠燃烧的原因是
__。(3)生成白色固体的化学方程式是 __。
(4)结合离子方程式说明NaOH溶液的作用是
__。
【解析】(1)该反应中产生的黄绿色气体是氯气,即HCl中氯元素失去电子转化
为氯气,氯元素化合价由-1价变为0价,则HCl是还原剂,故高锰酸钾作氧化剂,
体现氧化性;
(2)Na能在Cl 中燃烧,Na与H O反应放热,达到Na在Cl 中燃烧的着火点,从而
2 2 2
引起钠的燃烧;
(3)Na在Cl 中燃烧生成NaCl,则白色固体是NaCl,反应的化学方程式为2Na+Cl
2 2
2NaCl;
(4)氯气有毒不能直接排空,氯气和水反应生成酸,酸能和碱发生中和反应,所以
NaOH溶液作用是吸收氯气,防止其污染环境,反应的离子方程式为Cl +2OH-
2
Cl-+ClO-+H O。
2
答案:(1)氧化剂
(2)Na与水反应放热,达到Na在Cl 中燃烧的着火点
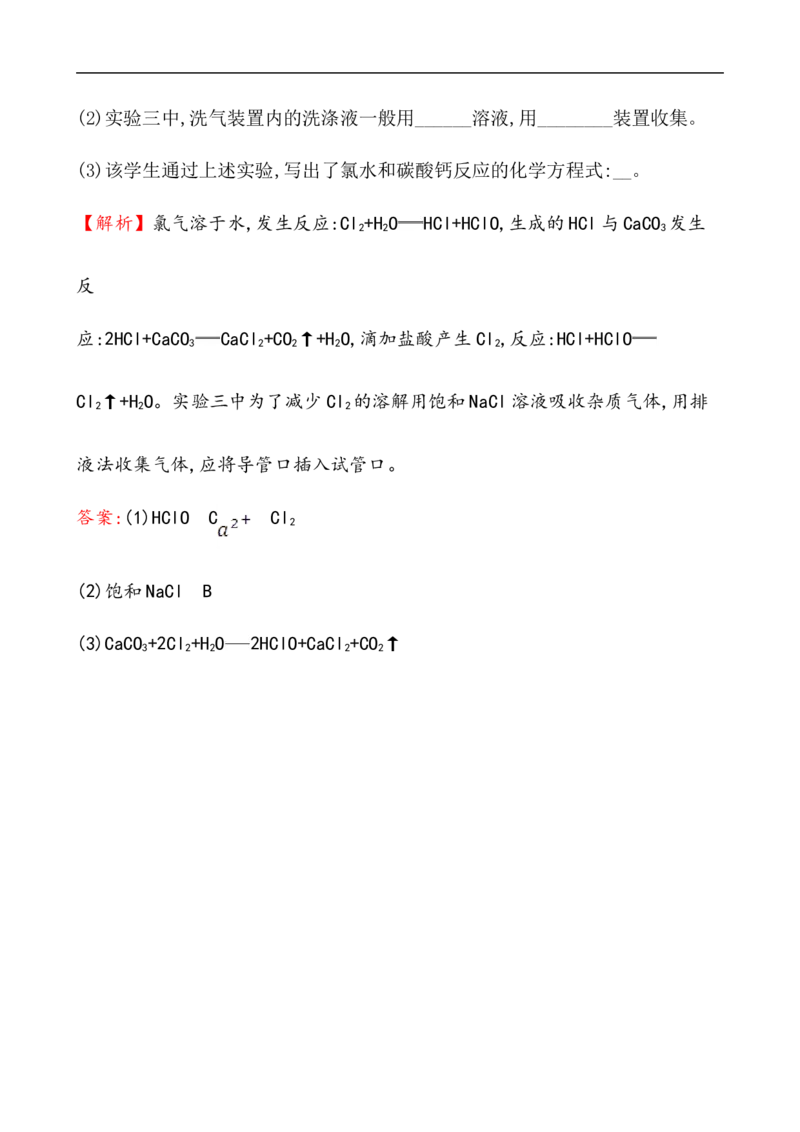
2(3)2Na+Cl 2NaCl
2
(4)Cl +2OH- Cl-+ClO-+H O,吸收氯气,防止其污染环境
2 2
【补偿训练】
为了探究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄
绿色褪去并同时产生气体。
实验二:取实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。
②该清液中滴加碳酸钠溶液产生白色沉淀。
③该清液中滴加盐酸可产生大量气体。
实验三:该学生设想用下列装置收集实验二中产生的气体做进一步检验。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有
_______________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清
液中含有________;清液中滴加盐酸产生的气体是________(用化学式表示)。(2)实验三中,洗气装置内的洗涤液一般用______溶液,用________装置收集。
(3)该学生通过上述实验,写出了氯水和碳酸钙反应的化学方程式:__。
【解析】氯气溶于水,发生反应:Cl +H O HCl+HClO,生成的HCl与CaCO 发生
2 2 3
反
应:2HCl+CaCO CaCl +CO ↑+H O,滴加盐酸产生Cl ,反应:HCl+HClO
3 2 2 2 2
Cl ↑+H O。实验三中为了减少Cl 的溶解用饱和NaCl溶液吸收杂质气体,用排
2 2 2
液法收集气体,应将导管口插入试管口。
答案:(1)HClO C Cl
2
(2)饱和NaCl B
(3)CaCO +2Cl +H O 2HClO+CaCl +CO ↑
3 2 2 2 2