文档内容
能层与能级 构造原理与电子排布式
重难点 题型 分值
1. 通过认识原子结构与核外电子的排布,理解
能层与能级的关系,理解核外电子的排布规
律。
重点
2. 证据推理与模型认知:结合构造原理形成核 选择题、填空
4-6分
外电子排布式书写的思维模型,并能根据思维 题
模型熟练书写1~36号元素的电子排布式。
难点 熟练书写1~36号元素的电子排布式
第1页【温故知新】开天辟地——原子的诞生
1. 原子的诞生
(1)原子的诞生
(2)人类对原子结构认识的演变
2. 宇宙中的元素
(1)宇宙的组成元素及含量
(2)地球的组成元素
绝大多数是金属元素
{ ¿¿¿¿
地球上的元素
一、能层与能级
1. 能层
(1)含义:根据多电子原子的核外电子的能量差异,将核外电子分成不同的能层(电
子层)。
(2)符号:能层序数一、二、三、四、五、六、七……分别用 K 、 L 、 M 、 N 、 O 、
P 、 Q ……表示。
【注意】不同的能层容纳的电子数目最多不超过2n2,n为电子层数。
(3)能量关系:由K能层→Q能层,能量逐渐增大。
能层 一 二 三 四 五 六 七
符号 K L M N O P Q
第2页电子离核远近 近→远
电子能量高低 低→高
2. 能级
(1)含义:根据多电子原子的同一能层的电子的能量也可能不同,将它们分为不同能
级。
(2)表示方法:分别用相应能层的序数和字母 s 、 p 、 d 、 f 等表示,如n能层的能级按
能量由低到高的排列顺序为ns、 n p 、 n d 、nf等。
【注意】n为能层序数
【解读】能层与能级的关系
可用楼层和楼梯表示能层和能级的关系,用楼层表示能层,则楼层间楼梯的阶级表示
能级。
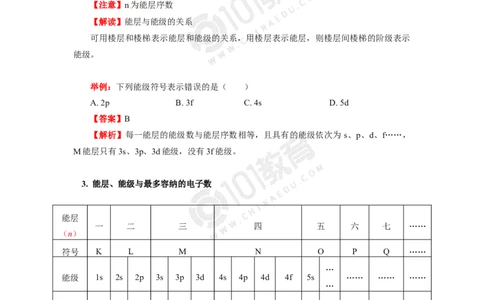
举例:下列能级符号表示错误的是( )
A. 2p B. 3f C. 4s D. 5d
【答案】B
【解析】每一能层的能级数与能层序数相等,且具有的能级依次为 s、p、d、f……,
M能层只有3s、3p、3d能级,没有3f能级。
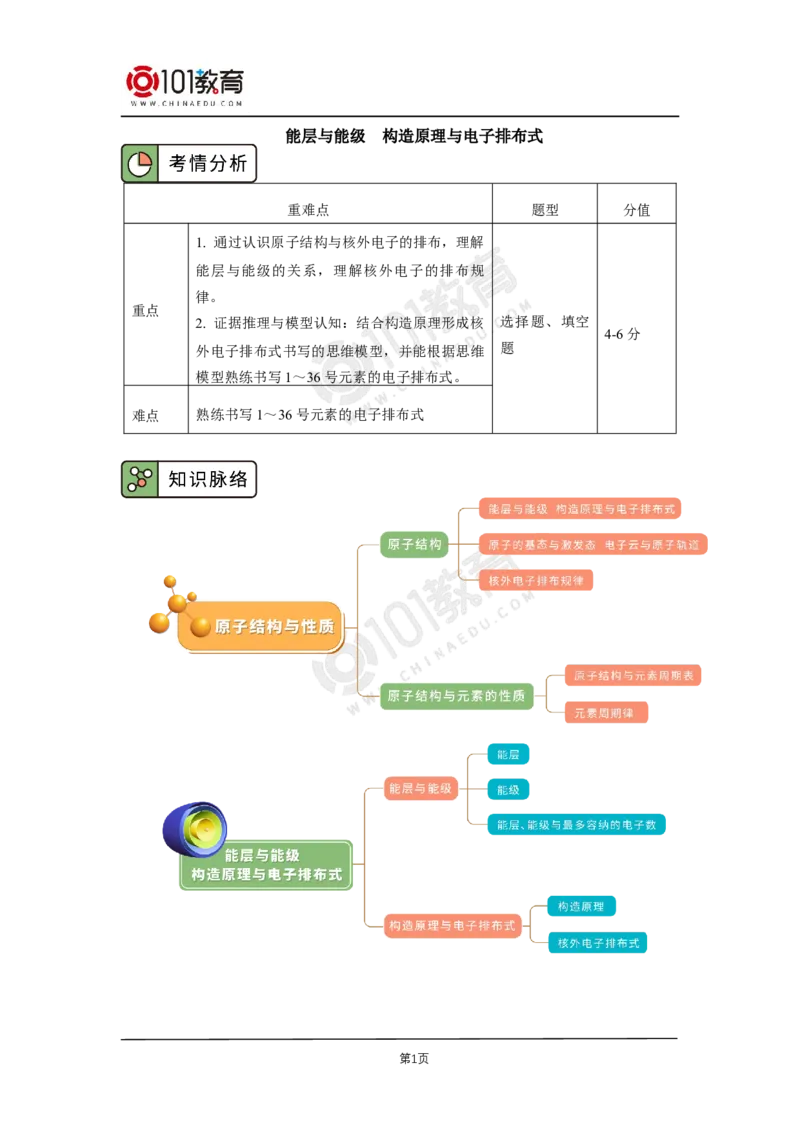
3. 能层、能级与最多容纳的电子数
能层
一 二 三 四 五 六 七 ……
(n)
符号 K L M N O P Q ……
…
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s …… …… ……
…
最多容 …
2 2 6 2 6 10 2 6 10 14 2 …… …… ……
纳的电 …
子数 2 8 18 32 …… …… …… 2n2
由上表可知:
(1)任一能层的能级总是从s能级开始,能层序数等于该能层所包含的能级数,如第
三能层有3 个能级。
(2)以s、p、d、f……排序的各能级可容纳的最多电子数依次为1、3、5、7……的2
倍。
第3页(3)英文字母相同的不同能级中所容纳的最多电子数相同。例如:1s、2s、3s、
4s……能级最多都只能容纳2个电子。
【总结提升】能层中各能级的能量关系
(1)在相同能层各能级能量由低到高的顺序是nsE >E 。
ns (n-1)s (n-2)s
③E <E <E <E (能级交错)
ns (n-2)f (n-1)d np
【易错警示】“能级交错”现象:由构造原理可知,核外电子排布的能级顺序为1s、2s、
2p、3s、3p、4s、3d、4p、5s、4d、5p、6s、4f、5d、6p、7s……从中可以看出,从第三能
层开始,各能级不完全遵循能层顺序,产生了能级交错排列,即产生“能级交错”现象。
如E >E :电子先进入4s而后进入3d能级属于能级交错现象,即能量小排在前面。
3d 4s
再比如:E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>E(7s)、E(4f)>E
(5p)、E(4f)>E(6s)等。
举例:比较下列原子轨道的能量高低。
(1)2s________3s;(2)2s________3d;
(3)3p________3s;(4)4f________5f。
【考点】能层与能级
【题点】不同能层、能级的能量比较
【答案】(1)< (2)< (3)> (4)<
【解析】根据构造原理,各能级能量由低到高的顺序为:1s、2s、2p、3s、3p、4s、
3d、4p、5s、4d、5p、6s、4f、5d、6p、7s、5f、6d、7p……。
2. 电子排布式
(1)概念:用数字在能级符号右上角表明该能级上排布的电子数的式子。
(2)表示方法
第5页(3)基态原子的电子排布式的书写步骤
第 一 步 : 按 照 构 造 原 理 写 出 电 子 填 入 能 级 的 顺 序 ,
1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s……。
第二步:根据各能级容纳的电子数填充电子。
第三步:去掉空能级,并按照能层顺序排列即可得到电子排布式。
(4)简单原子的电子排布式。
按照构造原理将电子依次填充到能量逐渐升高的能级中。
如:C:1s22s22p2
6
Ne:1s22s22p6
10
Cl:1s22s22p63s23p5,阴离子得到电子填入最外层能级(原子失去电子变为阳离子通
17
常由外而内依次失去)
K:1s22s22p63s23p64s1
19
(5)复杂原子的电子排布式。
对于较复杂的电子排布式,应先按构造原理从低到高排列,然后将同能层的能级移到
一起。
如 Fe:先排列为1s22s22p63s23p64s23d6,然后将同一能层的能级排到一起,即该原子的
26
电子排布式为1s22s22p63s23p63d64s2。
【注意】书写电子排布式的注意事项
能级的顺序不完全遵循构造原理,要按照能层序数从小到大的顺序排布。即当出现d
能级时,电子按照ns、(n-1)d、np的顺序填充,要把(n-1)d写在ns的前面,如Fe:
1s22s22p63s23p63d64s2。
(6)利用构造原理书写简化电子排布式。
为了书写方便,把内层电子排布已达到稀有气体电子层结构的部分写成原子实,用稀
有气体的元素符号外加括号来表示,此为简化的电子排布式。
如Cl原子简化的核外电子排布式可表示为 [Ne] 3s23p5;其中[Ne]代表Ne的核外电子
排布式,即 Ne:1s22s22p6
10
K:1s22s22p63s23p64s1,其简化电子排布式可表示为[Ar]4s1,其中[Ar]代表Ar的核外电子排
布式,即1s22s22p63s23p6。
Mn原子排布式:1s22s22p63s23p63d54s2
Mn原子简化的电子排布式:[Ar] 3d54s2
Fe原子排布式:1s22s22p63s23p63d64s2
第6页再如Fe的简化电子排布式为[Ar]3d64s2。
(7)价电子排布式(又称为外围电子排布式、特征电子构型)
①主族元素的价电子为最外层电子,如 K 的价电子排布式为:4s1。K:
1s22s22p63s23p64s1
②过渡元素的价电子包括最外层、次外层或倒数第三层的电子,如 Cr的价电子排布式
为:3d54s1,铜的价电子式为3d104s1。
【拓展提升】微粒结构示意图与电子排布式的关系
对于复杂的原子或离子,若直接书写电子排布式有困难,可先写出原子的原子结构示
意图,再据此写出电子排布式,如
微粒结构示意图表示原子或离子的核电荷数和核外电子在各电子层(能层)上的排布。
Fe核外电子排布式:1s22s22p63s23p63d64s2
Fe结构示意图:
Fe3+核外电子排布式:1s22s22p63s23p63d5
Fe3+结构示意图:
【易错辨析】
(1)能层就是电子层( √ )
(2)不同能层,s能级能量相同( × )
(3)s能级的能量一定比p能级的低( × )
(4)高能层的所有能级能量都比低能层能级能量高( × )
(5)各能层的能级数等于其所处能层序数( √ )
(6)任一能层的s能级最多容纳的电子数均为2( √ )
(7)3p3表示3p能级只能填充3个电子( × )
(8)各能级最多可容纳的电子数按s、p、d、f…的顺序依次为1、3、5、7…的2倍(
√ )
第7页【总结提升】
【归纳总结】
1. 各能层中的能级数等于其所处的能层序数
2. 每个能层最多能填充2n2个电子,但不是一定含有2n2个电子
3. 能级符号相同、电子层数不同的电子能量:
4. 核外电子排布的能级顺序为1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p、6s、
4f、5d、6p、7s……。
5. 在多电子原子中会发生能级交错现象,如E(3d)>E(4s)。
6. 书写电子排布式的关键是熟悉构造原理,根据构造原理,核外电子排布的能级顺序为
1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p、6s、4f、5d、6p、7s……。各能级能量由
低到高可记为ns<(n-2)f<(n-1)d