文档内容
硫及其化合物(1)
重难点 题型 分值
1. 了解硫的物理性质和化学性质
重点
2. 掌握二氧化硫物理、化学性质
选择和填空 4-6分
难点 二氧化硫的化学性质
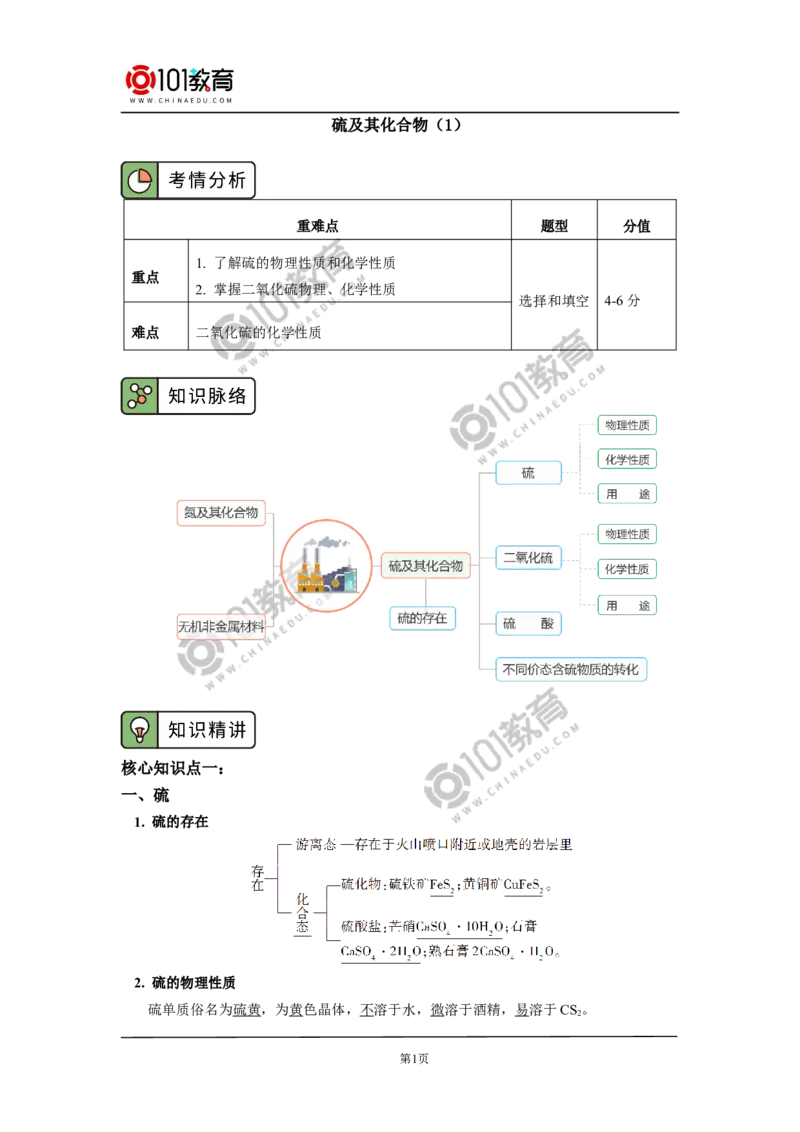
核心知识点一:
一、硫
1. 硫的存在
2. 硫的物理性质
硫单质俗名为硫黄,为黄色晶体,不溶于水,微溶于酒精,易溶于CS。
2
第1页3. 硫的化学性质
由于硫原子最外层有6个电子,比较活泼的非金属单质,常见化合价为-2,0,+4,
+6,以下是常见的硫化物。
化合价 -2 0 +4 +6
物质 FeS 、 NaS 、 S SO 、 HSO 、 SO 、 HSO 、
2 2 2 3 3 2 4
类别 HgS、HS NaSO 、NaHSO NaHSO、NaSO
2 2 3 3 4 2 4
可见,硫单质处于硫元素的中间价态,硫既有氧化性又有还原性。
(1)还原性:与O 反应:S+O=====SO 。
2 2 2
(2)氧化性
①与Fe反应:Fe+S=====FeS;
②与Cu反应:2Cu+S=====Cu S;
2
③与Hg反应:S+Hg===HgS。
(3)与NaOH溶液的反应:3S+6NaOH=====2NaS+NaSO +3HO。
2 2 3 2
注意:①粘有硫的试管可以用CS 或热的碱液洗涤。
2
②硫与变价金属反应时生成低价态的金属硫化物,而不是高价态。如 Fe与S反应生成
FeS而不是Fe S。
2 3
4. 硫的用途
硫是重要的化工原料,比如可以制造硫化橡胶、火柴、药品等
核心知识点二:
二、二氧化硫
1. SO 物理性质
2
颜色 状态 气味 密度 溶解性 毒性
刺激性 比空气 易溶
无色 气体 有毒
气味 大 于水
2. SO 的化学性质
2
①酸性氧化物的通性
与HO反应: ,此反应为可逆反应。
2
与碱反应:SO + 2NaOH == =N a SO + H O。(SO 尾气处理的方法,此法是NaOH过
2 2 3 2 2
量)
与碱性氧化物反应:SO + CaO == =CaSO 。
2 3
②还原性
与O 反应: ,此反应为可逆反应。
2
第2页③氧化性:SO +2HS===3S↓+2HO
2 2 2
④漂白性:与某些有色物质(如品红)生成不稳定的无色物质,加热或久置可恢复原
来的颜色。
注意:如果换做NaO 与SO 反应,由于NaO 有氧化性且不是碱性氧化物,所以两者
2 2 2 2 2
在一起反应只发生氧化还原反应,生成物质为NaSO 。
2 4
3. SO 的用途
2
①漂白纸浆、毛、丝、草帽辫等。
②用于杀菌消毒。
核心知识点一:
下列说法中错误的是( )
A. 自然界中硫是一种淡黄色难溶于水的固体
B. 硫的化合物常存在于火山喷出的气体中和矿泉水里
C. 硫与金属反应,生成金属的低价态化合物
D. 硫在空气中的燃烧产物是二氧化硫,纯氧中的燃烧产物是三氧化硫
【答案】D
【解析】A.硫是一种淡黄色、难溶于水的固体,A正确;B. 硫的化合物常存在于火山
喷出的气体中和矿泉水里,多为二氧化硫,B正确;C. 硫的非金属性比较弱,硫与金属反
应生成金属的低价态化合物,C正确;D. 硫在空气中的燃烧产物是二氧化硫,在纯氧中的
燃烧产物仍然是二氧化硫,D错误。答案选D。
【考点】硫的性质
关于硫的叙述正确的是( )
A. 硫的非金属性较强,在自然界中只以化合态存在
B. 可用水溶解过滤分离硝酸钾和硫黄的混合物
C. 硫与金属或非金属反应时都作氧化剂
D. 硫的氧化性比氯气强
【答案】B
【解析】硫在自然界中的存在形式既有化合态又有游离态;硝酸钾易溶于水,硫黄不
溶于水,用水溶解过滤可分离二者的混合物;硫与金属、氢气等反应时作氧化剂,硫与氧
第3页气等反应时作还原剂;硫的氧化性比氯气弱(硫与铁反应生成硫化亚铁,氯气与铁反应生
成氯化铁)。
【考点】硫的性质
核心知识点二:
向 FeCl 和 BaCl 的酸性混合溶液中通入 SO 气体,有白色沉淀生成,此沉淀是
3 2 2
( )
A. BaSO B. Fe (SO )
4 2 4 3
C. BaSO D. S
3
【答案】A
【解析】Fe (SO ) 不是沉淀,排除B项。题中隐含的条件为:该白色沉淀不溶于酸,
2 4 3
可以排除C项。由Fe3+有氧化性,SO 有还原性,两者可发生氧化还原反应,硫元素化合
2
价升高,生成的SO 2-与Ba2+结合成BaSO ,根据该题的隐含信息,可写出下列化学方程式:
4 4
2FeCl +SO +2HO===2FeCl +HSO +2HCl,BaCl +HSO ===BaSO ↓+2HCl。
3 2 2 2 2 4 2 2 4 4
【考点】二氧化硫的还原性
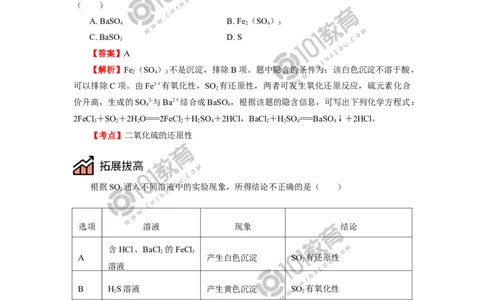
根据SO 通入不同溶液中的实验现象,所得结论不正确的是( )
2
选项 溶液 现象 结论
含HCl、BaCl 的FeCl
2 3
A 产生白色沉淀 SO 有还原性
2
溶液
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D NaSiO 溶液 产生胶状沉淀 酸性:HSO >HSiO
2 3 2 3 2 3
【答案】C
【解析】A对:SO 通入含HCl、BaCl 的FeCl 溶液中,发生反应:SO + 2Fe3+ +Ba2+
2 2 3 2
+ 2H O =BaSO ↓+ 2Fe2+ + 4H+,产生白色沉淀,该反应中SO 作还原剂,表现出还原性。B
2 4 2
对:SO 通入HS溶液中,发生反应:SO +2H S=3S↓+2H O,产生黄色沉淀,该反应中SO
2 2 2 2 2 2
第4页作氧化剂,表现出氧化性。C错:SO 通入酸性KMnO 溶液中,发生反应:5SO +2 MnO -
2 4 2 4
+2H O=5SO 2-+2Mn2++4H+,该反应中,SO 作还原剂,表现出还原性而不是漂白性。D对:
2 4 2
SO 通入NaSiO 溶液中,发生反应:NaSiO+SO+H O=HSiO↓+Na SO ,该反应符合“强
2 2 3 2 3 2 2 2 3 2 3
酸制弱酸”的反应规律,则酸性:HSO >H SiO。
2 3 2 3
【考点】二氧化硫的化学性质
(答题时间:25分钟)
一、选择题
1. 下列物质在一定条件下能够与硫黄发生反应,且硫作还原剂的是( )
A. O B. Fe C. H D. Zn
2 2
2. 常温下单质硫主要以S 形式存在。加热时,S 会转化为S 、S 、S 等。当温度达到
8 8 6 4 2
750 ℃时,硫蒸气主要以S 形式存在(占92%)。下列说法中正确的是( )
2
A. S 转化为S、S、S 属于物理变化
8 6 4 2
B. 不论哪种硫分子,完全燃烧时都生成二氧化硫
C. S、S、S、S 都是硫元素形成的单质,为同种物质
2 4 6 8
D. 把硫单质在空气中加热到750 ℃即得S
2
3. 大约4000年前,埃及人已经用硫燃烧所形成的二氧化硫漂白布匹。在古罗马著名诗
人荷马的著作里讲到硫燃烧有消毒和漂白作用。下列物质都具有漂白性:①潮湿的氯气、
②二氧化硫、③活性炭、④过氧化钠,其漂白原理相同的是( )
A. ①③B. ②③C. ①④D. ②④
4. 下列有关SO 的说法中正确的是( )
3
A. SO 极易溶于水,且与水反应生成HSO
3 2 4
B. 标准状况下,1 mol SO 的体积约为22.4 L
3
C. 硫粉在过量的纯氧中燃烧可以生成SO
3
D. SO 、SO 均具有漂白性,均能使紫色石蕊溶液褪色
2 3
5. 下列物质能将品红氧化使品红溶液褪色的是( )
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤臭氧
A. ①②③④⑤ B. ②③④⑤
C. ②③④ D. ②③⑤
6. 下列关于SO 变化和其相应性质对应关系不正确的是( )
2
A. 使品红溶液褪色——漂白性
B. 导致酸雨——酸性氧化物
第5页C. 使高锰酸钾溶液褪色——漂白性
D. 通入HS溶液中变浑浊——氧化性
2
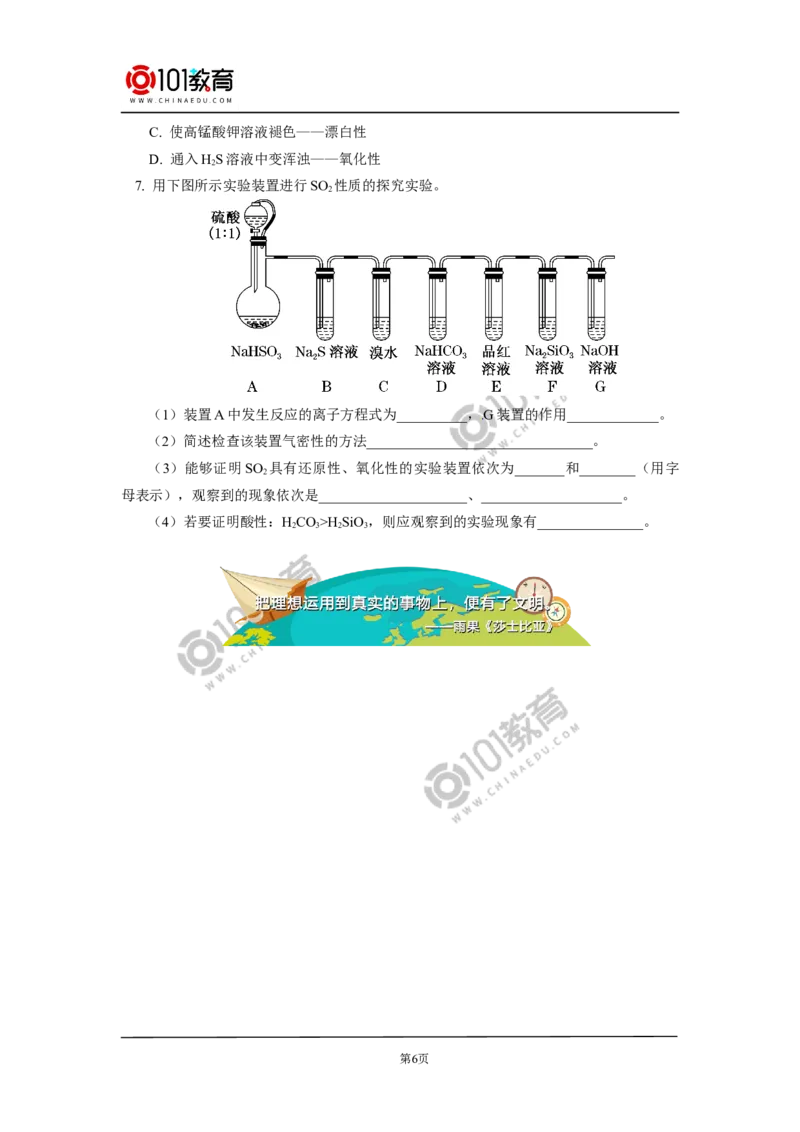
7. 用下图所示实验装置进行SO 性质的探究实验。
2
(1)装置A中发生反应的离子方程式为__________,G装置的作用_____________。
(2)简述检查该装置气密性的方法________________________________。
(3)能够证明SO 具有还原性、氧化性的实验装置依次为_______和________(用字
2
母表示),观察到的现象依次是_____________________、____________________。
(4)若要证明酸性:HCO>H SiO,则应观察到的实验现象有_______________。
2 3 2 3
第6页1. 【答案】A
【解析】硫是较活泼的非金属元素,能与许多金属、非金属发生反应。硫与活泼非金
属单质氧气反应时,表现出还原性;硫与金属单质、氢气等反应时,表现出氧化性;硫与
变价金属反应时,一般生成低价金属的硫化物。
2.【答案】B
【解析】硫单质之间的转化为化学变化,A不正确;不论哪种硫分子,完全燃烧的产
物均为二氧化硫,B正确;S 、S 、S 、S 都是硫元素形成的单质,但是,构成分子的原子
2 4 6 8
数不同,不是同种物质,C不正确;硫单质在空气中加热会燃烧生成二氧化硫,不可能与
S 相互转化,D不正确。
2
3.【答案】C
【解析】潮湿的氯气(有次氯酸生成)、过氧化钠都是强氧化型漂白;二氧化硫是化
合型漂白;活性炭是吸附型漂白。
4.【答案】A
【解析】SO 溶于水发生反应:SO +HO===H SO ,A正确;标准状况下,SO 呈固
3 3 2 2 4 3
态并非气态,体积远远小于22.4 L,B错误;不管氧气量有多少,硫在氧气中燃烧的产物
都是SO ,C错误;SO 具有漂白性,但不能使紫色石蕊溶液褪色,SO 不具有漂白性,D
2 2 3
错误。
5.【答案】D
【解析】活性炭具有吸附性,不是氧化性,①错误;过氧化钠具有强氧化性,能把品
红溶液氧化而褪色,②正确;氯水具有强氧化性,能把品红溶液氧化而褪色,③正确;二
氧化硫使品红溶液褪色的原理不是氧化,④错误;臭氧具有强氧化性,能把品红溶液氧化
而褪色,⑤正确。
6.【答案】C
【解析】SO 具有漂白性,能使品红溶液褪色,但是不能漂白酸碱指示剂;SO 具有酸
2 2
性氧化物的通性,能够与水反应生成亚硫酸,在空气中氧化为硫酸,随雨水落下形成酸雨
SO 具有还原性,能使高锰酸钾溶液褪色;SO 中的硫元素化合价处于+4价,具有弱氧化
2 2
性,能氧化HS:2HS+SO ===3S↓+2HO。故选C。
2 2 2 2
−
7.【答案】(1)HSO3 +H+===SO↑+HO 吸收尾气,防止CO 进入F
2 2 2
(2)G中加水至没过导管口,微热A中圆底烧瓶,若G中有气泡产生,停止加热,
冷却后导管末端形成一段水柱,说明气密性良好
(3)C B C中溴水褪色 B中出现淡黄色沉淀
(4)E中品红不褪色,F中出现浑浊
第7页【解析】(1)A中浓硫酸与亚硫酸氢钠反应生成二氧化硫气体和水,反应的离子方程
−
式为HSO3 +H+===SO↑+HO;SO 属于污染空气的气体,不能排放到大气中,空气中
2 2 2
的CO 气体也会和F中的NaSiO 溶液反应生成白色沉淀,所以G装置的作用是吸收尾气,
2 2 3
防止CO 进入F。(3)SO 能与溴水发生反应,化学方程式为SO +Br +2HO===2HBr+
2 2 2 2 2
HSO ,S元素由+4价升高到+6价,体现了SO 的还原性,SO 能与NaS发生反应,化
2 4 2 2 2
学方程式为SO +2NaS+2HO===3S↓+4NaOH,该反应SO 中的硫元素由+4价降低到0
2 2 2 2
价,体现了SO 的氧化性,则能够证明SO 具有还原性、氧化性的实验装置依次为C和
2 2
B,观察到的现象依次是C中溴水褪色,B中出现淡黄色沉淀。(4)D装置能生成CO ,
2
根据“强酸制弱酸”原理,CO 和SO 都能和NaSiO 溶液反应生成白色沉淀,需要先验证
2 2 2 3
SO 被除去,然后再验证酸性HCO>H SiO ,所以若要证明酸性:HCO>H SiO ,则应观
2 2 3 2 3 2 3 2 3
察到的实验现象有E中品红不褪色,F中出现浑浊。
第8页