文档内容
全面解读盖斯定律及其应用
重难点 题型 分值
1. 掌握盖斯定律,并用盖斯定律进行反应
热的计算
重点
2. 利用键能和物质反应前后的能量变化进
选择与填空 4-6分
行反应热的计算
难点 利用盖斯定律进行反应热的计算
一、盖斯定律
1. 盖斯定律的内容
在一定条件下,化学反应的反应热只与反应体系的始态和终态有关,而与反应进行的
途径无关。一个化学反应,不管是一步完成还是分几步完成的,其反应热是相同的。
2. 盖斯定律的特点
(1)反应体系的始态和终态一定时,中途不管分了几个步骤,每个步骤不管是吸热还
是放热,不管是否曾出现过其他物质参与,都不影响最终的反应热。如图:
第1页ΔH=ΔH+ΔH ΔH+ΔH+ΔH。
1 2= 3 4 5
(2)热化学方程式与数学上的方程式相似,可以移项同时改变正、负号,各项的系数
及△H的数值可以同时扩大或缩小相同的倍数。例如:H (g)+1/2O (g)=HO(1),
2 2 2
可以通过两种途径来完成这个反应过程,如图所示:
已知:H (g)+1/2O (g)=HO(g)ΔH =-241.8kJ·mol-1①HO(g)=HO(1)
2 2 2 1 2 2
ΔH=-44.0kJ·mol-1②,①+②得H(g)+1/2O (g)=HO(1)ΔH=-285.8 kJ·mol-1。
2 2 2 2
3. 盖斯定律的意义
因为有些化学反应进行得很慢,有些化学反应不容易直接发生或是反应的生成物不纯
(有副反应发生),不易直接测出该化学反应的反应热,此时应用盖斯定律,就可以间接
地将它们的反应热计算出来
【拓展】利用盖斯定律求未知反应的反应热
①在利用盖斯定律由已知反应热的热化学方程式计算另一热化学方程式的反应热时,
只要设法消去所求热化学方程式中不需要的物质即可。②求总反应的反应热,不能不假思
索地将各步反应的反应热简单相加。不论反应一步进行还是分步进行,始态和终态必须完
全一致,盖斯定律才成立。
4. 应用能量守恒定律对盖斯定律进行论证
假设反应体系的始态为S,终态为L,它们之间的变化用两段弧线(可以包含着任意
数目的中间步骤)连接,如图所示:
由图可知,反应体系先从S变化到L,体系放出能量(ΔH<0),再由L变回到S,体
系吸收能量(ΔH>0)。经过一个循环,体系仍处于S态,所有的反应物都和反应前一样。
2
如果ΔH+ΔH ≠0,那么在物质丝毫未损的情况下,体系能量发生了改变,违背了能量守恒
1 2
定律。因为ΔH+ΔH =0,所以化学反应的反应热只与反应体系的始态和终态有关,而与
1 2
反应进行的途径无关。
二、盖斯定律的应用
第2页根据盖斯定律,书写相关反应的热化学方程式有两种方法:
1. 虚拟路径法
若反应物A经反应生成生成物D,可以有两个途径:
a. 由A直接变成D,反应热为△H;
b. 由A经过B生成C,再由C生成D,每步的反应热分别为△H 、△H 、△H ,如图
1 2 3
所示:
则有△H=△H + △H + △H
1 2 3
【即时练】氢气与氧气生成液态水的反应,可以通过两种途径来完成,如图所示。已知:
①H(g)+1/2O (g)=HO(1)ΔH=-285.8 kJ·mol-1
2 2 2
②HO(g)=HO(1)ΔH=-44.0kJ·mol-1
2 2 2
求H(g)+1/2O (g)=HO(g)的反应热ΔH。
2 2 2 1
【答案】ΔH ΔH-ΔH
1= 2
【解析】已知:ΔH=ΔH+ΔH ,所以ΔH ΔH-ΔH =-285.8 kJ·mol-1+44.0kJ·mol-1
1 2 1= 2
=-241.8 kJ·mol-1
2. 加合法
即给出多个已知热化学方程式,通过将多个已知热化学方程式进行变形叠加,求出目
标热化学方程式的反应热ΔH或写出目标方程式的热化学方程式。
【关键】由已知方程式推导目标方程式
首先,观察目标方程式的反应物和生成物,利用已知方程式消去目标方程式没有出现
的中间产物,得到总反应方程式。最后,根据消元的途径求出总反应方程式焓变。
【运算规则】热化学方程式同乘以某一个数时,反应热的数值也必须乘以该数;热化学方
程式相加减时,同种物质之间可相加减,反应热也随之加减;将一个化学方程式调整方向
时,反应热与原反应的反应热数值相等,符号相反。
热化学方程式 方程式系数关系 焓变之间的关系
反应Ⅰ:A(g)=B(g) ΔH
1
Ⅰ=-Ⅱ ΔH=-ΔH
1 2
反应Ⅱ:B(g)=A(g) ΔH
2
反应Ⅰ:aA(g)=B(g) ΔH Ⅰ=a·Ⅱ ΔH=a·ΔH
1 1 2
第3页反应Ⅱ:A(g)=1/aB(g)
ΔH
2
【归纳】加合法四个要点
选取目标热化学反应方程式左侧物质为参考物,若目标方程式中参考物位置与已
倒 知
方程式没有在同一侧,则将已知热化学方程式调转过来。
乘 将已知热化学方程式中参考物的系数与目标热化学反应方程式中系数保持一致
消 调用剩余的已知方程式消去目标方程式没有出现的中间产物
加 将方程式叠加,代入焓变值进行运算
【详例分析】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+ 2KNO (s)+ 3C(s)=KS (s)+ N(g)+ 3CO(g) ΔH=x kJ·mol-1
3 2 2 2
已知碳的燃烧热 ΔH=a kJ·mol-1
1
S (s)+ 2K(s)=KS(s) ΔH b kJ·mol-1
2 2=
2K(s)+ N (g)+ 3 O (g)=2 KNO (s) ΔH=c kJ·mol-1
2 2 3 3
则x为多少?
【解析】(1)分析目标方程式和已知方程式
(2)S(s)+ 2KNO (s)+ 3C(s)=K S (s)+ N (g)+ 3CO (g) ΔH=x
3 2 2 2
-1
kJ·mol
-1
①式×3 3C(s)+3O
2
(g)=3CO
2
(g) ΔH, =3ΔH
1
=3a kJ·mol
-1
②式×1 S (s)+ 2K(s)=K
2
S(s) ΔH 2=b kJ·mol
第4页③式调转方向
2KNO(s)=2K(s)+N (g)+3O (g);ΔH”=-ΔH=-c kJ·mol-1
3 2 2 3
将调整后的三式相加:
=b+3a-c kJ·mol-1
【归纳】应用盖斯定律的一般技巧
①可将某个热化学方程式的反应物和生成物互换位置,把“减法“换成“加法”。
②如果已知方程式存在多种需要约去的物质,一般先约去出现两次的物质。
③书写未知的热化学方程式时,物质状态或产物若难以确定,可以联系燃烧热和中和
热的基本要求和题目所给时间、温度、压强等数据进行判断,如温度高于100℃,则水的
状态为气态。
例题1 用CH 催化还原NOx可以消除氮氧化物的污染。例如:
4
①CH(g)+4NO (g)=4NO(g)+CO(g)+2HO(g) ΔH=-574 kJ·mol-1
4 2 2 2
②CH(g)+4NO(g)=2N(g)+CO(g)+2HO(g) ΔH=-1 160 kJ·mol-1
4 2 2 2
下列说法不正确的是( )
A. 若用标准状况下4.48 L CH 还原NO 生成N 和水蒸气,放出的热量为173.4 kJ
4 2 2
B. 由反应①可推知:CH (g)+4NO (g)=4NO(g)+CO (g)+2HO(l)
4 2 2 2
ΔH>-574 kJ·mol-1
C. 反应①②转移的电子数相同
D. 反应②中当0.2 mol CH 反应完全时转移的电子总数为1.60 mol
4
【答案】B
【解析】根据盖斯定律,将①②相加得到如下热化学方程式CH(g)+2NO (g)=
4 2
N(g)+CO(g)+2HO(g) ΔH=-867 kJmol-1,标准状况下4.48 L CH 的物质的量
2 2 2 4
为0.2 mol,放出的热量为0.2 mol×867 kJ·mol-1=173.4kJ;由于液态水变为气态水需要吸
收热量,所以生成液态水的反应放出的热量多,放热越多,则ΔH越小,即ΔH<-
574kJmol-1;反应①②中每1 mol CH 反应完全时转移的电子总数为8 mol,0.2 mol CH 完
4 4
全反应时转移的电子总数为1.60 mol。
例题2 室温下,将1 mol的CuSO ·5H O(s)溶于水会使溶液温度降低,热效应为
4 2
ΔH,将1 mol 的CuSO (s)溶于水会使溶液温度升高,热效应为ΔH,CuSO ·5H O 受
1 4 2 4 2
△
热分解的化学方程式为:CuSO ·5H O(s) CuSO (s)+5HO(l),热效应为ΔH。
4 2 4 2 3
第5页则下列判断正确的是 ( )。
A. ΔH >ΔH B. ΔH<ΔH C. ΔH+ΔH=ΔH D. ΔH +ΔH>ΔH
2 3 1 3 1 3 2 1 2 3
【答案】B
【解析】由题干信息可得:①CuSO ·5H O(s)=Cu2+(aq)+ SO 2- (aq)+
4 2 4
5HO (l) ΔH>0,②CuSO (s)=Cu2+(aq)+ SO 2- (aq) ΔH<0,
2 1 4 4 2
③CuSO ·5H O(s)=CuSO (s)+ 5HO (l) ΔH,根据盖斯定律可知,ΔH=ΔH
4 2 4 2 3 3 1
-ΔH,由于ΔH>0,ΔH<0,故ΔH>ΔH,B项正确,C、D项错误;ΔH>0,ΔH<
2 1 2 3 1 3 2
0,故ΔH>ΔH,A项错误 。
3 2
例题 下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原
理。
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为
、 ,制得等量H 所需能量较少的是 。
2
【答案】HO(l)=H (g)+O (g) ΔH=286 kJ·mol-1 HS(g)=H (g)+S
2 2 2 2 2
(s) ΔH=20 kJ·mol-1 系统(Ⅱ)
【解析】①HSO (aq)=SO (g)+H O(l)+ O (g)ΔH=327 kJ·mol-1
2 4 2 2 2 1
②SO (g)+I (s)+2H O(l)=2HI(aq)+ H SO (aq)ΔH=-151 kJ·mol-1
2 2 2 2 4 2
③2HI(aq)=H (g)+ I(s) ΔH=110 kJ·mol-1
2 2 3
④HS(g)+H SO (aq)=S(s)+SO(g)+2H O(l)ΔH=61 kJ·mol-1
2 2 4 2 2 4
根据盖斯定律由①+②+③可得系统(Ⅰ)的热化学方程式:HO(l)=H(g)+O
2 2 2
(g)ΔH=286 kJ·mol-1;由②+③+④可得系统(Ⅱ)的热化学方程式:H S(g)=H
2 2
(g)+S(s) ΔH=20 kJ·mol-1。根据系统(Ⅰ)、系统(Ⅱ)的热化学方程式可知产生
等量的氢气,后者吸收的热量比前者少。
(答题时间:40分钟)
第6页一、选择题
1. 下列叙述不正确的是( )
A. 化学反应的反应热不仅与反应体系的始态和终态有关,也与反应的途径有关
B. 盖斯定律遵循能量守恒定律
C. 利用盖斯定律可间接计算难以通过实验测定的反应的反应热
D. 利用盖斯定律可以计算有副反应发生的反应的反应热
2. 盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)
有关,而与反应进行的具体途径无关。物质A在一定条件下可发生一系列转化,由如图判
断下列关系错误的是( )
A. A→F,ΔH=-ΔH
6
B. ΔH+ΔH+ΔH+ΔH+ΔH+ΔH=1
1 2 3 4 5 6
C. C→F,|ΔH|=|ΔH+ΔH+ΔH|
1 2 6
D. ΔH +ΔH+ΔH=-ΔH-ΔH-ΔH
1 2 3 4 5 6
3. 已知N 和H 合成氨的反应是放热反应,破坏1mol N≡N键消耗的能量为QkJ,破坏
2 2 1
1mol H-H键消耗的能量为QkJ,形成1mol N-H键放出的能量为QkJ,下列关系式中正
2 3
确的是( )
A. Q +3Q >6Q B. Q+3Q <6Q
1 2 3 1 2 3
C. Q+Q <Q D. Q +Q =Q
1 2 3 1 2 3
4. 发射火箭时使用的燃料可以是液氢和液氧,已知下列热化学方程式:
①H(g)+ O(g)=HO(l)ΔH=-285.8kJ·mol-1
2 2 2 1
②H(g)=H(l) ΔH=-0.92kJ·mol-1
2 2 2
③O(g)=O(l) ΔH=-6.84kJ·mol-1
2 2 3
④HO(l)=HO(g) ΔH=+44.0kJ·mol-1
2 2 4
则反应H(l)+ O(l)=HO(g)的反应热ΔH为( )
2 2 2
A. +237.46kJ·mol-1 B. -474.92kJ·mol-1
C. -118.73kJ·mol-1 D. -237.46kJ·mol-1
*5. 已知:①2C(s)+O (g)=2CO(g) ΔH=-221.0kJ·mol-1;②2H (g)+O
2 2 2
(g)=2HO(g) ΔH=-483.6kJ·mol-1。则制备水煤气的反应C(s)+HO(g)=CO
2 2
(g)+H(g)的ΔH为( )
2
第7页A. +262.6kJ·mol-1 B. -131.3kJ·mol-1
C. -352.3kJ·mol-1 D. +131.3kJ·mol-1
6. 已知:①C(s)+HO(g)=CO(g)+H(g) ΔH=+130 kJ·mol-1
2 2
②2C(s)+O(g)=2CO(g) ΔH=-220 kJ·mol-1
2
断开1 mol H—H键、O=O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键
需要吸收的热量为( )
A. 332 kJ B. 118 kJ
C. 462 kJ D. 360 kJ
二、填空题
6. 用NH 可除去烟气中氮的氧化物,主要反应如下:
3
①4NO(g)+4NH (g)+O (g) 4N (g)+6HO(g) ΔH =-1627.2
3 2 2 2 1
kJ·mol-1
②6NO(g)+4NH (g) 5N(g)+6HO(g) ΔH=-1807 kJ·mol-1
3 2 2 2
③6NO (g)+8NH (g) 7N(g)+12HO(g) ΔH=-2659.9 kJ·mol-1
2 3 2 2 3
则N(g)+O(g)=2NO(g) ΔH=________kJ·mol-1。
2 2 4
已知:O 、NO中的化学键键能分别为497.3 kJ·mol-1、631.65 kJ·mol-1,则N 中的化
2 2
学键键能为____________。
*7. (1)贮氢合金ThNi 可催化由CO、H 合成CH 的反应。温度为T时,该反应的热
5 2 4
化学方程式为____________________________________________。
已知温度为T时:CH(g)+2HO(g)=CO(g)+4H(g) ΔH=+165kJ·mol-1
4 2 2 2
CO(g)+HO(g)=CO(g)+H(g)ΔH=-41kJ·mol-1
2 2 2
(2)用O 将HCl转化为Cl,可提高效益,减少污染。
2 2
传统上该转化通过如图所示的催化循环实现。其中,反应①为:
2HCl(g)+CuO(s) =HO(g)+CuCl (s) ΔH
2 2 1
反应②生成1molCl (g)的反应热为ΔH,则总反应的热化学方程式为___________。
2 2
(反应热用ΔH 和ΔH 表示)。
1 2
(3)已知:①Fe O(s)+3C(s)=2Fe(s)+3CO(g) ΔH=+494kJ·mol-1
2 3
②CO(g)+ O(g)=CO(g) ΔH=-283kJ·mol-1
2 2
③C(s)+ O(g)=CO(g) ΔH=-110kJ·mol-1
2
第8页则反应 Fe O (s)+3C(s)+ O (g)=2Fe(s)+3CO (g)的 ΔH=
2 3 2 2
________kJ·mol-1。理论上反应________放出的热量足以供给反应________所需要的热量
(填上述方程式序号)。
*8. (1)已知:Al O(s)+3C(s)=2Al(s)+3CO(g) ΔH=+1 344.1 kJ·mol-1
2 3 1
2AlCl (g)=2Al(s)+3Cl(g) ΔH=+1 169.2 kJ·mol-1
3 2 2
由Al O、C和Cl 反应生成AlCl 和CO的热化学方程式为 。
2 3 2 3
(2)贮氢合金ThNi 可催化由CO、H 合成CH 的反应。温度为T时,该反应的热化
5 2 4
学方程式为 。
已知温度为T时:CH(g)+2HO(g)=CO(g)+4H(g) ΔH=+165 kJ·mol-
4 2 2 2
1
CO(g)+HO(g)=CO(g)+H(g) ΔH=-41 kJ·mol-1。
2 2 2
(3)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。
4 3 3
已知25 ℃,101 kPa时:4Fe(s)+3O(g)=2Fe O(s) ΔH=-1 648 kJ·mol-1
2 2 3
C(s)+O(g)=CO(g) ΔH=-393 kJ·mol-1
2 2
2Fe(s)+2C(s)+3O(g)=2FeCO(s) ΔH=-1 480 kJ·mol-1
2 3
FeCO 在空气中加热反应生成Fe O 的热化学方程式是 。
3 2 3
9. 近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
(1)反应Ⅰ:2HSO (l) 2SO (g)+2H O(g)+O (g)
2 4 2 2 2
ΔH=+551 kJ·mol-1
1
反应Ⅲ:S(s)+O (g) SO (g) ΔH=-297 kJ·mol-1
2 2 3
反应Ⅱ的热化学方程式: 。
第9页1. 【答案】A
【解析】化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关,
A项错误;反应物和生成物的能量一定,变化过程中的能量变化遵循能量守恒,而盖斯定
律是能量守恒定律的具体体现,B项正确;利用盖斯定律可以用已经精确测定的反应的反
应热来计算难以测量或不能测量的反应的反应热,C项正确;利用盖斯定律可以用已经精
确测定的反应的反应热来计算有副反应发生的反应的反应热,D项正确。
2. 【答案】B
【解析】F→A,ΔH=ΔH ,则A→F,ΔH=-ΔH ,A项正确;6个步骤相加即回到原
6 6
点,则ΔH +ΔH +ΔH +ΔH +ΔH +ΔH =0,B项错误;F→C,ΔH=ΔH +ΔH +ΔH ,
1 2 3 4 5 6 6 1 2
则C→F,|ΔH|=|ΔH +ΔH +ΔH|,C项正确;D→A与A→D的过程恰好相反,即ΔH +
1 2 6 1
ΔH+ΔH=-ΔH-ΔH-ΔH,D项正确。
2 3 4 5 6
3. 【答案】B
【解析】破坏1mol N≡N键消耗的能量为QkJ,则N≡N键能为QkJ/mol,破坏1mol H
1 1
-H键消耗的能量为QkJ,则H-H键键能为QkJ/mol,形成1molH-N键释放的能量为
2 2
QkJ,则H-N键能为QkJ/mol,对于3H (g)+N (g)═2NH (g),反应热△H=反
3 3 2 2 3
应物的总键能-生成物的总键能,故:反应热△H=3QkJ/mol+QkJ/mol-6QkJ/mol=
2 1 3
(3Q+Q -6Q )kJ/mol,反应热△H<0,即(3Q+Q -6Q )<0,所以3Q+Q <6Q ,故
2 1 3 2 1 3 2 1 3
答案为B。
4. 【答案】D
【解析】根据盖斯定律,将反应①-②-③× +④可得目标反应方程式,其反应热
ΔH=ΔH-ΔH-ΔH× +ΔH=-237.46 kJ·mol-1。
1 2 3 4
5. 【答案】D
【解析】根据盖斯定律,把已知两个反应相加减,可求得制备水煤气反应的 ΔH。①
-②得2C(s)+2HO(g)=2H (g)+2CO(g) ΔH=-221.0 kJ·mol-1-(-483.6
2 2
kJ·mol-1)=+262.6 kJ·mol-1,则C(s)+HO(g)=CO(g)+H (g)的ΔH=(+
2 2
262.6kJ·mol-1)÷2=+131.3kJ·mol-1。
6.【答案】C
【解析】热化学方程式①×2-②得2HO(g)=O (g)+2H (g) ΔH=[(+
2 2 2
130)×2-(-220)] kJ·mol-1=+480 kJ·mol-1,即4E(O—H)-E(O =O)-2E(H
—H)=4E(O—H)-496 kJ·mol-1-2×436 kJ·mol-1=480 kJ·mol-1,解得E(O—H)=
462 kJ·mol-1,C正确。
第10页二、非选择题
7. 【答案】+179.8 945.8 kJ·mol-1
【解析】由①-②得N (g)+O (g)=2NO(g)的ΔH =(-1627.2+1807)
2 2 4
kJ·mol-1=+179.8 kJ·mol-1。设N 中的化学键键能为E,由键能与反应热关系知,E+
2
497.3 kJ·mol-1-631.65 kJ·mol-1×2=+179.8 kJ·mol-1,解得E=945.8 kJ·mol-1。
8. 【答案】(1)CO(g)+3H(g)=CH(g)+HO(g)
2 4 2
ΔH=-206kJ·mol-1
(2)4HCl(g)+O(g)=2HO(g)+2Cl(g)
2 2 2
ΔH=2ΔH+2ΔH
1 2
(3)-355 ②③ ①
【解析】(1)已知:CH(g)+2HO(g)=CO(g)+4H(g)ΔH=+165 kJ·mol
4 2 2 2
-1①、CO(g)+HO(g)=CO (g)+H (g) ΔH=-41 kJ·mol-1②,由盖斯定律可
2 2 2
知,②-①即得所求热化学方程式:CO(g)+3H (g)=CH (g)+HO(g) ΔH=
2 4 2
-206 kJ·mol-1。
(2)2HCl(g)+CuO(s)=HO(g)+CuCl (s) ΔH ①
2 2 1
由图得2CuCl (s)+O(g)=2CuO(s)+2Cl(g) 2ΔH ②
2 2 2 2
运用盖斯定律:①×2+②得总反应:4HCl(g)+O (g)=2HO(g)+2Cl (g)
2 2 2
ΔH=2ΔH+2ΔH。
1 2
(3)根据盖斯定律,由①+3×②可得目标方程式,故其ΔH=-355 kJ·mol-1。
点评:建立盖斯定律应用的思维模型,首先根据目标热化学方程式调整已知热化学方
程式中各物质的化学计量数及焓变,然后将热化学方程式相加减,可写出目标热化学方程
式,进而求得目标反应的反应热,促进“模型认知”化学核心素养的发展。
9. 【答案】(1)Al O (s)+3C(s)+3Cl (g)=2AlCl (g)+3CO(g) ΔH=+
2 3 2 3
174.9 kJ·mol-1
(2)CO(g)+3H(g)=CH(g)+HO(g) ΔH=-206 kJ·mol-1
2 4 2
(3)4FeCO(s)+O(g)=2Fe O(s)+4CO(g) ΔH=-260 kJ·mol-1
3 2 2 3 2
【解析】(1)根据盖斯定律,将第一个反应减去第二个反应可得该热化学反应方程式。
(2)由题意知CH (g)+2HO(g)=CO (g)+4H (g) ΔH=+165 kJ·mol-1
4 2 2 2
①
CO(g)+HO(g)=CO(g)+H(g) ΔH=-41 kJ·mol-1 ②
2 2 2
应用盖斯定律,由②-①可得CO、H 合成CH 的热化学反应方程式:
2 4
CO(g)+3H(g)=CH(g)+HO(g) ΔH=-206 kJ·mol-1。
2 4 2
(3)将所给热化学方程式标号:
第11页4Fe(s)+3O(g)=2Fe O(s) ΔH=-1 648 kJ·mol-1①
2 2 3
C(s)+O(g)=CO(g) ΔH=-393 kJ·mol-1②
2 2
2Fe(s)+2C(s)+3O(g)=2FeCO(s) ΔH=-1 480 kJ·mol-1 ③
2 3
根据盖斯定律:③×(-2)+①+②×4可得:
4FeCO(s)+O(g)=2Fe O(s)+4CO(g) ΔH=-260 kJ·mol-1。
3 2 2 3 2
9. 【答案】 (1)3SO (g)+2H O(g) 2HSO (l)+S(s) ΔH =-254 kJ·mol
2 2 2 4 2
-1
【解析】(1)反应Ⅱ为3SO (g)+2H O(g)= 2HSO (l)+S(s),根据盖斯定
2 2 2 4
律,由(反应Ⅰ+反应Ⅲ)即得反应Ⅱ的逆反应,所以反应Ⅱ的ΔH=-(551-297)
kJ·mol-1=-254 kJ·mol-1。
第12页反应热大小的比较
重难点 题型 分值
重点 掌握反应热大小比较的常见方法和类型
选择题 4—6分
难点 反应热大小比较的常见方法和类型
一、反应热大小比较的方法
1. 根据反应物的性质比较
等物质的量的不同物质与同一种物质反应时,其反应热不同。如等物质的量的不同金
属(或非金属)与同一种物质反应,金属(或非金属)越活泼,反应越容易发生,放出的
热量就越多,ΔH越小。
如:(1)2K(s)+HO(l)=2KOH(aq)+H(g) ΔH
2 2 1
2Na(s)+HO(l)=2NaOH(aq)+H(g) ΔH
2 2 2
第13页ΔH<ΔH
1 2
(2)H(g)+Cl(g)=2HCl(g) ΔH
2 2 3
H(g)+Br (g)=2HBr(g) ΔH
2 2 4
ΔH<ΔH
3 4
(2)直接比较法(根据反应规律和影响ΔH的因素直接比较)
依据规律、经验和常识直接判断不同反应的反应热的大小的方法称为直接比较法。
①吸热反应的ΔH肯定比放热反应的ΔH大(前者大于0,后者小于0)。
②等量的可燃物完全燃烧所放出的热量肯定比不完全燃烧所放出的热量多。
④生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱(或强酸和弱碱)的稀溶
液反应放出的热量多。
⑤对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的热量要小于理
论值。例如:2SO (g)+O (g) 2SO (g) ΔH=-197 kJ/
2 2 3
mol,则向密闭容器中通入2 mol SO 和1 mol O ,反应达到平衡后,放出的热量要小
2 2
于197 kJ。
【易错警示】比较ΔH的大小时,要将其数值和前面的符号“+”“一”看作一个整体进行比
较,不能只比较数值的大小。
1. 若为放热反应,则有ΔH<0,反应放出的热量越多,ΔH越小。
2. 若为吸热反应,则有ΔH>0,反应吸收的热量越多,ΔH越大。
3. 吸热反应的ΔH大于放热反应的ΔH。
二、盖斯定律比较法(类型)
(1)同一反应的生成物状态不同时
A(g)+ B(g)=C(g)ΔH<0
1
A(g)+ B(g)=C(1)ΔH<0
2
比较ΔH 与ΔH 的大小关系
1 2
【方法】1(加合法):
因为:C(g)=C(1)ΔH<0
3
ΔH=ΔH-ΔH<0
3 2
所以ΔH<ΔH。
2
【方法】2(途径法):
因为ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0
1 3 2 1 2 3
第14页所以ΔH<ΔH。
2 1
(2)同一反应的反应物状态不同时
S(g)+O (g)=SO (g)ΔH<0
2 2 1
S(s)+O (g)=SO (g)ΔH<0
2 2 2
比较ΔH 与ΔH 的大小关系
1 2
【方法】1(加合法):
因为:S(g)=S(s)ΔH<0
3
ΔH=ΔH-ΔH<0
3 1 2
所以ΔH<ΔH。
1 2
【方法】2(途径法):
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0
2 3 1 1 2 3
所以ΔH<ΔH 。
1 2
(3)两个有联系的不同反应
C(s)+O (g)=CO(g)ΔH<0
2 2 1
C(s)+½O (g)=CO(g)ΔH<0
2 2
比较ΔH 与ΔH 的大小关系
1 2
【方法】1(加合法):
CO(g)+½O (g)=CO(g)ΔH<0
2 2 3
ΔH=ΔH-ΔH<0;
3 1 2
所以ΔH<ΔH。
1 2
【方法】2(途径法):
碳先燃烧生成一氧化碳,一氧化碳再燃烧生成二氧化碳。
因为ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0
2 3 1 1 2 3
所以ΔH<ΔH。
1 2
并且据此可写出下面的热化学方程式:
CO(g)+½O (g)=CO(g)ΔH=ΔH-ΔH。
2 2 3 1 2
(2)晶体类型不同,产物相同的反应
C(s,石墨)+ O (g)=CO(g) ΔH=-a kJ·mol-1
2 2 1
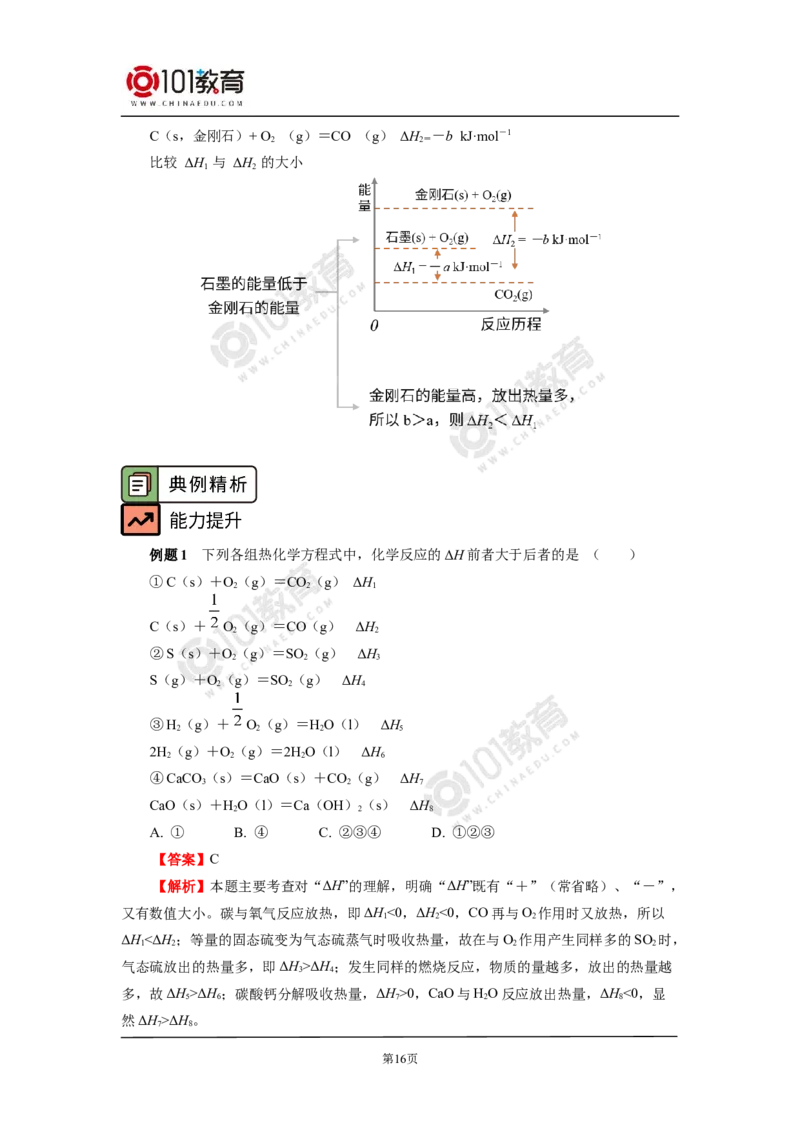
第15页C(s,金刚石)+ O (g)=CO (g) ΔH -b kJ·mol-1
2 2=
比较 ΔH 与 ΔH 的大小
1 2
例题1 下列各组热化学方程式中,化学反应的ΔH前者大于后者的是 ( )
①C(s)+O(g)=CO(g) ΔH
2 2 1
C(s)+ O(g)=CO(g) ΔH
2 2
②S(s)+O(g)=SO (g) ΔH
2 2 3
S(g)+O(g)=SO (g) ΔH
2 2 4
③H(g)+ O(g)=HO(l) ΔH
2 2 2 5
2H(g)+O(g)=2HO(l) ΔH
2 2 2 6
④CaCO (s)=CaO(s)+CO(g) ΔH
3 2 7
CaO(s)+HO(l)=Ca(OH)(s) ΔH
2 2 8
A. ① B. ④ C. ②③④ D. ①②③
【答案】C
【解析】本题主要考查对“ΔH”的理解,明确“ΔH”既有“+”(常省略)、“-”,
又有数值大小。碳与氧气反应放热,即ΔH<0,ΔH<0,CO再与O 作用时又放热,所以
1 2 2
ΔH<ΔH;等量的固态硫变为气态硫蒸气时吸收热量,故在与O 作用产生同样多的SO 时,
1 2 2 2
气态硫放出的热量多,即ΔH>ΔH;发生同样的燃烧反应,物质的量越多,放出的热量越
3 4
多,故ΔH>ΔH;碳酸钙分解吸收热量,ΔH>0,CaO与HO反应放出热量,ΔH<0,显
5 6 7 2 8
然ΔH>ΔH。
7 8
第16页例题2 根据以下三个热化学方程式:
①2HS(g)+3O(g)=2SO (g)+2HO(l) ΔH=-Q kJ·mol-1,
2 2 2 2 1 1
②2HS(g)+O(g)=2S(s)+2HO(l) ΔH=-Q kJ·mol-1,
2 2 2 2 2
③2HS(g)+O(g)=2S(s)+2HO(g) ΔH=-Q kJ·mol-1。
2 2 2 3 3
判断Q、Q、Q 三者关系正确的是(Q、Q、Q 均大于0)( )
1 2 3 1 2 3
A. Q>Q>Q B. Q>Q>Q
1 2 3 1 3 2
C. Q>Q>Q D. Q>Q>Q
3 2 1 2 1 3
【答案】A
【解析】由得:S(s)+O (g)=SO (g) ΔH= (ΔH1-ΔH )<0,所以 (-
2 2 2
Q +Q )<0,即Q>Q 。由得:HO(g)=HO(l) ΔH= (ΔH2-ΔH )<0,所以
1 2 1 2 2 2 3
(-Q2+Q)<0,即Q>Q。故Q>Q>Q。
3 2 3 1 2 3
例题 已知:C(s)+O (g)=CO(g) ΔH,
2 2 1
CO(g)+C(s)=2CO(g) ΔH,
2 2
2CO(g)+O (g)=2CO(g) ΔH,
2 2 3
4Fe(s)+3O (g)=2Fe O(s) ΔH,
2 2 3 4
3CO(g)+Fe O(s)=3CO(g)+2Fe(s) ΔH。下列关于上述反应焓变的判断
2 3 2 5
正确的是( )
A. 2ΔH>ΔH
1 3
B. ΔH=ΔH+ΔH
3 4 5
C. ΔH=ΔH+ΔH
1 2 3
D. ΔH<0,ΔH<0
2 4
【答案】C
【解题引导】找准相关热化学方程式 推出相关ΔH之间的关系。
【解析】将已知反应依次标记为①、②、③、④、⑤,则①×2-③得2C(s)+O (g)
2
= 2CO(g) ΔH=2ΔH -ΔH ,由于该反应放热,故2ΔH -ΔH<0,2ΔH<ΔH ,A项
1 3 1 3 1 3
错误;(④+⑤×2)÷3得2CO(g)+O (g)=2CO (g) ΔH ,即ΔH = ,
2 2 3 3
B项错误;②+③得C(s)+O (g)=CO(g)ΔH,即 ΔH=ΔH+ΔH,C项正确;反应
2 2 1 1 2 3
②是吸热反应,ΔH>0,D项错误。
2
第17页(答题时间:40分钟)
一、选择题
1. 已知1mol白磷(s)转化为1mol红磷(s),放出18.39kJ热量,又知:
4P(白,s)+5O (g)═2PO(s);△H
2 2 5 1
4P(红,s)+5O (g)═2PO(s);△H
2 2 5 2
△H△H 关系正确的是( )
1 2
A. △H<△H B. △H=△H C. △H>△H D. 无法确定
1 2 1 2 1 2
2. 在同温同压下,下列各组热化学方程式中,ΔH>ΔH 的是( )
1 2
A. 2H (g)+O(g)=2HO(l) ΔH;2H(g)+O(g)=2HO(g) ΔH
2 2 2 1 2 2 2 2
B. C(s)+ O(g)=CO(g) ΔH;C(s)+O(g)=CO(g) ΔH
2 1 2 2 2
C. S(g)+O(g)=SO (g) ΔH;S(s)+O(g)=SO (g) ΔH
2 2 1 2 2 2
D. H (g)+Cl(g)=2HCl(g) ΔH1; H(g)+ Cl(g)=HCl(g) ΔH
2 2 2 2 2
3. 已知以下三个热化学方程式:
2HS(g)+3O(g)=2SO (g)+2HO(l)ΔH=a kJ·mol-1
2 2 2 2
2HS(g)+O(g)=2S(s)+2HO(l)ΔH=b kJ·mol-1
2 2 2
2HS(g)+O(g)=2S(s)+2HO(g)ΔH=c kJ·mol-1
2 2 2
下列关于a、b、c三者关系的表述正确的是( )
A. a>b>c B. a>c>b
C. c>b>a D. b>a>c
*4. 氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为:
H(g)+ O(g)=HO(l) ΔH=-285.8 kJ·mol-1
2 2 2
CO(g)+ O(g)=CO(g) ΔH=-282.6 kJ·mol-1
2 2
C H (l)+ O(g)=8CO(g)+9HO(l) ΔH=-5 472 kJ·mol-1
8 18 2 2 2
CH(g)+2O(g)=CO(g)+2HO(l) ΔH=-889.6 kJ·mol-1
4 2 2 2
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
A. H (g) B. CO(g)
2
C. C H (l) D. CH (g)
8 18 4
*5. 如图所示,下列说法不正确的是( )。
第18页A. 反应过程(1)的热化学方程式为 A (g)+B (g)=C(g) ΔH =-
2 2 1
QkJ·mol-1
1
B. 反应过程(2)的热化学方程式为C(g)=A (g)+B (g) ΔH =+Q kJ·mol
2 2 2 2
-1
C. Q 与Q 的关系:Q>Q
1 2 1 2
D. ΔH >ΔH
2 1
6. 试比较下列三组ΔH的大小。
(1)同一反应,生成物状态不同时
A(g)+B(g)=C(g) ΔH<0
1
A(g)+B(g)=C(l) ΔH<0
2
则ΔH________ΔH(填“>”“<”或“=”,下同)。
1 2
(2)同一反应,反应物状态不同时
S(g)+O(g)=SO (g) ΔH<0
2 2 1
S(s)+O(g)=SO (g) ΔH<0
2 2 2
则ΔH _______ΔH。
1_ 2
(3)两个有联系的不同反应相比
C(s)+O(g)=CO(g) ΔH<0
2 2 1
C(s)+ O(g)=CO(g) ΔH<0
2 2
则ΔH________ΔH。
1 2
第19页1. 【答案】A
【解析】①4P(白)+5O ═2P O △H ;②4P(红)+5O =2PO △H ,①-②得到
2 2 5 1 2 2 5 2
4P(白)=4P(红)△H=△H -△H ,已知1mol白磷变成1mol红磷放出18.39KJ的热
1 2
量,所以△H-△H<0;△H<△H,故答案为A。
1 2 1 2
2. 【答案】B
【解析】物质的燃烧反应是放热过程,所以焓变是负值,放出的热量越多,ΔH越小。
液态水变为气态水的过程是吸热的,则ΔH<ΔH ,A项错误;1 mol碳单质完全燃烧生成二
1 2
氧化碳气体放出的热量多于不完全燃烧生成一氧化碳气体放出的热量,且该反应的焓变是
负值,则ΔH>ΔH ,B项正确;固态硫变为气态硫需要吸收热量,所以ΔH<ΔH ,C项错
1 2 1 2
误;热化学方程式的化学计量数加倍,焓变数值相应加倍,ΔH =2ΔH ,该化合反应是放
1 2
热的,所以焓变是负值,ΔH<ΔH ,D项错误。
1 2
3. 【答案】C
【解析】解本题时需注意比较反应热大小时要带符号。硫化氢完全燃烧放出的热量最
多,所以a最小;不完全燃烧时,生成液态水时比生成水蒸气时放出的热量多,因为液态
水转化成水蒸气需要吸收热量,所以c最大,故c>b>a。
4. 【答案】B
【解析】已知H 、CO、C H 、CH 的相对分子质量分别为2、28、114、16,所以相
2 8 18 4
同质量(假设均是 1 g)四种物质的物质的量分别为 0.5 mol、 mol、 mol、
mol, 燃烧放出热量分别为(0.5×285.8)kJ、 kJ、 kJ、
×889.6kJ,所以相同质量的上述物质完全燃烧时,放出热量最多的是H,最少的是CO。
2
5. 【答案】C
【解析】由图像数据可知,反应过程(1)的热化学方程式为A (g)+B (g)=C
2 2
(g) ΔH =-QkJ·mol-1。反应过程(2)的热化学方程式为C(g)=A (g)+B
1 1 2 2
(g) ΔH =+QkJ·mol-1,反应过程(1)与反应过程(2)中,反应物、生成物所涉及
2 2
物质及状态均相同,只是过程相反,故反应热的数值相等,符号相反。注意比较 ΔH的大
小时,要注意考虑其正负号。
二、非先择题
6. 【答案】(1)> (2)< (3)<
【解析】(1)C(g)=C(l) ΔH<0,故|ΔH|>|ΔH |,则ΔH<ΔH <0。
2 1 2 1
(2)S(s)=S(g) ΔH>0,故|ΔH|<|ΔH |,则ΔH<ΔH <0。
2 1 1 2
第20页(3)由CO(g)+ O(g)=CO(g) ΔH<0,故|ΔH|>|ΔH |,则ΔH<ΔH <0。
2 2 1 2 1 2
第21页