文档内容
第一节 有机化合物的机构特点
1.1.2 有机化合物中的共价键和同分异构现象
一、有机化合物中的共价键
1.共价键的类型
有机化合物的共价键有两种基本反应类型:σ键和π键
(1)σ键
①形成:在甲烷分子中,氢原子的1s 轨道与碳原子的一个 sp 3 杂化轨道沿
着两个原子核间的键轴,以“头碰头”的形式相互重叠。
②特点:通过σ键连接的原子或原子团可绕键轴旋转而不会导致化学键的
破坏。
③稳定性:键能相对较大,不易断开。
④断键与反应类型的关系:主要发生取代反应。
(2)π键
①形成:在乙烯分子中,两个碳原子均以 sp 2 杂化轨道与氢原子的1s 轨道
及另一个碳原子的 sp 2 杂化轨道进行重叠,形成 4个C—H σ键与一个C—C σ
键;两个碳原子未参与杂化的p 轨道以“肩并肩”的形式从侧面重叠,形成了π
键。
②特点:通过π键连接的原子或原子团不能绕键轴旋转。
③稳定性:π键的轨道重叠程度比σ键的小,所以不如σ键牢固,比较容
易断裂而发生化学反应。
④断键与反应类型的关系:主要发生加成反应。
(3)σ、π键个数的计算
一般情况下,有机化合物中的单键是 σ 键,双键中含有一个 σ 键和一个
π 键,三键中含有一个 σ 键和两个 π 键。
2.键的极性与有机反应
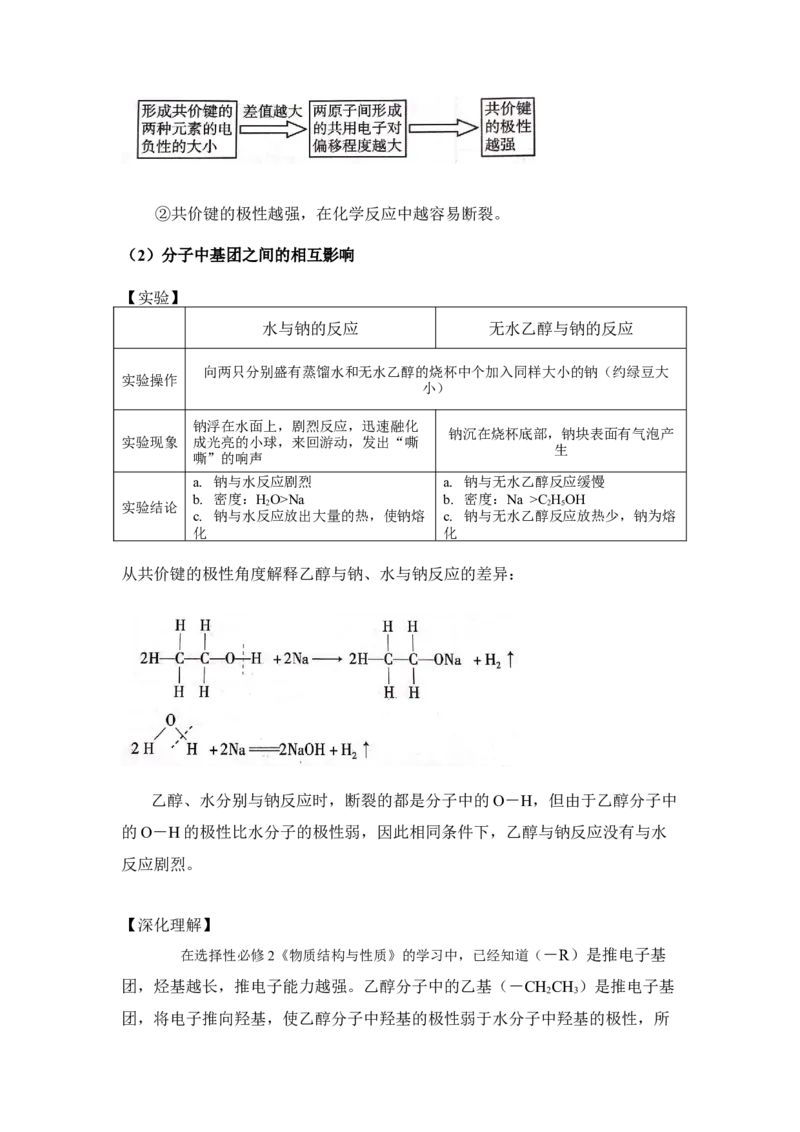
(1)共价键的极性与反应的活泼性
①共价键的极性强弱②共价键的极性越强,在化学反应中越容易断裂。
(2)分子中基团之间的相互影响
【实验】
水与钠的反应 无水乙醇与钠的反应
向两只分别盛有蒸馏水和无水乙醇的烧杯中个加入同样大小的钠(约绿豆大
实验操作
小)
钠浮在水面上,剧烈反应,迅速融化
钠沉在烧杯底部,钠块表面有气泡产
实验现象 成光亮的小球,来回游动,发出“嘶
生
嘶”的响声
a. 钠与水反应剧烈 a. 钠与无水乙醇反应缓慢
b. 密度:HO>Na b. 密度:Na >C HOH
实验结论 2 2 5
c. 钠与水反应放出大量的热,使钠熔 c. 钠与无水乙醇反应放热少,钠为熔
化 化
从共价键的极性角度解释乙醇与钠、水与钠反应的差异:
乙醇、水分别与钠反应时,断裂的都是分子中的O-H,但由于乙醇分子中
的O-H的极性比水分子的极性弱,因此相同条件下,乙醇与钠反应没有与水
反应剧烈。
【深化理解】
在选择性必修2《物质结构与性质》的学习中,已经知道(-R)是推电子基
团,烃基越长,推电子能力越强。乙醇分子中的乙基(-CH CH )是推电子基
2 3
团,将电子推向羟基,使乙醇分子中羟基的极性弱于水分子中羟基的极性,所以乙醇分子中羟基的活性弱于水分子中羟基的活性。
(3)有机反应与无机反应的比较
乙醇与HBr反应:CH —CH —OH + H—Br ――→ CH CH —Br + H O,反应
3 2 3 2 2
中乙醇分子中断裂的键是C—O,原因是 C—O 键极性较强 。
有机反应相对无机反应,有机反应一般反应速率较小,副反应较多,产物
比较复杂。
练习1. 有下列物质:①CH CH ②CH —CH===CH—CH
3 3 3 3
③CH —C≡CH ④CH CH OH
3 3 2
请思考回答:
(1)上述4种有机物分子中只含有σ键的有________(填序号)。
(2)②分子中σ键与π键的个数比为________。
(3)②③分子中碳原子的杂化类型有______________。
(4)④发生酯化反应时,一般断裂的共价键为________键。
(5)④与HBr反应时④中断裂的共价键为________键。
【答案】(1)①④ (2)11∶1 (3)sp3、sp2、sp
(4)O—H (5)C—O
练习2.计算1 mol下列有机物中σ键和π键的数目(用N 表示,N 为阿伏加
A A
德罗常数的值)。
【答案】 (1)13N 1N (2)14N 3N
A A A A
二、有机化合物的同分异构现象
1.概念:化合物具有相同的分子式,但具有不同结构的现象叫同分异构现
象,具有同分异构现象的化合物互为同分异构体。
2.分类
(1)同分异构体的类别
同分异构现象(2)构造类别的比较
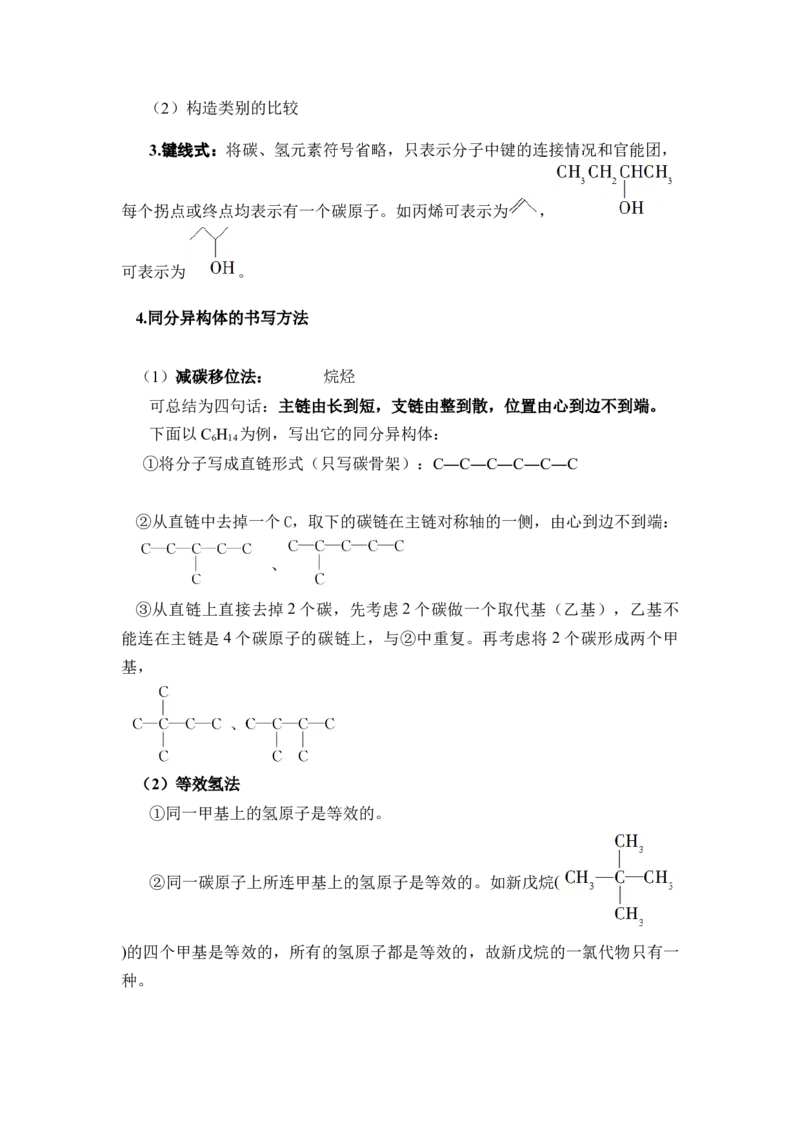
3.键线式:将碳、氢元素符号省略,只表示分子中键的连接情况和官能团,
每个拐点或终点均表示有一个碳原子。如丙烯可表示为 ,
可表示为 。
4.同分异构体的书写方法
(1)减碳移位法: 烷烃
可总结为四句话:主链由长到短,支链由整到散,位置由心到边不到端。
下面以C H 为例,写出它的同分异构体:
6 14
①将分子写成直链形式(只写碳骨架):C―C―C―C―C―C
②从直链中去掉一个C,取下的碳链在主链对称轴的一侧,由心到边不到端:
、
③从直链上直接去掉2个碳,先考虑2个碳做一个取代基(乙基),乙基不
能连在主链是4个碳原子的碳链上,与②中重复。再考虑将 2个碳形成两个甲
基,
(2)等效氢法
①同一甲基上的氢原子是等效的。
②同一碳原子上所连甲基上的氢原子是等效的。如新戊烷(
)的四个甲基是等效的,所有的氢原子都是等效的,故新戊烷的一氯代物只有一
种。③处于对称位置上的氢原子是等效的。如 的六个甲
基是等效的,18个氢原子都是等效的,因此该物质的一氯代物也只有一种。
(3)基元法
如丁基有4种结构、则丁醇(C H -OH)、一氯丁烷(C H -Cl)、
4 9 4 9
戊醛(C H -CHO)等都有4中同分异构体。
4 9
—CH: 1种
—C H :1种
2 5
—C H :2种
3 7
—C H :4种
4 9
—C H :8种
5 11
(4)换元法
如二氯苯(C H Cl )有3种同分异构体,则四氯苯(C H Cl )也有3种同分异
6 4 2 6 2 4
构体(将H换成Cl)。
(5)定一移一法
对于二元取代物的同分异构体的判定,可固定一个取代基的位置,在移
动另一个取代基,以确定相对分子质量。
【拓展】同系物、同分异构体、同位素、同素异形体的比较同位素 同素异形体 同系物 同分异构体
质子数相同
结构相似,分子组
而中子数不 分子式相同,但
由同种元素形成 成上相差一个或若
概念 同的同一种 结构不同的化合
的不同单质 干个CH 原子团的
元素的不同 2 物
物质
原子
对象 原子 单质 有机化合物 化合物
化学性质几
化学性质相似或
乎相同,物 化学性质相似, 化学性质相似,物
性质 不同,物理性质
理性质略有 物理性质不同 理性质不同
有差异
差异
化学式可相同,
、 、 正戊烷、异戊烷
实例 也可不同。如O 甲烷和乙烷
3 和新戊烷
和O
2
练习3.下列选项中的物质属于官能团异构的是( )
A.CH CH CH CH 和CH CH(CH )
3 2 2 3 3 3 2
B.CH ===C(CH ) 和CH CH===CHCH
2 3 2 3 3
C.CH CH OH和CH OCH
3 2 3 3
D.CH CH CH COOH和(CH ) CHCOOH
3 2 2 3 2
【答案】C [有机化合物分子式相同,但具有不同官能团的同分异构体属
于官能团异构。A项中的两种物质属于碳链异构;B项中两种物质的官能团均
为 ;D项中两种物质的官能团均为—COOH,均属于位置异构;C项
中两种物质的官能团分别是—OH(羟基)和 (醚键),官能团不同,
属 于 官 能 团 异 构 。 ]
练习4.称为同分异构体的物质不可能( )
A.具有相同的相对分子质量 B.具有相同的熔、沸点和密度
C.具有相同的分子式 D.具有相同的组成元素
【答案】B.
练习5. 下列化学用语正确的是A.全氟丙烷的球棍模型: B.丙醛的键线式:
C.次氯酸钠的电子式 D.异丙醇的结构简式:
CH CH(OH)CH
3 3
【答案】D
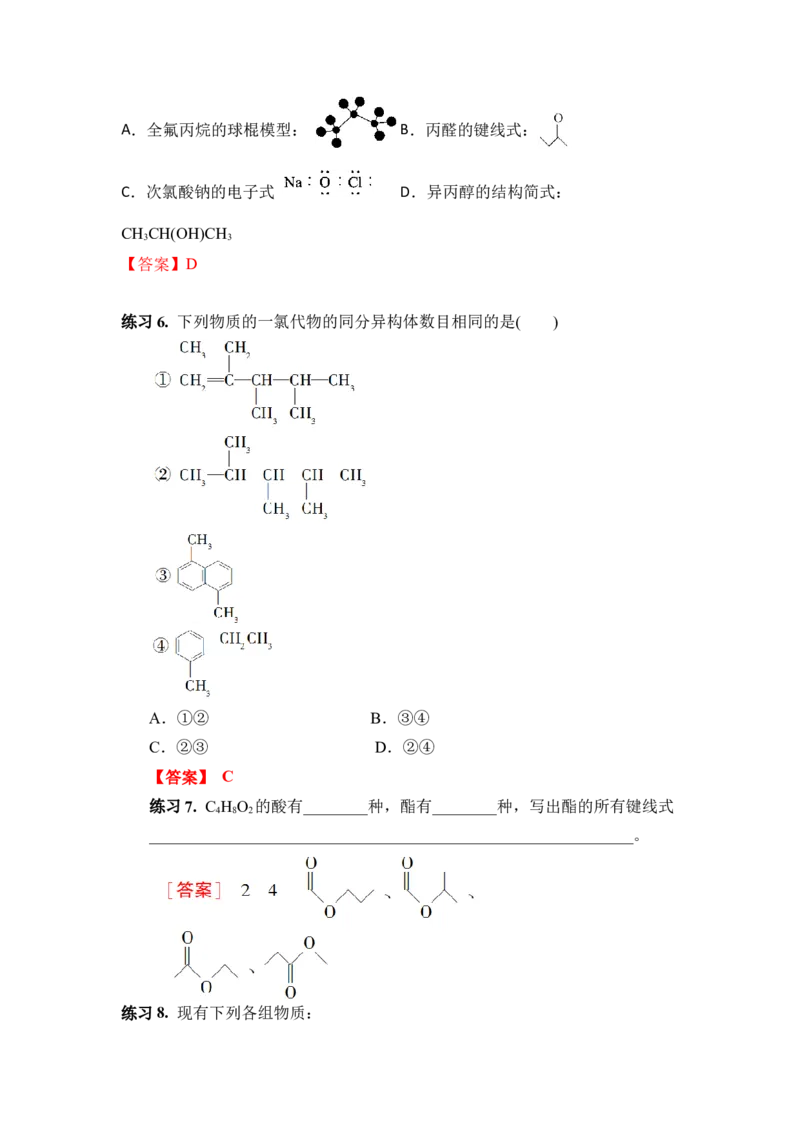
练习6. 下列物质的一氯代物的同分异构体数目相同的是( )
A.①② B.③④
C.②③ D.②④
【答案】 C
练习7. C H O 的酸有________种,酯有________种,写出酯的所有键线式
4 8 2
____________________________________________________________。
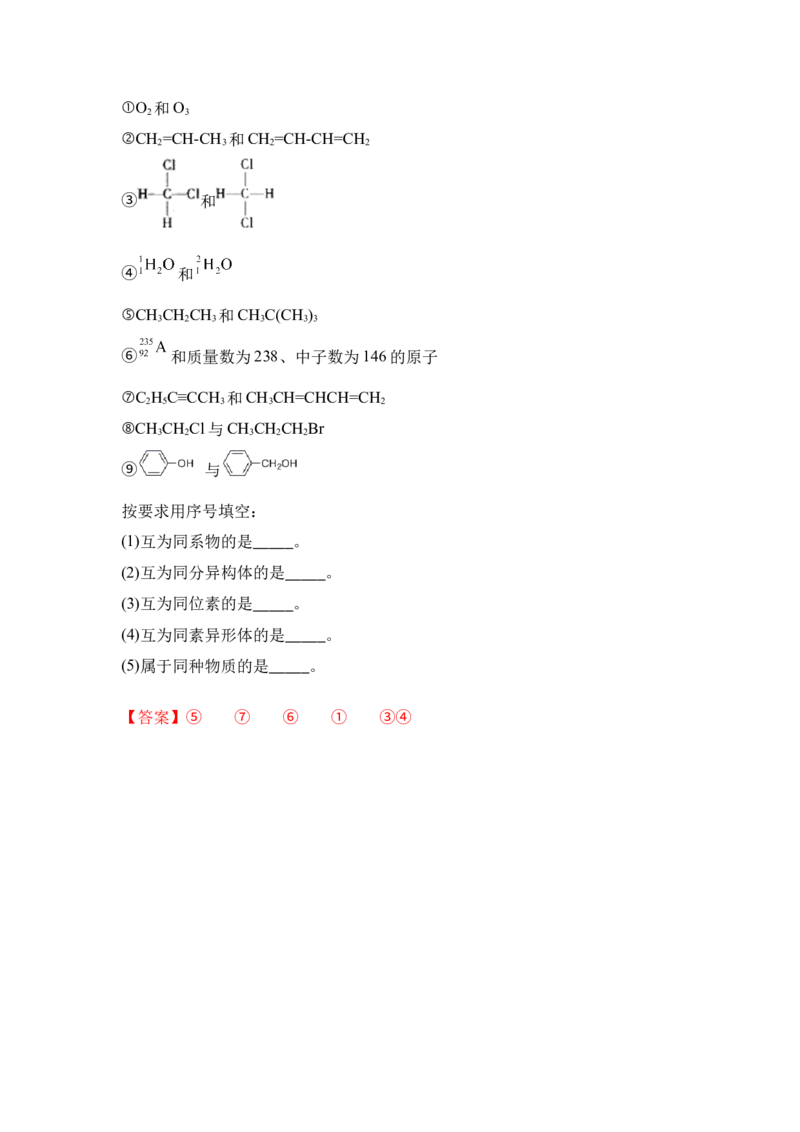
练习8. 现有下列各组物质:①O 和O
2 3
②CH =CH-CH 和CH =CH-CH=CH
2 3 2 2
③ 和
④ 和
⑤CH CH CH 和CH C(CH )
3 2 3 3 3 3
⑥ 和质量数为238、中子数为146的原子
⑦C H C≡CCH 和CH CH=CHCH=CH
2 5 3 3 2
⑧CH CH Cl与CH CH CH Br
3 2 3 2 2
⑨ 与
按要求用序号填空:
(1)互为同系物的是_____。
(2)互为同分异构体的是_____。
(3)互为同位素的是_____。
(4)互为同素异形体的是_____。
(5)属于同种物质的是_____。
【答案】⑤ ⑦ ⑥ ① ③④