文档内容
第一章 原子结构与性质
第二节 原子结构与元素的性质
1.2.1 原子结构与元素周期表
一.选择题
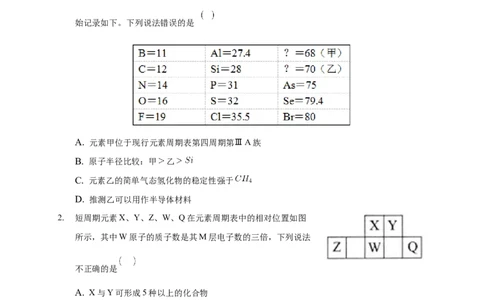
1. 2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性
质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原
始记录如下。下列说法错误的是
A. 元素甲位于现行元素周期表第四周期第ⅢA族
B. 原子半径比较:甲 乙
C. 元素乙的简单气态氢化物的稳定性强于
D. 推测乙可以用作半导体材料
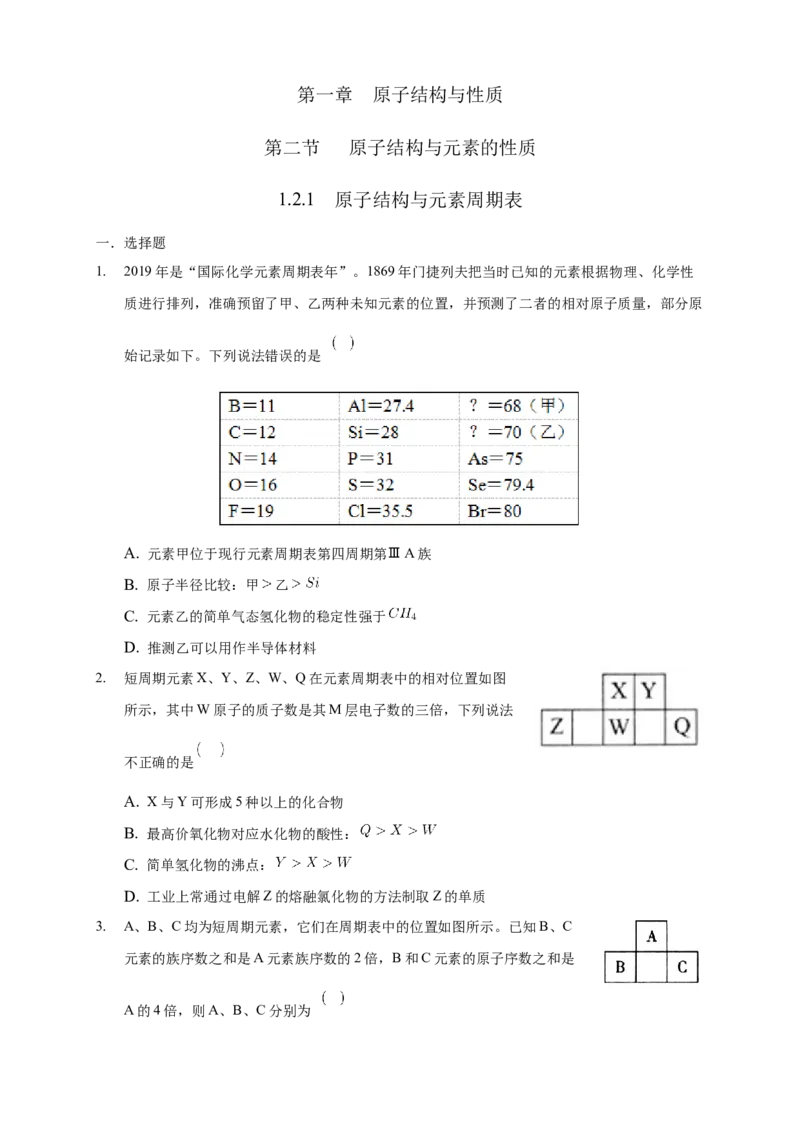
2. 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图
所示,其中W原子的质子数是其M层电子数的三倍,下列说法
不正确的是
A. X与Y可形成5种以上的化合物
B. 最高价氧化物对应水化物的酸性:
C. 简单氢化物的沸点:
D. 工业上常通过电解Z的熔融氯化物的方法制取Z的单质
3. A、B、C均为短周期元素,它们在周期表中的位置如图所示。已知B、C
元素的族序数之和是A元素族序数的2倍,B和C元素的原子序数之和是
A的4倍,则A、B、C分别为A. Be、Na、Al B. B、Mg、Si C. C、Al、P D. O、P、Cl
4. 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,
图中每个点代表一种元素,其中O点代表氢元素。下列说法中不正确的是
A. 离O点越远的元素原子半径越大
B. 虚线相连的元素处于同一族
C. B、C最高价氧化物对应的水化物可相互反应
D. A、B组成的化合物中可能含有共价键
5. 下列说法正确的是
A. 族序数等于其周期序数的元素一定是金属元素
B. 元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素
C. 从左到右,同周期非金属得电子能力、最高价氧化物对应水化物酸性依次增强
D. 从上到下,第ⅦA族元素氢化物的热稳定性和还原性均依次减弱
6. Se、Br两种元素的部分信息如图所示,下列说法正确的是
A. 原子半径:
B. 还原性:
C. Se在元素周期表中位于第4周期ⅥA族
D. Se、Br位于同一主族
7. 下列有关元素周期表的说法正确的是
A. Li是最活泼金属,F是最活泼非金属
B. 在周期表中金属与非金属的分界处,可找到做催化剂的材料
C. 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D. 同一周期 第一周期除外 的元素,从左到右由金属逐渐过渡到非金属
8. 下列关于元素周期表的说法正确的是
A. 每一周期都从碱金属元素开始,最后以稀有气体元素结束
B. 某元素原子最外层电子数为2,则该元素一定位于第ⅡA族C. 第二、三周期上下相邻的元素的原子核外电子数相差8
D. 元素周期表有7个横行,即7个周期,16个纵列,即16个族
9. 短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为16。Y
的单质是空气中含量最多的气体,Z原子的最外层电子数是其内层电子数的3倍,W是短周期
中金属性最强的元素。下列说法正确的是
A. X位于元素周期表中第2周期ⅤA族
B. 原子半径:
C. X、Y、Z的非金属性依次减弱
D. 由Z和W组成的化合物不止一种
10. 以下有关原子结构及元素周期律、元素周期表的叙述正确的是
A. 根据元素周期律,由 可以类推出氟元素也存在最高价氧化物的水化物
B. 元素周期表有十八个纵行,共十六个族
C. 第ⅦA族元素从上到下,其简单氢化物的稳定性逐渐增强
D. 在元素周期表的金属和非金属分界线附近寻找优良的催化剂
11. 短周期主族元素W、X、Y、Z的原子序数依次增大,它们在元素周期表
中的相对位置如图所示,Y原子的最外层电子数是其电子层数的2倍。下
列说法正确的是
A. W的最高价氧化物的水化物是与W同周期和与W同主族中酸性最强的酸
B. 简单离子的还原性:
C. 氢元素 与W、Z三种元素组成的化合物仅含有共价键
D. 简单气态氢化物的热稳定性:
12. 下列关于碱金属和卤素的说法正确的是
A. 随着原子序数的增大,密度均增大
B. 随着原子序数的增大,熔沸点均升高
C. 最高正价均等于主族序数
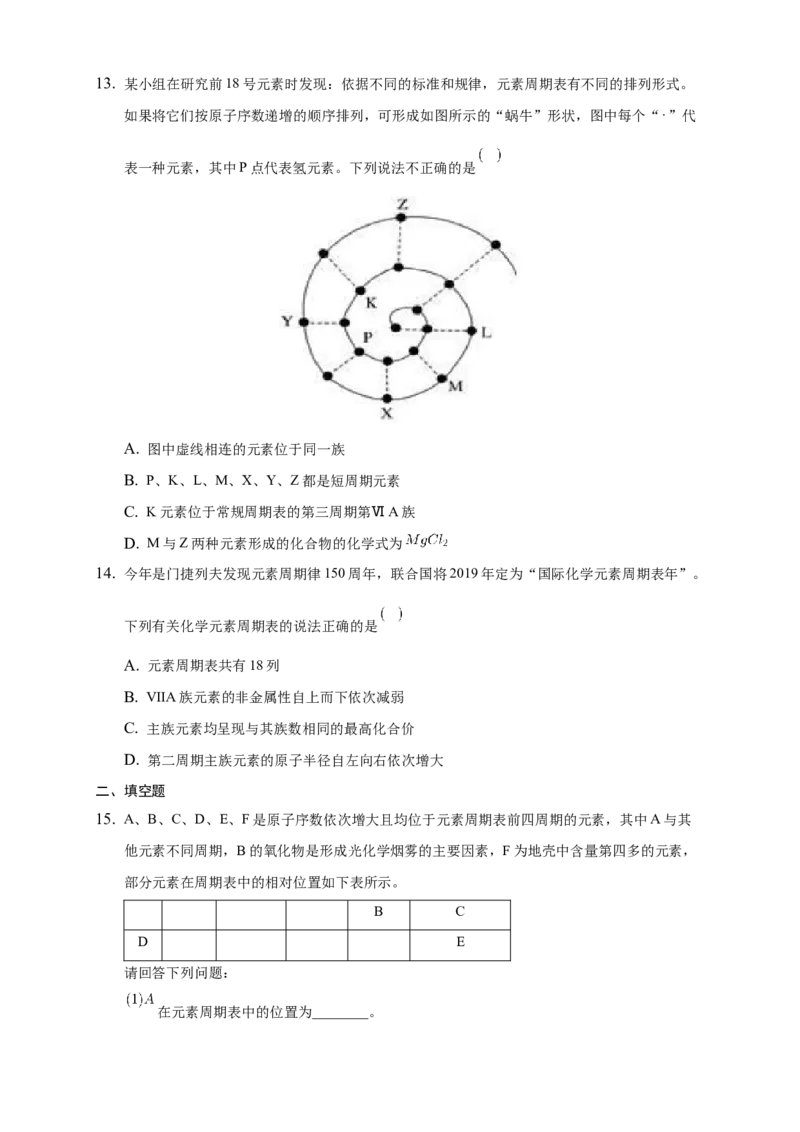
D. 电子层数均等于周期序数13. 某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。
如果将它们按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“ ”代
表一种元素,其中P点代表氢元素。下列说法不正确的是
A. 图中虚线相连的元素位于同一族
B. P、K、L、M、X、Y、Z都是短周期元素
C. K元素位于常规周期表的第三周期第ⅥA族
D. M与Z两种元素形成的化合物的化学式为
14. 今年是门捷列夫发现元素周期律150周年,联合国将2019年定为“国际化学元素周期表年”。
下列有关化学元素周期表的说法正确的是
A. 元素周期表共有18列
B. ⅦA族元素的非金属性自上而下依次减弱
C. 主族元素均呈现与其族数相同的最高化合价
D. 第二周期主族元素的原子半径自左向右依次增大
二、填空题
15. A、B、C、D、E、F是原子序数依次增大且均位于元素周期表前四周期的元素,其中A与其
他元素不同周期,B的氧化物是形成光化学烟雾的主要因素,F为地壳中含量第四多的元素,
部分元素在周期表中的相对位置如下表所示。
B C
D E
请回答下列问题:
在元素周期表中的位置为________。、D、E的简单离子半径由大到小的顺序为________ 填离子符号 ;B、C、E的最简单
氢化物的沸点由高到低的顺序为________________ 填化学式 。
常温下,F 的单质在加热条件下可溶于足量的 浓溶液,反应的离子方程式为
________________;检验反应后溶液中F的阳离子可选用的试剂为________ 填化学式,写一
种 。
三、推断题
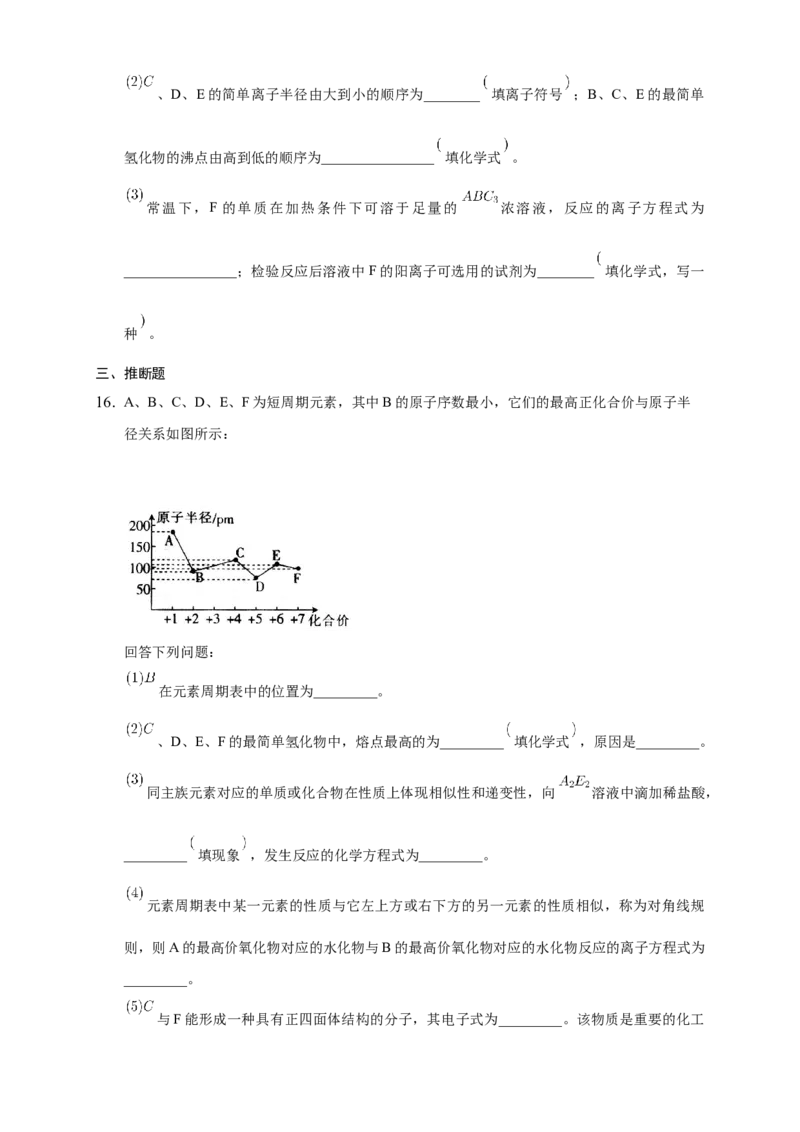
16. A、B、C、D、E、F为短周期元素,其中B的原子序数最小,它们的最高正化合价与原子半
径关系如图所示:
回答下列问题:
在元素周期表中的位置为_________。
、D、E、F的最简单氢化物中,熔点最高的为_________ 填化学式 ,原因是_________。
同主族元素对应的单质或化合物在性质上体现相似性和递变性,向 溶液中滴加稀盐酸,
_________ 填现象 ,发生反应的化学方程式为_________。
元素周期表中某一元素的性质与它左上方或右下方的另一元素的性质相似,称为对角线规
则,则A的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物反应的离子方程式为
_________。
与F能形成一种具有正四面体结构的分子,其电子式为_________。该物质是重要的化工原料,极易水解,在潮湿的空气中能生成两种酸,该反应的化学方程式为_________。